Introducción
La diabetes mellitus (DM) es una enfermedad endocrino-metabólica crónica que constituye un serio problema de salud pública mundial. 1 Estimados recientes calculan que el número de diabéticos se elevará desde 425 millones en 2017 hasta 629 millones en 2045.
El incremento de la prevalencia de la enfermedad se debe principalmente a la diabetes tipo 2 (DM2), que representa el 90-95% de todos los casos, y al proceso de envejecimiento poblacional. 1 Se estima que el gasto en los cuidados de salud de los pacientes diabéticos alcance 776 billones de dólares para el 2045. 2
En Ecuador, la DM ha tenido un incremento importante en los últimos años. 3 En 2006 se informaron 18 406 casos y una tasa de 137,27 x 100 000 habitantes; en 2013, fueron 115 690 y la tasa de 733,39.Un estudio en Cuenca, Ecuador, encontró una prevalencia de DM2 de 5,7% (femenino: 5,5%; masculino: 5,9%). 4 También, la DM es la segunda causa de muerte en la población ecuatoriana, con una tasa del 6,6%. 5
La DM es una enfermedad crónica no transmisible, caracterizada por complicaciones microvasculares y macrovasculares. Dentro de las complicaciones microvasculares se encuentran la retinopatía, nefropatía y neuropatía y en las macrovasculares, la enfermedad cardiovascular, enfermedad cerebrovascular y la enfermedad vascular periférica. 6
Tanto la neuropatía diabética como la enfermedad vascular periférica convierten al pie del diabético en un pie de alto riesgo, sobre el que factores desencadenantes, generalmente traumatismos crónicos y mantenidos, provocan úlceras. El pronóstico de la úlcera y por tanto de la extremidad va a estar en función de la mayor o menor extensión de la neuropatía, isquemia e infección asociada con la úlcera.7
La infección del pie diabético, asociada a isquemia, es la causa más frecuente de amputación de la extremidad inferior en la población general, de ingreso hospitalario y de disminución de la calidad de vida en los pacientes con DM. 7 El 15% de los diabéticos van a sufrir a lo largo de su vida una infección del pie, con una incidencia anual del 1-4%, precedida en más del 80% de los casos de una úlcera en el pie.
A pesar de los avances de los últimos años, la úlcera del pie diabético (UPD) representa una considerable carga para los servicios de salud, no solo por su elevada prevalencia, sino por el alto riesgo de amputación de los miembros inferiores. 8 En diabéticos, el 84% de las amputaciones no traumáticas de miembros inferiores son precedidas por úlceras del pie; este grupo tiene 25 veces mayor riesgo de amputaciones que las personas no diabéticas. 9
La supervivencia a los 5 años después de la aparición de la úlcera es de 50-60%, peor que la de muchos cánceres comunes. 8 También la recurrencia de la úlcera curada alcanza el 40% en los 12 meses.
El Ministerio de Salud Pública del Ecuador, ante este problema, ha implementado estrategias de atención integral y multidisciplinaria a los pacientes diabéticos, con el objetivo de prevenir y evitar la discapacidad por amputación de miembros inferiores, por lo, desde el año 2012, ciertos hospitales públicos del país han sido dotado con dosis del factor de crecimiento epidérmico humano recombinante (EGF).
EL EGF estimula la proliferación de fibroblastos, queratinocitos y células endoteliales vasculosas, de modo que potencia sus propiedades cicatrizantes. 10 Las investigaciones confirman que EGF acelera el desarrollo de tejido de granulación y el cierre de las heridas del pie diabético. 11
El Heberprot-P®, producto líder de la Biotecnología cubana, ha probado su efectividad, con pocas reacciones adversas, en el tratamiento de la UPD en diferentes estudios.12,13,14,15 Este producto utiliza como componente activo al EFG, evita las amputaciones y es un medicamento único en el mundo, con un considerable impacto económico, social y médico en Cuba y otros países. 16,17,18
Por la alta tasa prevalencia en Ecuador de la DM y sus complicaciones como UDP se realizó esta investigación en pacientes atendidos por esta complicación en el Hospital Provincial General Docente de Riobamba, para evaluar la efectividad terapéutica del Heberprot-P®.
Métodos
Se realizó un ensayo no aleatorizado no controlado, dirigido a valorar el grado de cicatrización de las úlceras de pie diabético ante la aplicación de la terapia Heberprot-P® en el Hospital Provincial General Docente de Riobamba, Ecuador, durante enero-diciembre del 2013.
Para esta investigación fue necesario el consentimiento y aprobación del Departamento de Docencia e Investigación del Hospital Provincial General Docente de Riobamba, Ecuador.
En el estudio participaron 51 personas con el diagnóstico de UPD de ambos géneros, durante el proceso de tratamiento. Hubo 3 casos que abandonaron la terapia y no se incluyeron en el estudio. Los criterios de inclusión fueron que presentasen UPD de grado II o mayores de acuerdo con la clasificación de Wagner, que no presentasen enfermedades crónicas descompensadas u oncológicas y hayan culminado el tratamiento.
Clasificación de Wagner en 6 categorías: 19
Grado 0: ninguna lesión, pie de riesgo (cabezas de metatarsianos prominentes, dedos en garra, deformidades óseas, callos gruesos).
Grado I: úlceras superficiales.
Grado II: úlceras profundas.
Grado III: úlceras profundas con osteomielitis.
Grado IV: Gangrena limitada.
Grado V: gangrena extensa (todo el pie afectado con manifestaciones sistémicas).
Para la recolección de la información se revisaron las historias clínicas de los pacientes y la base de datos de los pacientes del programa Pie Diabético del Hospital Provincial General Docente de Riobamba, Ecuador.
Se analizaron las variables edad, sexo, tipo de UPD, según su etiopatogenia, clasificación de la lesión (según la clasificación de Wagner), número de dosis de farmacoterapia aplicadas, tiempo transcurrido para el proceso de cicatrización, nivel de cicatrización, evaluando como respuesta mínima a las úlceras que no presentaron modificación relevante,
como cicatrización parcial a las úlceras con tejido de granulación útil y reducción significativa de la úlcera y cicatrización total por la ausencia de la úlcera o lesión.
La clasificación etiopatogénica de Mc CooK divide el pie diabético en neuroinfeccioso e isquémico. 20 En el pie diabético neuroinfeccioso están presentes todos los pulsos periféricos, predomina la neuropatía y la infección, conserva la temperatura y hay tendencia a la deformidad de la arquitectura ósea. Se presenta como flemón difuso o celulitis, absceso y mal perforante plantar.
En el pie diabético isquémico predomina la isquemia, con ausencia por lo menos de un pulso arterial periférico, y se conserva bastante la arquitectura ósea. Se presenta como úlcera isquémica y gangrena seca.
El fármaco utilizado en la terapia fue el factor de crecimiento epidérmico-Heberprot-P® (Heber Biotec, S.A. La Habana, Cuba), se administró en dosis de 75 µg, tres veces por semana, mediante infiltración intralesional y perilesional, hasta alcanzar la granulación completa de la lesión.
Análisis estadístico
Para el análisis y procesamiento de los datos, se utilizó el programa SPSS, versión 19. Los resultados se muestran en tablas estadísticas con números absolutos y porcentajes. Para comparar dos porcentajes se utilizó la prueba de comparación de proporciones para dos muestras independientes. La asociación entre variables cualitativas, mediante χ2. El nivel de significación escogido fue 5%.
Resultados
La edad promedio que presentaron los pacientes del estudio fue 64,7 años, con el 49% entre los 60 - 80 años. De ellos 28 fueron de sexo femenino (54,9%) y 23 masculinos (45,1%), sin diferencias significativas entre sexos (z=0,79; p=0,42).
Se halló asociación entre el sexo femenino y la edad avanzada de las pacientes y la aparición del pie diabético (p= 0,01).
En lugar de procedencia: Chimborazo 66,7%, Bolívar 15,7% Tungurahua 5,9%, Pastaza 5,9%, Guayas 3,9% y Cotopaxi 2,0%. El 98% presentó DM2 y el 2% diabetes tipo 1(DM1).
Según la etiopatogenia de las úlceras de pie diabético, se encontraron 30 pacientes (58,8%) con úlceras neuropatías y 21 (41,2%) con úlceras isquémicas.
El miembro inferior que se encontró afectado fue, en el 49%, el izquierdo, y el 51%, el derecho.
En relación con la clasificación de Wagner se encontró que 33 pacientes (64,7%) presentaron Wagner II, 13 (25,5%), Wagner III y 5 (9,8%), Wagner IV.
Presentaron asociación las variables grado de Wagner II y el tipo de úlcera neuro-infecciosa con p=0,01.
La media de dosis de Heberprot-P® aplicadas a los pacientes fue de 16,78 dosis, con un mínimo de 3, máximo de 30 y una moda de 24, con una desviación estándar de 9,2. Existió asociación entre mayor número de dosis y el tipo de lesión isquémica, con p= 0,01. También se observó relación entre menor grado de lesión, según la escala de Wagner, y menor número de dosis requerida para su tratamiento (diferencia estadísticamente significativa, p=0,01).
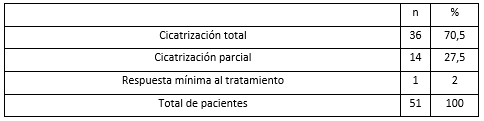
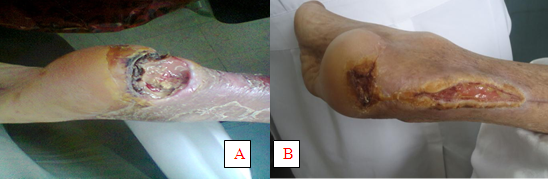
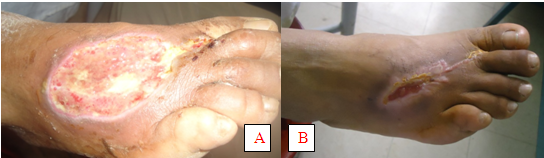
De acuerdo con la respuesta al tratamiento, se observó que en el 70,5 % de los casos tratados se logró la epitelización total de la lesión (figuras 1 y 2) y solo en el 2% se evidenció una respuesta mínima al tratamiento (tabla I).
Se evidenció relación entre el grado de la lesión II, según la escala de Wagner, lesiones neuroinfecciosas y la cicatrización total de la úlcera, con p= 0,01.
A: Inicio de tratamiento
B: Granulación y epitelización a las 25 dosis aplicadas de Heberprot-P®
Estos eventos ocurrieron con una media de 50,3 (desviación estándar 27,7) días de tratamiento para evidenciarse la epitelización, además de observarse un mínimo de 3 días y un máximo de 90 días. No se encontró asociación entre el tiempo de tratamiento y la edad de los pacientes (p ≥ 0,05).
En relación con los efectos adversos, de los 51 pacientes solo en 17, el 33,3%, presentó sintomatología leve en relación con la aplicación del fármaco, principalmente de escalofríos (tabla II). No se encontró asociación estadísticamente significativa con la aparición de efectos adversos y las variables edad y sexo (p ≥ 0,05).
Discusión
En esta investigación predominó el sexo femenino sin diferencia estadística significativa, lo cual difiere de otros estudios, que informan el predominio del sexo masculino de presentar pie diabético. 21,22,23 Estos resultados probablemente se deben a que la mayoría de las pacientes de esta investigación se encontraban entre la sexta y séptima décadas de vida y durante la posmenopausia se pierden los efectos vasodilatadores y protectores contra la aterosclerosis que proporcionan los estrógenos, lo que favorece la aparición del pie diabético.
En relación con la edad, los datos encontrados hacen referencia a una predisposición de presentar UPD entre los 60-70 años, lo que es similar a otros estudios.24) Es común encontrar en estos pacientes las complicaciones de la diabetes, como es el pie diabético, por la larga evolución de la enfermedad. El tipo de diabetes predominante en el 98% fue la DM2, que suele afectar a personas obesas y mayores de 40 años, grupo etario con prevalencia y presentación a menudo solapada.
Los pacientes diabéticos con una larga evolución de su enfermedad están predispuestos a presentar las complicaciones de la DM, como es la UPD, una de las complicaciones que mayor estadía hospitalaria provoca y contribuye al incremento de discapacidad física.
Sin duda es un problema de salud a nivel mundial, que requiere alternativas de tratamiento que disminuyan el índice de amputaciones y propicien la cicatrización de la UPD.
En respuesta a esta necesidad, se realiza este estudio para sustentar con datos estadísticos de Ecuador sobre la eficacia del factor de crecimiento en el tratamiento de la cicatrización de las UPD.
La clasificación fisiopatológica de Mc. Cook que se utilizó hace diferencia entre la úlcera neuropática no isquémica y la úlcera de origen isquémico, aunque frecuentemente hay una superposición de ambos parámetros. En este estudio se encontró predominantemente la úlcera neuropática no isquémica en el 58,8%, lo cual es similar a lo encontrado en la biografía consultada.25
Según la clasificación de Wagner, el grado II estuvo representado por el 64,7% de los pacientes, similar a lo reportado por otros estudios; 24) sin embargo, es importante resaltar que el 35,3% tratados con Heberprot-P® presentaron Wagner grado III y IV, pacientes candidatos a sufrir amputaciones.
En cuanto a la terapia realizada con Heberprot-P®, fue de 17 infiltraciones perilesionales, realizadas hasta evidenciar epitelización, con una moda de 24 infiltraciones, datos semejantes a los encontrados en estudios revisados.25,26 Se observó correlación entre la gravedad de la lesión y el número de dosis utilizadas de Heberprot-P®, lo que refuerza la teoría de que la prevención en el paciente afectado de pie diabético continua manifestándose como un pilar imprescindible en el tratamiento de esta enfermedad. 26
La efectividad del Heberprot-P® de 75 μg fue satisfactoria en el 98% de los pacientes, que lograron granulación el 27,5% y cicatrización completa de la lesión, el 70,5%, al final del tratamiento en un plazo de 50 días, resultados que se corresponde con diferentes estudios revisados.11,12,14,15,26
Los efectos adversos encontrados en el estudio fueron leves sin ninguna manifestación grave. El efecto adverso más frecuente encontrado fueron los escalofríos, lo que difiere de los estudios revisados, que hacen referencia principalmente al dolor en el área de la aplicación del fármaco; en el presente estudio este evento adverso se observó solo en 4 pacientes, posiblemente debido a que el fármaco se diluyó con solución salina.25,26,27
También el Heberprot-P® se ha ensayado con otras modalidades terapéuticas con resultados prometedores. Así, Fabelo et al. 28 encontraron que los pacientes con pie diabético tratados con el Heberprot-P® y ozonoterapia tuvieron una buena respuesta al tratamiento (60,5%), un tiempo de granulación entre 2 y 4 semanas (55,6%), con predominio de la estadía hospitalaria de 1 a 21 días.
Las principales limitaciones de esta investigación radican en que no existió grupo control y no hubo enmascaramiento de la asignación de los pacientes, por ser un solo grupo.
Conclusiones
Esta investigación ratifica la efectividad del Heberprot-P® en el tratamiento de los pacientes afectados por UPD, además de ser un fármaco eficaz y seguro para su aplicación local.
En el futuro se deberán continuar las investigaciones con diseños más robustos que involucren ensayos clínicos aleatorizados y controlados.