Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de Ciencias Médicas de Pinar del Río
versión On-line ISSN 1561-3194
Rev Ciencias Médicas vol.19 no.4 Pinar del Río jul.-ago. 2015
ARTÍCULO ORIGINAL
Anticuerpos antileptospirales en Intacglobín nueva posibilidad terapéutica para tratar la leptospirosis
Antileptospiral antibodies in Intacglobin, a new therapeutic possibility for treating leptospirosis
Juan Manuel Lemus Quintana1, Hildefonso Caridad Cabezas Alfonso2
1Especialista de Primer Grado Medicina Interna. Máster en longevidad satisfactoria. Hospital Provincial Clínico Quirúrgico "León Cuervo Rubio". Pinar del Río. Correo electrónico: clara@princesa.pri.sld.cu
2DrC. en Microbiología e Inmunología. Dr. en Medicina Veterinaria. Experto en Leptospirosis de la OPS. Profesor Consultante y Titular. Universidad de Ciencias Médicas de Pinar del Río. Correo electrónico: loidel@princesa.pri.sld.cu
RESUMEN
Introducción: el Intaglobin es un producto biológico obtenido en la Planta de Hemoderivados de La Habana, contiene inmunoglobulinas policlonales de las clases IgG, IgM e IgA, empleadas actualmente como complemento inmunológico en diversas afecciones.
Objetivo: demostrar la presencia y efectividad de anticuerpos de inmunoglobulinas antileptospirales en el Intacglobín para el tratamiento específico de la leptospirosis.
Material y método: se realizó un estudio en 13 lotes de Intaglobin para demostrar la presencia de inmunoglobulinas antileptospirales en este producto. Se emplearon dos técnicas de laboratorio, la técnica de microaglutinación con 10 serogrupos de leptospiras (técnica de referencia de la OMS), y la técnica UMELISA, con un Ag desarrollado por la Universidad de Ciencias Médicas. Las muestras de Intaglobin fueron diluidas a partir de 1:50 hasta 1.3200 para la técnica de microaglutinación y de 1:21 para UMELISA. Se consideró positiva la prueba cuando aglutinaba el 50% o más de los antígenos para técnica de microaglutinación y positiva según corte establecido para UMELISA.
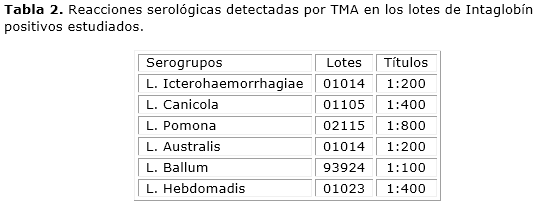
Resultados: en siete de los 13 lotes estudiados se detectaron reacciones serológicas frente a las dos técnicas empleadas. Hasta 1:1600, específicamente en el caso del serogrupo L. Hebdomadis 1:400, en el de L. Icterohaemorrhagiae, Canícola, Pomona y Australis 1:200, y Ballum 1:100.
Conclusiones: se abre una nueva posibilidad de tratamiento para la leptospirosis, aumentando el arsenal terapéutico con este producto el cual adquiere ahora un valor agregado.
DeCS: Intacglobín, Leptospira, Serogrupo, Hiperinmune.
ABSTRACT
Introduction: Intacglobin is biological product obtained in the Havana Hemoderivatives Plant, contains polyclonal immunoglobulins of the classes IgG, IgM and IgA, presently used as immunologic complement in diverse conditions.
Objective: to show the presence and effectiveness of antileptospiral immunoglobulins antibodies in Intacglobin for the specific treatment of leptospirosis.
Material and method: a study was carried out in thirteen lots of Intacglobin, in order to show the presence of antileptospiral immunoglobulins in this product. Two laboratory techniques were used: microagglutination with 10 serogroups of leptospira (WHO reference technique), and UMELISA, with an Ag developed the University of Medical Sciences. The Intacglobin samples were diluted from 1:50 to 1.3200 for the microagglutination and from 1:21 for UMELISA. The test was considered positive when agglutination of the antigens was 50% or higher for the microaaglutination technique and positive according to range stablished for UMELISA.
Results: in seven of the thirteen studied lots serologic reactions were detected before the two used techniques. Up to 1:1600, specifically in the case of the serogroup L. Hebdomadis 1:400, in the L. Icterohaemorrhagiae, Canicola, Pomona y Australis 1:200, and Ballum 1:100.
Conclusions: a new possibility of treating leptospirosis, increasing the therapeutic stock with this product, which acquires now an added value.
DeCS: Intacglobin, Lleptospira, Serogroup, Hyperimmune.
INTRODUCCIÓN
La utilización de preparados de inmunoglobulinas humanas polivalentes a títulos sustitutivos ha representado un gran progreso en la lucha contra el déficit inmunitario sérico, así como en la profilaxis o terapéutica.1 El Intacglobín surge como producto comercial en 1990 y constituye un medicamento genérico de origen sanguíneo, obtenido en la Planta de Hemoderivados "Arístides Viera", perteneciente a la Empresa de Sueros y Productos Hemoderivados "Adalberto Pesant" radicada en La Habana. Contiene inmunoglobulinas Polivalentes de las clases IgA, IgM e IgG.
Dicho producto es una solución inyectable para uso intravenoso de Inmunoglobulina Humana Normal 5%. Durante años fue una de las pocas inmunoglobulinas líquidas de molécula intacta en el mundo. Tiene varias aplicaciones desde el punto de vista del tratamiento de procesos infecciosos por Pseudomona aeruginosa1-3 enfermedades inmunosupresoras virales 4 y otras afecciones como el Síndrome de Guillen Barre, la enfermedad de Kawasaki 5 por ser rico en inmunoglobulinas policlonales.
El trabajo que se presenta no tiene referencias en el país puesto que constituye un estudio específico del producto como tal. Es un estudio intencionando la posibilidad de definir su rango de aplicación, en este caso se trata de que sirva como un agente terapéutico de primer orden en el tratamiento de la leptospirosis, es decir, que se aplique con conocimiento del nivel de inmunoglobulinas antilesptospirales específicas en esta enfermedad y no como un producto biológico más. Buscar nuevos métodos de tratamiento en el caso de la leptospirosis, a pesar de que la enfermedad se conoce bien clínicamente hace siglos atrás, renueva esperanzas de que se pueda perfeccionar un modelo para ello.
El objetivo de este trabajo demostrar la presencia y efectividad de anticuerpos de inmunoglobulinas antileptospirales en el Intacglobín para el tratamiento específico de la leptospirosis.
MATERIAL Y MÉTODO
El Centro de Leptospirosis de la Facultad de Ciencias Médicas de Pinar del Río en coordinación con la Planta de Hemoderivados de La Habana, desarrolló una investigación dirigida a detectar la presencia de anticuerpos antileptospirales (Igs), en diferentes lotes de Intaglobin, 13 en total. Para ello se utilizó la técnica de microaglutinación (TMA) que es la técnica de referencia de la OMS, empleando los serogrupos, serovares y cepas de referencia (procedentes del LNRL del IPK) siguientes:
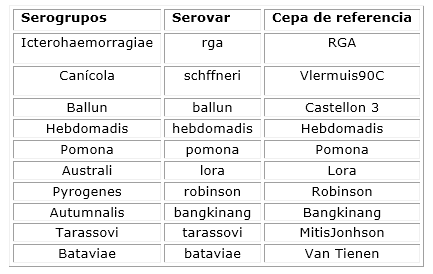
Las cepas poseían las características y condiciones idóneas. La dilución del producto se realizó a partir de 1:50 hasta 1:3200, considerando positiva una aglutinación de las leptospiras igual o superior al 50%. La otra técnica usada para determinar la presencia de anticuerpos antileptospirales de la clase IgG, fue el UMELISA. Para este sistema se empleó un Ag leptospiral obtenido en el Centro de Leptospirosis de la Facultad de Ciencias Médicas de Pinar del Río, que había sido avalado para este sistema por el IPK a propuesta de la Facultad en coordinación con el Laboratorio de Referencia de esta Institución. Para esta técnica la dilución base fue de 1:20. Diluciones sucesivas se hicieron hasta 1:160.
RESULTADOS
De los 13 lotes estudiados siete reaccionaron positivamente (códigos de los lotes positivos 03024, 01024, 01014, 04075, 01105, 09115 y el 02115). (Tabla 1)
Los hallazgos de reacciones serológicas importantes por la TMA se encontraron en cinco de los siete lotes positivos (01024, 01014, 01105, 02115, 03024) (Tabla 2 )
Hubo algunas reacciones similares entre el serogrupo Australis y el Icterohaemorrhagiae. Estas reacciones como las demás pueden encontrarse en cualquier lote ya que puede haber inmunoglobulinas para ambos o más serogrupos en el pull que contiene el lote.
DISCUSIÓN
En varias enfermedades el uso de concentrados de inmunoglobulinas (Intaglobin) ha resultado satisfactorio tanto por su actividad opsonofagocítica o directamente mediando en procesos alérgicos, autoinmunes o de otra naturaleza.2, 6-9
Respecto a la leptospirosis no existe precedente en cuanto a tratamiento con el Intaglobin, de suerte que el presente trabajo aborda por vez primera este tema en el país, a partir del estudio realizado y los hallazgos hechos acerca de la presencia de títulos de anticuerpos antileptospirales en varios lotes estudiados.
Aunque la coincidencia en la positividad por ambos métodos usados es del ciento por ciento, no equivale a decir que los niveles de anticuerpos o los títulos de las reacciones de todos los lotes, permitan un uso terapéutico o que todos los lotes puedan usarse en este sentido, pues hubo lotes con altos niveles de anticuerpos para unos serogrupos y no para otros.
La literatura plantea10-13 y en la práctica es así, la presencia de reacciones cruzadas entre varios serogrupos de leptospiras, por lo cual se requiere un proceso de enfrentamiento entre estos serogrupos de leptospiras en diluciones más elevadas para definir cual, ciertamente, es el serogrupo preponderante.
En este sentido lo que se hace es definir el título más elevado según el serogrupo y recomendar su uso específico para ese serogrupo. Un título importante y recomendable para el tratamiento es el de 1:200. El hecho es que un paciente puede presentar una infección por un serogrupo determinado y si el producto contiene títulos iguales para ese y otro serogrupo no hay interferencia terapéutica que impida su empleo para uno de ellos. Hamsters y gerbils vacunados contra la leptospirosis y retados con una carga infecciosa suficiente y cuyos títulos serológicos oscilaron desde 1:100 hasta 1:1600 se defendieron adecuadamente.
Los resultados registrados indican que se abre una nueva posibilidad terapéutica para la leptospirosis, por ello se recomienda que una terapia con este producto con un título de 1:200 como punto de partida es aplicable para tratar casos específicos de leptospirosis en humanos.
REFERENCIAS BIBLIOGRÁFICAS
1. Castillo Bellén J, Castellano Becerril ME, Cádiz Lahens. Capacidad opsonofagocítica de la inmunoglobulina endovenosa cubana (Intacglobín). Planta de Hemoderivados Ciudad de La Habana. MEDISAN 1999; 2: 18-23.
2. Arce Hernández AA, Marlín Linares JC, Villaescusa Blanco R, Padilla López M, González de Armas Y, Guerrero Hernández AM. Purificación de IgG1, IgG2 e IgG3 mediante cromatografía de afinidad a partir de intacglobín. Rev Cubana Hematol Inmunol Hemoter. 2001; 2: 138-141.
3. Zaldívar JM, Sosa J, García D. Miller Fisher. A propósito de un caso. Rev. Ciencias Médicas de Pinar del Rio[internet]. 2011[citado mayo 2015]; 12: 51-53. Disponible en: http://scielo.sld.cu/scielo.php?pid=S1561-31942011000200024&script=sci_arttext
4. Inoue M. Acute motor-sensory axonal Guillain Barré syndrome with unilateral facial nerve parálisis after rotavirus gastroenteritis in a 2 years old boy. J Infect Chemother. 2012; 1: 119-23.
5. Erazo Torricelli R. Guillain Barré syndrome in pediatrics. Medicina (B Aires)[ìnternet]. 2009[citado mayo 2015]; 1: 84-91. Disponible en: http://www.ncbi.nlm.nih.gov/pubmed/19240005
6. Bello M, Rodríguez L, Nazco M, Montalvo M. Evaluación serológica de la inmunización pasiva-activa en la profilaxis de la transmisión perinatal de la hepatitis B. Vaccimonitor. 2012; 2: 24-30.
7. Bencomo Hernández AA, Alfonso Valdés ME, Correa Palmero I, Macias Abraham C, Ávila Cabrera OM, Hernández Padrón C. Concentración de autoanticuerpos IgG en hematíes y respuesta al tratamiento en la anemia hemolítica autoinmune. Rev Cubana Hematol Inmunol Hemoter. 2013; 2: 173-182.
8. Silva Ballester HM, Bencomo Hernández AA, López Fernández R, Benet Rodríguez MM, Ballester Santovenia J. La hemovigilancia de las reacciones adversas a la donación de sangre. Rev Cubana Hematol Inmunol Hemoter. 2013; 2: 154-162.
9. Alfonso Valdés ME, Bencomo Hernández A. Tratamiento de las anemias hemolíticas autoinmunes Rev Cubana Hematol Inmunol Hemoter. Dic 2013; 4: 327-339.
10. Schereier S, Doungchawee G, Triampo D, Wangroongsarb P, Hartskeerl RA, Triampo W. Development of a magnetic bead fluorescence microscopy immunoassay to detect and quantify Leptospira in environmental water samples. Acta Trop. 2012; 1:119-25.
11. Pavan ME, Cairó F, Pettinari MJ, Samartino L, Brihuega B. Genotyping of Leptospira interrogans strains from Argentina by multiple-locus variable-number tandem repeat Analysis (MLVA). Comp Immunol Microbiol Infect Dis. 2011; 2: 135-41.
12. Moreno N, Agudelo-Flórez P. Application of conventional and multiplex PCR assays for identification of isolates of Leptospira spp. in Colombia. Rev Peru Med Exp Salud Pública. 2010; 4: 548-56.
13. Monte LG, Conceiçáo FR, Coutinho ML, Seixas FK, da Silva EF, Vasconcellos FA, et al. Monoclonal antibodies against the leptospiral immunoglobulin-like proteins A and B conserved regions. Comp Immunol Microbiol Infect Dis. 2011; 5: 441-6.
Recibido: 8 de marzo de 2015.
Aprobado: 9 de julio de 2015.
Dr. Juan Manuel Lemus Quintana. Especialista de Primer Grado Medicina Interna. Máster en longevidad satisfactoria. Hospital Provincial Clínico Quirúrgico "León Cuervo Rubio". Pinar del Río. Correo electrónico: clara@princesa.pri.sld.cu