INTRODUCCIÓN
La acuicultura registra un incremento en la productividad a nivel mundial; en la cual se manifiesta la contribución del pez gato africano, Clarias gariepinus, que reemplazó a la tilapia al ser el pez más cultivado desde el 2004 en África (FAO, 2012) y de marcada influencia en el rápido crecimiento del sector en Nigeria (Jimoh et al., 2021). Se considera uno de los peces gato tropicales más importantes en la acuicultura en Asia e incluso en Europa (Viveiros, So y Komen, 2000; Okoye et al., 2017) y actualmente se cultiva en sistemas modernos con recirculación de agua en Holanda (Fleuren, Nooijen y Roosendaal, 2013). En Cuba, ocupa el segundo lugar en las producciones dulceacuícolas, debido a su alta tasa de crecimiento, resistencia a condiciones ambientales y reproducción continua (De Graaf, Galemoni y Banzoussi, 1995).
El desove inducido implica sacrificar al macho para recolectar el semen de los testículos (Steyn y Van Vuren, 1987) lo que permite disponer de una cantidad de esperma limitada (Viveiros, So y Komen, 2000; Mansour, Lahnsteiner y Patzner, 2002). La colección seminal por masaje abdominal es casi imposible ya que la presión digital hará que el semen se mueva hacia la vesícula seminal y no a través del poro de la papila genital (De Graaf, Galemoni y Banzoussi, 1995; Viveiros et al., 2002). Se necesita disponer de semen con buena calidad para incrementar la eficiencia de la fertilización artificial en las especies piscícolas, para lo cual se requiere emplear reproductores machos con alta viabilidad espermática y alto volumen seminal (Solomon et al., 2015), pues se reconocen variaciones en la calidad del semen testicular entre machos (Mansour, Lahnsteiner y Berger, 2004). Por consiguiente, la determinación de los parámetros de calidad espermática del semen fresco es un prerrequisito para la evaluación satisfactoria de su capacidad reproductiva, puede ayudarnos a mejorar la reproducción artificial en granjas de peces (Alavi et al., 2009).
La capacidad del espermatozoide de fertilizar el ovocito es el principal factor que afecta las tasas de fertilización. Tal capacidad depende de parámetros cualitativos y cuantitativos tales como el volumen, la concentración, la motilidad, la viabilidad y la morfología espermática (Bustamante-González et al., 2016), de los cuales el volumen indica la eficiencia, y la concentración junto a la motilidad determinan la capacidad de fertilización del espermatozoide (Cabrita et al., 2014), debido a que las propiedades químicas del fluido seminal garantizan que los espermatozoides de los peces permanezcan inmóviles en dicho fluido (Coward, Campos y Parrington, 2008).
El objetivo de este trabajo fue caracterizar los cambios morfométricos y la calidad seminal en Clarias gariepinus durante las épocas pre-reproductiva y reproductiva.
MATERIALES Y MÉTODOS
Localización
Se trabajó con el banco de reproductores del pez gato africano Clarias gariepinus (Burchell 1822) de la Unidad de Desarrollo e Innovación (UDI) ¨El Dique¨, de la Empresa de Desarrollo de Tecnologías Acuícolas (EDTA).
Manejo de los reproductores
Los reproductores se mantuvieron en un estanque de concreto con circulación continua de agua y alimentación diaria con pienso comercial (36 % proteína bruta, PB y 2 964 Kcal/kg energía digestible, ED), al 1 % de la biomasa.
Diseño experimental y animales muestreados
Para el estudio se emplearon 42 reproductores machos seleccionados al azar, de 2 años de edad promedio, 23 en época pre-reproductiva y 19 en época reproductiva, con colecta de muestras de semen testicular (ST) y semen testicular más plasma seminal (ST-PS) en ambos períodos, como se describe en acápite ¨Colección del semen testicular y del plasma seminal¨.
Morfometría
Se evaluaron los indicadores morfométricos: peso vivo (PV, kg), largo total (LT, cm), peso de las gónadas (PG, g) y peso de las vesículas seminales (PVS, g). Para determinar el estado general de desarrollo del pez se utilizó el factor de condición (FC) de Fulton (1902), calculado mediante la fórmula:
PV
FC = ------ x 100
LT3
Se calculó el índice gonadosomático (IGS) (Ferrer, 1988) para determinar la madurez de las gónadas y el índice vesículas seminales-somático (IVS-S) (Viveiros, Eding y Komen, 2001) mediante las fórmulas:
PG PVS
IGS (%) = ----- x 100 e IVS-S (%) = ------- x 100
PV PV
El pesaje se realizó mediante dos balanzas digitales marca GRAM, con capacidades de 60 kg y 1 kg. Para medir el largo del pez se utilizó un ictiómetro.
Colección del semen testicular y del plasma seminal
La colección seminal se realizó en tubos aforados plásticos, inmediatamente después de sacrificados los animales, mediante disección del abdomen y extracción de los testículos (Elizarde et al., 2007). Para la colecta del semen testicular y del plasma seminal se realizaron múltiples cortes a los testículos y vesículas seminales con extensiones en formas de dedos, respectivamente. El material obtenido se filtró con malla de zooplancton (200 µm). Las muestras se conservaron a 4(C hasta su evaluación macro y microscópica dentro de 3 horas posteriores a la extracción.
Caracterización física del semen
Se caracterizaron las muestras en cuanto a: color, consistencia, volumen seminal testicular (VST, ml) y volumen del plasma seminal (VPS, ml). Se realizó la evaluación subjetiva de la motilidad (%) en la escala de 5 puntos de 0 a +4 propuesta por Ninhaus-Silveira et al. (2006), mezclando una gota de semen fresco con una gota de agua destilada, la cual se observó al microscopio usando lentes 10x y 40x. Posteriormente se evaluó el tiempo de activación espermática (TAE, sg) mezclando una gota de semen con agua común para la activación de la motilidad (López-Hernández et al., 2018). Se determinó la concentración espermática (CE, x109 sptz/ml) mediante una dilución 1:800 (0,01 ml de semen en 8 ml de solución salina al 3 %) realizando el conteo por duplicado en cámara de Neubauer con objetivo 40X, promediando las dos lecturas, según metodología tradicional utilizada para el recuento hematológico descrito por Oppenheim (1973). Por último, se determinó el valor del espermatocrito (SPCTO, %) mediante centrifugación de las muestras por duplicado durante 20 minutos a 3500 r.p.m. en centrífuga de microhematocrito marca Hawkley (Portales et al., 2021).
Análisis estadísticos
Los datos se analizaron obteniéndose los estadígrafos generales para las características morfométricas y físicas del semen y el plasma seminal. Se realizaron análisis de varianza con el modelo lineal general (GLM) para dichas características, considerando como fuente de variación la época de extracción de las muestras. A los datos de motilidad y espermatocrito se les halló el logaritmo natural para su transformación antes de su procesamiento. Se realizó un análisis de correlación de Pearson. Todos los análisis estadísticos se realizaron con MINITAB (2019).
RESULTADOS Y DISCUSIÓN
Indicadores morfométricos
Se encontraron diferencias significativas (p<0,05) en los indicadores PV, PG e IGS de los reproductores machos de Clarias gariepinus, a favor de la época reproductiva (Tabla 1).
Zacariah et al. (2016) también detectaron órganos reproductores más pequeños durante el período pre-reproductivo en esta especie mientras otros investigadores no encontraron diferencias en el peso de los testículos entre épocas en C. gariepinus silvestres (Idahor et al., 2014; Yusuf et al., 2015; Ali et al., 2022).
Aunque las diferencias estacionales no están bien definidas, se asocian con factores ambientales tales como: temperatura, disponibilidad del alimento, lluvias y fotoperiodo. Este pez muestra ciclo reproductivo discontinuo en su hábitat natural, influenciado por los cambios circadianos en la temperatura del agua y la fotoperiodicidad (Olaleye, 2005), con el incremento en el nivel del agua debido a las precipitaciones como mecanismo de activación para el desove. El peso corporal de los reproductores juega el mayor papel en el período de maduración espermática, y existe un amplio rango en el número de espermatozoides producidos, por lo cual se asocia el incremento en el peso testicular al mismo tiempo que el peso corporal, constituyendo un buen indicador de la eficiencia de la espermatogénesis (Bromage y Roberts, 1995; Jimoh et al., 2021) y de la cantidad de esperma producido (Billard, 1986; Ali et al., 2022).
Tabla 1 Rasgos morfométricos, índices somáticos y cambios en el aparato reproductor masculino entre épocas pre-reproductiva (N=23) y reproductiva (N=19).
| Rasgos | Época pre-reproductiva (febrero-marzo) | Época reproductiva (junio) | p | |||||
| M ± ES | DS | CV | M ± ES | DS | CV | |||
| PV (kg) | 2,14 ± 0,11 | 0,51 | 24 | 2,47 ± 0,10 | 0,45 | 18 | p<0,05 | |
| LT (cm) | 71,3 ± 1,90 | 9,09 | 13 | 73,05 ± 0,79 | 3,43 | 5 | ns | |
| PG (g) | 23,42 ± 2,58 | 12,37 | 53 | 34,74 ± 3,37 | 14,67 | 42 | p<0,05 | |
| PVS (g) | 13,73 ± 1,74 | 8,37 | 61 | 17,37 ± 1,85 | 8,06 | 46 | ns | |
| FC | 0,61 ± 0,04 | 0,17 | 28 | 0,64 ± 0,03 | 0,12 | 19 | ns | |
| IGS | 1,06 ± 0,08 | 0,37 | 35 | 1,41 ± 0,12 | 0,53 | 38 | p<0,05 | |
| IVS-S | 0,65 ± 0,08 | 0,36 | 56 | 0,70 ± 0,07 | 0,30 | 42 | ns | |
Leyenda: PV: peso vivo, LT: largo total, PG: peso de las gónadas (testículos), PVS: peso de vesículas seminales, FC: factor de condición de Fulton, IGS: índice gonadosomático, IVS-S: índice vesículas seminales-somático, p: nivel de significación, ns: diferencias estadísticamente no significativas.
En reproductores machos de Clarias gariepinus cultivados en Nigeria de peso corporal 2,54 ± 0,12 kg, Jimoh et al. (2021) encontraron un peso gonadal total e IGS en el rango de los hallados en el presente estudio (27,94 ± 8,17 g y 1,15 ± 0,38, respectivamente), aunque el factor de condición fue superior (0,84 ± 0,07). Los autores consideraron que el IGS y los rasgos reproductivos del macho explicarían la diferencia en el rendimiento reproductivo y la producción de semillas en cautiverio. Kumari (2014) demostró que existe una correlación positiva entre el peso testicular y la producción seminal; por lo cual el IGS se emplea para estimar el comportamiento reproductivo del pez. En ambas épocas este índice fue superior a 1; por lo que nuestros resultados contradicen los hallazgos de Urbányi et al. (1999), quienes refirieron que muchos silúridos incluyendo Clarias gariepinus son oligospérmicos (bajo recuento de espermatozoides) (IGS<1) y que el volumen colectado es generalmente bajo, aún con estimulación hormonal.
Por otra parte, el aumento de las VS no fue significativo y tampoco el IVS-S (0,70 ± 0,07 %), el cual se correlacionó positivamente con el IGS y con la actividad secretora testicular en la especie (Singh y Joy, 1999). El IVS-S fue superior a los referidos por Viveiros, Eding y Komen (2001) (0,29 ± 0,06 %) en machos con vesículas seminales bien desarrolladas con extensiones largas en forma de dedos a cada lado de los conductos espermáticos y tambien a los valores encontrados por Amer et al. (2005) (0,2 - 0,4 %).
Calidad seminal
Durante la extirpación de los testículos, se pudo apreciar su aspecto lobular, turgencia y color blanquecino (Figura 1A), asociados con los testículos tipo I o maduros (Mansour et al., 2004) productores de semen de excelente calidad; apariencia similar manifestaron las gónadas masculinas de C. gariepinus silvestres de un lago en Nigeria, durante la época de desove (Ali et al., 2022). Las glándulas genitales accesorias (vesículas seminales) presentaron múltiples lóbulos y produjeron una secreción altamente viscosa y rosada, en correspondencia con lo referido para la familia Clariidae (Van der Hurk, Resink y Peute, 1987; Singh y Joy, 1999).
Adicionalmente, se apreciaron testículos atrofiados, principalmente en la EPR (Figura 1B) y un caso patológico en ER (Figura 1C). Los testículos patológicos mostraron aumento de tamaño (60 g) y coloración grisácea, con un PVS de 30 g. El semen extraído mostró consistencia acuosa y transparencia, con un VST de 40 ml y VPS de 8 ml, superiores al promedio; con mala calidad (20 % de motilidad, CE de 2,4 x 109 sptz/ml y SPCTO de 2,4 %). A su vez, el perfil bioquímico del pez mostró valores altos de triglicéridos (36,28 mg/dL) y glucosa (13,69 mg/dL) en sangre, reflejando alteraciones metabólicas.
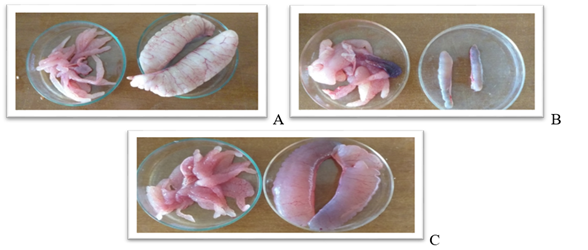
Fig 1 Testículos y vesículas seminales de reproductores de Clarias gariepinus: A. Testículos maduros tipo I, B. Testículos atrofiados y vesículas aumentadas de tamaño, C. Testículos asociados a mala calidad seminal (caso patológico).
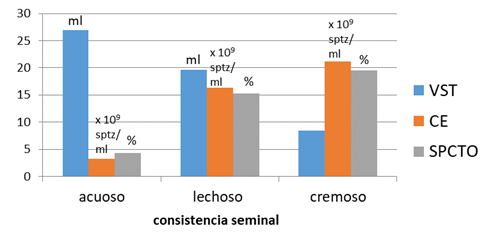
En general, el ST obtenido en ambas épocas mostró color blanco y consistencia lechosa, aunque se evidenciaron muestras con consistencia cremosa en EPR; coincidiendo con los parámetros observados en épocas de no desove y desove en C. gariepinus silvestres (Ali et al., 2022). El VST producido es elevado, consistente con los obtenidos en reproductores cultivados en Nigeria (17,69 ml); lo que indica que se requieren menos machos para fertilizar los huevos, debido a su abundante producción de semen (Jimoh et al., 2021).
Se observó una relación fisiológica entre la consistencia seminal y el VST, la CE y el SPCTO (Figura 2). El VST se redujo a medida que la consistencia cambió de acuosa a lechosa y cremosa. Se asoció un semen cremoso con la mayor densidad celular (21,14 ± 2,90 x 109/ml y 19,50 ± 1,24 % de SPCTO) en comparación con el semen acuoso (3,27 ± 0,87 x 109/ml y 4,30 ± 1,90 %).
Existen antecedentes que confirman la variación del espermatocrito y la viscosidad (consistencia) del semen entre machos, entre especies y a través de la época reproductiva (Rakitin, Ferguson y Trippel, 1999; Ali et al., 2022). En concordancia con estos autores, ésta especie puede producir gran número de semillas, así como es posible colectar semen de buena calidad en épocas de desove y no desove y emplear como criterio a priori la consistencia en la evaluación del semen durante las campañas de reproducción para descartar semen acuoso.
Esta especie, en ambientes naturales en Nigeria, mostró CE y VS inferiores (2,9 ± 0,4 y 2,6 ± 0,4 x 109/ml, 3,6 y 3,3 ml), en épocas de desove y no desove, respectivamente; relacionado con el menor peso de los reproductores (994,8 y 898,6 g) ya que peces con mayor peso produjeron los mayores volúmenes seminales (Ali et al., 2022). En general, existen variaciones en el número de espermatozoides entre especies de peces (2 x 106 a 5,3 x 1010), lo cual está relacionado con la estación reproductiva, el tratamiento hormonal, los porcentajes de fecundación, la disponibilidad y propiedades nutricionales del alimento y la calidad del agua (Murakami et al., 2014; López-Hernández et al., 2018).
En el presente estudio encontramos recuentos de espermatozoides superiores a los referidos por Viveiros, So y Komen (2000); Yusuf y Ilker (2017) y Okoye et al. (2017) e inferiores a los encontrados por Solomon et al. (2015) (35 - 97 × 109 sptz/ml), en éste último caso atribuidos al pico de la época de apareamiento. Ali et al. (2022) obtuvieron esperma también en época de no desove; incluso el semen lechoso obtenido tuvo una concentración media dentro del rango normal (1,8 - 7,2 x 109/ml), acorde lo referido por Viveiros, So y Komen (2000) y Yusuf y Ilker (2017) en el pez gato africano en Turquía. Esto se puede atribuir al hecho que los testículos de Clarias gariepinus macho están completamente desarrollados una vez que alcanzan aproximadamente los 200 g de peso (De Graaf y Janssen, 1996; Ali et al., 2022).
Por otra parte, no se encontraron diferencias en la motilidad, el SPCTO y el TAE entre ambos períodos, consistentes con semen de buena calidad. Los menores VST y VPS se obtuvieron en EPR, relacionados con una mayor CE (Tabla 2). El incremento del VS en ER se atribuye a la presencia de testículos maduros tipo I y al incremento en el PG y PVS. La actividad secretora de las VS de Clarias gariepinus es estimulada por la testosterona (Singh y Joy, 1997) y su apareamiento es estacional; el nivel de actividad testicular y espermatogénesis dependen mayormente del período de luz y la temperatura (Garg y Sundararaj, 1985).
Tabla 2. Comparación de las características físicas del semen y plasma seminal de los reproductores de Clarias gariepinus entre épocas.
| Características seminales | Época pre-reproductiva | Época reproductiva | p |
| M ± ES | M ± ES | ||
| VST (ml) | 11,10 ± 1,82 | 23,57 ± 2,25 | p<0,001 |
| VPS (ml) | 0,86 ± 0,28 | 1,93 ± 0,35 | p<0,05 |
| Motilidad (%) | 66,72 ± 6,17 | 79,74 ± 4,92 | ns |
| CE (x109 sptz/ml) | 19,08 ± 1,43 | 13,39 ± 1,60 | p<0,05 |
| SPCTO (%) | 16,9 ± 1,07 | 13,8 ± 1,21 | ns |
| TAE (sg) | 40,1 ± 2,54 | 35,6 ± 2,86 | ns |
Leyenda: VST: volumen de semen testicular, VPS: volumen de plasma seminal, CE: concentración espermática, SPCTO: espermatocrito, TAE: tiempo de activación espermática.
En Clarias gariepinus se identifican diferentes estadios de maduración gonadal, entre machos y también en el mismo testículo de un pez durante el desove natural. Esto afecta la consistencia, el volumen y la densidad espermática pero no la motilidad (Mansour et al., 2004). Este indicador no mostró diferencias significativas entre las dos épocas y se considera el mejor biomarcador de la calidad del semen, relacionado con la capacidad de fertilización (Oguntuase y Adebayo, 2014).
En contraste con otros indicadores, el TAE coincide con la duración de la motilidad espermática de 40 segundos referida por Mansour et al. (2004), la cual disminuyó alrededor del 50 % al transcurrir la mitad de ese tiempo; y concuerda con el tiempo referido en el bagre rayado Pseudoplatystoma metaense (39,5 segundos) por Ramírez-Merlano, Medina-Robles y Cruz-Casallas (2011). Su brevedad se asocia con el corto tiempo del que disponen los espermatozoides inmóviles para activarse al ponerse en contacto con el agua, mediante la adquisición de movilidad y velocidad de desplazamiento progresivo para lograr la fertilización, antes de que las ovas liberadas en el agua se hidraten y cierren su micrópilo; orificio del ovocito por el cual penetran los espermatozoides para la ocurrencia de la fecundación. Esto se debe a la ausencia de acrosoma en los espermatozoides de teleósteos, al contrario de los mamíferos (Quagio‐Grassiotto et al., 2001). Por tal razón, ambos gametos se liberan sincronizadamente al medio acuático, donde se activan y ocurre la fertilización (Dumorne et al., 2018).
Las características evaluadas permitieron constatar que C. gariepinus es un pez de espermiación continua, puede producir semen de alta calidad durante períodos en que las temperaturas y el fotoperiodo no son favorables para la reproducción de la hembra. Estos resultados sustentan la posibilidad de conservar semen en esta etapa puesto a que el desarrollo asincrónico de la espermatogénesis soporta la espermiación continua en C. gariepinus cultivados, una vez que pueden iniciar la producción de esperma a los 6 meses de edad, momento en que se identifican espermatozoides con capacidad para el movimiento progresivo unidireccional, indicando la madurez sexual del pez. Sin embargo, factores genéticos y condiciones de cultivo incluyendo la nutrición influyen en la edad de maduración de los peces cultivados (Okoye et al., 2016). Adicionalmente, los mayores IGS, volumen seminal, CE y SPCTO se encontraron en machos de 12 meses de edad, con mejora de la calidad seminal en peces mayores (Okoye et al., 2017), lo que justifica la elección de los reproductores en este momento.
Correlación entre características reproductivas y seminales.
En EPR se encontraron las mayores correlaciones entre rasgos morfométricos y seminales (Tabla 3).
Tabla 3. Relación entre el peso vivo del pez, peso de los testículos y vesículas seminales y algunos parámetros del semen de Clarias gariepinus en épocas pre-reproductiva y reproductiva.
| Parámetros | Época pre-reproductiva | Época reproductiva | ||
|---|---|---|---|---|
| Coeficiente de correlación de Pearson (r) | Valor de p | Coeficiente de correlación de Pearson (r) | Valor de p | |
| PV - PG | 0,73 | <0,0001 | 0,24 | 0,34 |
| PV -PVS | 0,32 | 0,13 | 0,40 | 0,09 |
| PV - VST | 0,71 | 0,0001 | 0,16 | 0,52 |
| PV - VPS | 0,12 | 0,64 | -0,21 | 0,58 |
| PG - PVS | 0,31 | 0,14 | 0,42 | 0,08 |
| PG - VST | 0,98 | < |
0,92 | <0,0001 |
| PG - VPS | 0,01 | 0,95 | 0,45 | 0,22 |
| PG - SPCTO | 0,10 | 0,64 | -0,31 | 0,21 |
| PG - CE | 0,55 | 0,0058 | -0,09 | 0,72 |
| PVS - VST | 0,36 | 0,09 | 0,32 | 0,20 |
| PVS - VPS | 0,86 | < |
0,22 | 0.56 |
| VST - SPCTO | 0,09 | 0,67 | -0,45 | 0,06 |
| VST - CE | 0,55 | 0,0057 | -0,15 | 0,55 |
| SPCTO - CE | 0,53 | 0,0073 | 0,33 | 0,18 |
Correlación es significativa para niveles de p<0,05
Hubo una correlación alta y significativa (p<0,001) entre PV y VST (r=0,71), PG y VST (r=0,98) y entre el PVS y VPS (r=0,86). Se detectó una correlación moderada y significativa (p<0,01) entre PG y CE (r=0,55), VST y CE (r=0,55) y entre SPCTO y CE (r=0,53). Nuestros hallazgos coinciden con los referidos por Yusuf et al. (2015), quienes encontraron correlaciones positivas pero superiores (r=0,72, p<0,05) del VS y PG con la CE en reproductores machos cultivados en Nigeria y similares entre el PG y VST (r=0,98, p<0,01).
En la ER se produjo un desarrollo aparejado de los testículos y las vesículas seminales, en respuesta a las condiciones ambientales favorables para la reproducción (incremento del PG, VST, VPS) y reducción de la CE. Sin embargo, solo mostró correlación significativa (r=0,92; p<0,0001) el PG con el VST y la asociación entre los indicadores de densidad espermática (CE y SPCTO) fue baja. La correlación (r=0,16, p>0,05) entre PV y VST en ER contrasta con los resultados de Ali et al. (2022) en la época de desove de C. gariepinus en ambientes naturales de Nigeria (r=0,36; p˂0,05). Asimismo, nuestros hallazgos difieren de éstos autores, quienes encontraron relaciones bajas y no significativas del peso de los testículos con el VS (r=0,20) y con la CE (r=0,28).
Los resultados obtenidos permiten utilizar al SPCTO como un indicador práctico de rápida medición para predecir la CE en peces solamente en EPR, en concordancia con Rakitin et al. (1999) y Portales et al. (2021). En otras especies de aguas frías se refieren correlaciones superiores (r=0,84), como en el pez del Himalaya Schizothoraichthys progastusis (Agarwal, Vandana y Raghuvanshi, 2013).
CONCLUSIONES
Se deben descartar los reproductores machos Clarias gariepinus con bajo índice gonadosomático y semen acuoso, por su baja densidad celular. Es posible predecir la concentración espermática a través de la determinación del espermatocrito y disponer de semen de buena calidad en época pre-reproductiva para implementar técnicas de conservación.