Introducción
EL agujero macular (AM) es un desorden de la interface vitreorretinal definido como un defecto de espesor completo desde la membrana limitante interna hasta los segmentos externos de los fotorreceptores que normalmente involucra a la fóvea.1) Es más frecuente después de los 55 años de edad, específicamente entre los 65 y 74 años, y entre el 10 y el 15 % desarrolla agujero macular en el ojo contralateral.2
Con el surgimiento y el desarrollo de la tomografía de coherencia óptica (ocular coherence tomography - OCT) se ha mejorado el entendimiento, el diagnóstico y el seguimiento de la enfermedades de la interface vitreorretinal.3,4,5
La clasificación internacional sobre la adhesión vitreomacular, la tracción y el agujero macular, publicada en el año 2013, basada en los datos obtenidos por tomografía de coherencia óptica (OCT), clasifica el agujero macular: en pequeño (< 250 µm), mediano (250-400 µm) o grande (> 400 µm), según su mínima apertura y si presenta o no tracción vítrea. Esta clasificación unifica criterios clínicamente aplicables; es fácil de recordar y permite profundizar en las enfermedades de la interface vitreorretinal, con lo que aporta nuevas perspectivas para el tratamiento quirúrgico de estas entidades.6
Kelly y Wendel fueron los primeros en iniciar y publicar la vitrectomía pars plana (VPP) como tratamiento para el agujero macular, quienes reportaron 52 casos en el año 1991, con una tasa de cierre del 58 %.7 Esta técnica quirúrgica ha sido en extremo beneficiada con el surgimiento y el desarrollo de la vitrectomía mínimamente invasiva (23G, 25G, 27G), el uso de la cromovitrectomía y el de pinzas endoculares. Hoy la VPP mínimamente invasiva se convierte en el gold estándar en la cirugía del agujero macular.
Una vitrectomía completa, el levantamiento de la hialoides posterior, el pelado de la membrana limitante interna (MLI), el uso de gases como tamponador y el posicionamiento del paciente son los pasos recomendados por la comunidad de cirujanos de vitreorretina ante un agujero macular con criterio quirúrgico.
Eckardt y otros, en el año 1997, describieron el pelado de la MLI y lograron una mayor tasa de éxito en el cierre del agujero.8,12) Con el continuo estudio de la interface vitreorretinal y el conocimiento sobre las células de Müller y su función como “cemento biológico”, Michalewska introdujo en el año 2010 el flap invertido de MLI (Inverted flap, IF ), una nueva opción para pelar dicha membrana, lo que favorece el cierre de agujeros maculares grandes.8,9) Sin embargo, la decisión de pelar o no pelar, cómo realizar la maculorexis y la recientemente introducida técnica del flap invertido de membrana limitante interna, siguen siendo controversiales y acaparan en buena medida las mesas de discusión de la cirugía macular en simposios nacionales e internacionales. Nuestro objetivo es determinar la ventaja del flap invertido de MLI en el agujero macular grande.
Presentación de caso
Paciente femenina, de 75 años de edad, hipertensa controlada, asidua lectora. Operada por facoemulsificación en ambos ojos. Presenta disminución de la visión central en el ojo derecho (OD) de 8 meses de evolución.
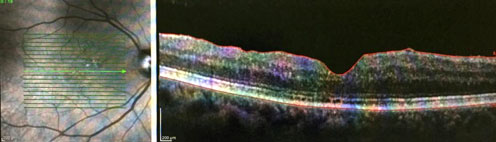
Examen Físico OD: Agudeza visual mejor corregida: 0,1 Snellen. Segmento anterior sin complicaciones, lente intraocular plegable en saco y centrado. Retina aplicada en la que se observa defecto redondo central en la fóvea con bordes de retina elevados, sin otras alteraciones en retina. Por OCT se corrobora agujero macular de espesor completo grande (810 µm) sin tracción vitreomacular a la fóvea o al disco (Fig. 1).
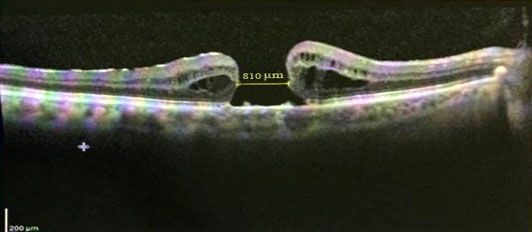
Fig. 1 Se corrobora agujero macular de espesor completo grande (810 µm) sin tracción vitreomacular a la fóvea o al disco.
Para el diagnóstico diferencial se descartaron entidades como el agujero macular lamelar, el pseudo agujero, el agujero macular asociado a la alta miopía o el agujero macular traumático. Se realizó vitrectomía pars plana central y periférica 23 G, levantamiento de la hialoides posterior, tinción de MLI con la realización de flap invertido de esta sobre el agujero. Intercambio fluido de aire, como tamponador de gas hexafluoruro de azufre (SF 6) en mezcla no expansible al 20 % en la cavidad vítrea. Posicionamiento del paciente mirando hacia abajo (face down position), principalmente las primeras 24 horas y alternando el segundo y el tercer día del posoperatorio. Tratamiento tópico con antibióticos y antinflamatorios durante 7 días poscirugía. Seguimiento a la semana, primer, tercer y sexto mes poscirugía.
Al mes de la cirugía, clínicamente y por OCT, se evidenció agujero macular cerrado y se observó una reposición o una nueva formación de las capas internas y externas de la retina a nivel de la fóvea, aunque todavía de forma discontinua y desorganizada (Fig. 2).
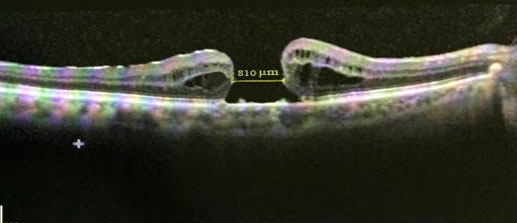
Fig. 2 Se evidencia agujero macular cerrado, y se observa una reposición o nueva formación de las capas internas y externas de la retina a nivel de la fóvea, aunque todavía de forma discontinua y desorganizada.
A los 6 meses de evolución hubo una ganancia en la agudeza visual mayor a 4 líneas, con agudeza visual mejor corregida de 0,6 Snellen; se evidencia por tomografía de coherencia óptica la integridad de la membrana limitante externa y de los segmentos internos y externos de los fotorreceptores (Fig. 3).
Discusión
En las últimas décadas, la necesidad de pelar la membrana limitante interna; por qué; cuándo y cómo realizar el pelado de esta membrana fina, pero extremadamente fuerte, y cómo usar de manera eficiente esta maniobra en la cirugía del agujero macular, es un importante punto de debate en la comunidad de cirujanos de vitreorretina.
La membrana limitante interna es la membrana basal de las células de Müller; está formada principalmente por colágeno tipo IV, asociado con glicoproteínas; colágeno tipo VI, que contribuye a la adhesión vitreorretiniana, y colágeno tipo XVIII, que une a la opticina.
La MLI, junto con el córtex vítreo, forman la interface vitreorretinal. Entre estas dos estructuras existe una matriz extracelular que funciona como un cemento biológico, constituida por moléculas de adhesión, como la fibronectina y la laminina, y proteoglicanos que interactúan con la opticina del gel vítreo.8,9)
Una relación anómala entre la hialoides posterior y la MLI a nivel de la fóvea puede ocasionar un agujero macular de espesor completo, como define la clasificación internacional sobre la adhesión vitreomacular, la tracción y el agujero macular, publicada en el año 2013.6
El pelado de la membrana limitante interna en la cirugía del agujero macular aumenta la tasa de cierre. Esta técnica, descrita por Eckardt y otros en el año 1997, consiste en pelar de forma circular la MLI, construir una maculorexis en 360° (técnica convencional) y preservar la capa de fibras nerviosas.
Varios estudios observacionales han sugerido un beneficio potencial en el cierre del agujero macular cuando se realiza un pelado de MLI y se logra un cierre anatómico del agujero entre el 90-98 %.1,2,8,9,10,11
Michalewska y otros introducen y describen una nueva técnica quirúrgica con el término flap invertido ( inverted flap, IF) de MLI para agujeros maculares grandes (> 400 micras); los cuales, cuando se realizaba una maculorexis convencional, tenían una baja tasa de cierre. Con la técnica de flap invertido propuesta por Michalewska se atribuye el éxito de cierre a que, sin separar de los bordes del agujero la MLI e invirtiendo esta sobre el opérculo, se induce gliosis dentro del propio agujero.8,9,10
Rossi y otros publicaron también recientemente variantes o modalidades para la técnica de flap invertido, y encontraron similares tasas de cierres con el llenado o la cobertura del agujero macular por la membrana limitante interna.9
Rizzo y otros estudiaron 620 ojos con agujero macular, y compararon el pelado convencional de la MLI (maculorexis en 360°) versus flap invertido. Encontraron que para los agujeros maculares grandes mayores de 400 micras, los asociados a la longitud axial mayor de 26,5 mm y el asociado a desprendimiento de retina en el miope, el flap invertido resultó ser más efectivo que el pelado convencional.10
Sborgia encontró el 98 % de éxito en el cierre anatómico de agujeros maculares grandes a los que les realizó flap invertido de membrana limitante interna. Observó por tomografía de coherencia óptica (OCT) la recuperación y la integridad de la membrana limitante externa y un reordenamiento de los fotorreceptores alrededor de la fóvea, así como la mejoría visual de los pacientes.11
En nuestra paciente con agujero macular grande (810 µm) de 8 meses de evolución, se decidió realizar vitrectomía pars plana lo más completa posible, levantar la hialoides posterior y realizar flap invertido de membrana limitante interna. Se utilizó SF6 en mezcla no expansible al 20 % y el posicionamiento del paciente (face down position) las primeras 24 horas, alternando el segundo y el tercer día del posoperatorio.
Basándonos en los conocimientos actuales y en las ventajas que ofrece el flap invertido, donde la MLI es el sustento para la proliferación tisular, su propio pelado contiene fragmentos de células de Müller, lo que produce proliferación celular y gliosis dentro del propio agujero. Esto favorece el medio para que los fotorreceptores se reposicionen próximos a la fóvea.12,13,14,15,16 En nuestro caso, se obtuvo el cierre del agujero, la recuperación anatómica de la fóvea y una mejoría mayor a 4 líneas Snellen en la agudeza visual de nuestra paciente, lo cual permitió su reincorporación a las actividades habituales.
El flap invertido de la membrana limitante interna está indicado y constituye una mejor opción de tratamiento en AM idiopáticos grandes, con más de 6 meses de evolución; AM asociados a la alta miopía con o sin desprendimiento de retina; y AM recidivados. Representa una nueva opción de tratamiento que no sustituye la maculorexis convencional, sino que amplía las posibilidades quirúrgicas y de éxito en el cierre anatómico del AM; previene la reapertura o el fallo en el cierre del AM y mejora los resultados funcionales y visuales de la vitrectomía en agujeros maculares grandes. Según la OCT, con el Flap invertido se observa mayor recuperación en la anatomía de la fóvea que con el pelado convencional de la membrana limitante interna.
Esta nueva técnica quirúrgica (flap invertido de membrana limitante interna) amplía y/o modifica los protocolos de tratamientos hasta el momento establecido, y ofrece nuevas posibilidades de recuperación visual a nuestros pacientes.