Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Cirugía
versión On-line ISSN 1561-2945
Rev Cubana Cir v.43 n.2 Ciudad de la Habana abr.-jun. 2004
Hospital Clinicoquirúrgico "Hermanos Ameijeiras"
Mioplastia en el tratamiento de fistulas broncopleurales
Dr. Edelberto Fuentes Valdés,1 Dr. Sixto B. Corona Mancebo,2 Dr. Albio R. Ferrá Betancourt3 y Dr. Miguel A. Martín González4
Resumen
Las fístulas broncopleurales posoperatorias asociadas o no a empiema constituyen una fuente importante de morbimortalidad en pacientes que han sufrido resecciones pulmonares, principalmente cuando se tratan enfermedades malignas. El objetivo de este artículo es revisar los resultados obtenidos en el tratamiento de 6 pacientes tratados entre 1997 y 2003. La operación previa fue neumonectomía derecha en 5 pacientes y lobectomía superior derecha en uno. Las causas de la operación fueron traumatismo, tumores benignos y malignos y tuberculosis. En los 6 pacientes se utilizó mioplastia con el dorsal ancho para la obliteración de la cavidad pleural remanente. Las técnicas complementarias comprendieron el uso de colgajos pediculados de músculo intercostal (3 pacientes), mioplastia con el músculo pectoral mayor y toracoplastia parcial en un paciente cada una. La complicación más frecuente fue la fuga aérea mantenida por más de 10 días. Todos los pacientes mantenían el cierre bronquial al año de la operación.
Palabras clave: Mioplastia, fístula broncopleural.
Las fístulas broncopleurocutáneas (FBPC) posoperatorias asociadas o no a empiema constituyen una fuente importante de morbimortalidad en pacientes que han sufrido resecciones pulmonares, principalmente cuando se tratan enfermedades malignas.1 Su incidencia fluctúa entre el 1,6 % y 6,2 %.2,3 Entre los factores de riesgo de aparición se encuentran las resecciones pulmonares amplias (neumonectomia), enfermedad maligna residual en el muñón bronquial, irradiación preoperatoria y diabetes mellitus. El 46 % ocurre en pacientes neumonectomizados y el 75 % en el lado derecho.3 La disección ganglionar mediastinal al producir desvascularización bronquial puede favorecer la dehiscencia bronquial y la subsecuente formación de una fístula. Constituye además una complicación tardía y grave de los procederes broncoplásticos, en los que suele ocurrir 3 a 4 semanas tras la operación y se reconoce como causa fundamental el fallo técnico.
El diagnóstico se sospechará en pacientes que en el periodo posoperatorio presenten expectoración copiosa de líquido serosanguinolento en los primeros días o de material séptico si ocurre tardíamente. Asimismo se tendrá en cuenta el diagnóstico cuando aparece un nivel hidroaéreo que aumenta de tamaño o cuando asociado a la expectoración el nivel aumenta su tamaño. La desviación del mediastino hacia el lado no operado es otro signo radiológico de esta complicación.
En todos los casos el manejo incluye control de la ventilación, evacuación del contenido de la cavidad pleural mediante pleurotomía, uso de antibióticos y apoyo nutricional .4,5
Un porcentaje importante de pacientes logra la cicatrización de la fístula con tratamiento conservador y técnicas endoscópicas, como inyección de cola biológica, tisuacril, n-butyl-2-cianoacrilato (histoacryl) 6 inyección de sustancias esclerosantes en los bordes del orificio7 y por supuesto la aseptización de la cavidad, pero en otros, es necesaria la cirugía correctora para alcanzar la solución del problema.
Las técnicas quirúrgicas utilizadas comprenden la resección del muñón a través del mediastino para evitar la zona séptica en la cavidad pleural, la sutura del bronquio y el relleno de la cavidad ya sea con músculos, epiplón o con su obliteración mediante una toracoplastia.8-10 Cuando el tratamiento quirúrgico es apropiado y no hay recidiva tumoral, los resultados suelen ser satisfactorios con éxito entre el 70 % y el 90 %.11
En este estudio se realizó la revisión de los resultados obtenidos con la utilización de mioplastias para obtener la cicatrización de la fístula.
MÉTODOS
Entre 1997 y 2003 se realizó mioplastia con el dorsal ancho (MDA) en 6 casos portadores de FBPC posoperatorias. El diagnóstico se hizo presuntivo por el cuadro clínico. La broncoscopía realizada a todos los pacientes demostró la presencia de la fístula y fue una herramienta importante en el control posoperatorio para evaluar el estado del muñón bronquial. También fueron utilizados en la evaluación preoperatoria, la radiografía simple del tórax, la TAC y los estudios radiográficos contrastados.
Cuadro clínico
El cuadro clínico se caracteriza por la expectoración de cantidades crecientes de líquido serohemático, cuando la fístula aparece en los primeros días del posoperatorio o de contenido purulento cuando se asocia a empiema. Puede haber en este último caso fiebre y toma del estado general. La disnea puede ser causada por la desviación mediastinal, por aspiración del líquido hacia el pulmón sano o por compresión traqueal por el empiema.
Exámenes de diagnóstico
La radiografía simple del tórax póstero-lateral puede sugerir el diagnóstico al demostrar la aparición de un nivel hidroaéreo o su aumento concomitando con la expectoración de líquido. Entre otros signos se encuentran: no se produce la desviación del mediastino hacia el lado operado o cuando esta se ha producido regresa a su posición normal o incluso se desplaza hacia el hemitórax no operado. Puede aparecer un moteado difuso del pulmón remanente secundario a broncoaspiración.
También se han utilizado la fistulografía a través del orificio cutáneo o inyectando el contraste por el tubo de pleurotomía y la inyección de azul de metileno en la cavidad pleural para determinar si el esputo se tiñe con el colorante. La TAC puede ser útil en la demostración de recidiva tumoral.
Por último la broncoscopía es de importancia capital, ya que demuestra el orificio fistuloso y sus características.
Fisiopatología
La fístula temprana (primera semana) se debe a fallo técnico en la sutura del muñón o del parénquima pulmonar. La intermedia (entre 8 y 10 días) se ocurre por el fallo de la cicatrización, como es el caso de cambios patológicos persistentes de la pared bronquial o cicatrización pobre en pacientes que recibieron radioterapia previa. Por último, la fístula tardía (más de 10 días) suele asociarse a empiema, que evita la cicatrización e incluso puede llevar a la ruptura del bronquio.
Preparación preoperatoria
El primer paso es la evacuación del líquido mediante pleurotomía por sonda, para evitar la inundación del pulmón remanente. Esta acción a su vez constituye una medida clave para tratar el empiema cuando existe. Se utilizarán los antibióticos adecuados (amplio espectro) y se atenderá el estado nutricional, pues pacientes con deficiencias nutricionales suelen evolucionar mal, con índices elevados de morbilidad y mortalidad. En todos los casos se practicó drenaje abierto (técnica de Clagett ) después de un mínimo de 2 semanas con sonda, así se asegura que el mediastino esté fijo. Este proceder garantiza la aseptización de la cavidad y en ocasiones se logra el cierre de la fístula y de la cavidad del empiema.
TÉcnica para la disecciÓn del mÚsculo dorsal ancho
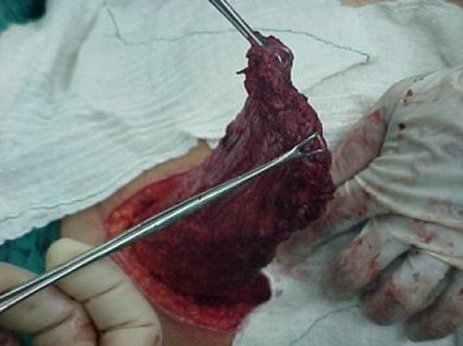
Se practica incisión que partiendo de la axila sigue el recorrido del borde anterior del músculo dorsal ancho.12 Se tendrá mucho cuidado en no lesionar el pedículo vásculonervioso a nivel axilar. Una vez separados piel y tejido celular subcutáneo del músculo, se procede a la sección de sus inserciones posteriores e inferiores como se muestra en la figura 1.
Fig. 1. Músculo dorsal ancho liberado de sus insersiones inferiores y posteriores.
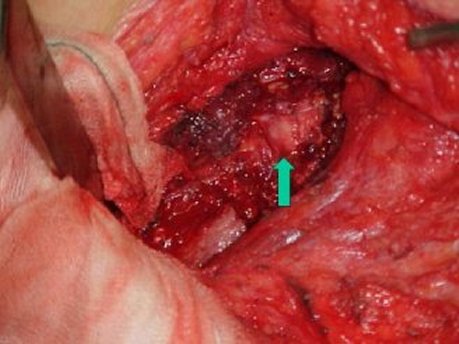
La hemostasia debe ser cuidadosa. En este momento es posible la trasposición del músculo al interior del tórax a través de un espacio intercostal previamente seleccionado para que el recorrido sea mínimo, según la figura 2. Se prefirió resecar al menos un arco costal, para evitar la compresión del músculo con la consiguiente isquemia y necrosis y se fijó el músculo a los bordes pleurales para evitar su retracción.
Fig. 2 . La flecha señala el músculo dorsal ancho rellenando la cavidad pleural residual
Todos los pacientes fueron seguidos en consulta externa un mínimo de un año, mediante evaluación clínica, estudios radiográficos y broncoscopía.
RESULTADOS
Características generales de la muestra:
- Sexo: masculino 5 y femenino 1.
- Edad: entre 30 y 64 años.
- Causas de operación primaria: traumatismo 2, neoplasia pulmonar 2, lesión inflamatoria crónica 1 y tuberculosis 1.
- Operación previa: neumonectomía 5 y lobectomía 1.
- Técnica quirúrgica empleada: mioplastia dorsal ancho 6
- Técnica quirúrgica asociada: mioplastia con músculo intercostal
- Complicaciones posoperatorias: fuga aérea mantenida 3 y sepsis local 2.
Las causas de operación fueron traumatismo 2 pacientes, neoplasia del pulmón 2 (adenocarcinoma y tumor carcinoide), lesión inflamatoria pulmonar crónica uno y tuberculosis pulmonar uno. En 5 enfermos la operación previa fue neumonectomía derecha y en el restante lobectomía superior derecha por tuberculosis. En 5 pacientes se practicó una ventana plerurocutánea. En los 6 pacientes se empleó el músculo dorsal ancho para rellenar la cavidad, en 3 se añadió un colgajo pediculado vascularizado de músculo intercostal que se utilizó en el cierre directo del muñón bronquial y en uno fue necesario utilizar además del dorsal ancho, el pectoral mayor para ocupar completamente la cavidad pleural residual y en otro se realizó la resección de 4 arcos costales. La fuga aérea mantenida por más de 10 días fue la complicación más frecuente (3 casos), seguida de sepsis local. Todos fueron evaluados en consulta externa hasta un año y en ninguno se produjo recidiva de la fístula.
Comentarios
Los objetivos del tratamiento de la FBPC son:1) esterilización del espacio pleural, 2) cierre de la fístula y 3) obliteración de la cavidad pleural remanente, los que se alcanzan mediante una serie de técnicas estandarizadas. La fístula que ocurre en la primera semana no es frecuente que se asocie a sepsis local por lo que se aconseja toracotomía inmediata, cierre del muñón bronquial y refuerzo con un pedículo vascularizado de músculo intercostal, pericardio o epiplón además de desbridamiento de la cavidad pleural.11 La que aparece más allá del décimo día suele concomitar con un empiema por lo que no se recomienda la toracotomía para cierre inmediato del muñón bronquial.
En el primer momento se colocará un tubo de pleurotomía y se indicarán antibióticos por 5 a 7 días. Muchos de tales enfermos requerirán de drenaje torácico abierto, sobre todo si se ha realizado previamente una neumonectomía.11 En estos casos la ventana pleurocutánea no se realizará antes de 2 a 3 semanas para que se produzca la fijación del mediastino. Esta técnica permite una mejor evacuación del pus y los esfacelos, requisito importante para lograr la mejoría del estado general del paciente antes de ser sometido a una reintervención con el fin de tratar directamente la fístula.
Cuando la fístula es amplia y dificulta la ventilación, se controlará con un bloqueador bronquial, con un catéter dotado de balón o con un tubo endotraqueal en el bronquio contralateral.11 Si la fístula se produce tras una lobectomía, el drenaje con tubo suele ser suficiente, pero en casos de neumonectomía es mejor el drenaje abierto (ventana pleurocutánea). Hasta el 30 % de las fístulas cierran con este método.13 El único de los pacientes a quien no se realizó la ventana pleurocutánea fue el que había sufrido una lobectomía superior derecha por tuberculosis. En los casos en que la fístula no cierra el tratamiento consistirá es la realización de una toracoplastia o reamputación transesternal del muñón bronquial.14 Esta última técnica tiene la ventaja de tratar la fístula en el mediastino donde no existe contaminación por la sepsis, pero resulta técnicamente compleja por la disección de los grandes vasos torácicos.
Meyer et al.15 intervinieron 13 pacientes con defectos de la vía respiratoria intratorácica de más del 50 % de la circunferencia, entre ellos 5 eran portadores de fístula broncopleural (FBP). Utilizaron los músculos dorsal ancho y serrato anterior y los resultados fueron satisfactorios en todos los casos.
Aunque el uso de colgajos miocutáneos o musculares pediculados no está exento de complicaciones, es un método efectivo y confiable para el manejo de pacientes con lesiones cardiotorácicas complicadas, entre las que incluyen empiema y FBP.16 En ocasiones la fístula puede presentar recidiva por atrofia del músculo traslocado y el consecuente fallo en llenar la cavidad pleural residual.17
En todos los casos se utilizó MDA, que se complementó con el cierre del muñón, suturando un pedículo vascularizado de músculo intercostal en 3 pacientes, en uno de estos también se utilizó el músculo pectoral mayor pues no se alcanzó a rellenar toda la cavidad con el dorsal ancho y en otro fue necesario además realizar la resección del segundo al quinto arcos intercostales.
No hubo mortalidad y las complicaciones se limitaron a sepsis local ligera en 2 casos y salida mantenida de aire por más de 10 días en 3 pacientes, los que alcanzaron el cierre de la fístula al mantener un catéter en cavidad para evitar acumulación de líquido y facilitar la evacuación del aire. En 2 casos la sonda de drenaje torácico posoperatorio se mantuvo por más de 30 días, mientras existió drenaje de líquido purulento y/o de aire.
Pairolero et al.18 abogaron por la transposición de músculos extratorácicos hacia el interior de la cavidad pleural en pacientes con empiema acompañado de FBP. Lograron la curación de la fístula en 24 de 28 pacientes a quienes previamente habían realizado drenaje abierto de la cavidad pleural.
Minniti et al.19 reportaron 29 pacientes a quienes realizaron toracoplastia para el tratamiento de empiema crónico y fístula broncopleural. Veintisiete pacientes alcanzaron la curación del empiema y el cierre de la fístula, pero tuvieron mortalidad de 6,8 %.
La toracoplastia es muy deformante y está sujeta a complicaciones graves18,19 por lo que se prefiere la mioplastia que en estos casos ha tenido buenos resultados, con poca morbilidad y la deformidad es mucho menor.
MYOPLASTY IN THE TREATMENT OF BRONCHOPLEURAL FISTULAS
The postoperative bronchopleural fistulas associated or not with empyema are an important source of morbimortality in patients that have suffered from pulmonary resections, mainly when malignant diseases are treated. The purpose of this article is to review the results obtained in the treatment of six patients from 1997 to 2003. The previous operation was right pneumonectomy in five patients and upper right lobectomy in one. The causes of the operation were traumatism, benign and malignant tumors and tuberculosis. In the six patients, it was used myoplasty with the wide dorsal for the obliteration of the remaining pleural cavity. The complementary techniques comprised the use of pedicled flaps of intercostal muscle (3 patients), myoplasty with the pectoralis major and partial thoracoplasty in a patient, each one. The most frequent complication was the aerial leakage maintained for more than ten days. All the patients kept the bronchial closure a year after the operation.
Key words: Myoplasty; bronchopleural fistula.
Referencias bibliográficas
1.Deslauriers J, Ginsberg RJ, Dubois P, Beaulieu M, Goldberg M, Piraux M. Current operative morbidity with elective surgical resection for lung cancer. Can J Surg 1989;32:335-9.
2. Vester SR, Faber LP, Kittle F, Warren WH, Jensik RJ. Bronchopleural fistula after stapled closure of bronchus. Ann Thorac Surg 1991;52(6):1253-7
3. Asamura H, Naruke T, Tsuchiya R, Goya T, Kondo H, Suemasu K. Bronchopleural fistulas associated with lung operation. Univariate and multivariate analysis of risk factors, management and outcome. J Thorac Cardiovasc Surg 1992;104(5):1456-64.
4. Eerola S, Vikkula L, Varstela C. Treatment of post-pneumonectomy empyema and associated bronchopleural fistula. Scand J Thorac Cardiovasc Surg 1988;22(3):235-9.
5. Pairolero P, Deschamps C, Allens MS, Trastek MS. Postoperatirve empyema. Chest Surg Clin North Am 1992;2:813-7.
6. Hirata T, Ogawa E, Takenaka K, Uwokawa R, Fujisawa I. Endobronchial closure of postoperative bronchopleural fistula using vascular occluding coils and n-butyl-2-cyanoacrylate. Ann Thorac Surg 2002;74(6):2174-6.
7. Takaoka K, Inoue S, Ohira S. Central bronchopleural fistulas closed by bronchoscopic injection of absolute ethanol. Chest 2002;122(1):374-8.
8. Koch H, Tomaselli F, Pierer G, Schwarzl F, Haas F, Smolle-Juttner FM, et al. Thoracic wall reconstruction using both portions of the latissimus dorsi previously divided in the course of posterolateral thoracotomy.Eur J Cardiothorac Surg 2002 ;21(5):874-8.
9. Kanno R, Suzuki H, Fujiu K, Ohishi A, Gotoh M. Endoscopic closure of bronchopleural fistula after pneumonectomy by submucosal injection of polidocanol. Jpn J Thorac Cardiovasc Surg 2002 Jan;50(1):30-3.
10. Refaely Y, Paley M, Simansky DA, Rozenman Y, Yellin A. Transsternal transpericardial closure of a postlobectomy bronchopleural fistula. Ann Thorac Surg 2002;73(2):635-6
11. Deslauriers J, Ferraro P. Late complications. En: Pearson FG, Deslauriers J, Ginsberg RJ, Hiebert CA, McKneally MF, Urschel HC Jr, eds: Thoracic Surgery. New York Churchill Livigstone;1995.p. 763-82.
12. Quevedo Guanche L, Cruañas Sospedra C, Rubinos Ruiz R, González Fierro G, Cairo Báez J, Navarro González A, et al. Injertos libres vascularizados con microcirugía. Rev Cubana Cir 1986;25(5):519-28.
13. Shamji FM, Ginsberg RJ, Cooper JD, Spratt EH, Goldberg M, Waters PF, et al. Open window thoracostomy in the management of postpneumonectomy empyema with or without bronchopleural fistula. J Thoroac Cardiovasc Surg 1983;68:618-22.
14. Gregoire R, Deslauriers J, Beaulieu M, Piraux M. Thoracoplasty: its forgotten role in the management of nontuberculous post pneumonectomy empyema. Can J Surg 1987;30:343-5.
15. Meyer AJ, Krueger T, Lepori D, Dusmet M, Aubert JD, Pasche P, et al. Closure of large intrathoracic airway defects using extrathoracic muscle flaps. Ann Thorac Surg 2004;77(2):397-404.
16. Dosios T, Papadopoulos O, Mantas D, Georgiou P, Asimacopoulos P. Pedicled myocutaneous and muscle flaps in the management of complicated cardiothoracic problems. Scand J Plast Reconstr Surg Hand Surg. 2003;37(4):220-4.
17. Watanabe N, Kanagawa T, Maeta K, Ohishi M, Kodera M, Yamashita Y.A new technique for muscle flap closure of the empyema space in complicated chronic bronchopleural fistula. Wedging the causative bronchus with a plug.Jpn J Thorac Cardiovasc Surg 2002;50(11):466-71.
18. Pairolero PC, Arnold PG, Trastek VF, Meland NB, Kay PP. Postpneumonectomy empyema. The role of intrathoracic muscle transposition. J Thorac Cardiovasc Surg 1990;99:958-68.
19. Minniti A, Dubrez J, Jougon J, Vona A, Cruz J, Velly JF. Thoracoplasty: the current role. G Chir 2002;23(4):121-4.
Recibido: 10 de agosto de 2004. Aprobado: 11 de octubre de 2004.
Dr. Edelberto Fuentes Valdés. Hospital Clinicoquirúrgico Hermanos Ameijeiras. San Lázaro No. 701. Centro Habana, Ciudad de La Habana, Cuba.
1Especialista de II Grado en Cirugía. Profesor Auxiliar.
2Especialista de II Grado en Cirugía. Profesor Titular y Consultante de Cirugía General.
3Especialista de II Grado en Cirugía. Profesor Auxiliar.
4Especialista de I Grado en Cirugía.