INTRODUCCIÓN
Las fistulas aerodigestivas se definen como comunicaciones anómalas entre los sistemas digestivo y respiratorio.1) Las fístulas traqueoesofágicas (FTEs) postintubación son lesiones graves que presentan alta frecuencia de complicaciones y mortalidad.2,3) La patogenia se relaciona con la insuflación, a presiones mayores de 30 mm Hg, del manguito del tubo endotraqueal (TET), que comprime la tráquea membranosa y la pared anterior del esófago contra la sonda nasogástrica, con la consiguiente isquemia, necrosis y formación de la fístula. En la mayoría de estos enfermos hay lesión estenótica circunferencial de la tráquea.
Aunque la incidencia disminuyó tras el uso de manguitos de alto volumen y baja presión, los pacientes tratados en unidades de cuidados intensivos continúan padeciendo esta grave complicación.4
Hace algunos años el autor publicó, conjuntamente con el profesor Sixto B Corona Mancebo, su experiencia inicial.5Posteriormente, se añadieron otros enfermos (no publicados). El tratamiento quirúrgico es la mejor opción actual, pero las técnicas varían.6
El objetivo del autor es actualizar los cuidados de pacientes con FTEs, porque la práctica de métodos y técnicas erróneas pueden entorpecer el tratamiento definitivo o producir resultados fatales.
MÉTODOS
Se revisó la literatura disponible sobre el diagnóstico y tratamiento de las FTEs postintubación, con la última fecha el 15 de mayo de 2018, en PUBMED e Infomed, con los vocablos y frases fístula, traqueoesofágica, fístula traqueoesofágica postintubación y las correspondientes en inglés. Los artículos seleccionados debían cumplir los siguientes requisitos: ensayo clínico aleatorizado, metanálisis, revisiones sistemáticas o tener más de 5 pacientes y que trataran la patogenia, los métodos de diagnóstico, la indicación del tratamiento quirúrgico y los resultados. No encontramos ensayos clínicos, metanálisis ni revisiones sistemáticas. Se revisaron las referencias bibliográficas de los artículos seleccionados en busca de publicaciones relevantes. Los informes de casos sólo se tomaron en cuenta cuando hacían referencia a técnicas novedosas.
DESARROLLO
La FTE traumática es una lesión poco frecuente, pero con potencial de una seria amenaza para la vida. El diagnóstico temprano y los cuidados perioperatorios son esenciales para obtener resultados positivos. La incidencia de esta complicación fluctúa entre 0,3 % y 0,76 %.7
La causaprincipal es el uso prolongado del TET con el manguito insuflado a presiones superiores a la presión capilar de la mucosa traqueal,2,4,8) además de la traqueostomía.9
Patogenia
En 1976, Grillo y otros10 hicieron una contribución fundamental al campo en desarrollo de la cirugía de la FTE, cuando reconocieron que tanto el esófago como la tráquea lesionada necesitaban ser reparados. Observaron que la compresión de la pared membranosa y la pared esofágica anterior, entre un manguito insuflable de alta presión y la sonda nasogástrica, era el componente crítico en el desarrollo de la fístula y presentaron un procedimiento simple, en un tiempo, para su tratamiento.
El daño mucoso, a nivel del manguito del TET, acompañado de inflamación y ulceraciones mucosas (en 3 a 5 días), rápidamente afecta la mayoría del área entre el manguito y los anillos traqueales. Finalmente, ocurre profundización de las úlceras y, como resultado, más cartílagos quedan expuestos. La infección contribuye a la destrucción traqueal adicional. Con la extubación, se produce una cicatriz circunferencial del segmento traqueal lesionado y estenosis. La exposición continuada a presiones altas, produce ablandamiento y fragmentación de los cartílagos y, en consecuencia, destrucción del sostén cartilaginoso, de manera que además de la formación de la cicatriz fibrosa y la obstrucción se puede producir una traqueomalacia. La afectación de mayor gravedad, con erosión de todo el espesor de la pared traqueal, produce una fístula traqueoinnominada o traqueoesofágica. Si la fístula se localiza anivel del estoma, el mecanismo patogénico podría ser lesión directa durante la traqueostomía.4
Factores de riesgo
Entre ellos se citan: la presión en la vía respiratoria (VR) durante la ventilación mecánica, movilidad excesiva del TET, intubación prolongada, tratamiento corticoesteroideo, diabetes mellitus insulinodependiente, pobre estado nutricional, hipoxia y anemia crónicas y enfermedades cardiovasculares, además de infección y reflujo gastrointestinal y el sexo femenino.4
Diagnóstico
Los síntomas más comunes son: incremento súbito de las secreciones respiratorias, dificultad para respirar, disnea, dolor torácico, tos y broncoaspiración e infección pulmonar frecuente; además del signo de Ono (crisis de tos incontrolada después de la deglución, también descrito como sensación de ahogamiento tras la deglución o “complejo deglución tos”). Además, se produce fuga gaseosa a pesar de la hiperinsuflación del manguito, distensión abdominal asociada con ruidos sincrónicos con la ventilación y signos de supuración pulmonar.7) Simões y otros11) alertan sobre el riesgo, no despreciable, de insertar la cánula en una “falsa vía”, hacia el esófago, durante el proceder, porque regularmente no se piensa en esta eventualidad.
Imaginológicos
La radiografía del tórax puede demostrar las secuelas de episodios repetidos de broncoaspiración, neumonía y otras complicaciones, además de dilatación esofágica (distal a la fístula) y gástrica.
La esofagografía muestra el paso del contraste hidrosoluble hacia la VR. Asimismo, puede realzar la transparencia causada por el manguito hiperinsuflado con diámetro mayor de 35 mm (signo indirecto de fístula) y signos radiológicos de infección pulmonar.
La tomografía axial computarizada (TAC) permite identificar la localización de la fístula y su tamaño, además del estado de los tejidos blandos adyacentes y de los órganos mediastinales y las lesiones del parénquima pulmonar.2,12)
Endoscópicos
La esofagoscopia y la broncoscopia pueden ser útiles en la identificación de la localización y tamaño de la fístula,2,12,13) pero la primera tiene pocas posibilidades de visualizar lasde pequeño calibre, al ser enmascaradas por los pliegues mucosos longitudinales del esófago.4
El EBUS (siglas inglesas de: endobronchial ultrasound) proporciona información del estado de los tejidos peritraqueales.4
La insuflación de CO2 puede descubrir fístulas no observadas con la esofagografía, al demostrar altas concentraciones del gas al final de la espiración.1,4
Anatomía patológica
Las dimensiones de las FTEs son variables, pero la mayoría son extensas (4-5 cm), con destrucción a todo lo ancho de la pared traqueal posterior.El proceso de formación de la fístula es largo. La inflamación perilesional une las paredes de la tráqueacon las del esófago, por lo que nunca ocurre mediastinitis, mientras que la cicatrización espontánea es ilusoria debido a que los bordes están epitelizados. La formación suele asociarsecon destrucción circunferencial de la tráquea, producida por el propio mecanismo de necrosis isquémica.
Tratamiento en el cuidado preoperatorio
El tratamiento preoperatorio comprende dos fases. En la primera se ha de resolver el déficit nutricional y se tratarán las lesiones asociadas, fundamentalmente la infección respiratoria. Mathiseny otros15 aconsejan el tratamiento en tres etapas. La primera medida es retirar la sonda nasogástrica, la segunda comprende la utilización de una cánula de traqueostomía con manguito de baja presión, no hiperinsuflado, que se coloca por debajo del orificio fistuloso, cuando es posible y, por último, la realización de la gastrostomía para impedir el reflujo y yeyunostomía para alimentación. La derivación esofágica raramente es necesaria, solo es recomendada en:
fístulas en posición supracarinal, no controlables con la cánula de traqueostomía;
cuando la broncoaspiración amenaza la vida y no se controla con el manguito insuflado.4
La pequeña cantidad de saliva producida no constituye un problema de importancia. En los casos raros en que fuera necesario realizarla, la esofagostomía será terminal con fístula mucosa proximal y cierre del cabo distal. La aspiración continua por la gastrostomía es suficiente para controlar el reflujo. El tratamiento con fármacos antisecretores y procinéticos ayuda a prevenir el reflujo gastroesofágico.
Uno de los pacientes del autor fue remitido con alimentación por sonda nasogástrica, la cual fue retirada y se realizó una yeyunostomía alimentaria y gastrostomía para aspiración, ya que se quejaba de reflujo gastroesofágico (RGE), incluso después de realizar la yeyunostomía. Otro tenía una sonda nasogástrica multifenestrada, al parecer con la intención de que la secreción gástrica fuera drenada sin pasar a través de la fístula. En realidad, tal proceder condicionó un intenso reflujo gastroesofágico con esofagitis y moniliasis graves, por lo que tal práctica debe ser condenada.
Un dilema planteado es si operar mientras el paciente está ventilado o esperar hasta que haya sido destetado del ventilador. Los intentos de operación en el paciente ventilado, generalmente conducen a un rotundo fracaso. Estos enfermos no deben ser intervenidos por el efecto negativo de la intubación traqueal sobre la anastomosis y la sutura esofágica, con riesgo muy alto de complicaciones graves, por lo que se recomienda tratamiento conservador, tomando en cuenta el pronóstico. Una opción, para el paciente que no puede ser destetado de la ventilación, es la inserción de prótesis esofágicas, traqueales o ambas.16
Si la traqueostomía es necesaria, se debe practicar distal a la FTE. El objetivo principal del tratamiento urgente es la separación del árbol traqueobronquial de la vía digestiva,12) mediante diferentes métodos.
El tipo de tratamiento, conservador o quirúrgico, se indica según el estado respiratorio, neurológico y nutricional del enfermo.4) El quirúrgico estaría indicado ante el fracaso delas medidas conservadoras o de acuerdo con el estado preoperatorio.12) El pronóstico malo a corto plazo excluye la cirugía.
Tratamiento conservador
Los objetivos fundamentales del tratamiento conservador son:
Frenar la contaminación de la VR con el contenido intestinal,
resolver la infección broncopulmonar,
mejorar el estado funcional y nutricional,
separar al paciente del ventilador.
Las consecuencias de la contaminación permanente con alimentos y secreciones digestivas pueden ser muy serias, con posible evolución fatal.4 La gastrostomía y la yeyunostomía se pueden realizar mediante técnicas de mínimo acceso: gastrostomía percutánea y yeyunostomía laparoscópica o técnica combinada percutánea y endoscópica. La elevación del torso en ángulo de 45°, durante unas horas después de la alimentación, ayuda a disminuir la broncoaspiración.
El manguito de la cánula de traqueostomía se coloca bajo control endoscópico, distal a la fístula, con la mínima cantidad de aire para sellar la tráquea. Se recomienda realizar aspiración bronquial repetida y se puede indicar tratamiento atropínico para minimizar la secreción salival.
La combinación de alimentación enteral y parenteral facilita la mejoría nutricional de los enfermos.
Tratamiento endoscópico
Para Osho y otros,17) la cirugía abierta es la única solución definitiva, porque el método endoscópico generalmente retarda el tratamiento quirúrgico y, en ocasiones, extiende la lesión esofágica y traqueal.18) No obstante, existen diferentes métodos para el tratamiento endoscópico de esta afección, los cuales se practicarán cuando la cirugía está contraindicada.4
El método mediante vacío (EVT, siglas inglesas de: endoscopic vacuum therapy y de clipado broncoscópico (OTSC), siglas inglesas de: over the scope clips, son técnicas novedosas, relativamente fáciles de usar y se señala que son seguras y efectivas en el tratamiento de perforaciones del sistema digestivo superior, incluyendo FTEs.19) Sin embargo, los datos de ambas técnicas son limitados, y no existen ensayos controlados. Por estas razones, se considera que son necesarios estudios adicionales para compararlas con otros métodos, y definir su papel real en los algoritmos de tratamiento.20,21
Se han descrito otros dispositivos y tecnologías como las endopróstesis degradables, válvulas endobronquiales de una sola vía en forma de sombrilla y técnicas novedosas como el trasplante de células mesenquimatosas. La cola de fibrina coagula inmediatamente y sella la fístula broncopleural. No obstante, las fístulas pequeñas (< 5 mm) tienen la mayor probabilidad de cicatrizar con el tratamiento endoscópico, mientras que no es apropiado para las de mayor diámetro.22
Por último, Pestrella y otros,23) utilizaron el trasplante de células madre mesenquimatosas de la médula ósea, para el cierre de una fístula broncopleural secundaria a neumonectomía por un mesotelioma de bajo grado.
Endoprótesis
En la tabla 2 se enuncian las indicaciones de las endoprótesis traqueales. Las indicaciones de las endoprótesis traqueales en estos casos son:
Existe lesión proximal, en la cual la prótesis esofágica podría interferir con la competencia del esfínter esofágico superior
Hay estenosis traqueal asociada por destrucción cartilaginosa
No se debe insertar en el esófago, por la posibilidad de obstrucción traqueal al expandirla
Si existe estenosis laringotraqueal sincrónica con la fístula
La endoprótesis debe sobrepasar 2 a 3 cm craneal y caudalmente, los límites de la fístula traqueal.
El tubo en T podría ser una alternativa apropiada para casos con FTE postintubación y estenosis laringotraqueal sincrónica.24
Las prótesis tienen desventajas. Las de silicona tienen un diámetro interno menor debido al grosor de la pared, alta frecuencia de dislocación (menor con los TET), ausencia de reepitelización y dificultad para expulsar las secreciones. Las metálicas pueden causar perforación de la pared traqueal (Fig. 1) con posibilidad de lesiones vasculares y producen tejido de granulación y estenosis. Las cubiertas tienen mejores resultados y facilidad para extraerlas.
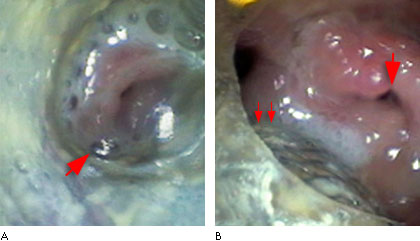
Figura 1 A. Dislocación distal de una prótesis traqueal metálica, hacia el bronquio principal derecho. B. La flecha simple muestra estenosis consiguiente de alto grado del bronquio. Las flechas dobles muestran una FTE extensa y la prótesis esofágica
Se han forjado esperanzas en las prótesis biodegradables, las cuales tienen menor posibilidad de dislocación y no necesitan ser extraídas,25) aunque en la actualidad solo existen las no cubiertas, lo que contraindica su uso en afecciones malignas o fístulas.
Por último, la endoprótesis magnética es útil en pacientes críticos con FTEs adquiridas, no malignas, hasta que sea posible realizar la operación.26
Tratamiento quirúrgico
La cirugía radical puede curar hasta 97,8 % de los casos, incluyendo las complicaciones.12) El cirujano que emprende el tratamiento de pacientes con FTEs, debe tener una comprensión exhaustiva de su etiología, diagnóstico y tratamiento para alcanzar el mejor resultado. La cirugía está indicada porque la fístula tiene pocas posibilidades de cicatrizar espontáneamente. El momento ideal para el tratamiento definitivo es:
el paciente se encuentra estable: estados nutricional y general adecuados;
la infección está controlada y,
ha sido destetado de la ventilación mecánica.
Las vías de acceso comprenden la cervicotomía y la cervicomediastinotomía en fístulas altas2,17 y toracotomía derecha para las bajas. En algunos casos puede ser necesaria la cervicotomía con esternotomía y toracotomía.
Detalles de técnica quirúrgica
Los aspectos esenciales del tratamiento quirúrgico son: aislamiento del trayecto fistuloso y la interposición de un colgajo hístico pediculado, entre la tráquea y el esófago, para prevenir la recidiva de la fístula. Los principios de la cirugía traqueal deben ser aplicados estrictamente en casos de FTEs, porque a menudo se trata de reoperaciones y la mayoría están asociadas a un alto grado de inflamación local. El cirujano debe realizar o estar presente cuando se practican la broncoscopia y la esofagoscopia para poder tomar la decisión en cuanto a si la fístula tiene indicación de sutura simple o si está justificada la resección y reconstrucción traqueal. Los mejores resultados se obtienen en servicios quirúrgicos especializados en cirugía traqueal y esofágica.27
Históricamente, se han utilizado un grupo de técnicas quirúrgicas:
sutura directa de la fístula, en un tiempo;
resección del segmento traqueal afectado con anastomosis primaria y sutura esofágica;
cierre de las fístulas con colgajos de tejidos blandos;
tratamiento en dos tiempos con derivación esofágica y cierre primario del defecto traqueal, seguido por sustitución esofágica y, finalmente,
colocación de endoprótesis autoexpansibles cubiertas. Como otros autores,6 preferimos la operación en un tiempo.
La técnica consiste en la resección traqueal con anastomosis terminoterminal, reparación de la pared membranosa o reparación sobre un tubo en T.24) En ocasiones, un defecto largo se cubre con un colgajo muscular o con una malla de material absorbible con interposición muscular. Se prefiere la resección y anastomosis traqueal5) (Fig. 2), porque con frecuencia la fístula se asocia con estenosis de este órgano. La lesión de la pared esofágica se sutura en uno o dos planos;2 pero en algunos casos, es necesaria la resección y anastomosis terminoterminal o injerto de piel de grosor total.

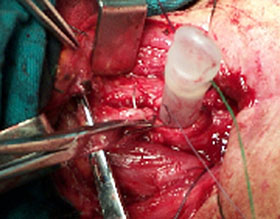
Figura 2 Tratamiento quirúrgico de una FTE. A. Se seccionó la zona traqueal estenótica. La flecha blanca indica el sitio de la fístula inmediatamente detrás de la traqueostomía. En el fondo se observa la sonda nasogástrica. B. se extirpando la zona estenótica de la tráquea. C. Sutura del plano mucosa esofágico. D. La cabeza de flecha señala el colgajo del músculo esternotiroideo que se interpone entre la tráquea y el esófago.
Figura 3Resección traqueal y anastomosis con sutura esofágica
Una vez incidida la VR, se buscan tejidos sanos y bien vascularizados, en ambos extremos traqueales, para garantizar una anastomosis satisfactoria y disminuir la probabilidad de fuga anastomótica y estenosis.
La mayoría de los pacientes se operan a través de un acceso anterior, en posición supina y el cuello ligeramente extendido. Si el enfermo tiene una cánula de traqueostomía se retira y se coloca un tubo estéril, preferiblemente anillado, a través del estoma. Se tendrá a mano un juego de mangueras para ventilación, estériles, para el momento en que la ventilación se realice a través del campo quirúrgico. Una sonda nasogástrica ayudará a identificar el esófago durante la disección. (Fig. 2) Cuando la fístula asienta en tráquea media se añadirá una esternotomía vertical parcial. Se disecan los colgajos cervicales, superior e inferior, por debajo del platisma y se crea un plano de disección pretraqueal hasta la carina. En la porción superior se secciona el istmo tiroideo y la glándula se separa de la tráquea.
La broncoscopia permite localizar el nivel de la fístula que se marca antes de comenzar la disección, la cual se mantendrá directamente sobre la pared traqueal para evitar la lesión de nervios recurrentes. Nunca se intentará visualizarlos. La disección traqueal lateral y circunferencial no debe ser mayor de 1 a 2 cm (usualmente no más de dos cartílagos sanos) por debajo del extremo distal de la fístula para no desvascularizar la tráquea. La disección circunferencial del esofágono es necesaria, aunque se deben movilizar las paredes anterolaterales para facilitar la sutura longitudinal del defecto, sin tensión.
La fístula alta, cuyo límite proximal está cerca del cricoides, a menudo excluye la disección posterior, debido al daño probable de los recurrentes a su entrada en la laringe. A continuación, se colocan suturas laterales de tracción, en los extremos traqueales, proximal y distal, seccionados. La disección traqueal se realiza inmediatamente distal al segmento estenótico. Seccionada la VR, la ventilación se continúa a través del campo quirúrgico. El extremo proximal de la tráquea se eleva y se realiza disección lateral completa de la fístula, la cual se secciona preservando tanta pared esofágica como sea posible. (Fig. 2) El extremo proximal de la fístula se alcanza disecando el espacio entre la tráquea y el esófago. Se secciona la tráquea proximalmente por encima del segmento estenótico y se extirpa la porción enferma junto con la fístula, limitando la resección a no más de 4 a 5 cm, si se considera que habrá tensión excesiva sobre la anastomosis. En ocasiones será necesario liberar la laringe para disminuir la tensión.
El esófago se repara en dos planos y en sentido longitudinal. El interno toma la mucosa y la submucosa con puntos separados de materiales absorbibles a largo plazo (vicryl, ácido poliglicólico, etc.), calibre 4/0 o 3/0, con los nudos hacia la luz esofágica. El segundo plano comprende la pared muscular con idéntico material, pero con los nudos hacia el exterior. La sutura en un plano tiene como desventaja que se puede romper con una menor tensión.
Para separar la sutura esofágica de la traqueal y evitar la recidiva de la fístula, se puedenutilizarcolgajos de músculos esternohioideo (Fig. 2), esternocleiodomastoideo, esternotiroideo, la glándula tiroides5) y el platisma,28) y para las torácicas músculo intercostal, pleura y periostio costal y, pericardio.5,29) La anastomosis traqueal comienza con la colocación de puntos laterales de soporte, en ambos extremos traqueales, de vicryl o ácido poliglicólico 2/0. Para la anastomosis utilizamos vicryl o ácido poliglicólico 4/0 en la pared membranosa y 3/0 en la cartilaginosa. En primer lugar, se anudan los puntos se soporte, que disminuirán la tensión sobre la línea de sutura. Los puntos de la anastomosis se anudan, comenzando por los posteriores. Los nudos quedarán hacia el exterior. Se comprueba la hermeticidad de la sutura con solución salina que cubre la tráquea y, aplicando ventilación a presión positiva, con el manguito desinsuflado. Si no es posible extirpar la zona estenótica se coloca un tubo en T (Fig. 3), de talla apropiada. La ventilación continúa a través de un tubo pequeño insertado en la rama externa del tubo en T. Se coloca un drenaje blando (penrose) o un drenaje plano con aspiración continua.17
.
Tubo en T en posición.
Es frecuente la asociación entre FTEs y traqueomalacia, lesiones que deben ser tratadas, en uno o dos tiempos. En una de las pacientes del autor se encontró traqueomalacia en la zona adyacente a la fístula y parálisis recurrencial bilateral. En el primer tiempo se reparó el esófago y el defecto de la membranosa. Después de tratada la lesión recurrencial mediante una cordoaritenodectomía posterior se extirpó la zona malácica (2 cm) y se colocó un tubo en T porque la calidad de la pared traqueal no era óptima. Seis meses más tarde fue posible decanularla.
Cuidados posoperatorios
Retiramos la sonda yeyunal entre 3 y 4 semanas después de la operación. En casos de resección traqueal el paciente mantendrá el cuello flexionado por 7 a 10 días; en pacientes de edad superior a los 50 años, entre 15 a 21 días. Para tratar que el paciente no extienda el cuello, se colocan uno o dos puntos de sutura fuerte, entre el mentón y la piel anterior del tórax. En el preoperatorio se insiste en la importancia de mantener la flexión cervical. Es necesario reconocer el valor de la extubación en el salón de operaciones, puesto que cualquier contingencia puede resolverse sin mayores problemas, porque los equipos quirúrgico y anestésico están preparados. La ventilación mecánica posoperatoria es un factor de riesgo importante para la dehiscencia de sutura. En caso de que fuera necesaria, el manguito del TET o de la cánula de traqueostomía se localizan distales a la anastomosis. La nutrición a través de la yeyunostomía se reinstaura entre 12 a 24 horas en el postoperatorio. En nuestra práctica, realizamos la esofagografía a los 7 días y si se comprueba que no hay fuga del material deglutido, se comienza la dieta líquida inmediatamente.
Complicaciones quirúrgicas
Las complicaciones de la FTE afectan hasta 55 % de los pacientes operados.2) Entre las más frecuentes tenemos: aspiración de sangre y neumonía asociada,5 neumomediastino, enfisema subcutáneo y fístula residual, estenosis traqueal retardada, disfagia y parálisis recurrencial.
También la salida persistente de alimentos a través de la traqueostomía por incoordinación de la deglución, además de infección respiratoria y de la herida cutánea,3,5) e infección de la herida.
RESULTADOS
La indicación adecuada y el momento oportuno de la operación, la técnica quirúrgica precisa y los cuidados postoperatorios son prerrequisitos indispensables para obtener resultados satisfactorios.4
Muniappany otros29) revisaron los resultados obtenidos en 35 pacientes operados entre 1995 y 2010. Se produjo recidiva en 3 enfermos (11 %) tratados con laringectomía y esofagectomía. Alcanzaron el cierre de la fístula en 94 %. Del total de pacientes, 83 % pudo alimentarse por vía natural y 71 % no necesitó traqueostomía.
Para algunos el cierre de la fístula puede ser superior al 90 %.2,5,29) La recidiva fluctúa entre 6,4 % y 8,3 %.
En ciertos casos, la recidiva de la fístula puede ser tratada con endoprótesis.2) Su mayor incidencia ocurre en pacientes que necesitan ventilación mecánica postoperatoria.
Se han publicado cifras de parálisis recurrencial del 6,3 % de los pacientes, mientras que la recidiva de la estenosis traqueal puede alcanzar hasta el 14, 2 %.3) En pacientes irradiados, sometidos a cirugía laríngea o esofágica y en reoperaciones existe riesgo importante de recidiva de la fístula y afectación del árbol respiratorio.17
Mortalidad
La mortalidad fluctúa entre el 3 % y el 12,5 %.2,3,17,29) Uno de nuestros pacientes falleció en el salón de operaciones por causa anestésica. La recidiva de la fístula y la infección respiratoria se relacionan con la posibilidad de fallecer.
Pronóstico
Si bien el tratamiento quirúrgico es efectivo, las complicaciones y la mortalidad son significativas, aun cuando los pacientes se traten en centros de referencia tras una evaluación preoperatoria adecuada.2
El pronóstico es reservado porque muchos pacientes están muy enfermos y dependientes de ventilación mecánica, con enfermedades neurológicas y cardiovasculares graves.4
CONCLUSIONES
La intubación endotraqueal prolongada es la causa principal de FTEs. Suele presentarse en pacientes con mal estado general y enfermedades graves. El mecanismo de producción fundamental es la isquemia producida por la compresión de las paredes posterior de la tráquea y anterior del esófago, entre el manguito insuflado del TET y la sonda nasogástrica. El diagnóstico positivo se obtiene con la broncoscopia y la esofagoscopia. La TAC informa sobre el estado de los tejidos vecinos y de los pulmones, que pueden estar afectados por la contaminación mantenida. El tratamiento conservador generalmente no cura la fístula, pero puede limitar la contaminación del árbol traqueobronquial y garantiza la nutrición. La derivación esofágica raramente está indicada, excepto cuando persiste entrada a la VR del contenido gastrointestinal.
Por lo regular es necesaria la resección traqueal y la sutura esofágica. La selección de los pacientes y del momento adecuado para la operación, constituye la clave fundamental para obtener resultados satisfactorios. El momento ideal para la cirugía definitiva es cuando el paciente se encuentra estable, el estado nutricional es adecuado, la infección está controlada, la ventilación mecánica ya no es necesaria y el estado general ha mejorado.