Introducción
El mucocele apendicular (MA) fue descrito por primera vez en 1842 por Karl Freiherr von Rokitansky y más tarde en 1976 definido por Feren. Se considera una lesión rara del apéndice, que se encuentra en el 0,3 al 0,7 % de las apendicectomías. Se caracteriza por la dilatación de la luz del órgano con acumulación de moco que puede ser benigno o maligno y consecuencia de procesos obstructivos o inflamatorios, cistadenomas mucinosos o cistadenocarcinomas. Además de estas causas, otras lesiones tumorales en el apéndice o el ciego, pueden presentarse como mucocele. El cistoadenoma se ha encontrado en 0,2 a 0,3 % de los apéndices resecados en Europa y Estados Unidos. La principal complicación de esta entidad es el pseudomixoma peritoneal (PMP).1-7
Para muchos autores, el término mucocele debería abandonarse en favor de una entidad patológica más específica. Para Agrusa y otros8 el término debería mantenerse por algunas razones: está profundamente utilizado en la literatura y es un término descriptivo simple, que permite al cirujano o radiólogo informar sobre una determinada lesión antes de cualquier caracterización patológica.
En esta enfermedad ha sido descrito un cuadro clínico inespecífico.9 Puede presentarse de diversas formas similar a otras enfermedades como la apendicitis aguda, como un dolor abdominal inespecífico o una masa asintomática.6 Su diagnóstico puede ser realizado en el preoperatorio mediante el empleo de medios diagnósticos, pero en gran número de casos se realiza en el acto operatorio.3 Sin embargo, Sun y otros2 recomienda que el diagnóstico se realice antes de la intervención quirúrgica con el objetivo de seleccionar la técnica operatoria más adecuada y evitar complicaciones.
Se clasificaron previamente en cuatro entidades patológicas según las características del epitelio: mucocele simple o de retención, mucocele con epitelio hiperplásico velloso local o difuso, adenoma/cistadenoma mucinoso y cistadenocarcinoma mucinoso. Actualmente el término mucocele apendicular se emplea para el manejo clínico, pero el diagnóstico debe ser según la histología.5
Cestino y otros4) hace referencia a que en 2016 el Peritoneal Surface Oncology Group International propuso una clasificación y una terminología diagnósticas en un consenso publicado en American Journal of Surgical Pathology, en el que las lesiones mucinosas de se clasifican de la siguiente forma: no neoplásico y neoplásico en las que incluyeron pólipos cerrados con o sin displasia de grado bajo o alto, adenoma con displasia de bajo o alto grado, neoplasias mucinosas de bajo o alto grado y adenocarcinoma mucinoso.
Este trabajo tuvo el objetivo de caracterizar un caso de mucocele apendicular de comportamiento benigno en un paciente adulto masculino.
Presentación de caso
Paciente de 52 años de edad blanco, masculino, con antecedentes patológicos personales de hipertensión arterial bajo tratamiento regular, operado de hernia epigástrica sin secuelas. Acude al hospital refiriendo dolor lumbar derecho de 1 mes de evolución, que se irradió a cuadrante inferior derecho (CID), que no cedía con analgésicos, de intensidad moderada y persistente, sin otros síntomas acompañantes. Al examen físico se constató abdomen doloroso a la palpación en CID donde se palpa zona empastada de aproximadamente 4 cm, poco movible, con defensa abdominal, por lo que se decide su ingreso en sala de Cirugía General con diagnóstico de posible tumor de vías digestivas complicado para tratamiento quirúrgico inmediato. No se constataron alteraciones hemoquímicas. Se realizan exámenes imagenológicos:
Rx de tórax: sin alteraciones
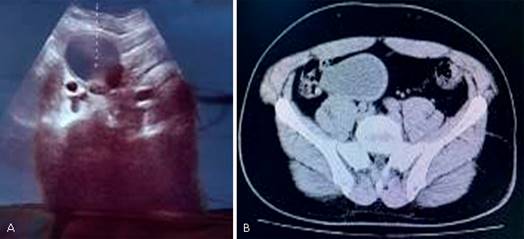
Ultrasonido abdominal (US): hipogastrio, línea media y a la derecha imagen hipoecogénica ovalada, heterogénea, vesícula normal con pared de 5 mm que mide 81 ( 49 ( 49 mm, bazo supernumerario a nivel del hilio esplénico de 19 mm; litiasis de 7 mm en riñón derecho, quiste en el polo superior de riñón izquierdo sin dilatación (fig. 1A).
Tomografía axial computarizada (TAC) de abdomen con doble contraste: engrosamiento parietal de un segmento de íleon distal. En íntimo contacto con asas intestinales delgadas en hipogastrio, línea media y a la derecha imagen hipodensa de 63 ( 52 mm pared regular hiperdensa que realza al contraste de 6 mm desplaza asas contiguas, pequeñas y múltiples adenopatías mesentéricas (fig. 1B).
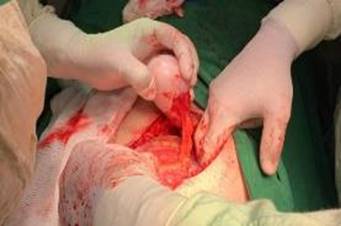
Se interviene quirúrgicamente y se halla masa blanquecina de aspecto quístico en la punta apendicular, sin adenopatías en el meso, ni lesión en colon o hígado. Se realizó apendicectomía convencional de punta a base, se toma muestra para biopsia de la lesión, sin accidentes operatorios (Fig. 2).
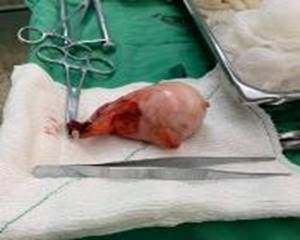
El estudio anatomopatológico informó apendicitis aguda con acúmulo de moco intramural, mucosa aplanada por compresión de moco detenido, ausencia de malignidad; se concluyó como mucocele apendicular benigno (fig. 3).
Discusión
El MA constituye la dilatación progresiva del apéndice vermiforme debido a la acumulación intraluminal de sustancia mucoide. El moco se retiene como resultado de la obstrucción o hiperproducción de la luz debido a enfermedades benignas (fecalitos, fibrosis posinflamatoria, pólipos hiperplásicos, adenomas serrados) o malignas. Las neoplasias mucinosas apendiculares (AMN) son raras, con una incidencia de 0,12 casos por millón de personas por año.7,8,10
Puede ser benigno o maligno. Las AMN de bajo grado (LAMN) se utilizan para referirse a los cistoadenomas mucinosos. Los tumores mucinosos representan el 58 % de los tumores malignos del apéndice y el resto son carcinoides.11
El MA es poco común constituyendo del 8 al 10 % de todos los tumores apendiculares. Agrusa y otros,8) Saad y otros12) y Pratap Singh7 afirman que esta afección es más común en mujeres con una proporción de 4:1 y en los mayores de 50 años.
Se plantea que el cuadro clínico es inespecífico, lo cual dificulta el diagnóstico preoperatorio. Puede presentarse de forma asintomática o manifestar síntomas que lo hacen común a otras enfermedades. Muchas veces es diagnosticado como un hallazgo incidental durante exámenes radiológicos y endoscópicos o una intervención quirúrgica, como sucedió con el caso que se presenta, constatado durante una ultrasonografía abdominal y posteriormente en la cirugía.
Puede presentarse como una masa asintomática en el CID del abdomen que crece lentamente. Los pacientes suelen presentar dolor abdominal en CID de carácter crónico o agudo, pérdida de peso, náuseas, vómitos, fiebre, cambios en el hábito intestinal, sangrado por el recto, o presentarse como un cuadro peritoneal agudo. Los síntomas urinarios son raros. Muhammad Ali y otros9) plantea que los que son sintomáticos tienen la posibilidad de ser malignos.1,2,6-8,12
Se ha descrito la torsión apendicular, la obstrucción intestinal, la perforación y la estrangulación intestinal como formas de presentación. La invaginación intestinal es extremadamente rara.2,6-8
Un alto por ciento en la mujer se presenta dolor abdominal y/o pélvico prolongado, con o sin pérdida de peso, asociada a masa anexial palpable simulando una patología tubo-ovárica. En otras se presenta de forma aguda con fiebre.5,7
La variedad en las formas de presentación representa un desafío para el cirujano, por lo que se establece que el diagnóstico final es intraoperatorio y se basa en la evaluación histopatológica.
Entre los medios diagnósticos para detectar esta enfermedad se encuentra el ultrasonido abdominal, el colon por enema, la colonoscopia y la tomografía axial computarizada del abdomen y pelvis simple, con contraste y el multidetector. El American College of Radiology plantea que la TAC es el método más preciso.1-3,6,8,9,11
El US es de primera línea para pacientes con dolor abdominal agudo. Los hallazgos ecográficos comprenden múltiples capas ecogénicas en una masa quística anecoica, conocido como “signo de piel de cebolla” además del realce nodular de la pared.7,9,10,12
La TAC se puede utilizar para descubrir los signos específicos del MA con alta precisión: luz del apéndice de más de 1,3 cm, masa quística bien encapsulada, de pared delgada, rodeada por el ciego, o patrón de “copa y bola”, atenuación de TAC mixta (debido al contenido de mucina) ubicada en las proximidades y que muestra continuidad al ciego junto con calcificación de la pared. La distinción entre mucocele y ciego es un desafío en masas más grandes.1,2,6,9
Muhammad Ali y otros9) plantea que el enema de bario se utilizó con frecuencia en el pasado para el diagnóstico de enfermedades colónicas (en nuestro país se emplea aún con una frecuencia elevada) y se ha observado un llenado deficiente de contraste en el apéndice.7
Mediante la colonoscopia se observa una masa brillante y redondeada que sobresale del orificio apendicular y una secreción mucosa amarillenta conocido como el signo del volcán. Es importante para el diagnóstico de cánceres de colon sincrónicos o metacrónicos. En aproximadamente 13 % - 42 % de los pacientes con neoplasia apendicular, está presente una lesión colónica sincrónica. Se recomienda la colonoscopia de vigilancia en pacientes con diagnóstico de cistoadenoma comprobado histopatológicamente.1,7,9-12
Cestino y otros4) es del criterio que el diagnóstico suele ser incidental y esta patología a menudo se descubre durante la evaluación radiológica o endoscópica en busca de molestias no relacionadas o dolor abdominal o puede ser una sorpresa durante una operación de apendicitis aguda.7
Los marcadores tumorales como el antígeno carcinoembrionario (CEA), CA 19-9 y CA-125 son inespecíficos, pero deben medirse después del diagnóstico de MA y repetirse de forma rutinaria para monitorear la progresión de la enfermedad. Su nivel elevado se correlaciona con el estadio avanzado del tumor.6,7
Cuando se sospecha el MA no se recomienda la citología por aspiración con aguja fina o el estudio de tomografía por emisión de positrones. El examen histopatológico minucioso es esencial y proporciona el diagnóstico final de la enfermedad apendicular.3,7,12
Se debe establecer el diagnóstico diferencial con enfermedades benignas del apéndice como apendicitis, leiomioma, neuroma, fibroma y lipoma y otras como quistes mesentéricos, hidrosalpinx, linfoma, invaginación intestinal, endometriosis y adenocarcinoma de apéndice.3,6,7
Uno de los principios cardinales del tratamiento quirúrgico es evitar la ruptura y el derrame de mucina en la cavidad peritoneal durante la resección con el posterior PMP. En la actualidad el tratamiento comprende varias estrategias: la espera vigilante hasta la cirugía citorreductora (CRS) extensa o con quimioterapia peritoneal intraoperatoria hipertérmica (HIPEC) o quimioterapia intraperitoneal posoperatoria precoz (EPIC).1,2
Muhammad Ali y otros1) y Saad y otros12) hacen referencia a los criterios de Dhage-Ivatury y Sugarbaker los cuales proponen un algoritmo para la selección del tipo de cirugía.
La apendicectomía simple es la elección para los pacientes con mucocele benigno. Se recomienda la hemicolectomía derecha cuando se sospecha un mucocele maligno por la presencia de un mucocele perforado, un ganglio linfático mesentérico agrandado; cecectomía parcial cuando la base del es ancha y sobresale hacia la pared cecal, o si el margen del muñón es positivo y los ganglios linfáticos negativos. Se recomienda una exploración precisa del abdomen debido a la asociación entre el MA y otros cánceres de células secretoras de mucina, como los de colon y de ovario.2,4,6,8
No está indicada una hemicolectomía derecha en ausencia de enfermedad metastásica en los ganglios linfáticos, a partir de un examen de sección congelada de estos dentro del mesenterio apendicular.11
Una vez obtenida la patología definitiva, se debe evaluar si está indicada una nueva cirugía, según estadificación. Esta decisión no es estandarizada, estos pacientes deben ser presentados en una reunión multidisciplinaria. Las opciones quirúrgicas incluyen una hemicolectomía derecha completa con linfadenectomía y CRS y HIPEC para tratar la enfermedad mucinosa peritoneal (PMP).4
En caso de rotura, la resección primaria debe ir acompañada de la extracción de todos los implantes macroscópicos y debe recuperarse cualquier líquido o moco para un examen citológico. El pronóstico de la neoplasia mucinosa apendicular depende de si el tumor progresa a PMP. Este último es una afección difícil de tratar. Pueden ser necesarias intervenciones quirúrgicas complejas que incluyen la extirpación de material mucinoso, CRS, peritonectomía y HIPEC.6,7,11
La cirugía abierta tiene dos objetivos: realizar la cirugía con cuidado para evitar la ruptura y el relleno no se esparza en la cavidad peritoneal y tener una inspección más completa, palpación e inspección directa de las zonas del abdomen donde los tumores mucinosos son más frecuentes.1,2,5,7,11
Sin embargo, Agrusa y otros8 aseveran que para la cirugía laparoscópica no existen pruebas sólidas a favor o en contra de su seguridad.4,7
Después de la apendicectomía, la tasa de supervivencia a 5 años para el MA simple es del 91-100 %, pero se reduce al 25 % para la AMN maligna.11
Pueden surgir ciertas complicaciones como invaginación intestinal, hemorragia, perforación que conduce a peritonitis, pionefrosis, rotura ocurriendo el posterior PMP, que, aunque son raras, pero pueden ser fatales. El PMP es su principal complicación, se asocia con una mayor morbilidad y mortalidad.1,2,3,11
Conclusiones
El mucocele apendicular es una enfermedad rara. Se presenta clínicamente de forma inespecífica, lo que imposibilita su diagnóstico preoperatorio y aumenta las probabilidades de ser un hallazgo imagenológico o quirúrgico incidental. La estrategia quirúrgica depende de los hallazgos intraoperatorios donde la apendicectomía y la hemicolectomía derecha son las técnicas más utilizadas. El pseudomixoma peritoneal es una complicación frecuente asociada a alta morbilidad y mortalidad.