Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Estomatología
versión impresa ISSN 0034-7507
Rev Cubana Estomatol vol.48 no.3 Ciudad de La Habana jul.-set. 2011
ARTÍCULOS DE REVISIÓN
Importancia de la semiología del dolor en el diagnóstico de un proceso inflamatorio pulpar
Significance of pain's Symptomatology in the diagnosis of pulpal inflammatory process
Andrés 0. Pérez RuizI, Julia María Martínez LimaII, Jannette Carmona BetancourtII, María Elena Urgelles JiménezIII
I Máster en Atención de Urgencias Estomatológicas. Especialista de II Grado en Fisiología Normal y Patológica. Doctor en Medicina. Profesor Auxiliar. Facultad de Estomatología "Raúl González Sánchez". Universidad de Ciencias Médicas de La Habana, Cuba.
II Máster en Atención de Urgencias Estomatológicas. Especialista de I Grado en Estomatología General Integral. Instructora. Facultad de Estomatología "Raúl González Sánchez". Universidad de Ciencias Médicas de La Habana, Cuba.
III Máster en Atención de Urgencias Estomatológicas. Especialista de I Grado en Estomatología General Integral. Instructora. Facultad de Ciencias Médicas "Enrique Cabrera". Universidad de Ciencias Médicas de La Habana, Cuba.
RESUMEN
El dolor es un síntoma de extraordinaria importancia en la práctica estomatológica y particularmente en lo concerniente a las alteraciones de la pulpa dentaria. Con el objetivo de profundizar en el conocimiento de las fases por las que atraviesa un proceso inflamatorio pulpar, que permiten predecir sus manifestaciones dolorosas, se realizó una revisión bibliográfica sobre el tema con un enfoque multidisciplinario y básico-clínico. Se utilizó el método documental para el análisis y tratamiento de la información ofrecida por las fuentes teóricas. El sitio en Internet Google fue empleado como fundamental motor de búsqueda y Lilacs, Hinari, Medline y PubMed fueron las bases de datos más revisadas. La clasificación del estado de inflamación pulpar, que atiende a eventos histopatológicos que no se pueden visualizar, resulta más difícil. Se podría lograr mayor precisión en un diagnóstico basado en el curso que sigue el dolor, de acuerdo a la magnitud del compromiso inflamatorio y apoyado en la rica semiología que se puede obtener si se sigue la trayectoria de las variables del estímulo nociceptivo. El incremento y profundización de los conocimientos en este campo contribuiyó significativamente a un mejor diagnóstico y tratamiento de los procesos inflamatorios pulpares.
Palabras clave: Infamación pulpar, semiología, dolor.
ABSTRACT
Pain is a symptom very important in the stomatologic practice and particularly in that concerning to dental pulp alterations. To deep in the knowledge of phases crossed by a pulpal inflammatory process allowing predicting its painful manifestations, authors made a bibliographic review on this subject with a multidisciplinary and basic-clinical approach, using the documentary method for analysis and management of information offered by theoretical sources. Google was used as a fundamental search tool and LILACS, HINARI, Medline and PubMed were the more reviewed databases. The classification of pulpal inflammation state, taking into account non-visualized histopathology events is more difficult and it may to achieve a great accuracy in a diagnosis based on course after pain, according the magnitude of inflammatory compromise and supported by the potential valuable symptomatology if we follow the trajectory of the nociceptive stimulus variables. The know ledges increase and deepening in this field will contribute in a significant way to a better diagnosis and treatment of pulpal inflammatory processes.
Key words: Pulpal inflammatory processes, symptomatology, dental pain.
INTRODUCCIÓN
Habitualmente se valora la magnitud del dolor por los síntomas que manifiesta el paciente. La esencia del dolor se imbrica en el psiquismo en forma imperceptible y directa; puede variar de tolerable a intolerable, según el estado anímico temporal de quien lo soporta. El dolor es parte de la enfermedad que experimenta el paciente, este se transforma con el tiempo y envuelve su vida, de manera que el ser humano adquiere y modula este estímulo sensorial a través de su psicología individual.1,2
El dolor constituye una reacción muy subjetiva, nadie sabe la intensidad del dolor que otra persona sufre, excepto por la descripción verbal que nos hace quien lo padece o por la angustia que refleja en su rostro.
El paciente que acude a la consulta estomatológica puede experimentar dolor causado por: un proceso inflamatorio pulpar, un absceso, enfermedad periodontal, aparatos ortodóncicos y protésicos o por otras enfermedades de los tejidos bucales blandos o duros. El dolor agudo provocado por una lesión es el resultado de múltiples interacciones de mecanismos bioquímicos, fisiológicos y psicológicos y necesariamente involucra la actividad sensitiva, motivacional y cognoscitiva, así como los mecanismos psicodinámicos del sujeto que lo padece. El dolor tiene una enorme importancia como mecanismo de alarma ante una injuria y también ha permitido la supervivencia del hombre.3-5
Para comprender la evolución de un proceso inflamatorio pulpar es importante hacer algunas consideraciones acerca de este tejido. La pulpa es un tejido conjuntivo especializado laxo, de consistencia gelatinosa, ubicada en una cavidad de paredes rígidas rodeada por dentina y cemento. Este tejido responde a cualquier agresión por medio de una respuesta inflamatoria, la cual adquiere una característica especial en la pulpa al estar confinada a una cavidad de paredes mineralizadas y con irrigación sanguínea terminal.6-9
Así, el tejido pulpar perfectamente protegido por su capa mineralizada (esmalte-dentina) no presentará sintomatología dolorosa, a no ser que se le apliquen estímulos térmicos (frío, calor) o eléctricos (mediante el vitalómetro). La manifestación dolorosa desaparece inmediatamente al ser retirado el estímulo.
La pulpa normalmente presenta un número relativo células como los fibroblastos que tienen un papel activo en la formación de sustancia intercelular, los odontoblastos que intervienen en la dentinogénesis y la formación de dentina reparadora y macrófagos (histiocitos) que representan la primera línea de defensa en la inflamación.
La pulpa es un tejido ricamente vascularizado, la mayoría de los vasos sanguíneos entran en la pulpa a través de los orificios apicales, sin embargo no es infrecuente que pequeñas arteriolas y en ocasiones otras mayores penetren desde la membrana periodontal a otros niveles de las raíces. Los vasos sanguíneos del tejido pulpar, de tipo arterial y de mayor calibre son las arteriolas, que se caracterizan por tener paredes delgadas y un mínimo de fibras musculares en la túnica media. Las arteriolas dan origen a un rico plexo sub-odontoblástico capilar, desde el cual, ramas curvadas pasan entre los odontoblastos hacia la pre-dentina. El plexo capilar desemboca en vénulas medianamente grandes que se unen en venas de mayor calibre.
La característica de las paredes delgadas de los vasos sanguíneos pulpares los hace particularmente favorables a la dilatación. Durante la respuesta inflamatoria de la pulpa la hiperemia asociada y los cambios exudativos conducen a un gran incremento de la presión tisular, debido a las sólidas paredes mineralizadas que forman la cavidad pulpar.
Un sistema de capilares linfáticos drena la pulpa lo que mantiene la presión del líquido intersticial en condiciones normales. Por otro lado el diente está profusamente inervado con fibras nociceptivas: unas 700 fibras A delta y 1 800 fibras C salen o entran por el agujero apical del primer premolar adulto.10-12
Las fibras vinculadas a la nocicepción (A delta y C) que encontramos en la pulpa presentan una serie de características que es importante recordar:
- Fibras A delta: son mielínicas, de uno a cuatro nanómetros de grosor, su velocidad de conducción es entre 4-30 m/seg y poseen un bajo umbral de excitación. Se desarrollan luego de la erupción dentaria y tienen baja capacidad de conservar la integridad funcional en situaciones de hipoxia tisular. Este tipo de fibra está vinculada al dolor de tipo agudo y punzante.
- Fibra C: son amielínicas, de pequeño grosor (un nanómetro) de baja velocidad de conducción (0,5 a 2 m/seg.), con un alto umbral de excitación. Se desarrollan previo a la erupción dentaria y presentan capacidad de conservación de su integridad funcional en situaciones de hipoxia tisular y están vinculadas al dolor de tipo lento y quemante.13,14
La estimulación de fibras nerviosas pulpares mediante: calor, frío, acción mecánica o química, produce una sensación dolorosa casi pura; la estimulación eléctrica con el vítalómetro también activa a dichas fibras.
En realidad hacer un diagnóstico del proceso inflamatorio pulpar basado en el aspecto histopatológico resulta irreal pues no tenemos como correlacionar esos hallazgos con los clínicos. En estos momentos resulta más objetivo y confiable establecer un diagnóstico de la condición pulpar según las características del dolor en cada una de las fases o etapas por las que transita un proceso inflamatorio pulpar.
Es importante considerar que el tejido pulpar no experimenta una extinción o muerte repentina, sino que sucumbe paulatinamente. La evolución de las condiciones pulpares se clasifican de la siguiente manera: pulpitis reversible, pulpitis transicional, pulpitis irreversible y pulpa necrótica.15 Este estudio se realizó con el objetivo de profundizar en el conocimiento de las fases por las que atraviesa un proceso inflamatorio pulpar que permiten predecir sus manifestaciones dolorosas.
MÉTODO
Se realizó una concertación básico-clínica entre los autores del trabajo, sobre la interpretación del síntoma dolor, de significación importante en el seguimiento de las fases por las que transita un proceso pulpar; se aportaron los conocimientos que brindaron sus especialidades y se trató de consolidar un material práctico, sencillo y útil, pero con el rigor científico necesario. En el mismo se utilizó el método documental o bibliográfico para el análisis y tratamiento de la información ofrecida por las fuentes teóricas.
La información básica se obtuvo a través de documentos primarios y secundarios. Google fue empleado como fundamental fuente de búsqueda. Las bases de datos más revisadas fueron HINARI, LILACS, Medline y PubMed. Los descriptores que más información nos brindaron fueron los siguientes: clasificaciones del dolor, calidad de la sensación y lugar del daño tisular. Se realizó una búsqueda que incluyó la velocidad de propagación del impulso nervioso a través de las vías vinculadas a la nocicepción. Luego se procedió a la selección, evaluación y recogida de la información correspondiente al tema, la cual fue analizada, interpretada y procesada en una computadora Pentium 4, para posteriormente elaborar el informe final.
DESARROLLO
La interpretación del síntoma dolor es de significación importante en el seguimiento de las fases o estadios por las que transita un proceso pulpar.
Existen varias clasificaciones del dolor, según diversos criterios, como la calidad de la sensación, lugar del daño tisular y otros, también de acuerdo a la velocidad de propagación del impulso nervioso a través de las vías vinculadas a la nocicepción; así se describe el dolor rápido y el dolor lento. Nos vamos a referir a esta última clasificación que alude al dolor de tipo rápido y lento, por ser de mucha vigencia en la literatura y de muy fácil interpretación y vinculable a cualquier otra que queramos exponer: 16,17
Clasificación del dolor
Según la cualidad de la sensación
Dolor punzante o rápido
Dolor quemante o lento
Según el lugar del daño tisular
Dolor superficial
Dolor Profundo somático (referido)
Dolor visceral (referido)
Dolor parietal
El dolor pulpar lo incluimos en la clasificación como dolor visceral y aunque las estructuras dentarias no son vísceras sí tienen en su interior a la pulpa, la cual se encuentra protegida por tejidos mineralizados del diente con una dotación neural similar a las vísceras con las consiguientes fibras A delta y C, anteriormente comentadas.
Siempre que vayamos a referirnos al dolor como modalidad sensorial debemos estudiar cuatro variables vinculadas al estímulo, las cuales determinan: su calidad o cualidad de la sensación, su frecuencia, su localización y su intensidad. Basado en lo anteriormente expuesto se analizan a continuación algunas características del dolor por inflamación pulpar.18
Cualidad o calidad de la sensación
Dolor punzante: es el dolor de tipo lancinante, vinculado a fibras de tipo A delta, mielinizadas, con velocidad de conducción rápida.
Dolor sordo: es el dolor levemente pulsátil, vinculado a fibras C desmielinazadas, con velocidad de conducción lenta, es el dolor que entraña un mayor sufrimiento. Ambos tipos de dolor presentan una aparición espontánea o provocada y una duración posterior al aplicar o remover el estímulo nociceptivo
Dolor provocado: es aquel que sólo aparece cuando el diente es sometido a algún estímulo, como: el frío, el calor, las sustancias ácidas, los alimentos azucarados, la masticación y la percusión, entre otros.
Dolor espontáneo: aparece sin causa aparente, es decir, independiente de algún estímulo, sin embargo, este tipo de dolor refleja mayor compromiso de la condición pulpar.
Duración del dolor: cuando aplicamos un estímulo sobre un diente, el dolor puede aparecer rápidamente o lentamente y al ser removido o retirado un estímulo sobre un diente, el dolor podrá desaparecer rápidamente, lentamente o mantenerse. Esta última condición traduce un mayor compromiso inflamatorio pulpar que los dos anteriores.
Frecuencia
El dolor analizado bajo este aspecto podrá ser intermitente o continuo. El dolor intermitente es aquel que entre las crisis dolorosas presenta periodos de ausencia del dolor, denominados periodos de calma. El periodo de calma puede ser largo o corto. Los periodos de calma largos representan capacidad favorable de respuesta del tejido pulpar, mientras que los cortos traducen mayores complicaciones para el mismo.
Los periodos de calma pueden ser espontáneos o inducidos (por acción de algún analgésico). Resultaría importante observar si el periodo de calma logrado tras la ingestión de un analgésico continúa después del término de la acción de éste y por cuánto tiempo persiste.
Los periodos sin dolor espontáneos y largos reflejan condiciones pulpares favorables.
Localización
El dolor pulpar en cuanto a localización puede seguir el siguiente patrón:
Localizado: se precisa fácilmente la estructura dentaria comprometida y se relaciona con los procesos pulpares comenzantes o incipientes.
Difuso o irradiado: a medida que el proceso inflamatorio se generaliza por la pulpa, el dolor pasa a ser difuso, con dificultad de ser localizado por el paciente, puede abarcar estructuras dentarias aledañas al diente comprometido y hacer difícil su localización, por ejemplo: una pulpitis en el segundo premolar superior y el dolor se hace difuso al primer premolar superior y primer molar superior.
Referido: es aquel que se manifiesta en un área distante de la región dañada, por ejemplo un proceso pulpar en 1º y 2o molares mandibulares, referido el dolor al oído y al ángulo de la mandíbula, en general a un área cutánea o mucosa alejada del sitio de lesión.
Intensidad
Es una dimensión sobresaliente del dolor, pero con un alto grado de subjetividad. Para su determinación acudiremos al método de la escala análoga-visual que dentro de sus ventajas incluye: su simplicidad, uniformidad, sensibilidad y confiabilidad para medir la intensidad del dolor.
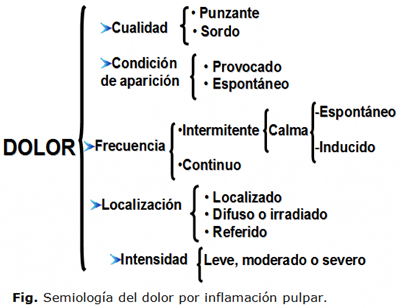
Los aspectos anteriormente discutidos referidos a la semiología del dolor aparecen resumidos en el cuadro sinóptico de la Fig.
Las pruebas térmicas representadas por el frío y el calor constituyen valiosos exámenes en la evaluación del proceso inflamatorio pulpar, la cual nos brinda una confirmación más de la fase por la que transita la pulpa inflamada; los resultados que arrojan estos métodos de exploración pulpar son bastante confiable.
La prueba térmica del frío permite evaluar la información que nos brinda el paciente durante el interrogatorio. Por ejemplo si éste relató la aparición de dolor al ingerir algún alimento frío con manifestación de dolor de instalación inmediata y persistencia del mismo al retirar el estímulo, esta condición de aparición y duración del dolor al aplicar y retirar un estímulo frío podrá ser perfectamente verificada con la prueba del hielo consistente en la simple aplicación de una barrita de agua helada en la superficie de la estructura dentaria comprometida.
La prueba térmica por calor, realizada con la denominada barra de gutapercha, permite también evaluar la condición de inflamación pulpar, aunque no con la misma eficacia que lo hace la prueba del frío.
En caso de que estos métodos aplicados al paciente que nos consulta por dolor no provean el resultado esperado en cuanto a obtener una adecuada respuesta de la manifestación sensorial dolor al explorar el tejido pulpar inflamado, podemos acudir al choque térmico que consiste sencillamente en aplicar calor sobre un diente e inmediatamente después aplicar un estímulo frío. El cambio brusco de temperatura podrá activar a las terminaciones nerviosas nociceptivas a nivel pulpar y generarse el dolor.19
La prueba eléctrica con el vitalómetro es un método bastante conocido y de una excelente eficacia al explorar la sensibilidad dolorosa que muestra el tejido pulpar cuando se encuentra vital.
La percusión constituye un método clínico de vital significación. El comprometimiento del tejido periodontal podrá ser diagnosticado a través de esta exploración. En general el dolor que aparece a la percusión vertical significa entre otras cosas, necrosis pulpar con extensión del proceso a la región periapical. El dolor resultante de la maniobra es de tipo, rápido o punzante, con localización en la estructura dentaria percutida ya que el periodonto involucrado está inervado por fibras Aä vinculada a las características del dolor que apuntamos anteriormente.
Es importante señalar que otras situaciones periodontales podrán mostrar sintomatología dolorosa a esta exploración y por esta razón el mismo deberá ser complementado con otros exámenes (tabla).20-25
CONCLUSIONES
El proceso inflamatorio pulpar transita por diferentes estadios, ya que constituye un tejido que al sucumbir paulatinamente de no tratarse el proceso inflamatorio, representa un excelente modelo para el estudio del dolor y sus características acompañantes.
El conocimiento de las variables asociadas al estímulo nociceptivo permite establecer, con bastante certeza, un diagnóstico preciso de la fase en que se encuentra el proceso inflamatorio en el momento en que el paciente nos visita aquejado por dolor. El examen clínico y las pruebas de vitalidad pulpar constituyen excelentes herramientas para el seguimiento y estudio del dolor en las diferentes fases de una pulpitis.
REFERENCIAS BIBLIOGRÁFICAS
1. Mizuta M. Oxidative stress in diabetes. Nippon Yakurigaku Zasshi. 2005;125(3):125-8
2. Chen C, Bazan NG. Endogenous PGE2 regulates membrane excitability and synaptic transmission in hippocampal CA1 pyramidal neurons. J Neurophysiol. 2005;93(2):929-41.
3. Son JK, Son MJ, Lee E, Moon TC, Son KH, Kim CH, Kim HP, et al. Ginkgetin, a Biflavone from Ginko biloba leaves, inhibits cyclooxygenases-2 and 5-lipoxygenase in mouse bone marrow-derived mast cells. Biol Pharm Bull. 2005;28(12):2181-4.
4. Das UN. COX-2 inhibitors and metabolism of essential fatty acids. Med Sci Monit. 2005;11(7):RA233-7.
5. Pacheco B. Aspectos psicológicos del dolor. 2008; [cited 2010 Nov 10]; Available from: http://www2.udec.cl/~papachec/psic_dolor.htm#1.
6. Silva TA, Lara VS, Silva JS, Oliveira SH, Butler WT, Cunha FQ. Macrophages and mast cells control the neutrophil migration induced by dentin proteins. J Dent Res. 2005;84(1):79-83.
7. Repolles PM, Brañas Garza P. Sensibilidad, resistencia y expresión del dolor: relación con la socialización del dolor. Rev Soc Esp Dolor [serial on the Internet]. 2010 Oct [cited 2010 Nov 10]; 17(7): 304-311. Available from: http://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S1134-80462010000700002&lng=en
8. Revuelta Evrard E, Segura Escobar E, Paulino Tevar J. Depresión, ansiedad y fibromialgia. Rev Soc Esp Dolor [serial on the Internet]. 2010 Oct [cited 2010 Dic 10]; 17(7):326-332. Available from: http://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S1134 -80462010000700006&lng=en
9. Gusman H, Santana RB, Zhnder M. Matrix metalloproteinase levels and gelatinolytic activity in clinically healthy and inflamed human dental pulps. Eur J Oral Sci. 2003;111(3):289.
10. Kantarci A, Van Dyke TE. Resolution of inflammation in periodontitis. J Periodontol. 2005;76(11 Suppl):2168-74.
11. Cruz PP, Fernández RM. Mecanismos del dolor pos-opertorio: bases anatómicas y fisiológicas. En: Navía Roque. Guía del dolor pos-opertorio agudo. Madrid: Ed. Ergon; 2006. p. 13-27.
12. Graff-Radford SB. Disorders of the mouth and teeth. En: Silberstein SD; Lipton RB; Dalessio DJ. Wolff's Headache and other head pain. 7 ed, New York: Oxford University Press; 2001.
13. Amer-Cuenca JJ, Goicoechea C, Lisón JF. ¿Qué respuesta fisiológica desencadena la aplicación de la técnica de estimulación nerviosa eléctrica transcutánea? Rev Soc Esp Dolor [serial on the Internet]. 2010 Oct [cited 2010 Dic 10; 17(7):333-42. Available from: http://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S1134-80462010000700007&lng=en
14. Abu-Bakra M, Jones NS. Prevalence of nasal mucosal contact points in patients with facial pain compared with patients without facial pain. J Laryngol Otolo. 2001;115:629-32.
15. Bender IB. Reversible and irreversible painful pulpitides: diagnosis and treatment. Aust Endod J. 2000;26(1):10-4.
16. Lluch Girbes E, Torres Cueco R, Butler D, Moseley L. Explicando el dolor. Rev Soc Esp Dolor [serial on the Internet]. 2010 July [cited 2010 Dic 10]; 17(5):253-4. Available from: http://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S1134-80462010000500006&lng=en
17. Aaron LA, Burke MM, Buchwald D. Overlapping conditions among patients with chronic fatigue syndrome, fibromyalgia, and temporomandibular disorder. Arch Inter Med. 2000;160:221-7.
18. Acosta Ortiz R. Diagnóstico diferencial del dolor orofacial. Asociado a desórdenes neuropáticos. Rev Fac Odont Univ Ant; 2001;13(1):29-39.
19. Martorell CL, García MB, Peñarrocha DM. Actualización en el tratamiento del dolor orofacial. Med Oral. 2004;9:293-9.
20. McNeil PL, Miyake K, Vogel SS. The endomembrane requirement for cell surface repair. Proc Natl Acad Sci U S A. 2003;15(8):4592-7.
21. Asselin-Paturel C, Trinchieri GJ. Production of type I interferons: plasmacytoid dendritic cells and beyond. J Exp Med. 2005;15(4):461-5.
22. Anderson LM, Dumsha TC, McDonald NJ, Spitznagel JK. Evaluating IL-2 levels in human pulp tissue. J Endod. 2002;28(9):651-5.
23. Artese L, Rubini C, Ferrero G, Fioroni M, Santinelli A, Piattelli A. Vascular endothelial growth factor (VEGF) expression in healthy and inflamed human dental pulps. J Endod. 2002;28(1):20-3.
24. Pérez A, Cabrera M, Santos P. Hipótesis actuales relacionadas con la sensibilidad dentinal. Rev Cubana Estomatol [serie en internet]. Mayo-ago. 1999 [citado 27 Febrero 2008]; 36(2): [aprox. p. 4]. Disponible en: http://scielo.sld.cu/scielo.php.
25. Insausti Valdivia J, Bedmar Cruz MD, Pozo Martín C, Abejón González D, Córdoba Benedicto JL, Calle Reviriego JL, et al. ¿Quo vadis dolor? Rev Soc Esp Dolor [serial on the Internet]. 2010 May [cited 2010 Dic 10]; 17(4):187-189. Availablefrom: http://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S113480462010000400001&lng=en
Recibido: 8 de abril de 2011.
Aprobado: 20 de mayo de 2011.
Dr. Andrés 0. Pérez Ruiz. Facultad de Estomatología "Raúl González Sánchez". Universidad de Ciencias Médicas de La Habana, Cuba. Correo electrónico: aperezruiz@infomed.sld.cu