Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Medicina Militar
versión impresa ISSN 0138-6557
Rev Cub Med Mil vol.42 no.1 Ciudad de la Habana ene.-mar. 2013
ARTÍCULO ORIGINAL
Ligadura endoscópica de várices esofágicas más propranolol para profilaxis secundaria del sangrado digestivo en pacientes cirróticos
Endoscopic variceal ligation plus propranolol for secondary prophylaxis of gastrointestinal bleeding in cirrhotic patients
Dra. C. Mirtha Infante Velázquez, Dra. Madeleine Fuentes Ramos, Dra. Marlén Pérez Lorenzo, Dr. Juan Yerandy Ramos Contreras, Dra. Rebeca Winograd Lay, Dr. Omar Angulo Pérez
Hospital Militar Central "Dr. Luis Díaz Soto". La Habana, Cuba.
RESUMEN
Introducción: la combinación de la ligadura endoscópica de las várices esofágicas más el uso de fármacos betabloqueadores constituye el tratamiento de elección para la profilaxis secundaria del sangrado.
Objetivo: determinar la probabilidad de no ocurrencia de un episodio de recidiva hemorrágica en un grupo de pacientes que recibió tratamiento combinado, y si la recidiva está relacionada o no con la causa de la cirrosis o con el grado de disfunción hepatocelular.
Métodos: se realizó un estudio descriptivo, prospectivo y longitudinal y la construcción de las curvas de supervivencia tomando como suceso o evento el resangrado. Se efectuó la comparación de acuerdo con la causa y el estado de la enfermedad según estadio de Child-Pugh.
Resultados: fueron incluidos 23 pacientes: 56,5 % masculinos y 43,5 % femeninos. La principal causa de la cirrosis fue la infección por el virus de la hepatitis C (52,2 %). Hubo 7 pacientes (30,4 %) en estadio A de Child; 10 (43,5 %) en B, y 6 (26,1 %) en C. Se realizaron 3,47 sesiones promedio de ligadura y la dosis media de propranolol administrada fue de 97,39 mg. Todos los pacientes erradicaron las várices. La tasa global de resangrado fue de 13,04 %. Existió empeoramiento o aparición de gastropatía hipertensiva en el 34,8 % de los casos. La probabilidad acumulada de supervivencia fue de 95,2 % a los tres meses; del 87,9 % a los 11 meses y del 79,1 % a los 14 meses. No se encontraron diferencias en la supervivencia en relación con la causa (p = 0,749), pero sí en relación con el estadio según Child (p = 0,002).
Conclusiones: la combinación terapéutica evaluada es útil para erradicar las várices y prevenir la recidiva del sangrado.
Palabras clave: cirrosis, ligadura con bandas, várices esofágicas, propranolol.
ABSTRACT
Introduction: the combination of endoscopic ligation of esophageal varices along with beta blockers drugs is the treatment of choice for secondary prophylaxis of bleeding.
Objective: to determine the probability of occurrence of an episode of recurrent bleeding in a group of patients who received a combination therapy, and if this recurrence is related or not to the cause of cirrhosis or to the degree of hepatocellular dysfunction.
Methods: adescriptive, prospective and longitudinal study was conducted. Survival curves were constructed taking as rebleeding as an event. Comparison was performed according to the cause and disease status according to Child-Pugh stage.
Results: 23 patients were included: 56.5 % male and 43.5 % female. The main cause of cirrhosis was hepatitis C virus infection (52.2 %). Seven patients (30.4 %) were in stage A of Child; 10 (43.5 %) in B and 6 (26.1 %) in C. 3.47 average ligation sessions were performed and 97.39 mg was the mean dose of propranolol administered. All patients had their varices eliminated. The overall rebleeding rate was 13.04 %. 34.8 % of cases suffered worsening or occurrence of hypertensive gastropathy. The cumulative probability of survival was 95.2 % at three months, 87.9 % at 11 months and 79.1 % at 14 months. No differences in survival were found related to the cause (p = 0.749), but there were found differences according to Child stage (p = 0.002).
Conclusions: the assessed combination therapy is useful to eliminate and prevent recurrent variceal bleeding.
Key words: cirrhosis, banding, esophageal varices, propranolol.
INTRODUCCIÓN
La hipertensión portal (HTP) es un síndrome clínico caracterizado por un incremento anormal de la presión hidrostática en el sistema venoso portal. Esto conduce a la formación de un sistema de ramificaciones venosas colaterales que derivan parte del flujo sanguíneo portal a la circulación sistémica sin atravesar el hígado. Como consecuencia de varios eventos fisiopatológicos, estas colaterales portosistémicas son causa de una importante complicación de la HTP: la hemorragia por várices.1 El episodio de sangrado se relaciona con una elevada mortalidad y es la causa de muerte más frecuente o la mayor indicación de trasplante hepático en los pacientes con cirrosis hepática.2
La prevalencia de várices es proporcional a la severidad de la enfermedad hepática, de modo que se encuentran presentes en el 30 % de los pacientes cirróticos compensados —en menos del 5 % de los casos se trata de várices de gran tamaño— y en el 60 % de los descompensados.3
En el tratamiento de la hemorragia por várices se distinguen tres situaciones clínicas diferentes: el episodio agudo, la prevención del primer episodio en pacientes que nunca han sangrado (profilaxis primaria) y la prevención de la recidiva hemorrágica en pacientes con antecedente de sangrado por várices o profilaxis secundaria.4,5 Las medidas terapéuticas se basan en el tratamiento farmacológico, cuyo objetivo es alcanzar una reducción "protectora" del gradiente de presión portal; el endoscópico, basado en la erradicación de las várices esofágicas por diferentes métodos, así como tratamientos derivativos, bien quirúrgicos o con radiografía intervencionista, que tratan de reducir la presión venosa portal mediante la creación de anastomosis venosas portosistémicas.2,3
Por ser la cirrosis una de las principales causas de muerte en Cuba, una de las acciones para disminuir la mortalidad en estos pacientes está dirigida a la profilaxis secundaria del sangrado por várices, y al no existir experiencias previas publicadas en Cuba ni tener datos disponibles de la prevalencia e incidencia anual de cirróticos con várices en el país, este trabajo se diseñó para determinar la probabilidad de que no ocurriera un nuevo episodio de sangrado en un grupo de pacientes que recibió tratamiento combinado con propranolol y ligadura endoscópica de las várices. También se investigó si la recidiva tuvo relación o no con la causa de la cirrosis o con el grado de disfunción hepatocelular.
MÉTODOS
Se realizó un estudio de tipo descriptivo, prospectivo y longitudinal en el Servicio de Gastroenterología del Hospital Militar Central Dr. "Luis Díaz Soto", en el período comprendido entre los meses de julio de 2008 y diciembre de 2009, y participaron pacientes mayores de 18 años, de uno y otro sexos, con diagnóstico de cirrosis hepática de cualquier causa, con várices esofágicas que tenían el antecedente de haber sobrevivido a un episodio de sangrado agudo.
Se excluyeron los casos con carcinoma hepatocelular u otra neoplasia maligna, enfermedad cardiovascular o pulmonar severa, o con historia de reacciones adversas o contraindicaciones para el uso de betabloqueadores: asma bronquial, diabetes mellitus, insuficiencia cardiaca, enfermedad vascular periférica, hipertrofia prostática, hipotensión arterial (tensión arterial sistólica menor que 100 mm Hg).
Otros criterios de exclusión fueron el sangrado por várices fúndicas, trombosis de la vena porta o embarazo. También, el presentar bradicardia (frecuencia cardiaca basal menor de 55 latidos/min) o bloqueo completo de rama.
Los pacientes fueron atendidos en la consulta externa especializada en enfermedades del hígado. Se utilizó la clasificación de Child-Pugh6 (tabla 1) para determinar el estadio funcional de la hepatopatía. Se les realizó endoscopia digestiva para determinar la presencia de várices esofágicas y su clasificación endoscópica (clasificación de Paquet7), de gastropatía portal hipertensiva (clasificación de McCormack8 y de várices gástricas (clasificación de Sarin9).
La ligadura endoscópica se realizó sin sedación, con el dispositivo ligador multibandas de la casa Wilson Cook. Las sesiones de ligadura se realizaron cada 21 días hasta erradicar las várices, lo que fue establecido cuando no hubo visualización de las venas en el tercio inferior del esófago o que las existentes, por su pequeño tamaño, no se aspiren por el cilindro del dispositivo ligador.
Para el tratamiento con propranolol se escogió una dosis inicial de 40 mg diarios, administrados preferentemente en el horario nocturno. Cada semana, en la consulta externa, se fue incrementando la dosis a razón de 20 mg cada vez, hasta que se logró una reducción de la frecuencia cardiaca en el 25 %, pero cuidando que este descenso no estuviera por debajo de los 55 latidos/min. Se vigilaron los efectos indeseables del fármaco y se efectuaron los ajustes necesarios hasta alcanzar la dosis óptima. Su valor fue el dato que se utilizó para el análisis estadístico. El monitoreo se realizó con una periodicidad mensual. El tratamiento con propranolol continuó después de erradicadas las várices, hasta el final del estudio.
En la consulta mensual se recolectó información de la evolución clínica, la aparición de complicaciones, pérdida o muerte y se registraron las fechas de estos sucesos. Los datos descriptivos se agruparon en tablas y gráficos, después de ser procesados con medidas de resumen. Para determinar la probabilidad de no ocurrencia de un episodio de resangrado se realizó un análisis de supervivencia, con el método del límite de producto de Kaplan-Meier, con el que se construyeron las curvas de sobrevida del total de pacientes, de acuerdo con la causa, y por estratos de acuerdo con la clasificación de Child-Pugh. El evento o suceso de interés fue la ocurrencia de un episodio de resangrado, definido según los criterios del consenso de Baveno IV.10 Para el análisis se estableció como tiempo cero el momento en que se confirmó el diagnóstico inicial de cirrosis y la presencia de várices esofágicas, con el requisito de haber presentado un episodio de sangrado. Los pacientes de quienes no fue posible conocer su estado, se consideraron como muertes para propósito del análisis.
La comparación de las curvas según las distintas causas y los grados de disfunción hepatocelular se realizó por el método del logaritmo de rangos. Se consideró un valor de p mayor que 0,05 como significativo. El protocolo de este estudio fue aprobado por el Comité de Ética de Investigaciones de la Institución.
RESULTADOS
La muestra quedó constituida por 23 pacientes: 13 del sexo masculino y 10 del femenino; con una edad promedio de 58,34 años; valor máximo, 77 años y valor mínimo, 42 años. La principal causa de cirrosis fue la infección por el virus de la hepatitis C (52,2 %). De acuerdo con la clasificación de Child: 7 pacientes (30,4 %) en estadio A, 10 (43,5 %) en B y 6 (26,1 %) en C. Las várices esofágicas fueron de grado II (8,7 %); grado III (60,9 %) y grado IV (30,4 %). En 6 casos se comprobó la existencia de signos endoscópicos de gastropatía portal hipertensiva, que fue ligera en 4 (17,4 %) y severa en 2. Las várices gástricas fueron detectadas en 4 pacientes.
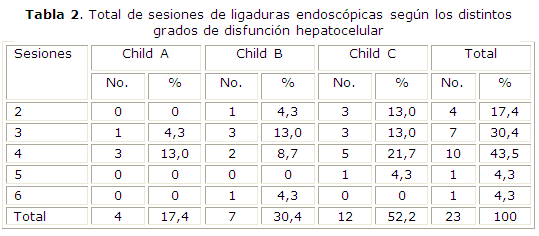
Todos erradicaron las várices. Para esto se realizaron como promedio 3,47 ± 0,59 sesiones de ligadura. Los casos con la enfermedad en estadio C de Child requirieron más sesiones de ligaduras que aquellos con una reserva funcional hepática mejor conservada. Estos resultados se muestran en la tabla 2.
El tratamiento endoscópico se combinó con la administración de propranolol, según el protocolo descrito. Después de alcanzar la dosis óptima, la media de la dosis fue de 97,39 ± 30,33 mg, con un margen entre 40 y 160 mg.
La tasa global de resangrado fue del 13,04 %. En todos los casos se trató de enfermos con alto grado de disfunción hepatocelular. Este suceso ocurrió en un paciente antes de lograr la completa erradicación de las várices mediante el tratamiento endoscópico y los 2 restantes lo hicieron durante el período de observación. En todos los casos se comprobó que la fuente del resangrado fueron las várices esofágicas que recidivaron.
La prevalencia de gastropatía congestiva antes de la ligadura fue del 13,04 % en toda la muestra; de ellos, 4,34 % con la enfermedad en estadio A de Child; ninguno de los Child B y 2 (8,7 %) en los C. Al finalizar el tratamiento endoscópico, el 21,73 % de los pacientes había presentado lesiones de gastropatía congestiva. La incidencia de várices gástricas antes de iniciar el tratamiento fue del 4,34 %. En un paciente se observó la presencia de várices gástricas neoformadas.
En relación con las complicaciones motivadas por la ligadura endoscópica (dolor retroesternal, sangrado, estenosis, aparición de una úlcera esofágica, febrícula y/o disfagia), estas fueron de presentación inmediata. Tuvieron lugar en 7 pacientes (30,4 %), aunque un mismo paciente presentó más de una complicación.
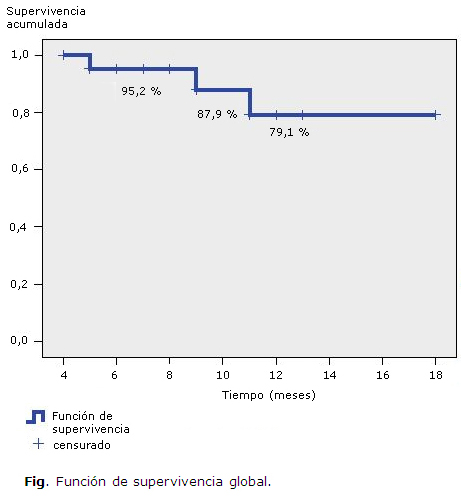
La probabilidad global de sobrevida acumulada para el total de los pacientes fue del 95,2 % a los 3 meses; del 87,9 % a los 11 meses y del 79,1 % a los 14 meses (Fig.).
La comparación de las curvas de supervivencia, según el grado de disfunción hepatocelular, mostró que la probabilidad de ocurrencia del resangrado es mayor en pacientes en estadio C de Child (p = 0,002). La probabilidad de no sangrar fue menor en los casos con enfermedad por infección por el virus de la hepatitis C o por hábito enólico, en comparación con las otras causas, pero las diferencias no fueron significativas (p = 0,749).
DISCUSIÓN
En los momentos actuales, la combinación de la ligadura endoscópica con el uso de fármacos betabloqueadores no selectivos es el tratamiento de elección para la profilaxis secundaria del sangrado por várices esofágicas.11 Se ha podido establecer que el paciente que ha experimentado un episodio de sangrado por várices esofágicas tiene un riesgo de resangrado en las 24 h subsiguientes del 30 al 50 %. Si no se le indican medidas terapéuticas, el riesgo de volver a sangrar, en el primer año es del 60 al 80 %.12
La tasa de erradicación de las várices que se alcanzó con la combinación terapéutica en el presente estudio (100 %), es similar a la que reportan Gómez Senent13 y otros autores,14,15 quienes han comunicado datos que oscilan entre el 31 y el 90 %. Estos resultados son menores en pacientes con un grado de insuficiencia hepatocelular avanzado (Child C).16
El número de sesiones de ligadura necesarias para erradicar las várices se encuentra dentro del rango del 2,7 al 4 %, que reporta un metaanálisis de 5 series realizado por D´Amico.17 Este factor se ha relacionado con el sangrado por la escara de la úlcera que produce la banda en la mucosa esofágica. También es importante el tiempo transcurrido entre cada sesión. Estos elementos contribuyeron a que no ocurriera hemorragia por esta causa en la serie estudiada.
Petrasch18 encuentra un resultado interesante: el sangrado desde el sitio de la ligadura es un fenómeno que ocurre con más frecuencia en pacientes a quienes se les realiza la ligadura de urgencia, en comparación con aquellos que reciben el tratamiento endoscópico de forma planificada o electiva, tal como ocurrió en esta investigación. Harewood19 resalta el valor de los elementos técnicos de la ligadura y un mayor tiempo entre las sesiones.
Con la adición del tratamiento farmacológico al esquema terapéutico endoscópico se produce una reducción sostenida de la presión portal y, con eso, de la presión de la circulación portocolateral hasta unos niveles en que se disminuye o minimiza el riesgo de hemorragia por várices.20,21
Hoy día, en los centros de mayor nivel de disponibilidad de recursos en el mundo, los betabloqueadores se indican de acuerdo con criterios de selección que definen la respuesta. Esto se realiza a través de la medición del gradiente de presión venosa hepática (HVPG, por su sigla en inglés). La reducción de este gradiente a valores menores o iguales que el 20 % de las cifras basales y/o mayores o iguales que 12 mm Hg, después de la estimulación con un bolo de propranolol por vía endovenosa (0,15 mg/kg), permite identificar a aquellos pacientes respondedores al tratamiento con los betabloqueadores.22 En estos casos se ha observado una menor probabilidad de sangrar o de aparecer complicaciones, así como una mejor supervivencia. Cuando no se dispone de la posibilidad de medir la presión venosa portal, se puede utilizar la clasificación de Child para estratificar a los pacientes en grupos de riesgo de resangrado con suficiente seguridad.23
En un metaanálisis de 12 ensayos clínicos que comparó el uso de betabloqueadores contra placebo se observó una reducción en la ocurrencia del resangrado entre los pacientes tratados, pero no se demostraron beneficios en relación con la supervivencia cuando se usaron en monoterapia.24 Mediante otro metaanálisis se ha podido demostrar que las tasas de hemorragias recurrentes (de todas las fuentes y várices) son menores con el tratamiento combinado de la ligadura endoscópica más los fármacos que con cualquier tratamiento solo, pero sin diferencias en la supervivencia.25
En estudios que han comparado la ligadura de várices con la farmacoterapia (betabloqueadores o nitritos), no se han encontrado diferencias entre las causas generales de resangrado. Se sabe que por las várices sangra el 26 % de los tratados con ligadura de várices frente al 32 % de la farmacoterapia.26 El porcentaje de resangrado observado en este estudio, inferior a estas cifras, se debe sin dudas al empleo de un tratamiento combinado, como se ha observado por otros autores.2,3,27
El cumplimiento de los criterios de selección de los pacientes y el protocolo seguido para el tratamiento farmacológico, que permitió hacer ajustes hasta lograr la dosis óptima, favorecieron que no ocurrieran complicaciones con el uso del propranolol. Las que se presentaron tuvieron que ver con el tratamiento endoscópico, pero ninguna de ellas graves, que hicieran peligrar la vida del paciente.
Otra observación en relación con las consecuencias del tratamiento fue el relativo empeoramiento de la gastropatía portal en un grupo de estos pacientes. Cuando se efectúa la obliteración de várices endoscópicas a través de escleroterapia o ligadura de várices, una cantidad considerable de flujo sanguíneo debe ser redistribuido hacia la microcirculación gástrica. Esta redistribución puede llevar a la aparición o empeoramiento de gastropatía portal.28 Aunque aún no se ha determinado el mecanismo exacto, la escleroterapia y la ligadura de várices parecen alterar el flujo colateral, lo que aumenta la frecuencia de gastropatía portal. Es importante destacar que a pesar de que la ligadura de várices se asoció con un aumento en la frecuencia de gastropatía portal hipertensiva, en la revisión hecha este aumento no provocó un número significativo de casos de sangrado por esta causa.
Los resultados de este trabajo muestran que el esquema terapéutico evaluado puede ser útil y seguro en pacientes cirróticos con várices esofágicas, como indicación de profilaxis secundaria del sangrado. Este acontecimiento debe esperarse en pacientes con mayor grado de disfunción hepatocelular. La causa de la cirrosis no parece ser un factor que influya en la probabilidad de que ocurra esa eventualidad. Sin embargo, es necesario continuar estudiando el tema en un número más amplio de pacientes, preferentemente mediante estudios multicéntricos.
REFERENCIAS BIBLIOGRÁFICA
1. Thalheimer U, Triantos C, Goulis J, Burroughs AK. Management of varices in cirrhosis. Expert Opinion on Pharmacotherapy. 2011;12:5:721-35.
2. Berzigotti A, Gilabert R, Abraldes JG, Nicolau C, Bru C, Bosch J. Noninvasive prediction of clinically significant portal hypertension and esophageal varices in patients with compensated liver cirrhosis. Am J Gastroenterol. 2008;103(5):1159-67.
3. Sharma BC, Sarin SK. Hepatic venous pressure gradient in cirrhosis: role in variceal bleeding, non-bleeding complications and outcome. Asian J Surg. 2006;29(3):113-9.
4. Kim MY, Baik SK, Lee SS. Hemodynamic alterations in cirrhosis and portal hypertension. Korean J Hepatol. 2010;16(4):347-52.
5. Rossi V, Cales P, Burtin P, Charneau J, Person B, Pujol P, et al. Prevention of recurrent variceal bleeding in alcoholic cirrhotic patients: prospective controlled trial of propranolol and sclerotherapy. J Hepatol. 1991;12(3):283-9.
6. Pugh R, Murray-Lyon I, Dawson J, Pietroni M, Williams R. Transection of the oesophagus for bleeding oesophageal varices. Br J Surg. 1973;60:646-9.
7. Paquet KJ, Raschke E, Esser G, Figge H. Management of acute bleeding from gastroesophageal varices. J Cardiovasc Surg. 1971;12(2):152-5.
8. McCormack T, Rose J, Smith P, Johnson A. Perforating veins and blood flow in esophageal varices. Lancet. 1983;2:1442-4.
9. Sarin SK, Kumar A. Gastric varices: profile, classification and management. Am J Gastroenterol. 1989;84:1244-9.
10. de Franchis R; Baveno V Faculty. Revising consensus in portal hypertension: report of the Baveno V consensus workshop on methodology of diagnosis and therapy in portal hypertension. J Hepatol. 2010;53(4):762-8.
11. García-Pagán JC, De Gottardi A, Bosch J. Review article: the modern management of portal hypertension-primary and secondary prophylaxis of variceal bleeding in cirrhotic patients. Aliment Pharmacol Ther. 2008; 28(2):178-86.
12. Villanueva C, Balanzó J. Variceal bleeding: pharmacological treatment and prophylactic strategies. Drugs. 2008;68(16):2303-24.
13. Gómez Senent S, Martín Arranz M, Froilán Torres C, Manceñido Marcos N, Martín Chavarri S, Carrión Alonso G, et al. Profilaxis secundaria mediante ligadura con bandas elásticas en varices esofagogástricas. Gastroenterol Hepatol. 2006;29(6):323-6.
14. Ytting H, Moller S, Henriksen JH, Larsen K, Bendtsen F. Prognosis in patients with cirrhosis and mild portal hypertension. Scand J Gastroenterol. 2006;41(12):1446-53.
15. García-Pagán JC, Reverter E, Abraldes JG, Bosch J. Acute Variceal Bleeding. Semin Respir Crit Care Med. 2012;33(01):46-54.
16. Lebrec D. Pharmacologic prevention of variceal bleeding and rebleeding. J Hepatol. 1993;17(Suppl. 2):29-33.
17. D´Amico G, Pagliaro L, Bosch J. The treatment of portal hypertension: A meta-analytic review. Hepatology. 1995;22:332.
18. Petrasch F, Grothaus J, Mossner J, Schiefke I, Hoffmeister A. Differences in bleeding behavior after endoscopic band ligation: a retrospective analysis. BMC Gastroenterol. 2010;10:5.
19. Harewood GC, Baron TH, Song LM. Factors predicting success of endoscopic variceal ligation for secondary prophylaxis of esophageal variceal bleeding (II). J Gastroenterol Hepatol. 2006;21(1)237-41.
20. Cichoz-Lach H, Celinski K, Slomka M, Kasztelan-Szczerbinska B. Pathophysiology of portal hypertension. J Physiol Pharmacol. 2008;59(Suppl. 2):231-8.
21. Blei AT, Mazhar S, Davidson CJ, Flamm SL, Abecassis M, Gheorghiade M. Hemodynamic evaluation before liver transplantation: insights into the portal hypertensive syndrome. J Clin Gastroenterol. 2007;41(Suppl. 3):323-9.
22. Gulzar GM, Zargar SA, Jalal S, Alaie MS, Javid G, Suri PK. Correlation of hepatic venous pressure gradient with variceal bleeding, size of esophageal varices, etiology, ascites and degree of liver dysfunction in cirrhosis of liver. Indian J Gastroenterol. 2009;28(2):59-61.
23. Benedeto-Stojanov D, Nagorni A, Bjelakovic G, Stojanov D, Mladenovic B, Djenic N. The model for the end-stage liver disease and Child-Pugh score in predicting prognosis in patients with liver cirrhosis and esophageal variceal bleeding. Vojnosanit Pregl. 2009;66(9):724-8.
24. Ravipati M, Katragadda S, Swaminathan PD, Molnar J, Zarling E. Pharmacotherapy plus endoscopic intervention are more effective than pharmacotherapy or endoscopy alone in the secondary prevention of esophageal variceal bleeding: a meta-analysis of randomized, controlled trials. Gastrointest Endosc. 2009;70(4):658-64.
25. Singh P, Pooran N, Indaram A, Bank S. Combined ligation and sclerotherapy versus ligation alone for secondary prophylaxis of esophageal variceal bleeding: a meta-analysis. Am J Gastroenterol. 2002;97(3):623-9.
26. Abid S, Jafri W, Hamid S, Salih M, Azam Z, Mumtaz K, et al. Terlipressin vs. octreotide in bleeding esophageal varices as an adjuvant therapy with endoscopic band ligation: a randomized double-blind placebo-controlled trial. Am J Gastroenterol. 2009;104(3):617-23.
27. Kuran S, O?uz D, Parlak E, Asil M, Ciçek B, Kiliç M, Di?ibeyaz S, Sahin B. Secondary prophylaxis of esophageal variceal treatment: Endoscopic sclerotherapy, band ligation and combined therapy-long-term results. Turk J Gastroenterol. 2006;17(2):103-9.
28. Poza Cordon J, Froilán Torres C, Burgos García A, Gea Rodríguez F, Suárez de Parga JM. Endoscopic management of esophageal varices. World J Gastrointest Endosc. 2012;4(7):312-22.
Recibido: 12 de octubre de 2012.
Aprobado: 4 de diciembre de 2012.
Dra. C. Mirtha Infante Velázquez. Hospital Militar Central "Dr. Luis Díaz Soto". Ave. Monumental y Carretera del Asilo. Habana del Este. La Habana, Cuba. Correo electrónico: minfante@infomed.sld.cu