Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Vaccimonitor
versión On-line ISSN 1025-0298
Vaccimonitor v.16 n.2 Ciudad de la Habana Mayo-ago. 2007
Rolando Felipe Ochoa1, Josué Acosta2, Xenia Rosa Ferriol1, Mónica Ginebra1.
1 Instituto Finlay. Centro de Investigación-Producción de Vacunas. Ave 27 No. 19805, e/ 198 y 202.
La Lisa, Ciudad de La Habana. Cuba.
Correo electrónico: ochoa@finlay.edu.cu
2 Centro Nacional de Genética Médica. Playa, Ciudad de La Habana.
El sistema inmune es inmaduro en los recién nacidos, lo que los hace susceptibles a las enfermedades infecciosas, sin embargo, pueden ser parcialmente protegidos por los anticuerpos adquiridos a través de la placenta. Por ello, nos propusimos evaluar la transferencia transplacentaria de anticuerpos contra algunas enfermedades prevenibles por vacunas. Se realizó un ensayo prospectivo, aleatorio, en el binomio madre–recién nacido. Para ello se analizó un total de 96 pares de muestras de suero, tomadas en el salón de preparto y al nacimiento en hospitales de Ciudad de La Habana, durante el año 2004. Se emplearon técnicas inmunoenzimáticas para determinar los niveles de antitoxina tetánica (ATT), antitoxina diftérica (ATD) y anticuerpos contra proteínas de membrana externa del meningococo B (PME), contra el polisacárido capsular del meningococo C (PSC) y contra el polisacárido Vi de Salmonella Typhi. Se detectó un nivel apropiado de ATT, tanto en las madres como en los recién nacidos, predominando los valores correspondientes a la protección de larga duración (>1 UI/mL), con 88,54% y 92,71%, respectivamente. Se observó niveles de ATD inferiores a 0,1 UI/mL, límite para una protección confiable, en el 54,17% y 45,83% de las madres y los recién nacidos. El 90,63% de las madres y el 96,88% de los recién nacidos presentaron concentraciones de anticuerpos contra PME superiores a 2 µg/mL, así como el 38,54% y el 41,67% para anticuerpos contra PSC. La seroprotección contra la Salmonella Typhi (>1 µg/mL) fue de 5,21% y 8,33%, respectivamente. La mayoría de los recién nacidos presentaron títulos superiores de anticuerpos al de sus madres, lo cual demuestra que la transferencia transplacentaria de anticuerpos es un mecanismo eficiente.
Palabras clave: Anticuerpos transplacentarios, vacuna, antitoxina tetánica, antitoxina diftérica, meningococo, Salmonella Typhi.
Introducción
El sistema inmune es inmaduro en los recién nacidos, pero pueden ser parcialmente protegidos por los anticuerpos adquiridos a través de la placenta, de ahí que la inmunización a la embarazada constituya una estrategia fundamental para la protección de los neonatos (1).
Sin embargo, muchos lactantes en los países en desarrollo todavía mueren de tétanos porque sus madres no poseen adecuados niveles de antitoxina tetánica durante el embarazo (2).
La difteria, enfermedad también inmunoprevenible, ha resurgido en los últimos años, afectando principalmente a los adultos que han perdido la inmunidad inducida por vacunas recibidas en la infancia y a los niños no vacunados, tal y como ha sucedido en los estados que surgieron de la antigua Unión Soviética y los países de la Europa Oriental (3).
Por otra parte, los serogrupos B y C de Neisseria meningitidis son responsables de la mayor parte de los casos de la enfermedad meningocócica en Latinoamérica (4) y la fiebre tifoidea es aún un serio problema de salud en los países en desarrollo (5).
La estrategia cubana para el control de estas enfermedades, se apoya en gran medida en el diseño de eficientes programas de inmunización.
A inicios de la década de 1960 comienzan las campañas masivas de vacunación con la vacuna trivalente contra la difteria, tos ferina y tétanos (DPT), la bivalente contra la difteria y el tétanos (DT) y el toxoide tetánico. En 1972 se erradica el tétanos neonatal, como consecuencia de la política inmunitaria con las embarazadas. El último caso de difteria se registra en 1979, y en los años 2004 y 2005 no se detectaron casos de tétanos (6).
Con relación a la enfermedad meningocócica, se habían descrito históricamente tan sólo casos esporádicos y peque-ños brotes, hasta que en 1976 comienza una importante epidemia de magnitud sin precedentes, a predominio del serogrupo C. Una vacunación masiva con una vacuna de polisacárido A/C redujo sustancialmente los casos debidos a ese serogrupo, pero no pudo revertir esta situación, pues la incidencia continuó en ascenso, ahora a expensas del serogrupo B. Ante la magnitud de la epidemia se crea en 1982 un grupo de investigación en el Instituto Finlay, que en tan sólo cinco años logra una vacuna contra los serogrupos B y C de Neisseria meningitidis: VA-MENGOC-BCâ. En 1988 comienza a emplearse, y hasta 1990 se realiza una campaña masiva de inmunización que provocó la erradicación de la epidemia. En 1991 se incorpora al Programa Nacional de Inmunización (6).
La prevención de la fiebre tifoidea en grupos poblacionales con riesgo de la enfermedad requirió inicialmente del empleo de una vacuna de células enteras inactivadas. A partir del año 2002 se emplea una vacuna de polisacárido Vi de Salmonella Typhi, producida también en dicha institución (6).
A pesar de estos logros, deben realizarse nuevos estudios inmunoepidemiológicos atendiendo a la situación existente en otros países y al intercambio actual con la comunidad internacional. Por todo ello, nos propusimos evaluar la transferencia transplacentaria de anticuerpos contra las enfermedades prevenibles por las vacunas seleccionadas y determinar la susceptibilidad de los recién nacidos a estas enfermedades.
Materiales y métodos
Diseño de la investigación
Se realizó un estudio prospectivo, aleatorio, en 96 madres y sus recién nacidos durante el año 2004. La aprobación ética del estudio fue emitida por el Comité correspondiente del Instituto Superior de Ciencias Médicas de La Habana. Se brindó una adecuada información previa y se obtuvo el consentimiento por escrito de ambos padres (6, 7).
Se tomaron en el salón de preparto las muestras de suero de la embarazada y las del recién nacido durante el proceso de corte del cordón umbilical. Las muestras de suero que se obtuvieron fueron identificadas y almacenadas a –20 °C hasta su procesamiento.
Determinación de los niveles de anticuerpos séricos en las madres y los recién nacidos
Se utilizaron ensayos inmunoenzimáticos en fase sólida (ELISA), previamente estandarizados y validados, para la cuantificación de antitoxina tetánica, antitoxina diftérica y anticuerpos contra proteínas de membrana externa de meningococo B (PME) y el polisacárido capsular del meningococo C (PSC), así como anticuerpos contra el polisacárido Vi de Salmonella Typhi (8, 9). La validación, cuantificación e impresión se realizó mediante el paquete de programas ELISA de los Centros para el Control de las Enfermedades (CDC, Atlanta) (GA) (10).
Métodos estadísticos
El cálculo del tamaño de la muestra se basó en las siguientes premisas: Prevalencia cuantificable de anticuerpos del 85%, confiabilidad del 95%, y precisión del 10% (6). El reclutamiento fue adicionalmente aumentado.
Se calculó la media geométrica (MG) y el intervalo de confianza al 95% (IC) de cada distribución de anticuerpos después de la transformación logarítmica. Los resultados se clasificaron según el nivel de anticuerpos. Antitoxinas tetánica y diftérica: < 0,1 UI/mL niveles de antitoxina no adecuados para conferir protección, ³ 0,1 UI/mL niveles de antitoxina para una protección confiable, y > 1,0 UI/mL protección confiable de larga duración (2, 4, 8, 9). Anticuerpos contra PME y PSC: > 2 µg/mL nivel de corte considerado protector (8, 9). Anticuerpos contra el polisacárido Vi: Se consideró 1 µg/mL como el valor protector (5).
El índice de transferencia se definió como la relación entre los niveles de anticuerpos de los recién nacidos y sus madres. Se consideró como eficiente un índice > 1.
Para los análisis estadísticos se empleó la prueba t de Student y la prueba exacta de Fisher. En todos los casos se consideró un error de primer tipo µ=0,05 (6).
Resultados
Se detectaron adecuados niveles de antitoxina tetánica. La mayor parte de las madres y los recién nacidos presentaron valores correspondientes a la protección de larga duración (Tabla 1).
Para la antitoxina diftérica se observaron niveles no adecuados (<0,1 UI/mL) en el 54,17% de las madres y el 45,83% de los recién nacidos (Tabla 2).
Tabla 1. Distribución de anticuerpos antitoxina tetánica.
| UI/mL | Madres (96) | Recién Nacidos (96) | ||
| n | % | n | % | |
| <0,1 | 0 | 0 | 0 | 0 |
| ³0,1 | 96 | 100 | 96 | 100 |
| >1 | 85 | 88,54 | 89 | 92,71 |
| MG | 3,260 | 4,688 | ||
| IC 95 % | 2,705 – 3,928 | 3,873 – 5,674 | ||
MG: Media Geométrica
IC 95 %: Intervalo de Confianza al 95 %
Tabla 2. Distribución de anticuerpos antitoxina diftérica.
| UI/mL | Madres (96) | Recién Nacidos (96) | ||
| n | % | n | % | |
| <0,1 | 52 | 54,17 | 44 | 45,83 |
| ³0,1 | 44 | 45,83 | 52 | 54,17 |
| >1 | 0 | 0 | 1 | 1,04 |
| MG | 0,085 | 0,102 | ||
| IC 95 % | 0,069 – 0,106 | 0,082 – 0,126 | ||
MG: Media Geométrica
IC 95 %: Intervalo de Confianza al 95 %
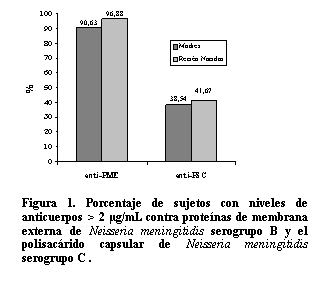
La mayor parte de los sujetos estudiados tenían anticuerpos protectores contra las PME (> 2 µg/mL). Se detectaron menores niveles de anticuerpos contra el PSC (Figura 1).
Se demostró insuficiente seroprotección contra la fiebre tifoidea, tanto en las madres como en los recién nacidos (Figura 2).
La media geométrica de los anticuerpos estudiados fue siempre mayor en los recién nacidos (p < 0,001) (Tablas 1-4), sin embargo, no se detectaron diferencias (p > 0,05) cuando los resultados se evaluaron según los niveles de anticuerpos protectores definidos en cada caso (Tablas 1, 2), Figuras 1, 2).
 | 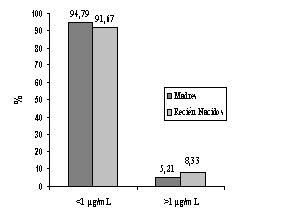 |
| Figura 2. Tasas de seroprotección contra fiebre tifoidea. |
Tabla 3. Anticuerpos IgG contra proteínas de membrana externa de Neisseria meningitidis serogrupo B y el polisacárido capsular de Neisseria meningitidis serogrupo C.
| µg/mL | Anti-PME | Anti-PSC | ||
| Madres (96) | R Nacidos (96) | Madres (96) | R Nacidos (96) | |
| MG | 4,497 | 5,916 | 1,591 | 2,025 |
| IC 95 % | 3,905-5,179 | 5,192-6,741 | 1,224-2,069 | 1,570-2,613 |
IC 95 %: Intervalo de Confianza al 95 %
Tabla 4. Anticuerpos IgG contra el polisacárido Vi de Salmonella Typhi.
| µg/mL | Anti-Vi | |
| Madres (96) | Recién Nacidos (96) | |
| MG | 0,349 | 0,422 |
| IC 95 % | 0,281-0,434 | 0,337-0,528 |
IC 95 %: Intervalo de Confianza al 95%
Tabla 5. Binomio madre –recién nacido con índice de transferencia de anticuerpos eficiente.
| Antitoxina tetánica | Antitoxina diftérica | Anti-PME | Anti-PSC | Anti-Vi | |
| Proporción | 0,81 | 0,66 | 0,81 | 0,76 | 0,69 |
| IC 95% | 0,72-0,88 | 0,56-0,74 | 0,72-0,88 | 0,67-0,84 | 0,60-0,77 |
La transferencia transplacentaria de anticuerpos fue eficiente, la mayor parte de los recién nacidos presentaron niveles superiores a los de sus madres (p<0,001) (Tabla 5).
Discusión
La antitoxina tetánica transferida de la madre al feto protege al recién nacido contra el tétanos neonatal (1, 2, 8, 9). Esta enfermedad ha desaparecido en Cuba gracias al establecimiento de la vacunación de las gestantes, con el objetivo de garantizar elevados niveles de inmunidad en los recién nacidos, lo que se corrobora con nuestros resultados. Sin embargo, se detectaron niveles insuficientes de antitoxina diftérica, lo que podría incrementar el riesgo de infección (3, 8, 9). Consideramos que el nivel de inmunidad antidiftérica debe declinar en la adolescencia, teniendo en cuenta el Esquema Cubano de Inmunización que contempla el toxoide diftérico en las vacunas combinadas utilizadas durante los dos primeros años de vida y un único refuerzo con DT a los 6 años de edad. Los adultos no tienen tampoco la posibilidad de refuerzos a través de infecciones subclínicas al desaparecer esta enfermedad en nuestro país, por todo ello, la probabilidad de poseer anticuerpos debe disminuir progresivamente con la edad.
Una respuesta de larga duración inducida por la vacuna antimeningocócica VA-MENGOC-BCâ pudiera explicar los niveles de anticuerpos contra las PME y el PSC (11, 12), aunque no puede descartarse la inmunidad natural en portadores de Neisseria meningitidis. Sin embargo, el meningococo C no se ha aislado en Cuba en los últimos años (12, 13). La reactividad cruzada con el polisacárido capsular de la Escherichia coli K92 tampoco puede ser rechazada (9).
La fiebre tifoidea no es endémica en Cuba, y hasta el año 2000 se empleó en el programa de inmunización una vacuna de células completas, de elevada reactogenicidad e insuficiente inmunogenicidad. Una nueva vacuna de polisacárido Vi de Salmonella Typhi (vax-TyViâ) está introduciéndose paulatinamente en escolares cubanos a partir del año 2002 (14). Esta situación pudiera explicar la baja tasa de seroprotección en la población estudiada.
La placenta humana regula la transferencia de anticuerpos de forma selectiva. No hay un criterio unánime sobre el nivel de anticuerpos que se alcanza; algunos autores han reportado valores superiores en los recién nacidos, y otros iguales e incluso inferiores a los de sus madres (15, 16). En nuestra investigación, la mayor parte de los recién nacidos presentaron valores superiores, lo que habla a favor de una excelente transferencia transplacentaria de anticuerpos contra las enfermedades prevenibles por las vacunas estudiadas, aunque en algunos casos no haya sido suficiente para conferir protección debido a los bajos niveles encontrados en sus progenitoras, por lo que, además del toxoide tetánico empleado en la inmunización de las gestantes, sugerimos añadir el toxoide diftérico, así como valorar otros inmunógenos vacunales.
Conclusiones
o La transferencia transplacentaria de anticuerpos es un mecanismo eficiente, su magnitud depende de los niveles de anticuerpos maternos.
o Algunos recién nacidos no están completamente protegidos contra las enfermedades prevenibles por las vacunas analizadas.
Referencias
1. Vicari M, Dodet B. Protection of newborns through maternal immunization. Vaccine 2003; 21:3351.
2. Vandelaer J, Birmingham M, Gasse F, Kurian M, Shaw C, Garnier S. Tetanus in developing countries: an update on the maternal and neonatal tetanus elimination initiative. Vaccine 2003; 21:3442-45.
3. Vitek CR, Diphtheria. Curr Top Microbiol Immunol 2006;304:71-94.
4. Stephens DS. Conquering the meningococcus. FEMS Microbiol Rev 2007; 31:3-14.
5. Cooke FJ, Wain J. The emergence of antibiotic resistance in typhoid fever. Travel Med Infect Dis 2004; 2:67-74.
6. Ochoa R. Inmunoepidemiología y Estrategias de Vacunación. Ciudad de La Habana: Finlay Ediciones; 2005.
7. World Medical Association Declaration of Helsinki. Ethical Principles for Medical Research Involving Human Subjects. Bull World Health Organ 2001;79(4):373-74.
8. Ochoa R, Ferriol X, Torres JC, Ginebra M, Céspedes A, Izquierdo L, et al. Evaluación simultánea de la inmunidad contra enfermedades prevenibles por vacunas. Saludarte 2005; 4(2):114-28.
9. Ochoa R. Sistemas ELISA en ensayos clínicos de vacunas y estudios seroepidemiológicos. Tesis presentada en opción al grado de Doctor en Ciencias Médicas. Ciudad de La Habana. Instituto Superior de Ciencias Médicas de La Habana; 2002.
10. Plikaytis BD, Carlone GM, Turner SH, Gheesling LL, Holder PF. Program ELISA [computer program] MS-DOS version. Centers for Disease Control. Atlanta (Ga); 1993.
11. Camaraza M, Martínez I, Ochoa R, Arnet A, Sotolongo F, Hernández D, et al. Respuesta de anticuerpos inducidos por la vacuna antimeningocócica cubana VA-MENGOC-BC frente a la cepa de Neisseria meningitidis B:4:P1.19,15 en adolescentes después de 12 años de inmunizados. VacciMonitor 2006;15(3):1-4.
12. Camaraza M, Ochoa R, Arnet A, Sotolongo F, Martínez I, Cuevas I, et al. Inmunogenicidad inducida por la vacuna antimeningocócica VA-MENGOC-BCâ contra la cepa de N meningitidis ATCC C11 en adolescentes después de 12 años de vacunados. Rev Cubana Med Trop 2004;56(1):26-30.
13. Martínez I, Sierra G, Núñez N, Iaquierdo L, Climent Y, Mirabal M. Caracterización de cepas de Neisseria meningitidis aisladas de portadores en Cuba durante 20 años. Rev Cubana Med Trop. [en línea]. Mayo-Agosto 2006 [citado 28 Agosto 2007]; 58(2). URL disponible en: http://www.scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0375-07602006000200005&lng=es&nrm=iso. ISSN 0375-0760.
14. Ochoa Azze RF, Martínez JC, Ginebra M, Ferriol X, Rodríguez V, Sotolongo FT. Immunogenicity of a new Salmonella Typhi Vi polysaccharide vaccine –vax-TyViâ– in Cuban school children and teenagers. Vaccine 2003; 21:2758-60.
15. Durbaca S. Anti tetanus and anti diphtheria immunity in newborns. Roum Arch Microbiol Immunol 1999;58:267-72.
16. Malek A. Ex vivo human placenta models: transport of immunoglobulin G and its subclasses. Vaccine 2003; 21:3362-4.
Evaluation of antibodies against vaccine-preventable diseases in mother–newborn pair in Havana City hospitals
Abstract
At birth, the immune system is still immature, that is why newborns are susceptible to infectious diseases. Nonetheless, newborns are partially protected by maternal antibodies. For that reason, transplacental transference of antibodies against some vaccine-preventable diseases. A prospective, randomized study was carried out in 96 mothers and their newborns. Serum samples were taken from the pregnant women before delivery in Havana City hospitals during 2004 and from the newborns in the delivery room. Immunoenzimatic assays were used for the quantitative determination of tetanus and diphtheria antitoxin, antibodies to meningococcus B outer membrane proteins (OMP), antibodies to meningococus C capsular polysaccharide (CSP), and antibodies to Vi polysaccharide of Salmonella Typhi. Suitable levels of tetanus antitoxin were found in mothers and newborns. The long-term protection levels (>1 IU/mL) were shown in 92.71% of newborns, and 88.54% of their mothers. Non-reliable levels of diphtheria antitoxin (<0.1 IU/mL) were found in 54.17% and 45.83% of mothers and newborns, respectively. Antibodies to OMP above 2 µg/mL were detected in 90.63% and 96.88% of mothers and newborns, and the 38.54% and 41.67% had proper antibodies against CSP. Seroprotection rates (>1 µg/mL) against Salmonella Typhi were 5.21% and 8.33%, respectively. Most of newborns showed higher antibody levels than that of their mothers, therefore the transplacental passage of antibodies is an efficient mechanism.
Keywords: Transplacental antibodies, vaccine, tetanus antitoxin, diphtheria antitoxin, meningococcus, Salmonella Typhi.
Recibido: Junio de 2007 Aprobado: Agosto de 2007














