INTRODUCCIÓN
En diciembre de 2019 un brote de neumonía de causa desconocida se presentó en Wuhan, provincia de Hubei, China, y se extendió rápidamente en todo el país en solo un mes.1 Estos pacientes estaban epidemiológicamente vinculados a un mercado mayorista de mariscos.1,2 El patógeno de esta enfermedad fue confirmada por métodos de biología molecular como un nuevo coronavirus, el 7 de enero de 2020, 3 cuando el mundo fue informado de este nuevo patógeno que inicialmente fue llamado nuevo coronavirus 2019 (2019-nCoV) por la Organización mundial de la Salud (OMS), y posteriormente el Comité Internacional de Taxonomía de estudio para coronavirus cambio su nombre, por el de síndrome respiratorio agudo grave por coronavirus-2 (SARS-CoV-2) basado en su filogenia, taxonomía y práctica, y la enfermedad que ocasiona fue nombrada coronavirus disease 2019 (COVID-19).4
El 30 de enero de 2020, la OMS declaró el brote de COVID-19 como la sexta emergencia de salud pública de interés internacional, por lo tanto, este brote constituye un riesgo para la salud pública, de propagación internacional y que requiere una coordinación de los sistemas de salud de todo el mundo.5
Los coronavirus se denominan así por los picos en forma de corona en su superficie, pertenecen a la familia coronaviridae dentro del orden nidovirales. Los coronavirus infectan ampliamente a los vertebrados, incluidos humanos, pájaros, murciélagos, serpientes, ratones y otros animales salvajes.6 A mediados de la década de 1960, se conocían siete coronavirus que infectaban los humanos (HcoV).7
En un estudio realizado, dos tipos de HCoV (229E, OC43) representaron aproximadamente del 15 % al 29 % de los patógenos de las vías respiratorias superiores, que incluyen: el virus de la influenza, el rinovirus, virus de parainfluenza, estreptococos del grupo A, B y el virus sincitial respiratorio, con virulencia relativamente baja en humanos.8 Otro estudio en adultos estimó que el coronavirus causa aproximadamente el 15 % de los resfriados comunes,9 pero dos tipos de coronavirus tienen una patogenicidad diferente y conducen a una mayor tasa de mortalidad en poblaciones humanas: en 2002-2003, el síndrome de dificultad respiratoria grave aguda (SARS-CoV), con más de 8000 pacientes infectados y 774 muertes,10 y en septiembre de 2012, el síndrome respiratorio del oriente medio (MERS-CoV), que informó 2 494 casos de infección, con 858 muertes.11
En esta revisión se presenta una descripción general de la información disponible actualmente sobre: la patogénesis, epidemiología, presentación clínica, diagnóstico y tratamiento de la COVID-19 hasta el 31 mayo de 2020.
MÉTODOS
Se realizó una búsqueda sistemática de publicaciones en la base de datos Medline-PubMed; se utilizaron los términos: COVID-19, COVID-2019, o severe acute respiratory syndrome coronavirus 2, 2019-nCoV, SARS-CoV-2, 2019nCoV, Wuhan y coronavirus. Se seleccionaron artículos originales y de revisión, revisiones sistemáticas y metanálisis escritos en inglés, los cuales fueron publicados entre diciembre de 2019 y el 27 de mayo de 2020. Estos artículos hacían una revisión de las características virológicas, epidemiológicas, y clínicas del COVID-19.
DESARROLLO
La búsqueda mediante los términos seleccionados arrojó un resultado de 133 publicaciones en PubMed-Medline; se descartaron 3 por duplicado. Se revisaron todos los resúmenes y se descartaron 5 que no contaban con el texto completo, 2 porque tenían resumen en inglés pero el texto completo en chino, y 82 porque no correspondían a una revisión. Finalmente, se seleccionaron 42 publicaciones que fueron consideradas de transcendencia, para describir las características clínico patológicas del COVID- 19 para la redacción de este manuscrito (Figura 1).

Figura 1 Publicaciones de PubMed de transcendencia, para describirlas características clínico patológicas del COVID- 19.
Hay evidencias de dos episodios en los últimos veinte años, en los cuales dos tipos de coronavirus de origen animal han infectado a humanos con enfermedad grave. El primer caso fue en 2002- 2003, cuando un nuevo coronavirus del género β, con origen en los murciélagos, cruzó a los humanos, a través del gato de civeta como intermediario en la provincia china de Guangdong. Este virus fue designado como SARS-CoV, afectó a 8 422 personas principalmente en Hong Kong (China), y causó 916 muertes (tasa de mortalidad del 11 %).12 Casi una década después, en el año 2012, en Arabia Saudita, surgió el coronavirus MERS-CoV, también de origen en murciélagos, y con transmisión a humanos a través de camellos y dromedarios como el anfitrión intermedio, afectó a 2 494 personas y causó 858 muertes (tasa de mortalidad del 34 %).13
En el último y actual episodio de aparición de brote de coronavirus, desde el 18 de diciembre de 2019 hasta 29 de diciembre de 2019, cinco pacientes fueron hospitalizados con neumonía de causa desconocida y uno de estos pacientes falleció. Los casos se vincularon al mercado mayorista de mariscos Huanan y al mercado de sur de China (en inglés Huanan Seafood Wholesale Market, South China Seafood Market), en Wuhan, provincia de Hubei, China, con una población de 11 millones de habitantes en diciembre de 2019.14
En respuesta al brote, el Centro Chino para Control y Prevención de Enfermedades, envió un equipo de respuesta rápida establecido después del brote de SARS-CoV; los investigadores tomaron muestras en 15 pacientes de líquido pulmonar, sangre e hisopado faríngeo para realizar pruebas de laboratorio. Estas pruebas de laboratorio estaban dirigidos a patógenos conocidos como: el SARS-CoV, MERS-CoV, influenza, influenza aviar, adenovirus y otros patógenos respiratorios comunes. El 31 de diciembre de 2019, China notificó el brote a la Organización Mundial de la Salud, y el 1 de enero de 2020, el mercado de marisco Huanan estaba cerrado. El 7 de enero el virus fue identificado como un coronavirus con más del 95 % de homología con el coronavirus del murciélago, y más del 70 % de similitud con el SARS-CoV. Aunque el SARS-CoV-2 se originó a partir de murciélagos, estos no están disponibles para la venta en el mercado de mariscos,15 por lo que el intermediario animal a través del cual cruzó hacia los humanos es incierto, se presume pudieran ser los pangolines.
Los coronavirus son virus de ácido ribonucleico (ARN) monocatenario, con un tamaño que va desde 60 nm a 140 nm de diámetro, con proyecciones como espiga en su superficie, que le dan una apariencia de corona bajo el microscopio electrónico, de ahí el nombre coronavirus. Su genoma varía de 26 000 a 37 000 bases; este es el genoma más grande conocido entre los virus de ARN.16) Hay genes accesorios intercalados dentro de los genes estructurales,17 algunos de los cuales han demostrado desempeñar un importante papel en la patogénesis viral.18 Está envuelto por una nucleocapside cubierta de una bicapa lipídica, que contiene la proteína S (spike) que es responsable de la unión al receptor, y posterior entrada viral en las células huésped; las proteínas M y E juegan un papel importante en el ensamblaje viral, y la proteína N es necesaria para la síntesis del ARN.19
Los diversos coronavirus de origen animal experimentan mutaciones que pueden ser altamente patogénicas y potencialmente mortales para los humanos.7 Para el SARS-CoV, se estimó que la tasa de mutación en el genoma es 0,80-2,38×103 sustituciones de nucleótidos por sitio por año, que son similares a la de otros virus de ARN.20 Esta mutación la experimentan ya sea dentro de la especie huésped o al saltar de una especie a otra. Estos cambios tienen el potencial de conducir a variantes que tienen un alto potencial patogénico cuando se transmiten a los humanos.21
Se analizó el genotipo de SARS-CoV-2 en diferentes pacientes de varios provincias de China, y se descubrió que este había mutado en diferentes pacientes, aunque en menor el grado que la mutación de la gripe aviar H7N9.22 Tang y colaboradores23 realizaron un análisis genético de 103 genomas de SARS-CoV-2, y clasificaron dos tipos prevalentes: el tipo L (~ 70 %) y tipo S (~ 30 %); las cepas derivadas del tipo S son evolutivamente más agresivas y contagiosas.
Los coronavirus (CoV) se dividen en cuatro géneros: α-CoVs, β-CoVs, γ-CoVs y δ-CoVs,24 de los cuales: α- y los β-CoV pueden infectar mamíferos, y los γ-CoVs y δ-CoVs pueden infectar a las aves y también podría infectar a los mamíferos.25) Hasta ahora se ha encontrado que siete tipos de coronavirus infectan a los humanos y causan enfermedades respiratorias, de los cuales, cuatro son comunes en humanos (HCoV): HCoV-229E, HCoV-OC43, HCoV-NL63 y HCoV-HKU1 y generalmente llevan a enfermedad respiratoria alta auto limitada.
Se conocen los dos primeros desde la década de 1960; posteriormente, en 2002 se identificó el SARS-CoV, y en 2004 y 2005 se identificaron el HCoV-NL63 y HcoV-HKU1, respectivamente.26 En 2012 se aisló el MERS-CoV, que tiene características similares al SARS-CoV ya que ambos pueden ocasionar neumonía y síndrome de dificultad respiratoria grave en humanos,27 con una tasa de letalidad de 35,5 % y 10 %, respectivamente.28 El SARS-CoV-2 fue aislado recientemente de células epiteliales de la vía aérea humana en enero de 2020, e identificado como un nuevo miembro de β-CoVs.14
La Organización Mundial de la Salud (OMS) ha clasificado el SARS-CoV-2 como un β CoV del grupo 2B.29 Diez secuencias de su genoma obtenidas de un total de nueve pacientes mostraron 99,98 % de concordancia.30 La secuencia genética del SARS-CoV-2 mostró más del 80 % de identidad con el SARS-CoV y el 50% con el MERSCoV,30,31 y tanto el SARS-CoV como el MERS-CoV se originan en los murciélagos.32) El SARS-CoV-2 representa el séptimo miembro de la familia de los coronavirus que infecta a los humanos y ha sido clasificado bajo la subfamilia ortocoronavirinas, subgénero sarbecovirus.33
Los coronavirus que son de origen zoonótico, pueden convertirse en una cepa que puede infectar a seres humanos y conducir a enfermedades fatales.7 Se requiere de un animal intermediario que sirva como hospedero en el cual se produce recombinación genética y mutación del virus.34 Las espigas de la corona del virus llamada glucoproteína S, permiten al virión la unión a la membrana celular del huésped.35
El SARS-CoV utiliza su proteína S en la superficie celular asociada a una serina proteasa 2 transmembrana36 y catepsina,37 a través del receptor de la enzima convertidora de angiotensina tipo 2 (ACE2),38 para permitir la invaginación del virus en la membrana celular de los neumocitos tipo 2 y las células epiteliales ciliadas bronquiales.31 El MERS-CoV usa la dipeptidil peptidasa 4, una glucoproteína transmembrana para infectar los neumocitos tipo 2 y células epiteliales bronquiales no ciliadas.39
En general, los coronavirus se replican en células epiteliales de las vías respiratorias y células entéricas, lo que conduce a cambios citopáticos.40 Los estudios más recientes aislaron SARS-CoV2 del lavado broncoalveolar de un paciente en Wuhan14 y se ha confirmado que la proteína S del SARS-CoV-2 usa la ACE2, como receptor de entrada celular similar al SARS-CoV.41
La unión de la glucoproteína S de SARS-CoV-2 y el receptor ACE2 es un paso crítico para la entrada del virus.42 Otro estudio mostró que la proteína S, y su unión a la ACE2, es de 10 a 20 veces más eficiente que el del SARS-CoV.43 La glucoproteína S incluye dos subunidades: S1 y S2.44) La S1 determina el rango de tropismo celular con el dominio clave de función, mientras que la S2 media la fusión de la membrana celular del virus por dos dominios en tándem, heptad repite 1 y 2 (HR1, HR2).45
Después de la fusión a la membrana, el genoma viral ARN se libera en el citoplasma, y el ARN no recubierto traduce dos poliproteínas, pp1a y pp1ab,35 las cuales codifican proteínas no estructurales, y forman el complejo de replicación-transcripción (RTC) en vesículas de doble membrana.46 La RTC replica y sintetiza continuamente un conjunto de ARN subgenómicos anidado,47 que codifican proteínas accesorias y proteínas estructurales a través del retículo endoplásmico de Golgi.48 El ARN genómico recién formado, las proteínas nucleocapsídicas y las glicoproteínas de envoltura, se ensamblan y forman brotes de partículas virales. Por último, las vesículas que contienen viriones se fusionan con la membrana plasmática para liberar el nuevo virus.
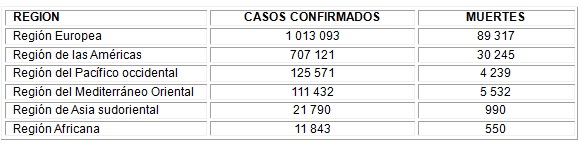
Desde el inicio del brote de la COVID-19 en Wuhan, a finales de diciembre de 2019 y hasta el 31 de marzo de 2020, la OMS declaró la pandemia y confirmó la propagación a 205 países, 750 890 casos fueron confirmados por biología molecular y 36 405 muertes por esta causa.49 Hasta el 16 de abril de 2020, la región geográfica más afectada por la infección por SARS-CoV-2 ha sido Europa con 1 013 093 casos confirmados y 89 317 muertes, y la menos afectada es la región africana con 11 843 casos y 550 muertes.50 (Tabla 1).
La mayoría de los casos informados en Wuhan fueron adultos, aunque todas las edades son susceptibles; se informó una edad media de 55,5 años (15 a 89 años) en tres estudios separados.51 Un hallazgo similar se observó en un estudio que incluyó 4 021 casos confirmados en 30 provincias de China, en los cuales, la edad media fue 49 años, y el 50,7 % de los pacientes tenían edades comprendidas entre 20 y 50 años.52 El equipo de epidemiología de respuesta a emergencias de neumonía por el nuevo coronavirus en China, informó que el 66,7 %, (n: 29 798) de 44 672 casos de COVID-19, estaban entre 20 y 60 años de edad.
Sobre los pacientes ancianos, un estudio mostró que el 14,6 % de los pacientes tenían 65 años,3 mientras que otro estudio mostró que el 15,2 % tenían 70 años. Según el reciente informe del Centro de control de enfermedades de China, el 12 % (n: 5 326) de los pacientes tenían 70 años de edad.53
Respecto a los niños, en un estudio se encontró que el 0,9 % de los pacientes con la COVID-19 tenían entre 0 y 14 años de edad. Otro estudio en China, con 416 pacientes, mostró que el 0,9 % de los pacientes eran menores de 10 años. Con respecto al género, la proporción de hombres varió de 51,4 % a 73,2 %.53,54,55
Según la información actual, la transmisión transplacentaria de mujeres embarazadas a su feto no ha sido descrita. Sin embargo, si se ha descrito la transmisión postnatal a neonatos en contactos con familiares infectados.56
La propagación nosocomial del SARS-CoV-2 es una seria preocupación, la Comisión nacional de salud de China el 14 de febrero de 2020 confirmó la transmisión a trabajadores sanitarios en un 3,8 %. Otros dos estudios mostraron que el 2,1 % (n: 23) y 3,8 % (n: 1 716) de los pacientes eran trabajadores de la salud.53,55 Un estudio en el Hospital de Zhongnan de la Universidad de Wuhan, mostró que el 29 % (n: 40) fue personal médico y el 12,3 % (n: 17) contrajeron la COVID-19 durante la hospitalización.51
El contacto directo con animales intermedios domésticos, o el consumo de animales salvajes, fue la ruta inicial de transmisión del SARS-CoV-2 a los humanos; sin embargo, se desconoce exactamente el mecanismo. La infección entre humanos se transmite a través de grandes gotas generadas durante la tos y estornudos de pacientes sintomáticos, pero también puede ocurrir en personas asintomáticas en la fase de incubación.57,58
Estas gotitas infectadas pueden extenderse uno a dos metros y depositarse en las superficies. El virus puede permanecer viable en las superficies durante días en condiciones atmosféricas favorables, pero se destruye en menos que un minuto con desinfectantes comunes como: el hipoclorito de sodio, peróxido de hidrógeno y otros.59 La infección se puede adquirir por: inhalación de estas gotas, o al tocar superficies contaminadas y luego tocarse la nariz, la boca y los ojos. El virus también está presente en las heces y la contaminación del suministro de agua y, según una hipótesis, pude producirse su posterior transmisión por aerosolización.60
Los estudios han demostrado mayores cargas virales en la cavidad nasal en comparación con la garganta, no hay diferencia en la carga viral entre personas sintomáticas y asintomáticas.61 Los pacientes pueden ser infecciosos mientras los síntomas duran, e incluso en la recuperación clínica, algunas personas pueden actuar como súper-transmisores según el número de personas con las que tenga contacto.60
Se ha encontrado que el SARS-CoV-2 tiene niveles más altos de transmisibilidad y riesgo de pandemia que el SARS CoV. Datos iniciales muestran que el número reproductivo efectivo o básico (R0) calculado para COVID es de 2,2; cada paciente puede, en promedio, contagiar de la infección a más de dos personas sanas. Por otra parte, el R0 de SARS-CoV fue de 2, y para la pandemia por gripe H1N1 en 2009 el R0 fue de 1,3.62 Diferentes estudios de la COVID-19 han estimado que el rango de reproducción básica (R0) está entre 2 y 6,4,63 y algunos estudios informaron un tiempo de duplicación de la epidemia de 1,8 días.64
El período de incubación corresponde al tiempo transcurrido entre el momento de la exposición al agente infeccioso, y la aparición de signos y síntomas de la enfermedad; es esencial conocerlo para el control de infecciones y determinar la duración del aislamiento. Se tomó en su inicio 10 casos y se determinó un período de incubación promedio de 5,2 días (intervalo de confianza del 95 % [IC 95 %], 4,1-7); el percentil 95 de la distribución fue de 12,5 días (IC 95 %, 9,2-18).65 Otro estudio con 125 pacientes indicó que la mediana del período de incubación fue de 4,75 días (rango intercuartil: 3 - 7,2).
Los coronavirus tienen como huésped el murciélago,30 por lo que se considera una enfermedad de origen zoonótico. Se han realizado esfuerzos para buscar el huésped intermedio a través del cual se propagó a los humanos, y se especula que los pangolines pudieran estar vinculados; sin embargo, hasta la fecha no hay certeza de esta teoría.65
En las últimas pautas de las autoridades sanitarias chinas se describieron tres rutas principales de transmisión para la COVID-19:
1) Transmisión de gotas. Se informó que la transmisión ocurre cuando gotitas respiratorias (como se produce cuando una persona infectada tose o estornuda), son ingeridas o inhaladas por individuos cercanos.
2) Transmisión de contacto. Puede ocurrir cuando un sujeto toca una superficie u objeto contaminado con el virus y posteriormente tocar su boca, nariz u ojos.
3) Transmisión por aerosol. Puede ocurrir cuando las gotas respiratorias se mezclan en el aire, en forma de aerosoles, y puede causar infección cuando se inhala una dosis alta de aerosoles en un ambiente relativamente cerrado.66,67
Un estudio también indicó el sistema digestivo como una ruta potencial de transmisión, dado que algunos pacientes tenían molestias abdominales y diarrea; se encontró que el receptor ACE2 se expresó altamente en enterocitos de íleon y colon.68
Datos limitados han demostrado que el ARN viral podría detectarse en el plasma o suero de pacientes con la COVID-19. De los primeros 41 pacientes en la ciudad de Wuhan, se encontró viremia en 6 (15 %), lo que sugiere una muy baja concentración de ARN, sin encontrar diferencia entre casos graves y leves.69 La Asociación americana de bancos de sangre, la administración de drogas y alimentos, conocida como FDA por sus siglas en inglés, y el centro de control de enfermedades de Estados Unidos (CDC) actualmente no recomendaron ninguna acción en la recolección y análisis de sangre, porque no hay datos que sugieran un riesgo de transmisión por transfusión de SARS-CoV-2.70
Hay informes que revelan que hay pacientes infectados asintomáticos con SARS-CoV-2 y que pueden propagar el virus.71 Algunos casos asintomáticos pueden serlo solo al inicio de contraer la enfermedad, y posteriormente desarrollar los síntomas; no está claro si pueden permanecer asintomáticos durante todo el curso de la enfermedad. Se informó que algunas personas con prueba molecular positiva para SARS-CoV-2 estaban afebriles o asintomáticos y eran contagiosos durante el período de latencia.72) La Comisión Nacional de Salud de China identificó que 130 de 166 nuevos infectados (78%) eran asintomáticos.73
Huang y colaboradores3 proporcionaron los primeros informes de las características clínicas de 41 pacientes ingresados en el hospital en Wuhan hasta el 2 de enero de 2020. Los síntomas al inicio de la enfermedad fueron: fiebre (98 %), aunque señalan que solo el 43,8 % de los pacientes tenía fiebre al inicio, tos (76 %), y mialgia o fatiga (44 %). Los síntomas menos comunes fueron: la producción de esputo, dolor de cabeza, hemoptisis y diarrea. La disnea se desarrolló en 22 de 40 pacientes (55 %), y 26 de 41 pacientes (63 %) tenían linfopenia. La mediana del tiempo desde el inicio de los síntomas hasta el primer ingreso hospitalario fue de 7 días, para dificultad respiratoria fue de 8 días, y para el síndrome de dificultad respiratoria aguda (SDRA) fue de 9 días, 12 pacientes desarrollaron SDRA y necesitaron cuidados intensivos, 5 pacientes tenían lesión cardíaca aguda, y 4 pacientes requirieron ventilación mecánica. Al final, 28 pacientes fueron dados de alta y 6 pacientes fallecieron (14,6 %).
En un estudio reciente con 1 099 casos confirmados y hospitalizados, se encontró que las manifestaciones clínicas incluyeron: fiebre (88,7 %), de esta el 30,9 % (286 / 926) tenían entre 37,5-38°C, un 46,9 % (434 / 926) entre 38,1-39,0°C, y 12,3 % (114 / 926) > 39°C, tos (67,8 %), fatiga (38,1 %), expectoración (33,4 %), disnea (18,6 %), dolor de garganta (13,9 %) y dolor de cabeza (13,6 %).55 Además, una parte de los pacientes manifestaron síntomas gastrointestinales, con diarrea (3,8 %) y vómitos (5 %).
Es importante tener en cuenta que hay similitudes en los síntomas entre la COVID-19 y el cuadro clínico producido por el SARS-CoV, como: fiebre, tos seca y disnea;3 sin embargo, la COVID-19 mostró síntomas de las vías respiratorias superiores como: rinorrea, estornudos y dolor de garganta,74 y son infrecuentes los síntomas intestinales como la diarrea.
Los ancianos y los que tienen trastornos subyacentes (hipertensión, enfermedad pulmonar obstructiva crónica, diabetes, enfermedad cardiovascular), desarrollan rápidamente: SDRA, shock séptico, acidosis metabólica difícil de corregir y disfunción de la coagulación, condiciones que llevan a la muerte.3
La enfermedad en neonatos, lactantes y niños se ha informado como leve, en una serie de 34 niños ingresados en un hospital en Shenzhen, China, entre el 19 de enero y el 7 de febrero, con mediana de edad de 8-11 meses, el 91 % eran asintomáticos, y el 9 % tenían enfermedad leve; los síntomas más comunes fueron fiebre (50 %) y tos (38 %).75,76
Aunque los factores de riesgo para la COVID-19 siguen sin estar claros, varios estudios informaron que una proporción significativa de pacientes tenía afecciones subyacentes.3,51,53,54,55 En un estudio con 51 pacientes con COVID-19 el 50,5% tenían enfermedades crónicas, las más frecuentes fueron afecciones cardiovasculares y cerebrovasculares (40,4 %).54
De 1 099 pacientes, el 23,2 % (n: 255) tenían comorbilidades: la hipertensión fue la más común (14,9 %), seguida de la diabetes mellitus (7,4 %).55 Otro estudio también mostró que la hipertensión era la enfermedad subyacente más frecuente (n : 2 683, 12,8 %), seguida por diabetes mellitus (n: 1 102, 5,3 %) y la enfermedad cardiovascular (n: 873, 4,2 %).53 Además, pacientes con síntomas graves tenían más probabilidades de tener comorbilidades que aquellos con enfermedades no graves (37,6 % versus 20,5 %, respectivamente, p < 0,001).55) Se observó una tendencia similar en otro estudio de 138 pacientes hospitalizados con neumonía por SARS-CoV-2, de los cuales, el 46,4 % (n: 64) de los pacientes tenían comorbilidades, y los pacientes en la unidad de cuidados intensivos (UCI) tenían más probabilidades de tener enfermedades subyacentes en comparación con pacientes no UCI (72,2 % versus 37,3 %, p < 0,001).51
En el estudio de Guan,55 con datos de 1 099 pacientes con SDRA en el curso de la COVID-19 de 552 hospitales en 31 provincias, hasta el 29 de enero de 2020, se encontró que al ingreso: el 82,1 % (731/890) de los pacientes tenían linfopenia (< 1,5 × 109/L), y el 36,2 % (315/869) trombocitopenia (< 150 × 109/L). En general, se observó leucopenia en el 33,7 % (330/978) de los pacientes. El 60,7 % (481/793) demostraron niveles elevados de proteína C reactiva (≥10 mg/L). Hubo elevación de niveles de alanina aminotransferasa (> 40 U/L) de 21,3 % (158/741), aspartato aminotransferasa (> 40 U/L) de 22,2 % (168/757), creatina quinasa (≥ 200 U/L) de 13,7 % (90/657) y dímero D (≥ 0,5 mg/L) de 46,4 % (260/560). Los casos graves tenían significativamente más anomalías de laboratorio en comparación con los casos no graves (p < 0,05).
leucopenia y linfopenia, que el tiempo de protrombina y dímero D estuvieron elevados en pacientes ingresados en la UCI, y que los pacientes de la UCI tenían niveles plasmáticos más altos de IL-2, IL-7, IL-10, G-SCF, IP-10, MCP-1, MIP-1α y TNFα, comparado con los que no estaban en la UCI.
Entre los biomarcadores relacionados con infección, los niveles de procalcitonina han sido normales entre la mayoría de los individuos; los niveles elevados fueron observados en aquellos con infecciones secundarias;3,56 sin embargo, Chen, y colaboradores54 expusieron elevación de la ferritina sérica en 63 % y proteína C reactiva en el 86 % de los pacientes; esto es similar a los hallazgos encontrados en la infección por SARS-CoV.
Se ha informado un aumento de los niveles plasmáticos de citocinas proinflamatorias (tormenta citosinas) como IL1B, IL1RA, IL7, IL8, y que estos se correlacionaron con la gravedad de la enfermedad.77
Basado en los hallazgos de 1 099 casos con la COVID-19: 926 pacientes (84,2 %) presentaron enfermedad leve a moderada, de estos, 173 pacientes (15,7 %) presentaron enfermedad grave: los hallazgos en la radiografía y la tomografía de tórax fueron significativamente más frecuentes en el grupo con enfermedad grave (p < 0,001).55
El 14,7 % de los pacientes tenía una radiografía de tórax anormal, con opacidad en vidrio esmerilado (33,9 %), parcheado local (47,5 %), parcheado bilateral (61,7 %) y anormalidades intersticiales (7,4 %). La sensibilidad diagnóstica de la radiografía es limitada, por lo que no puede ser un estudio único, y es necesario verificar los síntomas clínicos y la detección por biología molecular.55
En el mismo estudio, 840 pacientes (76,4 %) tenían anormalidades neumónicas en la tomografía de tórax, pero el 23,9 % de los casos graves no tuvo hallazgos en la presentación inicial. La anormalidad más común fue la opacidad en vidrio esmerilado (65,5 %), seguida del sombreado local irregular (48,7 %), y las anormalidades intersticiales (17 %).
El 50,1 % de los pacientes tenían compromiso bilateral.55 Sin embargo, en el estudio de Huang y colaboradores,3 que incluyó 41 pacientes, el 98 % tenían afectación bilateral. Los pacientes que ingresaron a la UCI tenían múltiples áreas de consolidación lobulares y subsegmentarias bilaterales. Los pacientes que no ingresaron a la UCI tenían opacidad en vidrio esmerilado bilateral y áreas subsegmentarias de consolidación.
En el estudio de Chen,54 las imágenes mostraron que el 74 %, de los 74 pacientes estudiados, tenían neumonía bilateral, 18,9 % tenían múltiples opacidades moteadas y en vidrio esmerilado, y un caso presentó neumotórax. En otro estudio que incluyó 138 pacientes, se encontró sombreado irregular, u opacidad en vidrio esmerilado en todos los pacientes.51
En un estudio de la Universidad Sun Yat-Sen se encontró opacidad en vidrio esmerilado en el 56,4 %, y parcheado bilateral en 51,8 % de los pacientes, respectivamente.55 A veces se encontró una morfología redondeada y una distribución pulmonar periférica en regiones subpleurales de ambos pulmones.78,79 El predominio de opacidad en vidrio esmerilado y el compromiso bilateral en el TC de tórax se encuentran de manera consistente en casi todos los estudios.78,80 En contraste, otros tipos de anormalidades, como: cavitación, derrame pleural o adenopatías, son muy poco frecuentes o no se encontraron en ningún estudio.78,81
A medida que progresa la enfermedad, se encuentran con más frecuencia lesiones de: consolidación, opacidad, afectación lobular múltiple bilateral y áreas subsegmentarias de consolidación, franjas fibrosas amplias, y nódulos sólidos.3,82 Los pulmones de los pacientes de edad avanzada mostraron imágenes más difusas y extensas que los pacientes más jóvenes.68 Por el contrario, los signos de mejoría mostraron franjas fibrosas pequeñas, y resolución de las opacidades en vidrio esmerilado.80,83
Los primeros casos de SARS-CoV-2 se identificaron como una neumonía de etiología desconocida, que se definió como una enfermedad de etiología desconocida que cursaba con: fiebre, evidencia radiográfica de neumonía, recuento de leucocitos bajo o normal y ausencia de mejoría o empeoramiento de los síntomas después de tres a cinco días de tratamientos antimicrobianos, según las pautas clínicas estándar.84
Se considera un caso sospechoso a un individuo con: fiebre, odinofagia y tos, que tiene antecedente de contacto con personas infectadas por SARS-CoV-2, o viajes a áreas de transmisión local persistente.
Un caso confirmado se hace por la detección molecular del virus. Se considera que la prueba de oro es la detección del ácido nucleico en la muestra de hisopados nasales y de garganta u otras muestras del tracto respiratorio por reacción en cadena de polimerasa en tiempo real (RT-PCR). Este diagnóstico se confirma por la secuenciación de genes virales con técnicas de secuenciación de próxima generación (NGS).72,85) Es posible detectar el virus en el plasma de casos con infección grave por SARS-CoV2,86 y en pocos casos se ha informado el virus en las heces.87
El diagnóstico diferencial incluye todos los tipos de infecciones virales de vías respiratorias, como: influenza, parainfluenza, virus sincitial respiratorio, adenovirus, organismos atípicos como micoplasma, clamidia e infecciones bacterianas; no es posible diferenciar la COVID-19 de estas infecciones a través de la clínica o de pruebas de laboratorio de rutina.72
Dada la falta de una terapia antiviral efectiva contra la COVID-19, basada en la experiencia contra la epidemia SARS-CoV y MERS-CoV, se han reutilizado algunas estrategias de tratamiento,88 medicamentos antivirales inhibidores de la neuraminidasa (oseltamivir), y otros como: aciclovir y ribavirina, pero no han resultado útiles y no se recomiendan para el tratamiento de la COVID-19.51,89
En la experiencia con la infección por SARS-CoV y MERS-CoV, los corticosteroides sistémicos como la metilprednisolona no redujeron la mortalidad,90,91 y podrían haber estado asociados con retraso en negativización de ARN viral, como sucedió en la infección por MERS-CoV con pacientes críticamente enfermos.90) El tratamiento con corticosteroides tempranos podría estar asociado con una mayor carga posterior de ARN viral en plasma. Es importante tener en cuenta los efectos adversos como la psicosis y la diabetes asociadas a corticosteroides, que se observaron en el tratamiento del SARS-CoV.92
En la COVID-19 se administraron corticosteroides en 18,6 % a 44,9 % de pacientes, para controlar la respuesta inflamatoria causada por el SARS-CoV-2 en 4 grandes estudios iniciales.3,51,54,55) Se utilizaron dosis bajas de corticosteroides para tratar a los pacientes ante un posible beneficio de reducir la lesión pulmonar inducida por la inflamación, basado en algunas directrices chinas que recomiendan la corticoterapia a corto plazo con dosis bajas a moderadas en el SDRA en el curso de la COVID-19;93 sin embargo, en la actualidad, la OMS basada en un consenso internacional, no ha aprobado su uso, por lo que tal tratamiento no se recomienda a menos que se indique por otras razones.94,95 Pautas detalladas para el enfoque de cuidados críticos para la COVID-19 han sido publicadas por la OMS.91
La remdesivir (GS-5734) es una adenosina análogo de nucleótidos que muestra actividad antiviral contra varios virus ARN; es un medicamento antiviral desarrollado para el tratamiento del virus ébola. Su eficacia es la que tiene más evidencia en la literatura hasta la fecha, y parece ser la droga más prometedora. Un estudio in vitro demostró que podría interferir con la polimerasa NSP12,102 y se han realizado varios estudios de farmacocinética para determinar la concentración efectiva del 50-90 %.96,97 El primer caso en los Estados Unidos (USA) mostró una respuesta clínica exitosa con remdesivir, una reducción de la carga viral a la hora de su administración.87 Sin embargo, un ensayo clínico que compara la remdesivir contra placebo en pacientes adultos con afectación grave por COVID-19, realizado entre el 6 de febrero de 2020 y el 12 de marzo de 2020, con 237 pacientes inscritos y asignados al azar (158 a remdesivir y 79 a placebo), encontró que el uso de remdesivir no se asoció con una diferencia en el tiempo de mejoría (HR 1,23 [IC 95 % 0,87-1,75]). Aunque no es estadísticamente significativo, los pacientes que recibieron remdesivir tuvieron un tiempo más rápido para la mejoría clínica que aquellos que recibieron placebo entre pacientes con duración de los síntomas de 10 días o menos (HR 1,52 [0,95-2,43]). Se informaron sucesos adversos en 102 (66 %) de los 155 asignados a remdesivir versus 50 (64 %) de los 78 asignados a placebo. La administración del remdesivir se detuvo temprano debido a los efectos adversos en 18 (12 %) pacientes versus 4 (5 %) pacientes que interrumpieron el placebo temprano.98
La cloroquina es otro fármaco prometedor que se ha utilizado para tratar la malaria99 y tiene efecto contra algunas infecciones virales por un mecanismo de acción aún desconocido; se postula que puede inhibir pasos dependientes del pH en la replicación viral.100 También tiene efectos de inmunomodulación, suprime la producción de TNF-α e IL-6, e inhibe la autofagia, que interfiere en la infección y replicación viral,101 ya había demostrado un importante efecto sobre la infección y propagación por SARS-CoV,102) porque interfiere con la glicosilación celular de los receptores.
La cloroquina se ha estudiado in vitro en células de cultivo infectadas con SARS CoV-2, y se encontró que redujo la entrada del virus a la célula y, en etapas posteriores, una combinación de remdesivir y cloroquina demostró que la cloroquina inhibe eficazmente in vitro el SARS-CoV-2.97 En un estudio reciente, donde se realiza un análisis de registros multinacionales, con 96 032 pacientes (edad media 53,8 años, 46,3 % mujeres) con COVID-19 que fueron hospitalizados, se distribuyeron en dos grupos, 14 888 pacientes estaban en los grupos de tratamiento (1868 recibieron cloroquina, 3783 recibió cloroquina con un macrólido, 3016 recibió hidroxicloroquina, y 6221 recibió hidroxicloroquina con un macrólido) y 81 144 pacientes estaban en el grupo control. De ellos, 10 698 (11, 1 %) pacientes murieron en el hospital. Después de controlar múltiples factores de confusión (edad, sexo, raza, índice de masa corporal, enfermedad cardiovascular subyacente, diabetes, enfermedad pulmonar, tabaquismo, enfermedades inmunosupresoras, y gravedad de la enfermedad basal), cuando se compara con la mortalidad en el grupo control (9,3 %), hidroxicloroquina (18,0 %; HR: 1,33, IC 95 % 1,22-1,45), hidroxicloroquina con un macrólido (23,8 %; HR: 1,44, IC 95 % 1,36-1,53), cloroquina (16,4 %; HR: 1,36, IC 95 % 1,21-1,53), y cloroquina con un macrólido (22, 2 %; HR: 1,36, IC 95 % 1,27-1,46), fueron asociados con un mayor riesgo de mortalidad hospitalaria en comparación con el grupo de control (0,3 %), hidroxicloroquina (6,1 %; HR: 2,36, IC 95 % 1, 93-2,90), hidroxicloroquina con un macrólido (8,1 %; HR: 5,10, IC 95 % 4,10-5, 98), cloroquina (4,3 %; HR: 3,56, IC 95 % 2,76-4,59), y cloroquina con un macrólido (6,5 %; HR: 4,01, IC 85 % 3,34-4,81) asociado independientemente con un mayor riesgo de arritmia ventricular de novo durante la hospitalización. Por estas razones no se puede confirmar un beneficio de la hidroxicloroquina o la cloroquina, cuando se usa solo o con un macrólido, sobre los resultados hospitalarios para la COVID-19. Cada uno de estos regímenes farmacológicos se asoció con una disminución de la supervivencia en el hospital, y con una mayor frecuencia de arritmias ventriculares cuando se usa para el tratamiento de la COVID-19.103 Basada en este estudio, la OMS ha generado una alerta internacional para suspender los estudios clínicos que buscaban determinar la utilidad de la cloroquina.
Los científicos confirmaron previamente que los inhibidores de la proteasa lopinavir y ritonavir, utilizados para tratar infecciones por el virus de inmunodeficiencia humana,104 podrían mejorar el resultado de pacientes MERS-CoV105 y SARSCoV.106 Se ha informado que las cargas virales de β coronavirus de un paciente con la COVID-19 en Corea, disminuyeron significativamente con tratamiento con lopinavir/ritonavir.107 Actualmente, se incluye en el protocolo terapéutico de algunos centros que atienden pacientes con la COVID-19.
La recomendación actual de la OMS,91 respaldada por el concepto emitido por la Comisión Nacional de Salud de la República Popular de China ( versión 6),66 para casos sospechosos y confirmados que requieren hospitalización, están centrados principalmente en el tratamiento de los síntomas y el soporte respiratorio, e incluyen oxigenoterapia, fluidos y administración de antimicrobianos para el tratamiento de infecciones bacterianas secundarias, y la prevención de la disfunción orgánica.
Los regímenes de tratamiento se clasificaron en tres categorías, en dependencia de la gravedad de la enfermedad: 1. leve a moderada: el tratamiento principal es la terapia de soporte,3,82 2. enfermedad grave: el uso de oxigenoterapia por máscara o cánula nasal por alto flujo o ventilación no invasiva. Se requiere una dinámica evaluación de parámetros de oxigenación con oximetría de pulso y evaluación con imágenes de tórax y estudios de laboratorio que tengan valor pronóstico en el curso de la enfermedad, y 3. enfermedad grave que progresa luego de ventilación no invasiva. Se requiere intubación traqueal y ventilación mecánica con o sin posición prono, y eventualmente la oxigenación por membrana extracorpórea, recomendada por la OMS en pacientes con hipoxemia refractaria.91
En la serie de 99 pacientes hospitalizados con la COVID-19, se administró: oxígeno al 76 %, ventilación no invasiva en 13 %, ventilación mecánica en 4 %, oxigenación por membrana extracorpórea en 3 %, terapia de reemplazo renal continua en 9 %, antibióticos en 71 %, antifúngicos en 15 %, glucocorticoides en 19 %, y terapia intravenosa con inmunoglobulina en 27 %.54
La terapia de inmunización pasiva y el uso de interferón en teoría podría ser útil, pero hasta la fecha no hay evidencia para validar esta hipótesis. Se ha propuesto tratamiento de rescate con plasma de pacientes convalecientes e inmunoglobulina G.108 También es importante considerar los síntomas y manifestaciones de la ansiedad y la depresión.
Puesto que la COVID-19 es una zoonosis, se debe abolir todo contacto con carne de caza para evitar esta forma inicial de transmisión, y hacer evaluaciones ambientales e investigaciones para identificar el animal intermediario causante del brote.82 En China también se ha considerado introducir legislación para prohibir la venta y comercialización de animales salvajes.109
La transmisión de persona a persona fue la mayor vía de propagación;110) varias propiedades de este virus dificultan el bloqueo de la propagación: la infectividad en el período de incubación asintomático, transmisión de personas asintomáticas, largo período de incubación, tropismo para superficies mucosas, la duración prolongada de la enfermedad y la posible transmisión incluso después de la recuperación clínica.111)
La COVID-19 se transmite como un patógeno de gotas lo que lo hace pertenecer a la Categoría B de agentes infecciosos, según la clasificación del CDC, al cual pertenecen: la fiebre Q, la brucelosis y la salmonella; sin embargo, la comisión nacional de salud China, tomó la recomendación de controlarlo como Categoría A, al que corresponden los agentes infecciosos más peligrosos que son de fácil diseminación y transmisión, que tienen alta mortalidad, y producen pánico en la población, al que pertenecen: la viruela, el botulismo, el ántrax y el ébola.112) Bajo esta política, varias medidas de salud pública fueron tomadas: el aislamiento de casos, la identificación y seguimiento de contactos, la desinfección ambiental, el uso de equipo de protección personal, y las medidas específicas para las zonas rurales y para la población de edad avanzada.113
Dado que en este momento no hay tratamientos aprobados o vacuna para la infección, la mejor prevención es evitar exponerse al virus.114 El aislamiento incluye aislar en la casa los casos confirmados o sospechosos con enfermedad leve, mantener la vivienda bien ventilada e iluminada con luz solar para permitir la destrucción del virus; los pacientes deben usar mascarilla quirúrgica simple, taparse la boca al toser o estornudar y practicar higiene de manos con frecuencia, deben ser colocados en habitaciones separadas o agruparse juntos -generalmente no se necesitan salas de ventilación con presión negativa-. Las habitaciones, superficies y equipos deben someterse a una descontaminación periódica, preferiblemente con hipoclorito de sodio.115 Sus cuidadores deben usar mascarilla quirúrgica cuando están en la misma habitación que el paciente y usar higiene de manos cada 15-20 minutos.72,115
Los pacientes pueden ser dados de alta de aislamiento una vez que están afebriles durante al menos 3 días; deben tener dos pruebas moleculares negativas consecutivas con intervalo de muestreo de un día.72
La cuarentena es una medida tradicional muy efectiva para contrarrestar una epidemia mortal, pero los protocolos de cuarentena pueden ser difíciles de aplicar. Se debe pedir a las personas que eviten áreas abarrotadas, evitar viajes a lugares con transmisión continua del virus, y prohibir las reuniones multitudinarias.
En las medidas preventivas de infección y control que pueden reducir el riesgo de exposición se incluyen: practicar la higiene de la tos y los estornudos, cubrir con pañuelos desechables la nariz y la boca que luego se eliminan de forma segura (o, si no está disponible, usar un codo flexionado), el lavado de manos regular con jabón o desinfección con desinfectante para manos que contenga al menos 60 % de alcohol (si no hay agua y jabón disponibles), evitar el contacto con personas infectadas y mantener una distancia apropiada de 1,5 a 1,8 metros entre personas, y abstenerse de tocarse los ojos, la nariz y la boca sin lavarse las manos.
A las personas con síntomas respiratorios se les recomienda que usen mascarillas quirúrgicas; sin embargo, el uso de mascarillas en personas sanas en lugares públicos, no ha demostrado proteger contra infecciones respiratorias virales y actualmente no es recomendado por la OMS; sin embargo, en China, se le ha pedido al público que use máscaras en público y especialmente en lugares concurridos.
La OMS emitió directrices detalladas sobre el uso de mascarillas en la comunidad, durante el cuidado en el hogar, y en los entornos de atención médica a la COVID-19. En ese documento se recomienda que los trabajadores de la salud utilicen mascarillas N95 o FFP2 que previenen la transmisión de partículas respiratorias, al realizar procedimientos de generación de aerosoles y usar máscaras médicas mientras se brinda atención a casos sospechosos o confirmados. Se recomienda a las personas con síntomas respiratorios usar mascarillas tanto en atención médica como en atención domiciliaria.116
Algunos procedimientos realizados en pacientes infectados podrían generar infección por aerosoles, como: la toma de muestras nasofaríngeas, inducción del esputo, succión abierta de vías aéreas, intubación y traqueotomías; estos procedimientos deben ser realizados con cautela, deben tener una sala de aislamiento de infecciones por aerosol, y el personal debe usar protección respiratoria y ocular, e higiene de manos, además debe evitarse la propagación ambiental, con una atención especial en la lavandería, los utensilios de servicio de alimentos y los desechos médicos.117
Hasta el 14 febrero de 2020, casi 1 716 trabajadores de la salud en China se habían infectado, con 6 muertes; requiere especial memoria la historia del oftalmólogo Dr. Li Wenliang.118
Es importante proteger a los trabajadores de la salud para garantizar la continuidad en la atención y para prevenir la transmisión de infección a otros pacientes. Estos deben estar provistos de mascarillas N95, trajes de protección y gafas, y deben ser monitoreados para el desarrollo de síntomas de la COVID-19.
Por último, es importante pedir a las personas a través de LAS redes sociales, mensajería de texto y medios de comunicación, no difundir mitos e información falsa sobre la enfermedad, y tratar de evitar caer en pánico y superar la ansiedad.
CONCLUSIONES
Este artículo muestra una revisión de la evidencia disponible en el inicio de la epidemia mortal por SARS-CoV-2, que ha desafiado la infraestructura de la salud pública, y afectado la economía mundial. Muchos estudios han sido publicados sobre: la epidemiologia, las causas, las manifestaciones clínicas, el diagnóstico, la prevención y el control del nuevo coronavirus. Se muestra que los pacientes afectados están en todos los grupos etéreos. Su presentación clínica va desde portador asintomático hasta neumonía con insuficiencia ventilatoria. Los síntomas más comunes son: la fiebre, debilidad generalizada y tos seca; los casos graves tienen más probabilidades de ser adultos mayores y con múltiples comorbilidades. Hasta la fecha, no hay un tratamiento antiviral específico; según el estado actual, el bloqueo de la transmisión, el aislamiento, la protección respiratoria y ocular, y la higiene de manos, son las estrategias más efectivas para prevenir la propagación del SARS-CoV-2. Es necesario realizar más estudios para determinar el mecanismo de la patogenicidad, probar medicamentos antivirales, y el desarrollo de una vacuna que permita prevenir nuevos brotes de esta enfermedad.