Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
MediSur
versión On-line ISSN 1727-897X
Medisur vol.16 no.1 Cienfuegos ene.-feb. 2018
ARTÍCULO ORIGINAL
Experiencia en la conducción de ensayos clínicos en Cienfuegos
Experience in conducting clinical trials in Cienfuegos
Olga Lidia Cuevas PérezI , Diana Rosa Fernández RuízI , Gredsy Escandón LópezII , Mayra Quirós EnriqueIII , Yuleidis García RodríguezII
I Centro Nacional Coordinador de Ensayos Clínicos, La Habana, Cuba
II Hospital General Universitario Dr. Gustavo Aldereguía Lima, Cienfuegos, Cuba
III Universidad de Ciencias Médicas de Cienfuegos, Cienfuegos, Cuba
RESUMEN
Fundamento: Cienfuegos se inserta en la Red Nacional de Ensayos Clínicos en la década de los 90. Ha tenido una participación importante en el registro de nuevos fármacos, lo que hasta el momento se ha difundido poco, de ahí la importancia de mostrar el crecimiento alcanzado por la provincia en esta actividad.
Objetivo: describir la experiencia adquirida y el desarrollo alcanzado por Cienfuegos en la conducción de ensayos clínicos.
Métodos: estudio descriptivo sobre ensayos clínicos realizados en Cienfuegos desde 1992 hasta mayo de 2016. Se analizaron las variables: centro promotor, producto evaluado, fase de desarrollo del ensayo clínico, especialidades médicas y número de pacientes incluidos.
Resultados: se ejecutaron 64 ensayos clínicos, procedentes fundamentalmente del Centro de Ingeniería Genética y Biotecnología y el Centro de Inmunología Molecular. Las especialidades médicas con mayor participación fueron oncología y hematología con 15 (23.4%) y 10 (15.6%) ensayos respectivamente. El mayor porcentaje de investigaciones estuvo dirigido a probar la eficacia y seguridad de productos para el tratamiento del cáncer, con la realización de 30 ensayos (46.8 %) en localizaciones como pulmón, sistema hematológico, mama, cabeza y cuello y próstata. Se incluyeron 2420 pacientes. Su ejecución se extendió hasta la Atención Primaria de Salud y se incorporó el Hospital Gustavo Aldereguía Lima al proceso de certificación de sitios clínicos.
Conclusiones: existe un trabajo sistemático en Cienfuegos en relación con la ejecución de los ensayos clínico; se ha contribuido al registro sanitario y comercialización de varios productos.
Palabras clave: ensayos clínicos como asunto, Cuba.
ABSTRACT
Foundation: Cienfuegos is inserted in the National Netork of Clinical Trials of the nineties. Decade. It has an important parrticipation in the registration of new drugs, which up to the moment has not been enough disseminated. This is the reason of the importance of showing the growth achived in the province in this activity.
Objective: To describe the experience and development achived in Cienfuegos in conducting clinical trials.
Methods: it is a descriptive study on the clinical trials conducted in Cienfuegos from May 1992 to May 2016. Variables such as: promoting center, evaluated product, stage of the clinical trials, medical specialties and number of patients included were analyzed.
Results: a number of 64 clinical trials were carried out, basically form Center for Genetic Engineering and Biotechnology and the Center of Molecular Inmunology. The medical specialties with most participation were oncology and hematology with 15 (23.4%) and 10 (15.6%) trials respectively. The highest percentage of research were aimed at confirming the efficacy and safety of product for the treatment of cancer. with the conduction of 30 clinical trials (46.8%) in locations as lungs, hematologic system, breast, head and neck and prostate. A number of 2420 patients were included. There implementation extended to the Primary Health Care System and the Gustavo Aldereguia Lima Provincial Hospital was incorporated to the process of certification.
Conclusion: There is a systemtic work in Cienfuegos related to the conduction of clinical trials. There has been a contribution and comercialization of several products.
Key words: clinical trial as topic, Cuba.
INTRODUCCIÓN
Los ensayos clínicos, experimentos en el que los sujetos se asignan a las diferentes intervenciones de manera aleatoria y simultánea (en un mismo período de tiempo), son supervisados también simultáneamente. Este tipo de estudio que permite la evaluación de la eficacia y seguridad de un fármaco o producto en sujetos humanos, se fundamenta en: comparaciones con el patrón terapéutico o diagnóstico; la existencia de al menos dos grupos concurrentes de pacientes a comparar entre sí, con tratamientos aleatorizados y enmascarados; con un diseño muestral específico y el posterior análisis estadístico de los datos obtenidos.1 Constituye la metodología idónea para evaluar una terapéutica o intervención en humanos, comúnmente conocido como el estándar de oro.2 Los ensayos clínicos favorecen, de igual forma, al seguimiento poscomercial de un producto médico, a la introducción de nuevas modificaciones a las terapéuticas en las prácticas médicas, a la educación de los médicos para fomentar el sentido crítico y a la correcta evaluación del uso de medicamentos, de otras terapias médicas y de medios de diagnóstico. También contribuyen a elevar la calidad de los servicios médicos mediante la aplicación de los métodos más avanzados en el diagnóstico, tratamiento y evaluación de las enfermedades en estudio.3 El desarrollo acelerado de la industria médico-farmacéutica y biotecnológica, así como el de las agencias regulatorias de medicamentos y equipos en el nuevo mundo, aumentó las exigencias para el registro de fármacos y productos biotecnológicos, lo cual obligó a Cuba a trazar una estrategia que contribuyera al registro y comercialización y lograr lo antes posible, a partir del momento de la obtención del producto, su rápida introducción en la práctica médica.4 Para lograr estos objetivos, se creó en Cuba en 1991 el Centro Coordinador de Ensayos Clínicos (CENCEC),4 el cual funciona como un Centro de Investigación por Contrato. Tiene un alcance nacional, pues cuenta con una red de coordinación que funciona en todas las provincias; su misión es la evaluación clínica de productos que deben ser registrados dentro y fuera del país, para su aplicación en la práctica médica y posterior comercialización.4 En la década de los 90, la provincia de Cienfuegos se inserta en la Red Nacional de Ensayos Clínicos, siendo el Hospital Universitario Dr. Gustavo Aldereguía Lima en aquellos momentos el único sitio donde se realizaban ensayos clínicos, con la participación de varias especialidades médicas. Esta institución hospitalaria participó en ensayos clínicos desde la década de los 80, antes de ser creada la Red Nacional. Son múltiples los ensayos clínicos de centros promotores, nacionales e internacionales, coordinados a través del CENCEC o en forma monocéntrica, entre la institución productora y diferentes sitios clínicos de la provincia. Cienfuegos ha tenido una participación importante en el registro de nuevos fármacos, lo que hasta el momento se ha difundido poco, por lo que merece la pena mostrar el crecimiento alcanzado por la provincia en la actividad. Este trabajo tiene como objetivo describir la experiencia adquirida y el desarrollo alcanzado por Cienfuegos en la conducción de ensayos clínicos.
MÉTODOS
Se realizó un estudio descriptivo sobre ensayos clínicos realizados en Cienfuegos desde 1992 hasta mayo de 2016. Se revisó la documentación de cada uno de los ensayos clínicos, tales como carpeta del investigador y carpeta del farmacéutico, ubicados en los sitios clínicos, así como los informes de las visitas del CENCEC para la preparación del Hospital Gustavo Aldereguía Lima para la certificación. Se analizaron las variables: centro promotor, producto evaluado, fase de desarrollo del ensayo clínico, especialidades médicas y número de pacientes incluidos. Los datos se recogieron y procesaron utilizando una base de datos EXCEL. Los resultados se presentan en tablas mediante números absolutos y porcentajes.
RESULTADOS
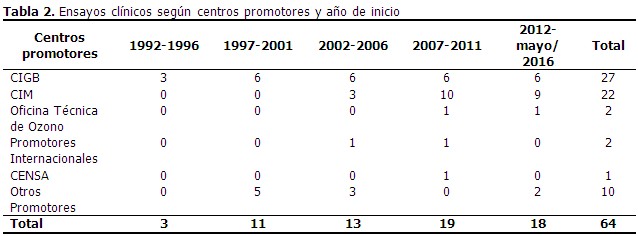
En el período de tiempo comprendido entre 1992 y mayo 2016, se realizaron en Cienfuegos 64 ensayos clínicos multicéntricos nacionales en 18 sitios clínicos, lo cual permitió la evaluación de 30 productos de diferentes centros promotores. De los productos estudiados, 11 han sido evaluados en enfermedades oncológicas con la realización de 30 ensayos (46,8 %), en localizaciones como pulmón, sistema hematológico, mama, cabeza y cuello y próstata. Se incluyeron 2420 pacientes en todo el periodo. (Tabla 1). Dentro de los centros promotores que han ejecutado ensayos clínicos en Cienfuegos se destaca el Centro de Ingeniería Genética y Biotecnología (CIGB) con 27 ensayos y el Centro de Inmunología Molecular (CIM) con 22 ensayos. Una vez establecida la infraestructura y el marco regulatorio en Cuba, el CIGB fue el primer promotor que comenzó a ejecutar ensayos clínicos en la provincia, el primero fue el titulado “Uso de la estreptoquinasa recombinante en el infarto agudo de miocardio (IAM)”, para evaluar la seguridad y la e?cacia de este producto obtenido por ingeniería genética. A partir del 2001 ocurrió un incremento en la participación de la provincia en estas investigaciones nacionales. (Tabla 2). Los productos de investigación más utilizados en la provincia han sido los interferones, el CIMAvaxEGF, el nimotuzumab, la eritropoyetina y los supositorios de estreptoquinasa (proctoquinasa). Con los interferones se han ejecutado ensayos clínicos en diferentes fases de desarrollo, así como con la eritropoyetina y proctoquinasa. La mayor cantidad de ensayos ejecutados fueron en fases avanzadas del desarrollo de medicamentos (fase III y IV). (Tabla 3). Varías especialidades médicas tanto de la atención secundaria como de la atención primaria han participado en la ejecución de algún ensayo clínico. Las de mayor participación en cuanto a la cantidad de ensayos realizados han sido oncología y hematología con la ejecución de 15 (23,4%) y 10 (15,6%) ensayos respectivamente. En cuanto a los pacientes incluidos vale destacar los 1135 pacientes incluidos en el ensayo clínico “ Evaluación de la inmunogenicidad y eficacia del candidato vacunal heptavalente contra neumococos en niños entre 1 y 5 años. Fase II/III”, que comenzó su ejecución en el 2014 y en el que participaron pediatras y médicos generales integrales de la atención primaria; así como la inclusión rápida de 54 niños voluntarios sanos en el ensayo clínico fase III de la vacuna contra el cólera. La especialidad de hematología del Hospital Gustavo Aldereguía se ha destacado en la inclusión de pacientes en todos los ensayos en que ha participado. (Tabla 4). En el sitio clínico Hospital Gustavo Aldereguía Lima se ejecutaron Programas de Uso Expandido (PUCE) de productos para el cáncer en los cuales se incluyeron pacientes sin otra opción terapéutica: Entre otros resultados alcanzados en la provincia con la ejecución de ensayos clínicos tenemos que el Hospital Gustavo Aldereguía Lima participó en el Proyecto de Ensayos Clínicos en Psiquiatría con la Universidad de Dalhouse, Canadá, con lo cual se logró elevar la capacidad de los investigadores en la conducción de ensayos clínicos, para evaluar terapias psicofarmacológicas, lo que además ha permitido elevar la calidad de la atención médica en esa área terapéutica. El Hospital General Universitario Dr. Gustavo Aldereguía Lima, de Cienfuegos se encuentra inmerso en el proceso de preparación para la certificación, en cada una de las áreas ya se realizó la autoevaluación, el diagnóstico y dos visitas de seguimiento, en las cuales se propusieron soluciones y recomendaciones a cada una de las dificultades encontradas. Constituye un objetivo en curso, y la voluntad político- administrativa de las personas con poder de decisión de la institución, será decisiva para alcanzar esta condición. La provincia ha logrado llevar los ensayos clínicos hasta la atención primaria de salud (APS), ejecutándose varios ensayos en este nivel de atención. Se aplicó la vacuna cubana contra el neumococo en más de mil niños desde uno hasta cinco años de edad, en ensayo clínico fase II/III, con la participación del Hospital Pediátrico Paquito González Cueto y los policlínicos de la atención primaria de salud. Además, se realizó un ensayo con la vacuna terapéutica Cimavax-EGF contra el cáncer de pulmón avanzado de células no pequeñas, donde participaron policlínicos de cuatro áreas del municipio de Cienfuegos y los policlínicos de Palmira y Cumanayagua. Se incluyeron 32 pacientes. En este nivel de atención se han ejecutado otros dos ensayos clínicos en conjunto con el Hospital Gustavo Aldereguía Lima, ambos en cáncer de pulmón, con las vacunas registradas en Cuba para esta indicación. El “Ensayo clínico multicéntrico, aleatorizado, estratificado, abierto y comparado en pacientes con CPCNP avanzado tratados con Racotumomab o Nimotuzumab, vs Docetaxel después de la primera línea de tratamiento oncoespecífico”, se desarrolló en cuatro áreas de salud del municipio de Cienfuegos y en los municipios de Palmira y Cumanayagua y ya culminó su ejecución. El ensayo titulado “Seguridad de la vacuna cimavax-egf® para el tratamiento del cáncer de pulmón de células no pequeñas en estadios avanzados. Exploración de la efectividad según concentraciones basales de egf. Fase Iv”, actualmente está en ejecución y en él participan dos policlínicos del municipio Cienfuegos y un policlínico por cada uno de los restantes municipios.
DISCUSIÓN
El Centro Nacional Coordinador de Ensayos Clínicos (CENCEC) surgió en 1991,4 uno de sus propósitos es diseñar y organizar la ejecución de los ensayos clínicos que evalúan los diferentes productos para el registro y la comercialización de medicamentos, reactivos, productos biológicos, instrumental, equipos y procedimientos terapéuticos; todo ello en rigurosa observancia de las buenas prácticas clínicas y a un costo razonable.5 Extendió su trabajo a todo el país a través de la Red Nacional de Ensayos Clínicos de la cual forma parte Cienfuegos, donde existen coordinadores encargados de la conducción, control y aseguramiento de la calidad de los ensayos clínicos, los cuales se ejecutan en los diferentes sitios clínicos que tienen convenios de trabajo con el CENCEC. Se desarrollan otros ensayos clínicos que son coordinados y conducidos directamente por el promotor sin la participación del CENCEC. Los ensayos clínicos que se han ejecutado en la provincia han sido fundamentalmente con productos biotecnológicos indicados en el tratamiento de las enfermedades oncológicas en diversas localizaciones y estadios, lo cual se ha comportado de igual manera en otras provincias del país.6,7 Los centros de investigación del país, principalmente el CIGB y el CIM dan prioridad a la investigación en el campo de la oncología pues el cáncer constituye un problema de salud para Cuba y el mundo.8 En Cuba el cáncer constituyó la primera causa de muerte para todos los grupos de edades en el 2012,9 manteniéndose como la segunda causa de muerte en el 2014 y el 2015,10,11 todo lo cual justifica que la mayoría de las investigaciones clínicas ejecutadas en Cienfuegos estén dirigidas al tratamiento del cáncer, con participación destacada del servicio de oncología y hematología, además del apoyo de otras especialidades como dermatología, urología, gastroenterología y ginecología. La importante y decisiva participación de la provincia en la evaluación de nuevos productos en el tratamiento del cáncer, influye positivamente en la modificación del cuadro de salud. Numerosos ensayos se han conducido en la provincia, no solo para evaluar novedosos productos para el registro sanitario (fase III), sino, además, para facilitar su extensión a toda la población a través de la implementación de estudios fase IV. Los estudios de poscomercialización de seguridad y confirmación de efectividad de productos ya registrados han permitido la implementación de algunos programas nacionales a través del Ministerio de Salud Pública,4 y la comercialización de tratamientos para varios tipos de cáncer (incluyendo cabeza, cuello, pulmón, cerebro, mama y esófago).5 De esta manera se han brindado soluciones a problemas serios de salud con elevados patrones y evidencias científicas y se ha generado un creciente interés mundial en los productos biotecnológicos y farmacéuticos cubanos, y se están negociando más intercambios científicos.5 La certificación de sitios clínicos en buenas prácticas garantiza la credibilidad, confiabilidad y trazabilidad de los resultados de los ensayos clínicos, lo cual garantiza la seguridad y eficacia de los medicamentos que se comercializan, además de proporcionar mayor prestigio a la institución de salud que obtiene este certificado.12 En Cuba es necesario obtener esta certificación ante el empuje de su propia industria biotecnológica y farmacéutica, con un alto número de nuevos productos o indicaciones de productos ya registrados, que necesitan de la etapa de investigación clínica. Además, ante la necesidad de que sus resultados científicos sean totalmente confiables frente a las exigencias de registros extranjeros, se impone desarrollar un proceso de certificación de sitios clínicos para ensayos clínicos.13 Por estas razones el Hospital Gustavo Aldereguía Lima se encuentra inmerso en este proceso, constituyendo un objetivo a alcanzar por la institución. La investigación en la atención primaria de salud (APS) debe ser un componente más de las actividades del médico, junto con la clínica y la docencia. El desarrollo de ensayos clínicos en el nivel primario de atención contribuye a elevar la calidad científica de los recursos humanos y de los servicios de atención médica.14 En Cuba ha sido posible debido al sistema fortalecido y bien estructurado de la asistencia médica, la Atención Primaria de Salud, que existe en todo el país, con la participación de un especialista de formación en Medicina General Integral y un equipo médico que trabaja en la promoción, prevención, curación y rehabilitación no solo del paciente, sino de la familia y la comunidad. En este nivel se atiende a grandes grupos de pacientes, existen registros donde se hallan bien caracterizados, reflejado en las fichas familiares e historias clínicas de los Consultorios Médicos de la Familia, lo cual ha sido una oportunidad y una rápida solución, ya que constituyen fuentes de posibles sujetos a incluir en las investigaciones, fundamentalmente en el logro del ritmo adecuado de inclusión necesario de los estudios.7 La administración de estos productos en el escenario de la APS ha sido posible por la demostrada seguridad de los productos biotecnológicos cubanos que están siendo objeto de investigación clínica. Estas novedosas terapias, de acción mucho más específica y con menor potencial tóxico, pueden ser utilizadas de forma crónica durante largos periodos de tiempo, además la conducción de los EC en un contexto cercano al domicilio del paciente facilita la accesibilidad al centro asistencial y hace el tratamiento más económico para él y sus familiares, por lo que el escenario de la APS resulta ideal para la mejor cumplimentación de estos tratamientos. Se puede concluir que desde su incorporación a la Red Nacional de Ensayos Clínicos Cienfuegos ha mantenido un trabajo sistemático en la actividad de ensayos clínicos, contribuyendo al registro sanitario y comercialización de varios productos, principalmente de aquellos que constituyen nuevas terapias en el tratamiento de enfermedades oncológicas y son productos líderes de centros promotores nacionales, como el Centro de Inmunología Molecular (CIM) y el Centro de Ingeniería Genética y Biotecnología (CIGB) principalmente. Limitación del estudio La limitación más importante de este estudio radica en el hecho de que no poseemos información suficiente sobre los ensayos clínicos realizados en Cienfuegos no conducidos por el CENCEC.
REFERENCIAS BIBLIOGRÁFICAS
1. Laporte JR. Glosario. En: Laporte J, editores. Principios básicos de la investigación clínica. 2da. ed. Madrid: AstraZeneca; 2002. p. 111-194
2. Calva-Mercado JJ. Estudios clínicos experimentales. Sal Púb Méx [revista en Internet]. 2000 [citado 6 Nov 2016];42(4):[aprox. 8p]. Disponible en: http://www.scielosp.org/pdf/spm/v42n4/2883.pdf
3. ICH Harmonised Tripartite Guideline. ICH E8 General considerations for clinical trials. Geneva: ICH Steering Committee; 1997
4. Pascual López MA, Jiménez Rivero G, Torres Pombert A, Fors López MM, López Zayas I. Surgimiento, evolución y principales resultados del Centro Nacional Coordinador de Ensayos Clínicos. Rev Cubana Farm [revista en Internet]. 2011 [citado 21 Jul 2016];45(1):[aprox. 28p]. Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0034-75152011000100002&lng=es
5. Gorry C. El ABC de los ensayos clínicos en Cuba. MEDICC Rev. 2016;8(3):9-14
6. Negret Hernández M, Naranjo Rodríguez S, Cárdenas Garabito D, Ramos Castro G. Experiencia en la conducción de ensayos clínicos en la provincia de Matanzas. 2005-2012. Rev Méd Electrón [revista en Internet]. 2014 [citado 21 Jul 2016];36(4):[aprox. 11p]. Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S1684-18242014000400004
7. Veguilla Alomar G, Boizant Crombet LM, Hernández Turiño L, Pérez Andrés L. Antecedentes, estado actual y perspectivas de la conducción de ensayos clínicos en Ciego de Ávila. Rev Mediciego [revista en Internet]. 2008 [citado 21 Jul 2016];14 Suppl 2:[aprox. 5p]. Disponible en: http://bvs.sld.cu/revistas/mciego/vol14_supl2_08/articulos/a6_v14_supl208.htm
8. Fors López M, Costa Castro N, Viada González C, Pérez Rodríguez O. Desde la investigación biomédica a la clínica: avances del Centro Nacional Coordinador de Ensayos Clínicos. MediMay [revista en Internet]. 2014 [citado 21 Jul 2016];20(1):[aprox. 8p]. Disponible en: http://revcmhabana.sld.cu/index.php/rcmh/article/view/191/html
9. Ministerio de Salud Pública. Dirección Nacional de Registros Médicos y Estadísticas de Salud. Anuario Estadístico de Salud. 2013 [Internet]. La Habana: MINSAP; 2014 [citado 21 Jul 2016]. Disponible en: http://files.sld.cu/dne/files/2014/05/anuario-2013-esp-e.pdf
10. Ministerio de Salud Pública. Dirección Nacional de Registros Médicos y Estadísticas de Salud. Anuario Estadístico de Salud. 2014 [Internet]. La Habana: MINSAP; 2015 [citado 21 Jul 2016]. Disponible en: http://files.sld.cu/bvscuba/files/2015/04/anuario-estadistico-de-salud-2014.pdf
11. Ministerio de Salud Pública. Dirección Nacional de Registros Médicos y Estadísticas de Salud. Anuario Estadístico de Salud. 2015 [Internet]. La Habana: MINSAP; 2016 [citado 21 Jul 2016]. Disponible en: http://files.sld.cu/dne/files/2016/04/Anuario_2015_electronico-1.pdf
12. Cuevas Pérez O, Fernández Ruiz D, Díaz Díaz J. La certificación de sitios clínicos en buenas prácticas clínicas para la realización de ensayos. Medisur [revista en Internet]. 2015 [citado 21 Jul 2016];13(4):[aprox. 2p]. Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S1727-897X2015000400003
13. Marañon Cardonne T, León Robaina R. La investigación clínica. Un primer acercamiento. Rev Hum Med [revista en Internet]. 2015 [citado 22 Jul 2016];15(1):[aprox. 19p]. Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S1727-81202015000100010&lng=es
14. Extremera Montero F, Ordóñez Montesinos JJ, Díez García E, Mejías Úbeda AB. Publicaciones de los centros de salud andaluces en Medline. Med Fam [revista en Internet]. 2002 [citado 22 Jul 2016];3(4):[aprox. 6p]. Disponible en: http://www.samfyc.es/Revista/PDF/v3n4/02.pdf
Recibido: 14 de julio de 2017.
Aprobado: 14 de febrero de 2018.
Olga Lidia Cuevas Pérez. Licenciada en Ciencias Farmacéuticas. MSc. en Investigación y Desarrollo de Medicamentos. Profesora Asistente. Investigadora Agregada. Centro Nacional Coordinador de Ensayos Clínicos. La Habana. Cuba. Correo electrónico: olgalcp@infomed.sld.cu