Introducción
La insuficiencia respiratoria aguda moderada y grave (IRAMG) hipoxémica es la más temida complicación de la COVID-19 por su alta incidencia, se presenta cerca de un 20 % de todos los casos y por la letalidad que se le asocia.1,2,3
La oxigenoterapia es una de las intervenciones terapéuticas para estos pacientes e incluye desde el oxígeno suministrado con una cánula nasal hasta el aportado por un ventilador mecánico.1) Entre estas variantes, la ventilación mecánica no invasiva (VMNI) se recomienda para evitar la intubación orotraqueal y la ventilación mecánica invasiva (VMI),1,2,3,4 que condiciona más complicaciones y una mayor letalidad por la enfermedad.2,5
La VMNI es una variante de soporte respiratorio, los gases se suministran al paciente por un equipo de ventilación con una máscara facial o nasal, aunque pueden existir otras interfaces como un casco presurizado. A diferencia de la VMI, no usa un tubo traqueal para la entrega de gases, no se necesita la sedación profunda ni la relajación del paciente.
La VMNI se ha utilizado en otras neumonías virales graves como las originadas por virus de influenza A H1N1 y variantes de coronavirus1 En los pacientes con formas moderadas y graves de COVID-19, los reportes son variados; en Italia, Estados Unidos y China, se refieren a porcentajes de uso en el 11, 19 y 20,1 por ciento respectivamente de los ingresados.1,4 En un estudio realizado en China se reportó su uso en 33 % de los pacientes como primera línea en la IRAMG.1 En el Reino Unido, en una serie de casos, se utilizó sola o en combinación con VMI en el 17,6 % de los ingresados.6
Hay criterios divergentes sobre el uso de la VMNI en la COVID-19.7 Un grupo considera que su utilización no evita la VMI, que solo retrasa su uso, ya que se asocia a un inadecuado control del volumen tidal y de la presión transpulmonar, lo cual se eleva el riesgo de lesión pulmonar inducida por la ventilación.5 Otros esperan más evidencias científicas de su utilidad para tomar su decisión,6,8 mientras un tercer grupo la defiende, la recomienda y la integra en los protocolos por la posibilidad de reclutar alveolos y mejorar el trabajo respiratorio.3,4
La COVID-19 ha impuesto retos por la cantidad de pacientes que necesitan asistencia ventilatoria y porque el número de camas en unidades de cuidados intensivos no ha sido suficiente en la mayoría de los países, por lo que se crearon espacios para atender enfermos con IRAMG en salas convencionales y en centros creados para estos fines, donde ha sido necesario emplear la VMNI.5
En la República de Panamá se implementó la estrategia de expandir y garantizar camas con similares prestaciones a las hospitalarias. Como parte de ello, “Figali”, un antiguo centro de convenciones, fue uno de los espacios empleados por las autoridades de salud para constituir un centro integral de atención provisional para pacientes con formas moderadas de COVID-19 (CFigali). Este centro disponía de 160 camas, y de ellas 40 estaban destinadas a la atención semi-intensiva de cuidados respiratorios especiales, donde se realizó la VMNI como parte de su protocolo médico de actuación.9 Tres de los autores pertenecieron a la brigada médica cubana “Henry Reeve” que laboró entre enero y agosto de 2021 en el CFigali.
En América Latina existen pocos trabajos publicados que se refieren al uso de la VMNI en los pacientes con la COVID-19 fuera de los servicios de cuidados intensivos. Este modo ventilatorio es utilizado de manera muy heterogénea3 y en la literatura son pocas las investigaciones que incluyen todos los indicadores para una adecuada evaluación de sus resultados.6,8,10 La presente investigación tuvo como objetivo describir las características y la evolución de los pacientes con formas moderadas y graves de la COVID-19 tratados con VMNI.
Métodos
Se realizó un estudio descriptivo, retrospectivo, longitudinal en 78 pacientes, 47 hombres y 31 mujeres con la COVID-19, con edad media de 46,2 años (DS=10,5), que recibieron ventilación mecánica no invasiva en el Centro Integral de Atención Provisional para Pacientes Moderados con la COVID-19 en “Figali”, Panamá, egresados entre el 1 de junio y el 31 de julio de 2021 y que utilizaron la VMNI como estrategia de oxigenoterapia en cualquier momento de su evolución. No se excluyeron pacientes.
La infección con el SARS-Cov-2 se confirmó por la reacción en cadena de la polimerasa en tiempo real (PCR-RT) o por prueba rápida de antígeno (ambos aprobados por el laboratorio central de referencia del Ministerio de Salud de Panamá), realizados en los laboratorios habilitados en diferentes instituciones de salud de donde fueron remitidos al CFigali. En el momento del ingreso, todos presentaban una enfermedad clasificada como moderada, por la disnea, la radiografía de tórax con infiltrados típicos de la COVID-19 y la oximetría de pulso con valores de saturación periférica de oxígeno (SpO2) inferiores a 95 %.
Se consideraron obesos los individuos con un índice de masa corporal ≥ 30kg/m2 medido en el momento del ingreso. No hubo fallecidos en la institución ni indicación de VMNI como parte de brindar cuidados paliativos o de alguna variante de techo terapéutico.
La decisión de utilizar la VMNI y su seguimiento se realizó según el protocolo médico de actuación del centro y del país9 y se tomó por criterios clínicos, radiográficos, hemogasométricos y algunas relaciones de sus valores en escalas como el índice ROX [saturación periféricas de oxígeno /fracción inspirada de oxígeno/frecuencia respiratoria (SpO2FiO2/FR)],11 escala HACOR (frecuencia cardiaca, pH, índice de Glasgow, razón de la presión arterial de oxígeno/fracción inspirada de oxígeno (PaO2/FiO2) y la frecuencia respiratoria]12 y la presión arterial de oxígeno/ fracción inspirada de oxígeno (PaO2/FiO2) según protocolo del CFigali (anexo 1).
Antes de iniciar la VMNI, el escalado de oxigenoterapia incluyó la cánula nasal (hasta 5-6 L/min y FiO2 de 40 %), seguido de la máscara facial con reservorio (hasta 14-15 L/min y FiO2 de 80 %), y la cánula nasal de alto flujo (CNAF) (hasta 70 L/min de flujo y 100 % de FiO2) se siguió el protocolo médico de actuación de CFigali y del país.9 Las muestras para las gasometrías arteriales fueron tomadas por los médicos y procesadas inmediatamente en un gasómetro (GEM 3500, Estados Unidos de América) en la unidad de cuidados respiratorios especiales.
Para diagnosticar el síndrome de dificultad respiratoria aguda (ARDS) y establecer su gravedad se consideraron los criterios de Berlin,13 por su amplio uso y por estar incluidos en los protocolos clínicos de la Organización Mundial de la Salud y de Panamá. El escalado en la oxigenoterapia permitió que todas las PaO2/FiO2 se midieran con una FiO2 mayor del 0,5 % y un valor de presión continua positiva de la vía aérea (CPAP) superior a 5 cmH2O luego de iniciada la VMNI.
La VMNI se realizó con interface de máscara facial, y ventiladores Puritan Beneth 980 (Medtronic, Estados Unidos de América) o eVolution 3e (eVent Medical, Estados Unidos de América).
Se aseguró el confort y la sincronía paciente-ventilador con el uso de sedación (se utilizó la dexmetodomidina, la cual solo tuvo entre sus efectos adversos la bradicardia sinusal que fue corregida con reajuste de dosis), con el apoyo psicológico desde el momento de decidir el proceder y los reajustes iniciales de los parámetros del ventilador (presión soporte, trigger inspiratorio, trigger espiratorio y velocidad de flujo) hasta que el paciente refirió una ventilación cómoda y adecuada a sus necesidades. Las modificaciones de la CPAP y FiO2 se encaminaron a lograr una adecuada PaO2/FiO2.
Se definió como falla en la VMNI (principal indicador de resultado de la VMNI) cuando el paciente no logró las metas de oxigenación (SpO2 ≥ 95 %, PaO2/FiO2 > 200 y escala HACOR entre 0-1 puntos) y empeoró clínicamente (frecuencia respiratoria ≥ 25 x min o disnea intensa en dos o más evaluaciones separadas por más de una hora). Una vez diagnosticada la falla de la VMNI los pacientes fueron intubados, acoplados a un ventilador mecánico y trasladados a otros centros con unidades de terapias intensivas de mayor resolutividad. Dado que fueron centros con variados protocolos de manejo de la VMI, y el desenlace de la VMI obedecer a diversas causas no atribuibles a la VMNI en el CFigali, no pareció correcto utilizar el indicador de mortalidad posterior como medidor de calidad de la VMNI.
Los datos de cada paciente se recogieron en un cuestionario elaborado por los autores (Anexo 2), cuya fuente primaria fue la historia clínica individual digital.
Se emplearon estadísticas descriptivas y los resultados se expresaron en porcentajes, medias y desviaciones estándar (DS).
Los pacientes se trataron según el protocolo de actuación del CFigali que se basa en el protocolo nacional panameño9 e incluyó: Remdesivir (5 dosis, si ingresaba en los primeros 10 días de síntomas), heparina de bajo peso molecular (dosis desde profiláctica a terapéutica según niveles de dímero D, hasta el alta), esteroides (dexametasona o metilprednisolona, hasta salida de oxigenoterapia), Tocilicimab (una o dos dosis según valores de proteína C reactiva e interleucina 6), antibioticoterapia (esquema inicial azitromicina/ceftriaxona, que cambió a otros antibióticos según criterios clínicos, radiológicos y valores de procalcitonina) y medidas generales. Se evaluó la evolución clínica de los pacientes dos veces por día.
La investigación fue autorizada por las autoridades administrativas y académicas de CFigali por no existir en el centro un comité de ética de la investigación y la información se conservó bajo los criterios de confidencialidad y sin revelar la identidad de las personas.
Resultados
En el período de estudio egresaron 217 pacientes que en el momento del ingreso se clasificaron como casos moderados, de los cuales 137 (63,1 %); utilizaron la CNAF en algún momento de su evolución (con una media de 5, un mínimo de 2 y máximo de 12 días con el procedimiento) y de ellos 77 (56,2 %); requirieron ventilación mecánica por agravarse el cuadro respiratorio y pasaron a VMNI. Los 60 restantes (43,8 %); resolvieron la hipoxemia con la CNAF. Una paciente con criterio de recibir oxigenoterapia con CNAF no la utilizó por contraindicaciones anatómicas e inició con VMNI luego de fallar la máscara facial con reservorio.
Entre los 78 pacientes con VMNI, las enfermedades crónicas no transmisibles las más frecuentes fueron la obesidad (62,8 %), la hipertensión arterial (29,5 %), y la diabetes mellitus (21,8 %). Estos factores no influyeron en el éxito o el fracaso de la VMNI (Tabla 1).
Tabla 1 Distribución de los pacientes según sexo y antecedentes patológicos personales y resultado de la VMNI
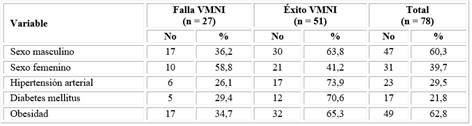
VMNI ventilación mecánica no Invasiva.
En 27 pacientes de los 78 (34,6 %) la VMNI no fue exitosa y se trasladaron a otros centros para iniciar VMI o en el mismo CFigali. La media de duración del procedimiento en esos casos fue 2,8 días (DS=1,7). En 14 pacientes de 27 (51,9 %) el fallo ocurrió en las primeras 48 h y en los 51 pacientes (65,4 %) en los que la VMNI tuvo éxito, la media de la duración de la ventilación fue 4,6 días (DS=1,4). En el 78,43 % (40 pacientes de 51 con VMNI exitosa) la ventilación se retiró entre el tercero y el quinto días.
Según los criterios de Berlín, 12 pacientes de 78 egresados (15,4 %) tuvieron un ARDS grave, el 47,4 % uno moderado y el resto entre leve o no lo presentaron. Cuanto menor la gravedad del ARDS, fue mayor el porcentaje de éxito de la VMNI. El 72,2 % de los casos leves, el 56,8 % de los moderados y el 50 % de los graves, no necesitaron procederes más invasivos. El 81,5 % de los que tuvieron una VMNI fallida presentaron un ARDS moderado o grave (Tabla 2).
Tabla 2 Clasificación del ARDS en los pacientes según criterios de Berlín13 para una mínima PaO2/FiO2 durante la ventilación y resultado de la VMNI
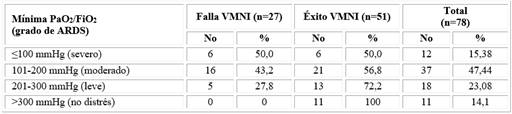
ARDS distrés respiratorio agudo; VMNI ventilación Mecánica No Invasiva; PaO2/FiO2 presión arterial de oxígeno / fracción inspirada de oxígeno.
Los pacientes que precisaron de VMNI ingresaron entre el séptimo y octavo días después del inicio de los síntomas y necesitaron la VMNI dos días después. En este grupo, el 75,6 % escaló de CNAF a VMNI en las primeras 24 h de iniciada la CNAF, un 15,4 % entre las 24 y 48 h y el resto con posterioridad (Tabla 3).
Tabla 3 Valores medios y (desviación estándar) de los principales indicadores de oxigenación y ventilación, en el momento de iniciar VMNI, a las 24 h de su utilización y sus valores mínimos durante la hospitalización; según resultado de la VMNI.
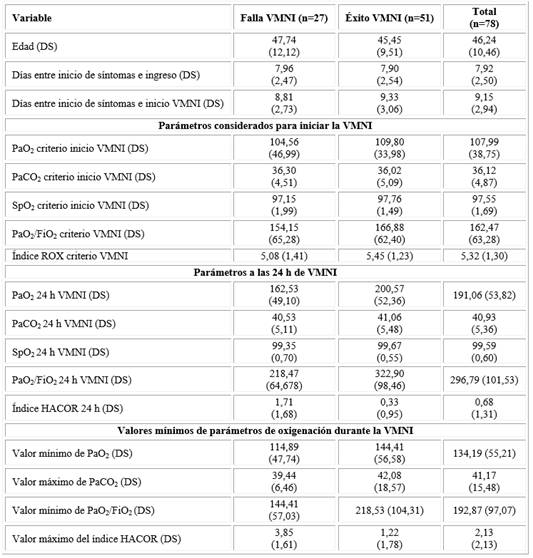
PaO2 presión arterial de oxígeno; SpO2 saturación periférica de oxígeno; índice ROX ([SpO2/FiO2]/FR); VMNI ventilación mecánica no invasiva; PaO2 presión arterial de oxígeno; PaCO2 presión arterial de dióxido de carbono; PaO2/FiO2 presión arterial de oxígeno/fracción inspirada de oxígeno.
Dentro de los parámetros hemogasométricos y sus relaciones en el momento de decidir el inicio de la VMNI en la tabla 3 solo la PaO2/FiO2 mostró medias más bajas entre los que tuvieron falla de la VMNI, con valores de 154,1 (DS=65,3) y generales de toda la serie en 162,5 (DS=63,3). A las 24 h de ventilación, se le sumaron a este indicador la PaO2 y el índice HACOR. El resto, al igual que los demás componentes del equilibrio ácido básico (bicarbonato de sodio, PaCO2 y PH) no mostraron valores alterados ni diferencias entre el éxito o la falla de la VMNI. Los principales criterios para cambiar de la oxigenoterapia con CNAF para la VMNI fueron el aumento o persistencia de una frecuencia respiratoria alta y la disminución de la PaO2/FiO2, con un 56.41 % para ambos (Tabla 4).
Tabla 4 Distribución porcentual de los principales criterios para el inicio de la VMNI y resultado de la VMNI
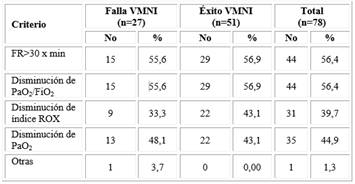
FR frecuencia respiratoria; PaO2/FiO2 presión arterial de oxígeno/fracción inspirada de oxígeno; índice ROX ([SpO2/FiO2]/FR); PaO2 presión arterial de oxígeno.
Los principales criterios para declarar la falla de la VMNI fueron una PaO2/FiO2<150 mantenida en dos o más ocasiones (62,9 %); unida a dos elementos clínicos principales: una frecuencia respiratoria ≥30 (55,5 %); y/o el agotamiento físico por el esfuerzo respiratorio (51,8 %) mantenido. También se consideraron un índice HACOR > 4 en 3 ocasiones (29,63 %) y la intolerancia a la VMNI (sensación de ahogo o ansiedad por el proceder y lesiones traumáticas en la cara por la máscara) en el 11,11 %. Si se agrupan estos elementos en un solo paciente, en todos hubo un criterio clínico (frecuencia respiratoria, agotamiento, intolerancia) unido en el 88,89 % a algún grado de descenso de la PaO2/FiO2.
Se utilizó un modo ventilatorio con dos niveles de presión con combinación de CPAP más presión soporte (PS). Los valores medios de PS y CPAP al inicio de la VMNI fueron 8 cmH2O para ambas, mientras el de FiO2 fue 74 %; estos no tuvieron relación con el éxito o el fracaso de la VMNI. La necesidad de elevar estos parámetros a valores de CPAP de 11 cmH2O, de PS a 10 cmH2O y de FiO2 a valores cercanos a 78 % el durante la VMNI fue más frecuente en los pacientes en los que falló la VMNI (Tabla 5).
Tabla 5 Valores medios y (desviación estándar) de los principales parámetros iniciales y máximos programados al ventilador; según resultados de la VMNI
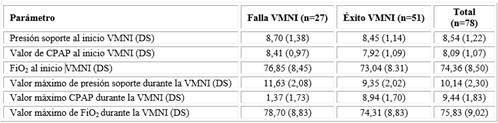
VMNI ventilación mecánica no invasiva; CPAP presión continua positiva de la vía aérea; FiO2 fracción inspirada de oxígeno
Las principales complicaciones de la VMNI fueron las lesiones faciales, fundamentalmente sobre el puente nasal, por los ajustes frecuentes de la máscara. Aunque por protocolo a todos los ingresados se les administraba un esquema de anticoagulación (con heparinas de bajo peso molecular), no se reportaron sangramientos, ni aún en sitios de punción arterial; tampoco se presentaron lesiones isquémicas de la mano, debidas a punciones de la arteria radial.
Discusión
El uso de la VMNI fuera de las unidades de cuidados intensivos ha sido una práctica común durante la epidemia por SARS-CoV-2. En Italia, en un estudio multicéntrico, se reportó su uso en el 10,4 % (909/8740) del total de los pacientes ingresados por la enfermedad.5
Las características clínicas de los pacientes tratados con VMNI en nuestro trabajo son similares a las descritas en otras series de casos.10) Más frecuente en hombres con comorbilidades como hipertensión arterial, diabetes mellitus y obesidad. En otras series las edades medias son superiores; en la de Carrillo y otros2) fue de 60 años, el 77,1 % eran hombres y el 55,7 % obesos; en el estudio de Rubio14 fue 67 años (DS=16), con presencia de hipertensión en el 50 % de los casos y diabetes mellitus en el 19,2 %. El promedio de edad más bajo en los pacientes del presente estudio se debió a que previo al período en que tomamos los datos, toda la población con más de 60 años en Panamá fue vacunada y la incidencia de la enfermedad en personas mayores fue menor.
El empleo de la VMNI después del uso fallido de la CNAF se ha denominado terapia de rescate y se le señala como desventaja la posibilidad de demorar el escalado en la oxigenación y que por ello se obtengan resultados desfavorables.7) Esto no constituyó un problema en esta serie, pues el 60 pacientes (43,8 %) de los 137 que utilizaron CNAF resolvieron la hipoxemia con ese proceder y el paso de CNAF a VMNI en el 75,6 % de los pacientes que no resolvieron con la primera, el cambio demoró menos de 24 h.
La COVID-19 es una enfermedad que evoluciona por etapas. En los casos con peor evolución, luego de una infección temprana y replicación viral con sintomatología variada, sigue la etapa pulmonar entre el octavo y el duodécimo días15,16,17 cuando comienzan manifestaciones como la disnea y la hipoxemia que deberán tenerse en consideración para establecer una terapéutica precoz y agresiva, pues en las siguientes 48 h puede hacerse ostensible que el paciente empeora clínicamente (etapa de hiperinflamación)15,16,17 y necesita la VMNI, como ocurrió a los pacientes en el presente estudio.
En un estudio multicéntrico en España, Rubio Rivas14 encontró que la media de los días transcurridos entre inicio de los síntomas y el ingreso fue 6,7 (DS=7), y Bellani5 reportó que entre el primero y el cuarto día tras el ingreso ya se define la necesidad de VMNI, tanto en los que tuvieron una evolución satisfactoria como los que no la tuvieron. La duración de la VMNI es generalmente corta; se reportan medias de 3 días en el Reino Unido,6 y 6,6 (DS=4,5) días en una serie de pacientes en Italia.10 Esto varía según la evolución de los pacientes en los que la VMNI es exitosa, la duración es ligeramente mayor, en los que no tienen éxito se detiene casi siempre en las primeras 48 h para pasar a la VMI.
La IRAMG por la COVID-19 es hipoxémica, se manifiesta principalmente en una PaO2/FiO2 baja, que es el criterio más utilizado y recomendado.7,8,9,14 Valores bajos de este indicador (aún con una media de 289 mmHg al ingreso), han sido también un predictor de mortalidad.14
Los reportes de la hemogasometría en otros trabajos muestran que al inicio de la VMNI el paciente tiene hipoxia e hipocapnia moderadas, como ocurrió en los pacientes de esta serie. Habitualmente la PaO2/FiO2 se encuentra por debajo de 200 mmHg, con valores medios de 172 (DS=102),5) o de 120,1 ± (DS=46,1),10 y se han reportado valores más bajos (83 mmHg).2) La PaCO2 puede ser 36,5 (DS=6,2) mmHg10 lo que puede provocar un esfuerzo ventilatorio en el paciente por tratar de corregir la hipoxemia con manifestaciones clínicas.
Los pacientes de este estudio que necesitaron VMNI ingresaron principalmente por un ARDS moderado, pero un alto porcentaje evolucionó a un cuadro grave en pocas horas. De acuerdo con la clasificación de Berlin,13 el 85,9 % (67/78) presentó en algún momento de su evolución un ARDS con diversos grados de gravedad. Para la COVID-19, expertos chinos propusieron reajustar estos criterios18 y la clasificación de gravedad se basó en una PaO2/FiO2<150 mmHg y con ese punto de corte, el 42,3 % de los casos con VMNI (33/78) del CFigali serían incluidos en este subgrupo y el 66,7 % (18/27) integrarían el grupo con falla de la VMNI.
Un aspecto contradictorio en el análisis de esta serie es que hubo pacientes con PaO2/FiO2 bajas y ARDS cuyos valores de PaO2 y SpO2 no se correspondieron con hipoxemia grave, lo cual se reporta con frecuencia en la literatura. Menzella10 encontró una PaO2 de 67,3 (DS=20,2) mmHg y Xie J19 una SpO2 ≤90 %.
En el protocolo del CFigali, la PaO2/FiO2 se utilizó como criterio fundamental para iniciar y mantener la VMNI lo que coincide con revisiones del tema3 y con las guías internacionales.9 La VMNI se indica en la insuficiencia respiratoria moderada a grave, representada principalmente por una PaO2/FiO2 <200 mmHg.3,9 y es un indicador que se relaciona con el fracaso de la ventilación y con un peor pronóstico.
La explicación de esta contradicción radica en la posibilidad de disponer de un patrón de hipoxemia basado en el cociente PaO2/FiO2 lo cual permite hacer valoraciones más tempranas en el curso del protocolo de oxigenación para el uso de la VMNI que con valores de PaO2 y FiO2 independientes. Por ejemplo, el criterio de inicio de VMNI tuvo dos parámetros clave: una frecuencia respiratoria por encima de 30, además de un descenso del índice ROX a menos de 3 con solo SpO2 de 94, y la escalada de FiO2 a valores ≥90 %. Este valor de SpO2 es indicador para oxigenoterapia en la mayoría de los protocolos (pues la FiO2 con que se relaciona es baja) pero en este contexto es indicador de inicio de VMNI.
De forma similar, la relación PaO2/FiO2 ≥200 mmHg (ARDS ligero) como meta durante la VMNI, obliga a que los valores de PaO2 y SpO2 tengan cifras normales para mantener adecuada esta relación. Por ejemplo, con VMNI, el cociente PaO2/FiO2 solo llega a 190 mmHg, para valores de FiO2 de solo 50 % y PaO2 de 95 (valor normal), es considerado como ARDS grave con un valor del cociente por debajo de la meta de oxigenación.
Los valores de la SpO2 no muy bajos en los estadios iniciales, asociados a valores bajos de PaO2 se han relacionado con el desvío de la curva de disociación de la hemoglobina a la izquierda como consecuencia de alcalosis respiratoria por aumento del esfuerzo respiratorio (aspecto no encontrado en este estudio). Machado y González,16 consideran que por esta razón la SpO2 no es la guía ideal para el manejo inicial de la oxigenoterapia.
Para el inicio de la VMNI se siguió un protocolo escalonado de oxigenoterapia, en los pacientes en los que la CNAF no fue suficiente para lograr la meta de oxigenación sin esfuerzo respiratorio aún con FiO2 por encima de 90 %. Este protocolo del CFigali permitió definir el momento adecuado para iniciar la VMNI y pudo influir en el alto porcentaje de éxito, en una casuística que incluyó 50 % de casos con ARDS grave e infiltrado inflamatorio pulmonar bilateral.
Una terapéutica oportuna con medicamentos que inhiban la liberación de citocinas, la prevención temprana y el manejo correcto de la hipoxemia son claves para evitar el inicio o la progresión de la cascada inflamatoria típica de la COVID-19 y con ello el ARDS.16,20 Por esta razón se recomienda que se inicien temprano los métodos ventilatorios no invasivos para evitar períodos de hipoxemia que podrían entorpecer la buena evolución clínica de los pacientes.16
Algunos autores cuestionan la meta de lograr una SpO2 entre 92-96 %, porque consideran que debe ser superior.16,20,21Barrot21) encontró una diferencia de 9,9 % de mortalidad al alta y del 14 % a los 90 días entre quienes utilizaron un esquema conservador de oxigenoterapia (meta de PaO2 entre 55 and 70 mm Hg) y los que optaron por uno menos cauteloso (entre 90 and 105 mm Hg). En este último hubo una mortalidad más baja, la PaO2 fue superior a 100 mmHg y la SpO2 se mantuvo en 97 %.
En la literatura7,10 se reportan valores de FiO2 en la VMNI más bajos (entre 50-60 %) que los utilizados en CFigali, por el efecto tóxico de las altas concentraciones de oxígeno. En relación con otros parámetros del ventilador, hay autores que utilizaron valores menores de PS y CPAP (6 cmH2O para ambos),7 otros centros protocolizan valores de CPAP de 10-12 cmH2O5,10 y de presión inspiratoria positiva en la vía aérea de 20-22 cmH2O (con lo cual la presión soporte también oscila entre 10-12 cmH2O).10 Al respecto se plantea que en los primeros estadios de la IRAMG prevalece un fenotipo “L” pulmonar que puede ser manejado con VMNI con valores moderados de CPAP e incrementos de la FiO2.8
Las modalidades ventilatorias utilizadas en CFigali están incluidas en las dos principales reportadas y recomendadas en la literatura.2,4,7,16 En todos los pacientes se utilizó un doble nivel de presión mediante la unión de PS más CPAP por las características de los ventiladores. En otro reporte5 en el 85 % de los pacientes se utilizó la modalidad CPAP, y el casco fue empleado en el 68 % de los casos. Esta interface fue poco utilizada en el CFigali aunque se disponía del recurso, porque hubo varios intentos fallidos por intolerancia a la claustrofobia, porque no fue confortable para los pacientes, por el ruido que produce y en menor medida por dificultades técnicas para su uso. Este es un proceder del que se tiene mayor experiencia en Europa,2,5 y tiene defensores y detractores,4 por las mismas consideraciones sobre la VMNI y la ausencia de fuertes evidencias de su efectividad.
Puede considerarse que la VMNI en el CFigali fue efectiva, por el alto porcentaje de éxito aun en pacientes con síntomas, signos y estudios complementarios que indicaban la gravedad de la enfermedad. Las tasas de éxito de la VMNI reportadas son de 15-25 % en otras variantes de neumonías virales.1 En la revisión de Ogawa4) los reportes de falla se encuentran entre el 10,9 y 44,6 %. Bellani en Italia,5 reportó que el 33 % de los casos precisó de un proceder ventilatorio invasivo tras una media de 5 (3 a 9) días de VMNI. En la revisión de Radovanovic3 la tasa de fracasos fue 55,5 % (necesidad de pasar a VMI, intolerancia o fallecimiento). Las frecuencias de falla de VMNI son variables porque no hay homogeneidad en el procedimiento y en los criterios para su uso.
Muchas guías de actuación definen el fracaso de la VMNI cuando no se logran las metas de oxigenación por un período de tiempo más corto (1 a 2 h) que el empleado en el presente estudio.7 Los principales indicadores de falla son que se mantengan la PaO2 y la PaO2/FiO2 bajas (generalmente por debajo de 150 cmH2O),7,8 o entre 100 y 200 cmH2O;10 valores que junto a la clínica fueron utilizados en el CFigali. Las causas de falla de la VMNI son variables: la edad avanzada, las comorbilidades y los valores de PaO2/FiO2 más bajos5 parecen influir en un desenlace desfavorable.
Los datos clínicos fueron fundamentales para decidir el inicio de la VMNI, su seguimiento y criterio de fracaso. Si hay polipnea y estertores crepitantes la enfermedad puede considerarse grave y es posible que el paciente requiera soporte a la ventilación, aunque los valores de la gasometría se encuentren dentro del rango normal. Los pacientes en los que se usó la VMNI presentaban disnea y/o polipnea, como se reporta en la literatura,5 marcada ansiedad, intolerancia a la interface e hipoxemia refractaria a otras alternativas previas de oxigenoterapia.3) Su importancia se manifiesta en que los principales criterios para el inicio o el fracaso de la VMNI lo determinaron elementos clínicos, hemogasométricos o sus interrelaciones en índices como el ROX y HACOR. En el estudio de Xie,19 la disnea fue un factor independiente de muerte.
Una vez que se logran las metas de oxigenación no se recomienda modificar los parámetros ventilatorios por un periodo de 48-72 h porque el ARDS en la COVID-19 no es un proceso de corta duración15) y los cambios frecuentes en el ventilador pueden asociarse a desreclutamiento alveolar, asincronía paciente-ventilador y a la pérdida de los beneficios obtenidos en confort y oxigenoterapia. Por esas razones no se utilizó la estrategia de alternar la VMNI y la CNAF para la oxigenación ni aun para alimentar a los pacientes, sino que se colocó una sonda nasogástrica en el momento de decidir el empleo de VMNI para utilizarla en la nutrición y la hidratación.
La ventaja del protocolo de actuación del CFigali fue que se dispuso de diagramas y guías de actuación2,10 que son necesarios para homogenizar el manejo del paciente y orientar a profesionales más jóvenes en una conducta que tiene matices clínicos variados. El éxito de la VMNI depende del cumplimiento de un protocolo de manejo integral con varias intervenciones.
Uno de los aspectos controvertidos en la VMNI es la bioseguridad del personal de salud, en particular por el riesgo de infección con el SARS-Cov-2 por los aerosoles.1,3,4 No se reportaron casos de COVID-19 en el personal sanitario que trabajó en el centro durante el período de estudio, se debió a que el centro tenía flujos y espacios independientes para los diversos procesos asistenciales y logísticos, un sistema de presión negativa en la unidad de cuidados especiales respiratorios, suficientes medios para la protección personal y colectiva, los trabajadores sanitarios mantuvieron una alta adherencia al protocolo de bioseguridad y todos los trabajadores estaban vacunados.
Por el alto porcentaje de pacientes con ARDS (muchos de ellos con criterios de VMI) y el porcentaje de éxito de la VMNI, nuestros resultados coinciden con lo reportado por otros autores;1,6 de que la VMNI es una estrategia segura, factible y útil que evita la intubación y la VMI en pacientes seleccionados, principalmente en los que tienen un ARDS moderado.
Entre las ventajas atribuibles de la VMNI están que puede realizarse fuera de las unidades de cuidados intensivos, requiere menor número de personal altamente especializado, menor nivel de sedación, facilita una mayor interacción con el paciente, y menores gastos.4,6,7,10 A estas ventajas se añaden menores complicaciones y menor mortalidad atribuibles a la ventilación. Para el éxito es importantes la selección de los pacientes, los criterios para iniciar la VMNI3,7 y la individualización del tratamiento.8
Se concluye que la ventilación mecánica no invasiva es un proceder efectivo en pacientes con síndrome de dificultad respiratoria aguda por la COVID-19, aunque su éxito se relaciona más con las formas menos graves. La razón presión arterial de oxígeno/ fracción inspirada de oxígeno baja junto a las variables clínicas, fueron indicadores clave para decidir el inicio, el éxito o el fracaso de esta modalidad de ventilación, pero no ocurre igual con los valores de la presión arterial de oxígeno, la presión arterial de dióxido de carbono y la saturación periférica de oxígeno. La necesidad de aumentar valores en los parámetros del ventilador durante la VMNI puede indicar falla del proceder.














