Introducción
El estrés por déficit hídrico (sequía) es uno de los más comunes y con más alto impacto en la agricultura, debido a que genera, junto con otros estreses abióticos, disminuciones cercanas al 50 % en la productividad de diferentes cultivos de interés agroeconómico (Sharma et al., 2019; Ullah et al., 2019). Este factor ambiental estresante puede provocar en las plantas un amplio rango de respuestas morfológicas, anatómicas, bioquímicas y moleculares altamente complicadas, como eficiencia disminuida en el uso del agua por la planta, transpiración y fotosíntesis reducida, producción de especies reactivas del oxígeno (ROS, por sus siglas en inglés), membranas celulares dañadas y otras más, que conllevan a la caída de los rendimientos en los cultivos (Takahashi et al., 2020). Una de las opciones para garantizar rendimientos aceptables en el pasto durante la temporada seca es la utilización de especies resistentes al estrés ambiental. Andropogon gayanus (Kunth) se considera una especie forrajera importante para los trópicos, ya que esta gramínea se cultiva de forma extensiva en ecosistemas áridos y semiáridos en varios países, pues es capaz de desarrollarse y crecer en condiciones de estrés de sequía y en condiciones de humedad (Funes et al., 1998).
Entre las estrategias dirigidas a garantizar una nutrición adecuada de los cultivos está el manejo de la simbiosis micorrízico-arbuscular, por sus potencialidades para mejorar la productividad de los cultivos y, a la vez, reducir la necesidad de fertilizantes, ya que las plantas ceden a los hongos micorrízico-arbusculares (HMA) compuestos carbonados procedentes de la fotosíntesis, mientras que estos transfieren a la planta nutrientes minerales, especialmente aquellos menos asequibles (Ezawa y Saito, 2018). Los HMA se consideran los hongos del suelo más abundantes en los sistemas agrícolas, donde pueden representar más del 30 % de su masa microbiana. Debido a esa ubicuidad, la simbiosis micorrízica ha sido considerada la más importante de todas las que involucran a las plantas (Gutjahr y Parniske, 2017). Algunos estudios indican que la inoculación con rizobacterias promotoras del crecimiento vegetal (PGPR, por sus siglas en inglés) puede modular los procesos morfológicos y bioquímicos fundamentales para mitigar el estrés por sequía en las plantas (Jochum et al., 2019; Yaseen et al., 2020). Está comprobado que Azospirillum brasilense posee múltiples propiedades de promoción del crecimiento vegetal, tales como: fijación de N2, actividad 1-Amino-Ciclopropano-1-Carboxilato (ACC)-desaminasa, solubilización de P y producción de fitohormonas, entre otras (Osman et al., 2020).
Por todo lo antes expuesto, este trabajo tuvo como objetivo evaluar la respuesta de A. gayanus a la inoculación con Glomus cubense y A. brasilense, en presencia de estrés por sequía.
Materiales y Métodos
Localización del experimento. El experimento se inició el 29 de abril del 2018 y se evaluó el 24 de septiembre del mismo año (148 días), en la Estación Experimental de Pastos y Forrajes Sancti Spíritus, situada a 21o 53´ 00´´ de latitud Norte y los 79o 21´ 25´´ de longitud Oeste, altura de 40 msnm.
Composición agroquímica básica del suelo experimental. El suelo del área experimental se clasifica como pardo mullido carbonatado (Hernández et al., 2015). El contenido de macronutrientes fue muy bajo en fósforo y potasio y en materia orgánica (tabla 1).
Tabla 1 Características básicas del suelo del sitio experimental.
| Tipo de suelo | P2O5, mg/100g | K2O, mg/100g | MO, % | pH (KCl) |
|---|---|---|---|---|
| Pardo mullido carbonatado | 2,63 | 6,0 | 1,51 | 5,9 |
Temperatura y humedad relativa. Las temperaturas promedio más altas en el período experimental ocurrieron entre junio y septiembre (tabla 2), mientras que hubo predominio de una alta humedad relativa, especialmente en los meses de mayo, agosto y septiembre.
Tabla 2 Valores promedios de temperatura y humedad relativa.
| Mes | Temperatura promedio, °C | Humedad promedio, % |
|---|---|---|
| Abril | 24,3 | 78 |
| Mayo | 24,6 | 86 |
| Junio | 26,4 | 79 |
| Julio | 27,2 | 77 |
| Agosto | 26,7 | 80 |
| Septiembre | 26,3 | 83 |
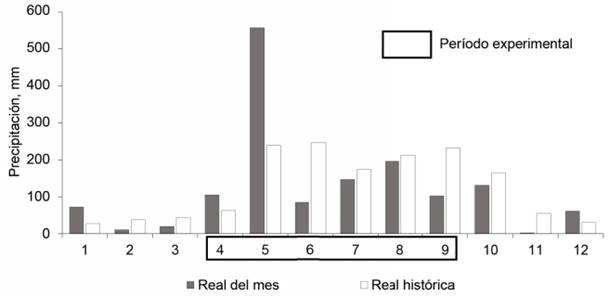
Precipitaciones. En la figura 1 se muestran las precipitaciones del año 2018. En el período experimental, se caracterizaron por ser muy bajas en abril (105,2 mm), junio (84,6 mm) y septiembre (102,3 mm). Excepto en abril y mayo, en el resto de los meses estuvo por debajo de la media histórica. En mayo, a pesar de un total alto de precipitaciones, en las dos primeras decenas fueron muy escasas (Centro Meteorológico Provincial, 2019). En esos dos primeros meses (abril, hasta la segunda decena de mayo), acontecieron importantes etapas fenológicas del cultivo experimental (desde la germinación hasta el desarrollo incipiente de la planta), que coincidieron con muy bajas precipitaciones.
Estado de la sequía agrícola. La intensidad de la sequía agrícola durante el tiempo que duró el experimento (tabla 3) varió de severa (tercera decena de abril, primera y segunda decena de mayo), moderada (segunda y tercera decena de julio y primera decena de agosto), ligera (tercera decena de mayo, mes de junio, primera decena de julio y segunda decena de agosto), y el resto se consideró muy ligera. Este dato indica que el experimento, en general, transcurrió en condiciones de sequía agrícola, la cual se acentuó en las decenas mencionadas de abril, mayo, julio y agosto (Centro Meteorológico Provincial, 2019).
Tabla 3 Categoría de la intensidad de la sequía agrícola en la Estación Experimental de Pastos y Forrajes de Sancti Spíritus.
| Mes/decena | Categoría de intensidad de la sequía agrícola | Clave |
|---|---|---|
| Abril 03 | 4 | Sequía severa |
| Mayo 01 | 4 | Sequía severa |
| Mayo 02 | 4 | Sequía severa |
| mayo 03 | 2 | Sequía ligera |
| Junio 01 | 2 | Sequía ligera |
| Junio 02 | 2 | Sequía ligera |
| Junio 03 | 2 | Sequía ligera |
| Julio 01 | 2 | Sequía ligera |
| Julio 02 | 3 | Sequía moderada |
| Julio 03 | 3 | Sequía moderada |
| Agosto 01 | 3 | Sequía moderada |
| Agosto 02 | 2 | Sequía ligera |
| Agosto 03 | 1 | Sequía muy ligera |
| Septiembre 01 | 1 | Sequía muy ligera |
| Septiembre 02 | 1 | Sequía muy ligera |
| Septiembre 03 | 1 | Sequía muy ligera |
Las decenas de mayor intensidad de sequía correspondieron al período de montaje del experimento, con el rebrote y el desarrollo inicial de las plantas. Por tanto, se infiere que la gramínea, como los microrganismos que se inocularon, se sometieron a un estrés hídrico considerable durante ese espacio de tiempo.
Material vegetal. Se evaluó A. gayanus Kunth (Poaceae), procedente del banco de germoplasma de la Estación Experimental Sancti Spíritus.
Diseño experimental. Se aplicó un diseño experimental de bloques completamente aleatorizados (Melo et al., 2020) con siete tratamientos y ocho réplicas (tabla 4). Las parcelas medían 1 x 5 m (5 m2) y la distancia entre parcelas fue de 1 m. El área experimental neta fue de 16 x 42 m (672 m2).
Tabla 4 Tratamientos que se utilizaron en el experimento.
| No. | Tratamiento |
|---|---|
| T1 | EcoMic® (inmediatamente después del corte) |
| T2 | INICA-8 (inmediatamente después del corte) |
| T3 | INICA-8+ EcoMic® (inmediatamente después del corte) |
| T4 | EcoMic® (inmediatamente después del corte) + INICA-8 (15 días después del corte) |
| T5 | INICA-8 (inmediatamente después del corte) + EcoMic® (15 días después del corte) |
| T6 | Control absoluto (CA) |
| T7 | Testigo fertilizado (TF) con 150 kg de N/ha (NH3NO4) |
Cepa bacteriana. Se utilizó la cepa INICA-8, de A. brasilense, provista por el Instituto de Investigaciones de Pastos y Forrajes (IIPF). Según recomendaciones del fabricante, el preparado se diluyó en agua común, en una proporción de 1:10. La inoculación se realizó inmediatamente después del corte de establecimiento (o a los 15 días después del corte, según correspondía), con un inóculo con concentración celular de 109-1010 UFC/mL. Se utilizó una bureta graduada de 1 L, cuyo contenido se vertió sobre las macollas recién cortadas (o a los 15 días después del corte, de forma que, al regular el surtidor, cada macolla recibió alrededor de 125 mL del inóculo líquido (40 L/ha).
Cepa de hongos micorrízicos arbusculares. Se utilizó el producto EcoMic®, basado en G. cubense, provisto por LABIOFAM 1 Sancti Spíritus, que contenía 30 esporas/g de sustrato. Según recomendaciones del fabricante, el preparado se diluyó en agua común, en una proporción de 1:10. Se inoculó al aplicar la dilución acuosa sobre las macollas recién cortadas (o a los 15 días después del corte, según el tratamiento), a razón de 125 mL/macolla, con dosis equivalente a 50 kg/ha.
Agrotecnia del experimento. El experimento se realizó en un área previamente establecida, de 20 x 46 m (920 m2), destinada a la producción de semilla de Andropogon. Se efectuó un corte y un cultivo con bueyes después de la cosecha de la semilla, para proceder inmediatamente a la inoculación, y no se aplicó riego durante el período experimental.
Determinación del estado de sequía agrícola. El estado de sequía agrícola se determinó a través del índice de aridez o índice de sequía agrícola (IE) (Solano y Vázquez, 1999), que se utilizó para comprobar si el experimento se efectuaba en condiciones de estrés hídrico:
donde:
ETR-Evapotranspiración real estimada, dependiente del estado de humedad del suelo. ETP- Evapotranspiración potencial estimada, dependiente de las condiciones atmosféricas.
Cuando ETR=ETP, el aprovisionamiento de agua del suelo es adecuado.
Cuando ETR<ETP, hay insuficiencia de agua.
Variables. Peso seco de la parte aérea (PSPA, kg/ha: extrapolado. Se pesó la biomasa aérea, compuesta de hojas, tallos, órganos de reproducción y material senescente. Previamente se secó a 60 oC, durante 48 horas, en estufa. La longitud del tallo (LT, cm) se midió desde la superficie del suelo hasta la inserción de la primera inflorescencia. La longitud de la sección floreciente del tallo (LSFT, cm) se midió desde la inserción de la primera inflorescencia, hasta la inserción de la inflorescencia terminal. Para la longitud de la inflorescencia (LInfl., cm) se midió la longitud del pedúnculo conjuntamente con la de las espiguillas. En lo que respecta al peso seco de los racimos (PSRAC, g), se pesaron los racimos con espiguillas maduras, para lo que se secaron a 60 oC, durante 48 horas, en estufa y floración (flor, %). Se contó el número de tallos con flores y se calculó el por ciento con respecto al total.
Índice de eficiencia de la inoculación (IEI, %), según la fórmula de Santillana et al. (2012):
Análisis estadístico. Se realizó un análisis de varianza. Las diferencias entre medias se determinaron por LSD de Fisher. Los datos porcentuales se transformaron por 2arcosen√P para garantizar el cumplimiento de los supuestos (López y González, 2016). Se utilizó el programa estadístico StatGraphics Centurion XV (STATGRAPHICS Centurion, 2007).
Resultados y Discusión
Peso seco de la parte aérea. Esta variable (fig. 2) se caracterizó por la superioridad (p < 0,0001) de los valores del testigo fertilizado sobre todos los tratamientos (12 036,1 kg/ha). Los tratamientos EcoMic® (9 612,5 kg/ha), EcoMic®+INICA-8 (8 475,0 kg/ha) y EcoMic®(corte)+INICA-8 (15 días) fueron superiores al control absoluto (6 822,2 kg/ha), así como al resto de los tratamientos inoculados.
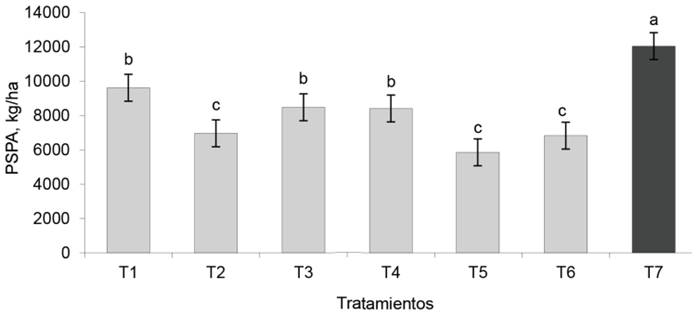
Figura 2 Efecto de los tratamientos en el peso seco de la parte aérea (PSPA) de A. gayanus. Dato de un corte (datos extrapolados)
Los valores totales en el PSPA fueron superiores a los que obtuvieron Reyes-Pérez et al. (2018), para A. gayanus en 75 días de cultivo, pero similares a los de Argel et al. (2007), para Brachiaria hibrido cv Mulato II, en 105 días de cultivo. De acuerdo con los resultados en dicha variable, por encontrarse el experimento en condiciones de sequía agrícola, no se descarta que uno de los factores que propició la tolerancia de la planta al estrés hídrico, haya sido la utilización de Azospirillum en las combinaciones microbianas correspondientes.
Tiwari et al. (2018) afirmaron que muchas rizobacterias contienen la enzima 1-aminociclopropano-1-ácido carboxílico (ACC) desaminasa, que escinde el precursor del etileno, el ACC, en α-cetobutirato y amonio. Por lo tanto, reduce los niveles de etileno en las plantas sometidas a estrés por sequía. Esto permite que el sistema radical se pueda desarrollar sin la inhibición propia de este compuesto, lo que propicia mayor absorción de nutrientes por la planta y, por tanto, su mayor desarrollo.
Hubo efecto superior en la aplicación simple de G. cubense, así como en su inoculación inmediatamente después del corte de establecimiento, seguido de la inoculación con Azospirillum. Es posible que la formación de micorrizas en las raíces de la planta a través de la inoculación con los hongos micorrizicos arbusculares (HMA) facilitara la entrada posterior de la bacteria en el tejido radical, donde la producción de sus metabolitos tendría mayor efecto en la planta.
Bécquer et al. (2019) obtuvieron valores superiores de la biomasa aérea de Cenchrus ciliaris L., en comparación con el control absoluto, al inocular la rizobacteria Bradyrhizobium sp., y Funneliformis mosseae, en condiciones de estrés hídrico. Djonova et al. (2016) hallaron que la combinación de HMA y A. brasilense conllevó a valores superiores de la biomasa aérea en las gramíneas Festuca arundinacea (Schreber) y Phleum pretense L.
Al calcular el IEI sobre la base del PSPA (fig. 3), se observó que el tratamiento inoculado con EcoMic®, fue el que más eficiencia presentó, seguido de EcoMic®+INICA-8 y de EcoMic® (corte)+INICA-8(15 días), mientras que fue insignificante en INICA-8, y nulo en INICA-8(corte) + EcoMic® (15 días).
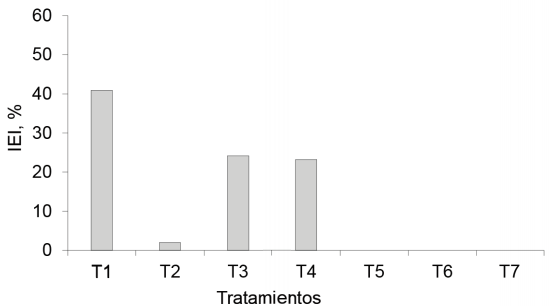
Figura 3 Índice de eficiencia de la inoculación sobre la base del PSPA en Andropogon gayanus, en un corte.
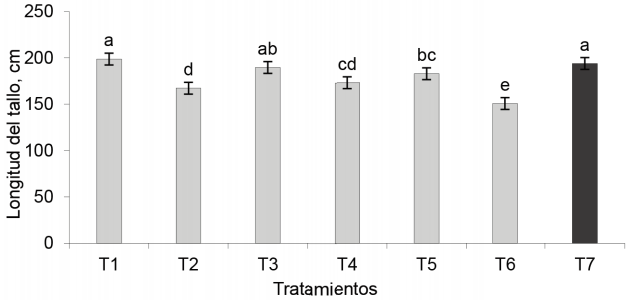
Longitud del tallo. El tratamiento inoculado con EcoMic® fue superior (p < 0,001) al control absoluto, a INICA-8, a EcoMic® (corte)+INICA-8(15 días después del corte) y a INICA-8 (corte)+ EcoMic® (15 días después del corte), aunque no difirió del testigo fertilizado y con EcoMic®+INICA-8 (fig. 4).
Estos resultados concuerdan con los de Díaz-Franco et al. (2008), quienes observaron que la aplicación simple de Glomus intraradices en sorgo, tuvo un efecto superior a la aplicación de A. brasilense, en la altura de la planta.
Castillo-Pacheco et al. (2018), en experimentos con tomate, observaron que la longitud del tallo se incrementaba más con la aplicación de G. cubense, que con otras especies de dicho género.
Sanclemente-Reyes et al. (2018) consideran que a través de la simbiosis que se establece entre los HMA y las plantas, se incrementa la absorción de algunos nutrientes de difícil movilidad en el suelo (P, Fe, entre otros), debido a la acción del micelio externo de los HMA, unido a los sistemas radicales de las plantas, mayor absorción de agua, de N, K y de algunos micronutrientes.
Diversos estudios han mostrado que comunidades de diversas bacterias asociadas a HMA potencian la micorrización y el crecimiento de las plantas (Agnolucci et al., 2015), lo que se aplica también al presente experimento, por ser la combinación de G. cubense con A. brasilense en el momento del corte, uno de los tratamientos que mostró superioridad estadística.
Mohamed y Massoud (2017), al inocular una combinación de Azotobacter y HMA en naranja, observaron un sinergismo que se evidenció en el crecimiento de las plantas, en la extracción de N, P y K en las hojas, y en el rendimiento. Bécquer et al. (2021)) hallaron que la inoculación combinada de G. cubense y A. brasilense (cepa INICA-8) ejerció un efecto superior en las variables estudiadas, sobre todo en la longitud del tallo y el número de ramas. No obstante, Sánchez-de-la-Cruz et al. (2008) encontraron que, en experimentos de invernadero, la inoculación simple de G. intraradices, así como de A. brasilense, incrementó la altura de la planta en trigo, pero la combinación de estos microorganismos no tuvo un efecto perceptible en las variables estudiadas.
Longitud de la sección floreciente del tallo. En esta variable se corroboró el efecto en la planta de la aplicación combinada de los biofertilizantes, aunque solo el tratamiento combinado EcoMic® (corte) + INICA-8 (15 días después del corte) fue superior (p < 0,01) a la aplicación simple de EcoMic®, a INICA-8 y al control absoluto. EcoMic® (corte) + INICA-8 (15 días después del corte) no difirió de INICA-8 (inmediatamente después del corte) + EcoMic® (15 días después del corte), con EcoMic+INICA-8, así como con el testigo fertilizado. Estos tres últimos tratamientos, a su vez, fueron estadísticamente similares al control absoluto (fig. 5).
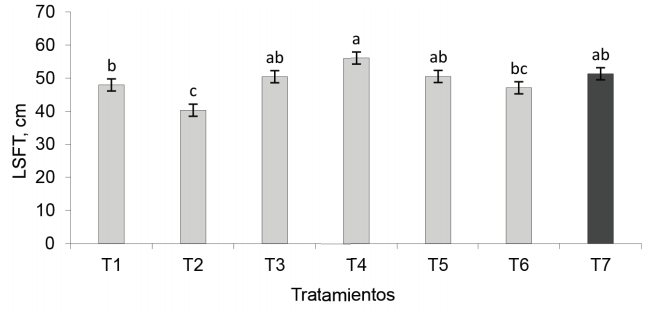
Figura 5 Efecto de la inoculación de A. gayanus en la longitud de la sección floreciente del tallo (LSFT).
La aplicación inicial de los HMA y la aplicación posterior de Azospirillum a través del producto INICA-8 influyó en el efecto positivo de ese tratamiento. Se conoce que los HMA son componentes integrales de la rizosfera, cuyas plantas permanecen estrechamente asociadas mediante una red de hifas interconectadas que incrementan el volumen de suelo que exploran las raíces, mejoran su estructura y facilitan la absorción de los nutrientes y el agua, entre otras funciones (Motta et al., 2017; Busso y Fernández, 2018). Omar et al. (2017) informaron que A. brasilense aumenta la disponibilidad de nutrientes a la planta y modula el nivel de hormonas en las plantas, ya que sintetiza ácido indolacético (AIA), ácido giberélico (GA3) y ácido absísico (ABA). También disminuye la producción de acetileno en las plantas por la vía de la ACC-desaminasa (Renoud et al., 2022). Tiwari et al. (2019) aseguran que Azospirillum es una rizobacteria capaz de contrarrestar el efecto de la sequía en las plantas a través de sus mecanismos de promoción del crecimiento vegetal.
La interacción entre HMA-bacteria incrementa la colonización de ambos microrganismos en el hospedero. Por una parte, se aumenta la germinación y el crecimiento de las hifas de los endófitos y, por otra, se acrecienta la población de bacterias en la rizosfera de las plantas en presencia de los HMA (Long et al., 2017).
Reyes-Rouseaux et al. (2020), mediante la inoculación combinada de Azospirillum y HMA en Urochloa hibrido vc. Mulato II, sin la aplicación de nitrógeno, observaron que los indicadores agroproductivos estudiados alcanzaron valores similares a los registrados con la adición de 100 kg de N/ha.
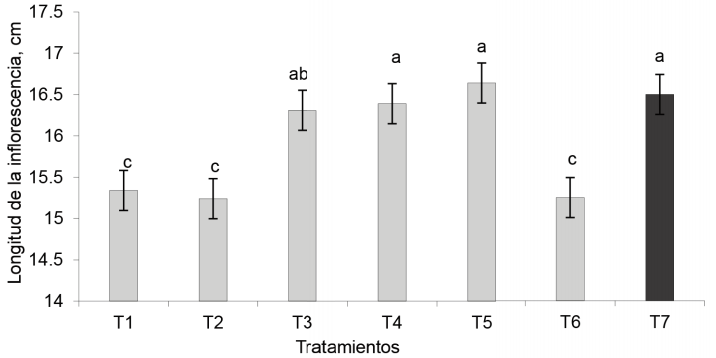
Longitud de la inflorescencia. Los tratamientos EcoMic® (corte) + INICA-8 (15 días) (16,39 cm) e INICA-8 (corte)+ EcoMic® (15 días) fueron superiores (p < 0,05) al control absoluto, a EcoMic® y a INICA-8. Además, fueron similares al testigo fertilizado y con EcoMic®+INICA-8 (figura 6).
El experimento se encontraba en condiciones de sequía agrícola en determinados momentos de su desarrollo, por lo que no se descarta que Azospirillum haya influido en la tolerancia de las plantas al estrés hídrico. Según Pereyra et al. (2012), las plántulas de trigo, inoculadas con cepas de Azospirillum, se benefician con un nivel de agua mejorado durante el estrés salino y estrés osmótico, debido a que los conductos del xilema se ensanchan, así como se mejora la conductancia hídrica coleóptila. Azospirillum, al igual que otras rizobacterias, es capaz de inducir la síntesis de enzimas antioxidantes en las plantas, lo que reduce el efecto destructivo de las especies reactivas del oxígeno (Fukami et al., 2018).
Se conoce que la simbiosis micorrízica tiene un efecto marcado en las relaciones hídricas de las plantas y del suelo en condiciones de estrés, pues modifica positivamente la conductancia estomática, la tasa fotosintética, el potencial hídrico foliar, la concentración de osmolitos, la eficiencia en el uso del agua y la asimilación de nutrientes; mientras que los exudados fúngicos promueven la cohesión de las partículas del suelo e incrementan la retención de agua ( van der Heijden et al., 2017). También, en esta variable, la combinación de estos dos microorganismos influyó de manera significativa en la planta. Meenakshisundaram et al. (2011) encontraron efecto beneficioso en el crecimiento, la biomasa y en el contenido de nitrógeno y de clorofila, al inocular Delonix regia con una cepa de Azospirillum, sola o en diferentes combinaciones con HMA.
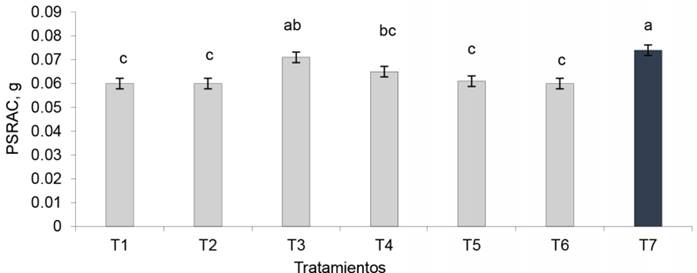
Peso seco de los racimos. El tratamiento EcoMic®+INICA-8 (fig. 7) fue superior (p < 0,05) al control absoluto, a EcoMic®, a INICA-8 (0,060 g cada uno), así como a INICA-8 (corte)+EcoMic (15d) (0,061 g), pero fue estadísticamente similar al testigo fertilizado (0,074 g) y a EcoMic® (corte)+INICA-8 (15d) (0,065 g). El IEI fue mayor para EcoMic®+INICA-8 (18,3 %). Aunque no se puede considerar alto, fue el de mayor impacto en esta variable (fig. 8.
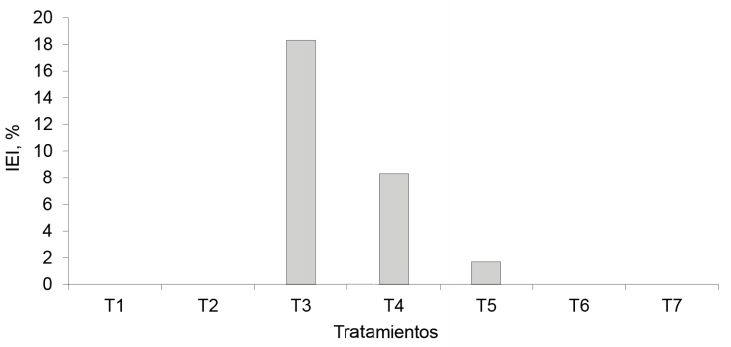
Figura 8 Índice de eficiencia de la inoclución (IEI) en los tratamientos inoculados de A. gayanus, sobre la base del peso seco de los racimos.
Al igual que en las variables anteriores, la aplicación simple de INICA-8, no ejerció efecto superior. Esto se pudiera atribuir a que diversos factores bióticos y abióticos afectaron el comportamiento de la bacteria y produjeron respuestas inconsistentes de la biofertilización. Entre estos factores están las condiciones físico-químicas del suelo, el genotipo del hospedante y la capacidad de la bacteria para establecerse y para competir con la microflora nativa (Pecina-Quintero et al., 2005). También se debe añadir a estos factores, el estrés por sequía, que pudo haber afectado a las plantas como a la rizobacteria que se inoculó.
Sin embargo, se observó que la combinación de ambos biofertilizantes en un mismo espacio de tiempo resultó superior en cuanto a su efecto en las plantas con respecto a su aplicación simple. Por ello, se infiere que hubo efecto sinérgico positivo de los microorganismos que componen estos productos.
Bécquer et al. (2019b) informaron de que la combinación de Bradyrhizobium sp. con G. cubense influyó en los resultados de todas las variables agroproductivas y bioquímicas que se evaluaron en el pasto Mulato II.
Según Olalde-Portugal y Serratos (2008), la combinación simultánea de rizobacterias promotoras del crecimiento y hongos micorrízicos arbusculares induce sinergismo, que se expresa en un incremento del crecimiento, del contenido de fósforo en las plantas y del rendimiento, comparadas con las inoculadas por separado. Bona et al. (2017) consideran que el resultado de la simbiosis mutualista tripartita entre HMA-bacteria-hospedero es el incremento en el desarrollo de la planta, ya que se aumenta su capacidad para absorber del suelo más agua y nutrientes como nitrógeno, fósforo, potasio y microelementos.
Floración. Los tratamientos inoculados con EcoMic®+INICA-8 y EcoMic® (corte)+INICA-8(115 días después del corte) fueron superiores (p<0,05) al control absoluto. EcoMic®+INICA-8 tuvo también valores superiores a INICA-8 (0,4462), pero no difirió del testigo fertilizado (0,7129), de EcoMic® (corte)+INICA-8 (15 días después del corte), de INICA-8 (corte)+ EcoMic® (15 días después del corte) y de EcoMic® (figura 9). El IEI (fig. 10) fue superior para EcoMic+INICA-8 (84,19 %), seguido por EcoMic® (corte)+INICA-8(15d) (61,97 %).
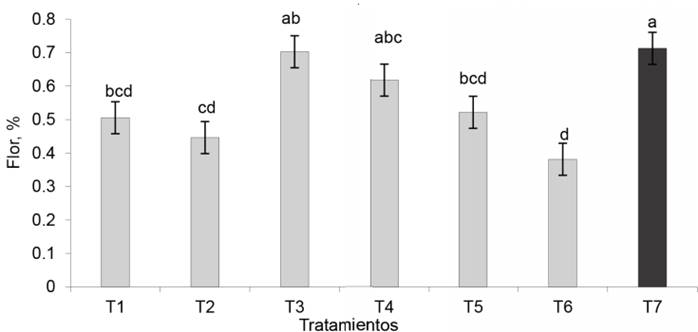
Figura 9 Efecto de la inoclución de A. gayanus en la floración. Se muestran valores transformados con 2arcosen√P en el eje Y, y valores originales dentro de las barras.
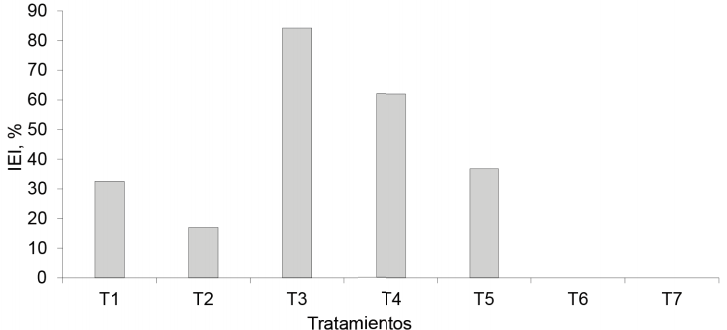
Figura 10 Índice de eficiencia de la inoculación (IEI) en los tratamientos inoculados de la A. gayanus, sobre la base de la floración.
Aunque en el presente estudio no se cuantificó la cantidad de fósforo en la planta, se conoce que entre las múltiples funciones de este macroelemento está la de influir positivamente en el desarrollo de las flores (Ávila, 2005).
La marcada diferencia en el número de tallos con flores entre los tratamientos micorrizados en el momento del corte y combinados con Azospirillum con el control, se pudo deber a la cantidad de P absorbido por las plantas por la acción de los HMA, que se aplicaron desde el primer momento. Esta hipótesis se fundamenta por diferentes autores que corroboran que el P es uno de los nutrientes cuya absorción se favorece por la acción de las micorrizas, pues además de su baja movilidad, sobre todo en las regiones tropicales, entre 95 y 99 % de las cantidades de este elemento se encuentran en formas no disponibles para las plantas (Zhang et al., 2018). Estos beneficios se deben, en parte, a la exploración de las hifas en el suelo en la búsqueda de nutrientes y agua, lo que amplía las capacidades de las raíces por sí solas. También Omar et al. (2017) y Osman et al. (2020) informaron acerca de la capacidad de A. brasilense para solubilizar los fosfatos. Por otra parte, eexisten evidencias de que la combinación de estos microorganismos puede desempeñar un efecto superior en las plantas (Bona et al., 2017).
En este experimento, no se observó incremento de la floración al inocular el cultivo con Azospirillum, o HMA por separado, sino que, de forma similar a las demás variables estudiadas, solo la combinación de estos microorganismos, en el mismo espacio de tiempo, como de forma fraccionada, influyó de forma eficiente en esta variable. No obstante, Pérez et al. (2018) hallaron que la inoculación simple con HMA en Plukonetia volubilis favoreció la formación de flores, debido a la influencia de las fitohormonas que producen dichos hongos, que inciden en el crecimiento y floración. Es posible que la ubicación taxonómica de las plantas influya en su respuesta a dicho estímulo.
Conclusiones
La aplicación simple de INICA-8 no tuvo efecto en ninguna de las variables estudiadas. Sin embargo, el EcoMic® en el momento del corte, de forma simple, o combinada con Azospirillum, fue determinante en la mayoría de las variables. Estos resultados demuestran la importancia de la aplicación de EcoMic® en este cultivo, bajo condiciones de estrés por sequía, así como la sinergia entre los microorganismos que se inocularon, debido a un efecto superior en la planta, al combinarse entre sí.
Recomendaciones
Se recomienda evaluar los tratamientos seleccionados en otros ensayos de campo con Andropogon, en diferentes condiciones edafoclimáticas y en varios cortes.