INTRODUCCIÓN
La lepra es una de las enfermedades más antiguas que recuerda la humanidad. Es una enfermedad granulomatosa sistémica, crónica y contagiosa, producida por el Mycobacterium leprae -ML- (bacilo de Hansen). Es un bacilo ácido alcohol resistente, gram positivo intracelular obligado, que presenta tropismo hacia células del sistema reticuloendotelial y del sistema nervioso periférico, principalmente las células de Schwann (única micobacteria con estas características).1,2 Fue descubierto por Gerhard Armaeur Hansen en 1873 en Bergen, Noruega, pero no es hasta siete años después que el alemán Albert Neisser logra teñir las micobacterias.3
Se transmite de persona a persona. Aproximadamente el 90% de las personas son resistentes al bacilo y no desarrollan la enfermedad a pesar de infectarse.4,5 La lepra es una neuropatía periférica desde su comienzo,6 la duración de los síntomas puede variar desde pocos meses (seis) hasta 20 años.7
Se presenta un paciente con pocos meses de evolución de la enfermedad con alteración sensorial como único síntoma.
INFORMACIÓN DEL PACIENTE
Paciente masculino de 19 años de edad, con antecedentes de salud aparente. A inicios de enero del año 2019 el paciente acudió a la Consulta de Neurología del Policlínico Universitario “Chiqui Gómez” de la Ciudad de Santa Clara, Provincia de Villa Clara, por parestesias en ambos miembros inferiores, con distribución en parches, y que ulteriormente aparecían estas manifestaciones en ambos miembros superiores, sin presencia de lesiones cutáneas ni otros síntomas aparentes. No se recogieron antecedentes epidemiológicos.
Al examen físico el paciente se encontraba en buenas condiciones generales y no tenía lesiones cutáneas. Al examen neurológico se encontraron reflejos osteotendinosos disminuidos en ambos miembros inferiores, con zonas de hipoestesia y anestesias que alternaban principalmente a nivel de distribución del nervio peroneo y tibial, así como con zonas de hipoestesia en la cara lateral del antebrazo derecho.
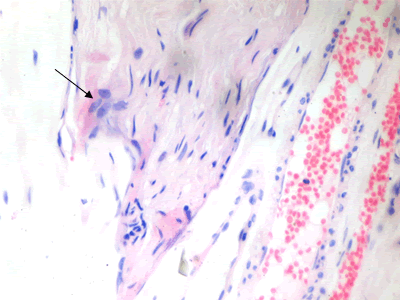
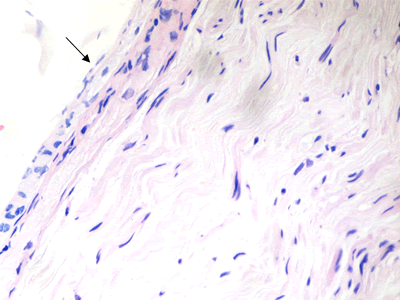
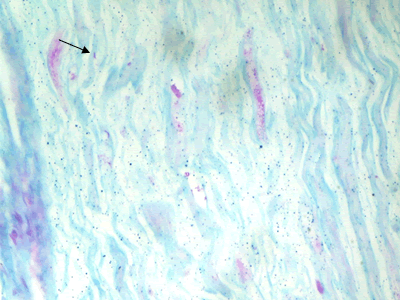
Se le realizaron estudios complementarios: hemograma, coagulograma, hemoquímica, proteínas C reactivas, determinación de antígenos de hepatitis B y C, determinación proteína Bense-Jones, virus de inmunodeficiencia humana y prueba serológica para la sífilis, anticoagulante lúpico, factor reumatoideo y determinación de inmunoglobulinas IgA, IgM, IgG, C3 y C4. El único resultado fue IgM discretamente aumentada (13,9 g/l). Se estudió el líquido cefalorraquídeo (LCR) citoquímico, bacteriológico, citológico y T gram en LCR, con características normales. Se le practicó estudio de conducción nerviosa (ECN) motora, que fue normal; el ECN sensitiva no se exploró por dificultad técnica del equipo. Se realizó baciloscopia y biopsia de piel, normal. Se le practicó biopsia del nervio sural, que confirmó el diagnóstico clínico presuntivo: pequeños granulomas de células epitelioides (Figura 1), macrófagos y linfocitos, dentro de los fascículos y alrededor de ellos con fibrosis del perimisio (Figura 2 y Figura 3), con la técnica de Fite-Faraco se observan numerosos bacilos en las células de Schwann y en los granulomas (Figura 4).
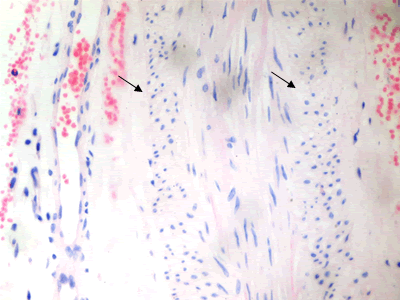
Figura 1 Corte longitudinal de nervio sural en el que se observan dos granulomas de células epitelioides (flechas) entre las fibras nerviosas (H/Ex40)
Impresión diagnóstica: neuropatía sensitiva secundaria a lepra neural.
El tratamiento depende de la clasificación de la lepra neural pura (LNP); no obstante, se tiene en cuenta el número de troncos nerviosos comprometidos. En este caso en particular se evidenció un compromiso de más de un tronco nervioso, lo que derivó en comenzar tratamiento con rifampicina, dapsona y clofazimina por un total de 12 meses.
DISCUSIÓN
La LNP es una forma clínica de la enfermedad que se presenta usualmente en hombres jóvenes y cursa como una neuropatía periférica con ausencia de lesiones en la piel. Compromete principalmente los nervios auricular, mediano, cubital, peroneo y ciático poplíteo externo y los afecta en su trayecto más superficial, puede comprometer uno o varios troncos nerviosos y se manifiesta con neuritis, definida como engrosamiento neural, hipersensibilidad neural al tacto y pérdida de la función sensitiva y motora.8
La aspiración mundial era declarar la erradicación de la lepra en enero de 2015, pero ese reto fue incumplido debido a que cada año aparecen en el mundo 515 000 nuevos casos, de los que el 12% corresponden a edades pediátricas.9
En Cuba la lepra no constituye un problema de salud desde 1993, año en que se alcanza una tasa de prevalencia de menos de un caso por cada 10 000 habitantes; no obstante, anualmente son diagnosticados entre 250 a 300 casos, con informes en todas las provincias.9
Patogenia: se considera que el único reservorio de importancia epidemiológica del Mycobacterium leprae (ML) es el ser humano enfermo bacilífero. Hay evidencia sólida de la transmisión entre humanos pero, hasta el momento, ningún estudio ha demostrado inequívocamente cuáles serían los mecanismos exactos de transmisión del ML, para lo que se admite que es necesario el contacto directo, cercano y prolongado entre un enfermo bacilífero y una persona susceptible. La vía de transmisión más aceptada es la respiratoria. El contagio desde heridas cutáneas podría ser una opción factible, pero no ha sido validada del todo.
La aparición o no de la enfermedad está íntimamente relacionada con la respuesta celular del huésped ante el ML, aunque los mecanismos inmunológicos subyacentes no están claros. Se ha establecido que el 90% de las personas son resistentes naturales al ML, es decir, se pueden infectar, pero no enfermar. Esta condición de enfermar o no proviene tanto de la respuesta inmune del huésped (determinada genéticamente) como de la magnitud de la carga bacilar, el tiempo de exposición al bacilo y la vacunación previa con BCG. Solo el 5% de las personas no tiene una respuesta inmunológica adecuada para evitar la infección y, de ellas, solo un 10% evoluciona a enfermedad. La lepra está relacionada con genes ligados al sistema HLA y no HLA, los que impactan en la susceptibilidad del huésped al ML tanto en la resolución de la infección como en el tipo de presentación clínica que tendrá la enfermedad. A este factor genético se le suman factores ambientales relacionados con las condiciones de vida de las personas como son la desnutrición y las condiciones de hacinamiento.10,11
Fisiopatología: una vez que el ML entra al organismo es fagocitado y destruido por los polimorfonucleares neutrófilos. Si logra evadir esta barrera defensiva el bacilo es fagocitado por macrófagos o las células de Langerhans, atraviesa las paredes de los endotelios y llega a los vasos y los ganglios linfáticos, en donde los macrófagos presentan los antígenos del ML a los linfocitos T CD4 y T CD8, lo que determinará la forma de la enfermedad. El complejo bacilo-macrófago se aloja en la piel, en las mucosas y alrededor de vasos sanguíneos y los nervios. En la piel se ubica en la unión dermoepidérmica, el folículo piloso, la glándula sebácea, la glándula sudorípara, el músculo piloerector y alrededor de vasos sanguíneos y los nervios. La forma de la enfermedad que desarrolle el huésped dependerá del mecanismo inmunogenético que se active; puede ser hiperérgico o anérgico. Si el mecanismo que se activa en el huésped es hiperérgico (vía linfocito T CD4) habrá una alta reactividad inmune contra el ML que llevará a la destrucción de los anexos cutáneos, a la compresión de los vasos sanguíneos y a la destrucción de los filetes nerviosos. Si el mecanismo que se activa es anérgico (vía linfocito T CD8) habrá tolerancia inmunológica, de modo que el ML se desarrollará libremente en el interior de los macrófagos, producirá cambios lipídicos intracelulares, dará paso a las llamadas células de Virchow y determinará la formación de granulomas de células espumosas que contienen los bacilos y sin las características destructivas del mecanismo hiperérgico. El ML es la única bacteria patógena que es capaz de invadir la célula de Schwann de los nervios periféricos humanos. El tropismo del ML por la célula de Schwann estaría dado por la unión del bacilo al dominio G de la cadena alfa 2 de laminina 2, que es un componente exclusivo de la lámina basal de los nervios periféricos. El desarrollo de la enfermedad y su presentación clínica dependen del estado inmunológico del paciente que, a su vez, está determinado genéticamente. El cromosoma 10p13 relacionado con el gen que codifica para receptores de manosa tipo 1 (que corresponden a receptores fagocíticos de los macrófagos) se ha asociado a la susceptibilidad genética. También existe una relación entre genes de clase II del complejo mayor de histocompatibilidad y el tipo de enfermedad que se desarrolla. Los HLA DR2 y HLA DR3 se asocian al desarrollo de formas tuberculoides, mientras que el HLA DQ1 se relaciona con la forma lepromatosa. Cuando la respuesta inmune del huésped es intensa se desarrollan las formas tuberculoídeas de la lepra, con presencia de granulomas con abundantes histiocitos epitelioides, células gigantes multinucleadas y linfocitos T CD4 productores de interferón gamma; la ausencia o la poca presencia de bacilos ácido-alcohol resistentes es uno de los hallazgos histológicos más importantes. En cambio, la ausencia de inmunidad específica determina el desarrollo de las formas lepromatosas de la lepra, en las que existe proliferación de los bacilos en los tejidos, se observan macrófagos espumosos, pocos linfocitos CD4 y CD8 y, característicamente, no hay formación de granulomas.11,12
Diagnóstico: la exploración clínica, junto con los frotis cutáneos, son los medios más habituales para diagnosticar la lepra en los países endémicos. Son las lesiones cutáneas características, asociadas a la pérdida de la sensibilidad o al aumento de volumen de los nervios periféricos asociados a la presencia de bacilos ácido-alcohol resistentes en una biopsia y frotis de piel (o ambos), los hallazgos fundamentales para confirmar el diagnóstico.
La LNP es la forma de presentación en la que no hay lesiones en piel, es poco frecuente en el medio y su sospecha diagnóstica y tratamiento representa un reto para el personal médico.
Diagnóstico diferencial: cada una de las manifestaciones clínicas principales de la lepra tiene un diagnóstico diferencial distinto: la neuritis hanseniana es menester diferenciarla de una neuropatía diabética, por fármacos o por alcohol o por amiloidosis neural primaria; la neuropatía sensitiva de Wartenberg y el síndrome de Bernhardt o de distensión del nervio fémorocutáneo; la toxicidad por medicamentos: talidomida, DDS, isoniacida; los síndromes compresivos de troncos nerviosos: túnel del carpo; la neuropatía paraneoplásica y la simulación de alteración sensitiva.
Aunque la lepra es muy poco frecuente en el medio, no se puede dejar de considerarla entre los diagnósticos diferenciales en la práctica clínica diaria porque la enfermedad no se encuentra ni mucho menos erradicada. Lo interesante de este caso radica en que, a pesar de solo mostrar el paciente manifestaciones sensitivas, con escaso tiempo de evolución, sin historia de contactos previos y varias pruebas practicadas negativas, se haya logrado, gracias al pensamiento clínico coherente, un diagnóstico certero y concluyente que influyó en la recuperación de este enfermo, sin secuelas demostrables.