Introducción
En los últimos años la aparición de los fármacos antiangiogénicos ha revolucionado el tratamiento de numerosas enfermedades de la retina. Su asociación con la hipertensión ocular tras las inyecciones ha sido objeto de estudio en numerosas ocasiones, estableciéndose una relación directa, tanto en el momento agudo, como a largo plazo.
Dado que la coexistencia de pacientes con glaucoma y degeneración macular asociada a la edad (DMAE) es una realidad, se plantea un nuevo escenario en la práctica clínica. De ahí que sea necesario categorizar mejor a los pacientes e individualizar el riesgo de desarrollo o empeoramiento de su glaucoma si están sometidos a una terapia intravítrea intensiva y adoptar medidas que eviten o reduzcan las posibles consecuencias negativas derivadas de dicho procedimiento.
Caso clínico
Se presenta el caso de una paciente de 78 años de edad con diagnóstico de glaucoma primario de ángulo abierto (GPAA) de cinco años de evolución en ambos ojos (AO). Su mejor agudeza visual corregida (MAVC) era de 0,7 en su ojo derecho (OD) y de 0,8 en su ojo izquierdo (OI). El estado de su enfermedad era estable y se encontraba en tratamiento con colirio de bimatoprost 0,3 mg/ml en AO, cada 24 horas, alcanzando un buen control de las cifras de presión intraocular (PIO). El campo visual (CV) de su OD era normal. Su OI presentaba un escotoma paracentral. La paquimetría en OD 520 µm y OI 512 µm. En el examen funduscópico se objetivó una excavación papilar de 0,5 en OD, con muesca en inferior y aspecto más pálido que en ojo contralateral. El OI presentó una excavación de 0,3. Se objetivaron drusas en el polo posterior y alteraciones del epitelio pigmentario en AO, mayor en el OI.
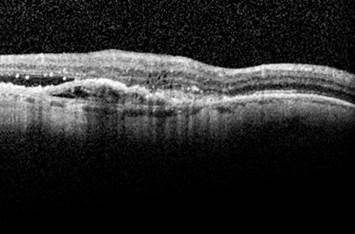
En un examen rutinario de su enfermedad, la paciente refirió una disminución de visión en su OI (MAVC en su OI de 0,4) de días de evolución que resultó ser secundaria al desarrollo de una membrana neovascular tipo 2 objetivada en el examen con tomografía de coherencia óptica (OCT) y a la presencia de una hemorragia macular en el FO (fig. 1). La paciente inició tratamiento con aflibercept intravítreo en régimen de treat and extent. Actualmente recibe inyecciones intravítreas (IIV) con un intervalo de seis semanas.
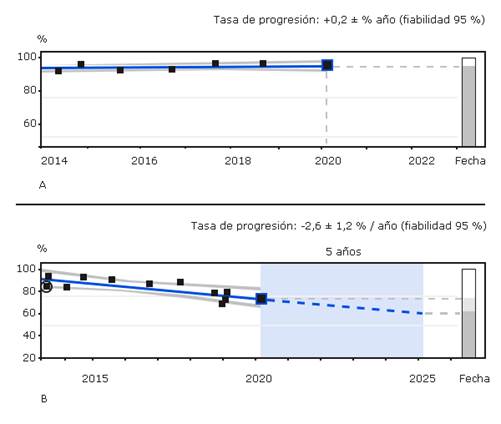
Durante los más de tres años que precisó de tratamiento para su DMAE se acentuó la progresión de su glaucoma, aumentando el defecto en la capa de fibras nerviosa de la retina (CFNR) objetivado con OCT (fig. 2) y el daño en el CV con una progresión evidente, si se compara con el ojo contralateral (fig. 3). Se sospechó de una posible relación causal entre el empeoramiento de su glaucoma y la intensa terapia intravítrea administrada en el OI, por lo que se ajustó el tratamiento de la paciente prescribiéndose colirio de latanoprost y timolol y colirio de brimonidina en el OI antes de cada inyección intravitrea.
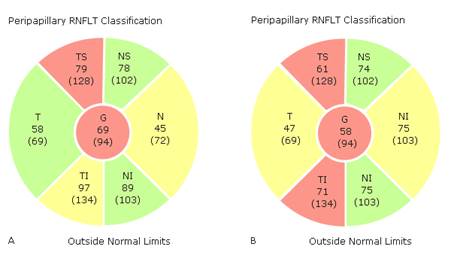
Fig. 2 - Imagen comparativa de la pérdida de CFNR en el ojo izquierdo. A) inicio del tratamiento intravítreo. B) actual.
Discusión
El glaucoma y la DMAE son dos de las enfermedades más frecuentes en la práctica oftalmológica habitual. El glaucoma supone la segunda causa de ceguera a nivel mundial y la segunda causa de ceguera y discapacidad visual. Por otro lado, la DMAE es la principal causa de ceguera en mayores de 55 años de edad y tiene una elevada prevalencia en las últimas décadas de la vida. Tanto el glaucoma como la DMAE suponen una causa importante de discapacidad y una disminución y empeoramiento de la calidad de vida.1
El tratamiento con anti-VEGF intravítreos es uno de los procedimientos oftalmológicos más realizado en las consultas oftalmológicas de todo el mundo y es en la actualidad el principal tratamiento para numerosas enfermedades de la retina y, en concreto, para la DMAE. Se han asociado aumentos tanto agudos como crónicos en la presión intraocular tras la administración de estos fármacos.2
Se ha demostrado que la inyección de anti-VEGF aumenta la PIO a corto plazo en todos los casos, produciéndose un aumento inmediato en todos los pacientes entre 0 y 30 minutos, siendo transitorio y normalizándose antes de los 60 minutos tras pinchazo. Parece que la producción de un pico hipertensivo posterior a la inyección es un resultado lógico al producirse una expansión de volumen en el globo ocular. Se ha descrito que hasta un tercio de los pacientes pueden tener un pico de hipertensión ocular de hasta 50 mmHg.2
Tras un análisis post hoc de los ensayos Marina y Anchor3) se demostró una elevación sostenida de la PIO tras las inyecciones de anti-VEGF, hallazgo apoyado por estudios posteriores.4,5,6
Entre los factores que se han asociado con un aumento del riesgo de HTO sostenida2 están un elevado número en la cantidad de inyecciones al año (más de 7 por año),7 así como un intervalo de tiempo corto entre ellas (< 8 semanas).7 Otros factores para tener en cuenta son: el diagnóstico previo de glaucoma, los pacientes fáquicos y aquellos con cámara estrecha.2 No existe consenso sobre el tipo de anti-VEGF empleado. La paciente es hipermétrope, con cámara estrecha, fáquica y con una frecuencia de inyecciones de 6 semanas, lo que la convertía en una paciente de riesgo de desarrollar HTO tras IIV.
Se ha documentado una exacerbación del glaucoma después del uso de anti-VEGF. Algunos estudios asocian un aumento en el riesgo de necesitar cirugía de glaucoma en la mayoría de los pacientes, el que aumenta en cuanto mayor sea el número de inyecciones,7 una tasa más alta de disminución del campo visual o la pérdida de capa de fibras nerviosas de la retina (CFNR) y la capa de células ganglionares (CCG).8 La paciente experimentó un deterioro en su enfermedad glaucomatosa por lo que planteó realizar en un futuro próximo opciones de tratamiento quirúrgico, por ejemplo, la facoemulsificación combinada con implante XEN® o trabeculectomía.
Existe una serie de intervenciones que mitigarían el riesgo de pico hipertensivo después de cada inyección.2 Con una alta evidencia se encontró que hubo tratamiento previo con fármacos hipotensores tópicos como la brimonidina, timolol o acetazolamida,9 la punción o descomprensión de la cámara anterior con paracentesis o el reflujo de vítreo tras la inyección (por el empleo de una aguja de mayor calibre e inyección recta no tunelizada). Todos ellos buscan evitar o reducir la fluctuación y, por consiguiente, el aumento de la PIO tras inyección. El más sencillo, cómodo y con menos riesgo para los pacientes sería la administración antes del pinchazo de colirios hipotensores, como es el caso presentado en el que se aplicaron rutinariamente colirio de brimonidina. Además de ser efectivo en la reducción del pico hipertensivo, se ha asociado con una tasa menor de hemorragias subconjuntivales tras pinchazo.
Por otro lado, es conveniente analizar las características clínicas de los pacientes e identificar aquellos de alto riesgo, haciendo una estrecha monitorización para detectar el posible desarrollo de HTO o el empeoramiento de glaucoma. Por lo que se evalúan periódicamente mediante control de PIO, examen de OCT y CV.
Valorar el riesgo de HTO tras IIV es fundamental en los pacientes sometidos a terapia intravítrea, especialmente aquellos que padecen glaucoma. Adoptar medidas como la individualización de los tratamientos, la monitorización con controles de PIO y OCT, así como el empleo de fármacos hipotensores antes de la inyección intravítrea ayuda a optimizar el manejo de los pacientes.