Introducción
El envejecimiento ocasiona cambios progresivos, irreversibles, morfológicos y fisiológicos en el organismo y aumenta el riesgo de las diversas enfermedades cutáneas, entre estas el cáncer de piel, que según la Organización Mundial de la Salud, representa uno de cada tres casos de cáncer en el mundo, sobre todo en ancianos, personas de piel clara y aquellos con cultura del bronceado. 1
El cáncer de piel constituye la neoplasia maligna más común a nivel mundial y su incidencia ha ido en alza en las últimas décadas. Se divide en dos grandes grupos: melanoma y no melanoma; dentro de este último se engloban el carcinoma basocelular (CBC) y carcinoma espinocelular (CEC). (2-4
El cáncer de piel no melanoma tiende a crecer lentamente con una muy baja mortalidad, muchos enfermos son tratados sin estudio histopatológico confirmatorio, con lo cual surge un subregistro de casos. (5,6
El CBC es el cáncer de piel más frecuente en el ser humano, representa aproximadamente entre un 70 y un 80 % de los cánceres cutáneos no melanoma en la población de color de piel blanca, este es un tumor maligno de estirpe epitelial y es el más frecuente en la consulta dermatológica, soliendo afectar a individuos mayores de 50 años con máxima incidencia entre la sexta y octava década de la vida.7,8
Este un tumor epitelial maligno de localización cutánea, que surge de células pluripotentes de la zona basal de la epidermis y de la vaina radicular externa del pelo a nivel del istmo inferior y de la protuberancia. Considerado como un tumor de bajo grado de malignidad, ya que puede conducir a una invasión local, destrucción tisular y recurrencias, que compromete la función y estética de la persona, con baja capacidad de producir metástasis. 9-11
El CBC es el tumor cutáneo más frecuente con una incidencia anual estimada del 0,1 al 0,5%. En España, la incidencia del CBC se estima en 113,05 /100.000 personas-año contando un solo tumor por persona. (12
En países como Estados Unidos, la prevalencia y la incidencia alcanzan respectivamente las cifras de 226 y 362 por cada 100.000 habitantes por año. 13
En el año 2019, en Cuba, se presentaron 10 432 casos de cáncer de piel, cifra que lo posiciona como el más frecuente, este constituye el 83 % de este tipo de cáncer con mayor incidencia en zonas como Holguín, Las Tunas, Camagüey y Santiago de Cuba. (14
El CBC puede tratarse de diversas formas, en dependencia de diversos factores: variedad clínica, localización, tamaño de la lesión y otros factores que dependen del paciente. Sin embargo, el tratamiento debe encaminarse a obtener la erradicación completa del tumor y en conseguir resultados funcionales óptimos y estéticos aceptables. Dentro de las opciones del proceso se encuentra el manejo quirúrgico y no quirúrgico. (15-17
El tratamiento de elección ante cualquier forma clínica es la resección quirúrgica (cirugía micrográfica de Mohs o cirugía convencional), debido a que permite el control histológico de los márgenes del tumor y presenta menos tasas de recurrencias. El uso de escisión quirúrgica para el tratamiento de CBC obtiene tasas de curación cercanas al 90 % a los 5 años. (18,19
Dentro de las terapias no quirúrgicas encontramos: la terapia fotodinámica, los inmunomoduladores, la quimioterapia tópica o sistémica, el imiquimod tópico, 5-fluorouracilo tópico, el interferón intralesional, la radioterapia o los medicamentos inhibidores de la vía de Hh (vismodegib y sonidegib). (18,19
La necesidad de encontrar nuevas variantes terapéuticas para el tratamiento del CBC hizo factible una formulación, en la que se combinan interferones (IFNs) alfa y gamma, denominada HeberFERON; 2,18 desarrollado por el Centro de Ingeniería Genética y Biotecnología de la Habana, se han obtenido excelentes resultados con la administración perilesional en CBC con regresión total de las lesiones.8 Su administración logra un efecto anti proliferativo, estimulador de la apoptosis y la inmunomodulación, que puede lograr la desaparición del tumor o reducirlo.18,19
Precisamente, está descrito que el HeberFERON puede utilizarse como tratamiento alternativo oadyuvante de otros procederes (quirúrgicos o no). 18
Teniendo en cuenta lo novedoso de esta nueva alternativa terapéutica y la alta morbilidad por carcinoma basocelularque existen en las consultas de dermatología del Hospital Provincial Universitario ‟Carlos Manuel de Céspedes” de Bayamo, provincia de Granma, se decidió aplicar el HeberFERON a pacientes portadores de carcinoma basocelular con el objetivo de evaluar la efectividad del medicamento en esta patología.
Métodos
Se realizó un estudio, observacional, de serie de casos, de vigilancia temprana del medicamento en condiciones de práctica médica habitual. La investigación se ejecutó en la consulta de oncodermatología, que tiene su sede en el Hospital Provincial Universitario ‟Carlos Manuel de Céspedes” de Bayamo, durante el período comprendido entre enero 2018 a diciembre 2019.
La muestra quedo constituida por 92 pacientes con diagnóstico de CBC, una vez aplicados los criterios de inclusión y exclusión.
Variables y plan de análisis estadístico
Con las variables de respuesta
Análisis de efectividad
Variable principal de efectividad: Respuesta Clínica.
Se estimó la distribución de frecuencia (frecuencia, porcentaje), los intervalos de confianza (IC 95 %) para la proporción de pacientes en cada categoría.
Se estimó el tiempo en alcanzar la respuesta clínica (semanas) Se estimó el intervalo de confianza al 95% para la media y la mediana en que se alcanza la respuesta objetiva de la lesión.
Análisis de Seguridad
Presencia de eventos adversos.
Se determinó la frecuencia de pacientes que desarrollaron eventos adversos, (frecuencia absoluta, porcentaje, Intervalo de Confianza IC 95%).
Se realizó la descripción del evento adverso en cuanto a (tipo, intensidad y gravedad).
Variables secundarias de efectividad.
Se consideró como variables secundarias de efectividad: respuesta dermatoscópica, evaluación histológica, calidad de la cicatrización.
Se estimó la distribución de frecuencias (frecuencia, porcentaje), los intervalos de confianza (IC 95%) para la proporción de pacientes en cada categoría.
Se estimó la curva de Kaplan-Meier para calcular el tiempo hasta la respuesta clínica.
Con las variables de control
Variables de control cuantitativas: Edad, tamaño inicial de la lesión, número de lesiones.
Se estimaron los estadígrafos de tendencia central y dispersión (media, mediana, desviación estándar, valores mínimos y máximos).
Variables de control cualitativas: Sexo, estadio de la enfermedad, fototipos de piel.
Se estimó la distribución de frecuencia (frecuencia, porcentaje).
Se estimaron los intervalos de confianza (IC 95%) para la proporción de pacientes en cada categoría.
Los análisis del balance riesgos-beneficios fueron hechos considerando como beneficio la respuesta objetiva y como riesgo los eventos adversos severos más la interrupción del tratamiento por cualquier causa.
Todos los modelos de estadística bayesiana producen un análisis favorable (factor de Bayes> 1), indicando que, cualesquiera de las condiciones que se tengan en cuenta, el beneficio-riesgo del tratamiento con HeberFERON es absolutamente favorable.
Resultados
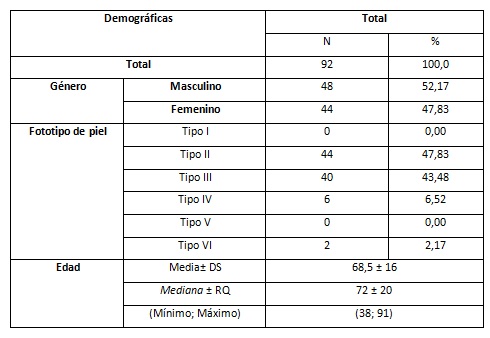
Se refleja en la Tabla 1, que predominó el género masculino 48 (52,17, fototipo de piel tipo II 44 (47,83 %), una mediana de edad de 72 ± 20 años oscilando entre 38 y 91 años.
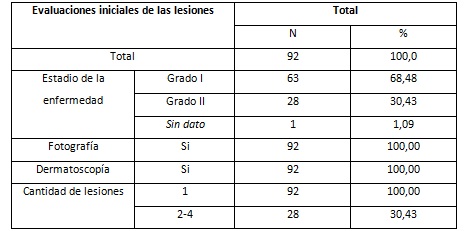
La Tabla 2, refleja que 63 pacientes (68,48 %) corresponde al estadio I, el 30,43 % (28 pacientes) se clasificaron como estadio II. Se le tomó fotografía inicial y se le realizó dermatoscopía a la totalidad de los pacientes incluidos.
La Tabla 3 muestra que del total de pacientes, al realizar la evaluación histológica postratamiento se evidenció presencia de tumor en el 19,57% (18 pacientes). Para la calidad de la cicatrización, se observó que el 92,45 % (49 pacientes), tuvo buena calidad de cicatrización.
Tabla 3 Distribución de pacientes según respuesta clínica al tratamiento.
| Evaluaciones finales | Total | ||
|---|---|---|---|
| N | % | ||
| Total | 92 | 100,00 | |
| Respuesta clínica | Completa | 53 | 57,61 |
| Parcial | 29 | 31,52 | |
| Estable | 8 | 8,70 | |
| Progresión | 2 | 2,17 | |
| Evaluación histológica | Evidencia de tumor | ||
| No evidencia de tumor | |||
| Calidad Cicatrización N=53 | Buena | ||
| Regular | |||
Fuente: Historias clínicas.
Se reportaron en total 12 tipos diferentes de eventos adversos. De los 92 pacientes, el 89,13 % (82 pacientes), presentaron al menos un evento adverso para un total de 501. Los eventos considerados muy frecuentes (≥10%) fueron: escalofríos, dolores articulares, mialgias y anorexia. (Tabla 4)
Tabla 4 Caracterización de eventos adversos.
| Eventos adversos | No | % |
|---|---|---|
| Fiebre | 40 | 7,98 |
| Escalofrío | 61 | 12,18 |
| Astenia | 30 | 5,99 |
| Mareos | 14 | 2,79 |
| Cefalea | 50 | 9,98 |
| Malestar general | 47 | 9,38 |
| Somnolencia | 12 | 2,40 |
| Edema palpebral | 10 | 2,00 |
| Dolores articulares | 78 | 15,57 |
| Vómitos | 26 | 5,19 |
| Mialgias | 79 | 15,77 |
| Anorexia | 54 | 10,78 |
| Total | 501 | 100,00 |
Fuente: Historias clínicas.
Del total de notificaciones, el 74,45 % de los eventos fueron de intensidad grado 1, mientras que el 22,16% eran grado II, según la gradación del CTCAE. El 95,61 % de los eventos no ponían en riesgo la vida del paciente. Durante el estudio no se presentaron eventos adversos graves mortales. (Tabla 5)
Tabla 5 Caracterización global de los eventos adversos según intensidad y gravedad.
| Caracterización | Número de eventos adversos N=501 | ||
| Intensidad | |||
| Grado 1( Leve) | 373 | 74,45 | |
| Grado 2 (Moderado) | 111 | 22,16 | |
| Grado 3 (Severo) | 1 | 0,20 | |
| 16 | 3,19 | ||
| Gravedad | |||
| No grave | 479 | 95,61 | |
| Pone en peligro la vida | 1 | 0,20 | |
| 21 | 4,19 | ||
Fuente: Historias clínicas.
Discusión
El Heberferon es la combinación de interferón-alfa e interferón-gamma se desarrolló en base a dos criterios esenciales; primero, la potenciación in vitro e in vivo de la actividad biológica común de ambos interferones en cierta proporción definida previamente; y segundo, su similar farmacocinética. El estudio clínico con voluntarios sanos indicó que esta formulación era un buen candidato para tratar algunas enfermedades oncológicas, sin interferencias farmacocinéticas ni toxicidad adicional. 18,19
En nuestro estudio predominó el género masculino 48 (52,17%), esta razón está dada porque los hombres suelen estar mucho más tiempo expuestos al sol, aunque en nuestra sociedad las mujeres tienen ocupaciones laborales similares; lo que implica un aumento en el sexo femenino en las últimas décadas. En un hospital universitario, en Irbid, norte de Jordania, la razón hombre/mujer fue de 1,8:1, con un promedio de edad para las mujeres de 65,4 años y para los hombres fue de 61,9 años. En la investigación realizada por Greylis Marrero y colaboradores, encontraron que el 59,2 % de los pacientes fueron del sexo masculino; el grupo entre 61 y 80 años fue el más afectado (62,1 %). En el Hospital de Ayacucho, en ese mismo país, 74,9 % de los pacientes con CBC tenían 61 años o más; sin embargo, difieren con este estudio en cuanto al género, ya que en su muestra 60,7 % eran de sexo femenino. En 520 pacientes de una Universidad Federal de Brasil, el promedio de edad fue de 68,8 años, con rangos de 30 a 98 años; aunque no coincidió con el género, ya que las mujeres predominaron. (11,15
El CBC es más frecuente en pacientes mayores de 40 años; aunque el promedio de edad del primer diagnóstico es aproximadamente 60 años. A pesar que las tasas de CBC varían de acuerdo con la región y la composición étnica de la población. 15
El foto tipo de piel tipo II, el cual se observó en 44 pacientes (47,83 %), demostraron ser la coloración de piel de mayor frecuencia en la aparición de esta patología y coincidiendo con los resultados de otros estudios. La piel clara es un factor de riesgo de padecer CBC al según la mayoría de los investigadores.
Con respecto a las lesiones presentadas por los pacientes se refleja que 63 pacientes (68,48 %) corresponde al estadio I, el 30,43 % (28 pacientes) se clasificaron como estadio II. No tuvimos pacientes en estadio III y IV de acuerdo a la clasificación del TNM en su 8va edición. Estos datos no fueron comparados con otros estudios, pues en los artículos revisados no se recogen, lo que implica un dato estadístico novedoso para este tipo de investigación.
La mayoría de los pacientes tratados con HeberFERON tuvieron una respuesta completa al tratamiento, con desaparición total de las lesiones, que fue estadísticamente significativo (p<0,05). Esto confirmó la hipótesis de que el medicamento tiene un efecto favorable en pacientes con CBC.
El HeberFERON elimina o reduce la masa tumoral. La respuesta antitumoral se alcanza rápidamente y es más prolongada que la lograda por los interferones separadamente, lo cual es expresión de una elevada potencia biológica. Al ser usada en la región periocular evita complejas cirugías y sus secuelas, con un buen perfil de seguridad, al tiempo que logra excelentes resultados estéticos, ofreciendo al paciente una buena. 17
Algunos estudios en Cuba muestran resultados similares al de esta investigación, en cuanto a respuestas favorables. Los pacientes tratados en la provincia de Matanzas tuvieron el siguiente resultado al ser evaluados en la semana 52: respuesta completa (52 %), respuesta parcial (14 %), enfermedad estable (19 %) y un caso mostró enfermedad progresiva (5 %). En el servicio de Oftalmología del hospital general docente “Abel Santamaría Cuadrado”, de Pinar del Río, 66,7 % tuvo una respuesta completa; mientras el resto se comportó de la siguiente manera: respuesta parcial (16,7 %), enfermedad estable (8,3 %) y enfermedad progresiva (8,3 %), estos dos últimos con un caso. En el municipio Puerto Padre, Las Tunas, los 9 pacientes que tenían CBC y que se atendían en el hospital “Guillermo Domínguez López” fueron tratados con HeberFERON. De ellos, 5 casos (55,6 %) tuvieron respuesta completa y 3 casos (33,3 %) respuesta parcial; el otro paciente no se evaluó. En el hospital “Arnaldo Milián Castro”, de Villa Clara, fueron tratados 7 pacientes con CBC periocular, y 6 de ellos (85,7 %) tuvieron una respuesta completa. 17,19
Cuando se realizó la evaluación estética de la respuesta al tratamiento, se encontró que fue muy buena, factor muy importante a tener en cuenta por la localización de las lesiones. De manera general se puede decir que el tratamiento con HeberFERON es bueno en cuanto a los resultados estéticos, por lo que se convierte en una opción válida para aquellos pacientes con lesiones localizadas en regiones anatómicas donde la cirugía puede causar desfiguración, con sus secuelas de depresión, retraimiento social y baja autoestima.18
En esta investigación se reportaron en total 12 tipos diferentes de eventos adversos, de los 92 pacientes, el 89,13 % (82 pacientes), presentaron al menos un evento adverso, siendo la fiebre el más frecuente. No se reportaron casos con gravedad de eventos adversos, por lo que fueron leves las manifestaciones presentadas por los pacientes.
Drake-Sosa y Rojas-Barlys reportaron fiebre, malestar general, decaimiento y artralgias en todos los pacientes tratados con HeberFERON. Uno de ellos presentó eritema y edema local. Todos los pacientes incluidos en el ensayo clínico en Villa Clara presentaron eritema perilesional. La fiebre, escalofríos, astenia y anorexia también fueron frecuentes. Un paciente presentó náuseas, vómitos y mialgia. 2,18
Conclusiones
En la presente investigación se demostró la efectividad en el tratamiento del carcinoma basocelular con HeberFERON, la mayoría de los pacientes tuvieron una respuesta completa al tratamiento, con desaparición total de las lesiones y muy buena calidad en la cicatrización. Los eventos adversos reportados no fueron graves.