INTRODUCCIÓN
La diabetes mellitus (DM) comprende una gama de trastornos metabólicos comunes producto de diversos mecanismos patógenos que tienen como consecuencia la hiperglucemia. En su patogenia, influenciada por factores genéticos y ambientales, se incluyen la secreción insuficiente de insulina, la reducción de la respuesta a la insulina endógena o exógena, el incremento en la producción de glucosa o las anomalías en el metabolismo de grasas y proteínas.1,2
El número de individuos con diabetes se incrementa con rapidez en todo el mundo, de modo que ya en el año 2011 la Federación Internacional de Diabetes informó cerca de 336 millones de personas con este padecimiento. Esta enfermedad, además de provocar aproximadamente 4,6 millones de fallecimientos cada año, disminuye considerablemente la calidad y la expectativa de vida de los pacientes, sin contar los elevados costos destinados a su tratamiento.3
La Organización Mundial de la Salud calcula que actualmente existen en el mundo más de 250 millones de personas con diabetes, de las que el 90% son diagnosticados como diabetes mellitus tipo 2 (DM2); se considera probable que esta cifra aumente a más del doble para el año 2030 y además se estima que hasta un 30% de la población real con DM2 no ha sido aún diagnosticada.4,5
El uso de animales como modelos de experimentación en el estudio de la fisiopatología de la diabetes ha permitido comprender algunas de sus causas y consecuencias, además de obtener avances en su tratamiento y su control, a pesar de que sus signos y alteraciones no se reproducen con exactitud en el modelo animal. En la literatura se informa el uso de modelos experimentales de diabetes en diferentes especies que van desde el perro, el gato, el conejo, el cerdo y el borrego hasta la rata. Estos modelos permiten simular algunos fenómenos que se observan en la clínica y contribuyen al conocimiento de los factores fisiológicos, bioquímicos y ambientales que predisponen a la enfermedad.4
Específicamente en la rata la diabetes se puede producir de forma espontánea o inducida experimentalmente mediante distintos métodos. Históricamente el más importante fue la pancreatectomía, que develó la importancia de los islotes de Langerhans para la regulación de la glicemia. Otro método muy empleado para inducir experimentalmente la DM2 es la destrucción química de los islotes con aloxana o estreptozotocina (STZ).1,4,6,7,8
El zinc (Zn) es un micronutriente esencial y fundamental para el ser humano y otros organismos que resulta imprescindible para la síntesis y la transcripción del ácido desoxirribonucleico (ADN), la estabilización de proteínas y la actividad de más de 300 enzimas vinculadas directamente a procesos celulares como la división celular y la apoptosis. En los pacientes con diabetes se observa un aumento significativo de la excreción de Zn en orina y en la DM2 también se ha constatado una disminución significativa en los niveles plasmáticos de este micronutriente, lo que sugiere un deterioro de sus niveles asociado directamente a la enfermedad. A diferencia de la DM2, en la DM1 tienden a aumentar los niveles plasmáticos de Zn, probablemente como resultado de la destrucción de las células beta del páncreas, lo que conlleva a un incremento en el aporte de este micronutriente a la sangre. La causa de este fenómeno radica en las altas concentraciones de Zn presente en los islotes pancreáticos, en los que participa en la conversión de proinsulina en insulina y en la cristalización de la insulina para su posterior liberación, lo que demuestra claramente la importancia del mismo en el metabolismo de esta hormona.9,10,11,12
El Zn se secreta en forma conjunta con la insulina y, de hecho, la hipersecreción de insulina puede agotar las reservas de este elemento en las células beta de los islotes. En 1938 se informó por primera vez que los niveles de Zn en cadáveres de pacientes diabéticos resultaban un 50% menor en comparación con los cadáveres de pacientes no diabéticos, lo que sugiere una asociación entre la concentración de Zn y la diabetes, motivo que impulsó la realización de esta investigación.9,13,14,15
MÉTODOS
El presente trabajo respondió a un proyecto de investigación de las Ciencias Básicas Biomédicas desarrollado en la Unidad de Investigaciones Biomédicas de la Universidad de Ciencias Médicas de Villa Clara, Cuba, en el que se reprodujo un modelo de diabetes con hiperglucemias moderadas y otras condiciones clínicas de diabetes mellitus tipo 2 a través de la inducción neonatal con estreptozotocina (STZ) en ratas Wistar hembras en el período comprendido desde enero de 2016 hasta diciembre de 2018.
Se realizó un estudio descriptivo, transversal, experimental con enfoque cuantitativo que utilizó un sistema de métodos morfométricos. Se utilizaron ratas Wistar, hembras, provenientes del Centro Nacional de Producción de Animales de Laboratorio, sometidas a condiciones de alimentación convencional todo propósito, fórmula CMO 1000 y libre acceso a agua, así como ciclo de luz/oscuridad de 12/12, temperatura ambiente de 25°C y humedad controlada de 50 a 70%. La muestra quedó constituida por 32 ratas hembras gestadas (diabéticas: n=16 y sanas: n=16). Se formaron cuatro grupos experimentales de forma aleatoria de ratas gestantes diabéticas y sanas (grupo control, grupo control-Zn, grupo diabético y grupo diabético-Zn), de ocho animales cada uno; a los grupos control y control-Zn se les administró vehículo (agua) o la dosis de sulfato de zinc (50 mg/kg), respectivamente, la inducción de la diabetes se realizó en los grupos diabético y diabético-Zn, a los que se les aplicó, al segundo día de nacidas, una inyección subcutánea de STZ. Cada uno de los grupos proporcionó cinco parámetros morfométricos (número de islotes por láminas, diámetro mayor del islote, diámetro menor del islote, área del islote y circularidad del islote).
El estudio morfométrico de los islotes pancreáticos se realizó a partir de las muestras de páncreas fijadas en formol neutro al 10%, procesada por la técnica clásica de inclusión en parafina procedente del estudio. Los cortes para biopsia fueron fijados durante 72 horas en formol al 10% y lavados en agua destilada durante una hora, se procesaron por la técnica de la parafina debido a su pequeño tamaño y se siguió el esquema: deshidratación, alcohol absoluto al 50, 60, 70, 80, 86 y 100% durante 10 minutos cada uno, aclaración, alcohol-Xilol a partes iguales por cinco minutos, alcohol-Xilol hasta aclarar y alcohol-Xilol puro por cinco minutos, inclusión, parafina 10 minutos, parafina 20 minutos y parafina de inclusión 20 minutos, todas a 56°C. De esta forma se obtuvieron bloques solidificados, enfriados en hielo y cortados a 5 micrómetros, en un micrótomo vertical, que permitió obtener cortes seriados de grosor uniforme, que se colocaron en láminas histológicas teñidas con hematoxilina-eosina bajo control de pH.
El proceso para aplicar la hematoxilina-eosina fue el siguiente:
Las láminas se colocan en la gradilla
Alcohol-Xilol para desparafinar (cinco minutos en cada alcohol-Xilol, debe haber cuatro alcoholes-Xilol)
Alcohol. Se usan tres alcoholes lavadores de degradaciones decrecientes
Agua
Hematoxilina, de uno a tres minutos
Agua, se escurre bien y se aplica alcohol ácido al 1% durante un minuto y luego agua por uno a dos minutos (viraje del ph)
Eosina, de uno a tres minutos
Alcoholes deshidratadores de gradación creciente (seis alcoholes)
Alcoholes-Xilol.
Se procedió a la realización del examen morfométrico de la muestra comenzando por la separación, la clasificación y el ordenamiento de las láminas. La captación de imágenes se realizó con una cámara digital Olympus G11 semiprofesional, acoplada a un microscopio binocular Olympus BH-2 CCD Scion (lente objetivo 4x y 20x y lente ocular 10x).
Las mediciones se determinaron mediante el programa de análisis y procesamiento de imágenes de dominio público ImageJ®, versión 1.44p (National Institutes of Health, Estados Unidos). Los análisis se llevaron a cabo sobre las fotografías al 100% de su tamaño. Una escala de 10 µm (434 píxeles) fue utilizada para realizar las medidas.
Las mediciones fueron ejecutadas con la consiguiente comprobación para reducir al mínimo los errores y fueron respaldadas con sus trazos y anotaciones para consultas posteriores. Las opciones de cálculo fueron área y conteo. Se realizó el conteo de los islotes pancreáticos y posteriormente se procedió a determinar el diámetro mayor, el diámetro menor, el área y la circularidad de los islotes. Los datos se guardaron en una hoja de cálculo de Microsoft Excel 2016, diseñada para este fin, que posteriormente fue importada al paquete de programas estadísticos SPSS (Statistical Package for the Social Sciences) versión 20.0 para Windows, para el procesamiento estadístico de la información.
Operacionalización de las variables
Las variables se correspondieron con los parámetros histológicos analizados: diámetro mayor, diámetro menor, área y circularidad de los islotes. Además, se realizó el conteo del número de islotes por láminas. Las variables se operacionalizaron de la siguiente manera:
Número de islotes: se obtiene al contar la cantidad de islotes pancreáticos por láminas
Diámetro mayor del islote: se logra al marcar con cuidado del borde externo de un extremo del islote pancreático hasta el borde externo del extremo contrario, es una imagen plana. La computadora brinda su valor de forma automática en micrómetros
Diámetro menor del islote: se logra al marcar con cuidado del borde interno de un extremo del islote pancreático hasta el borde interno del extremo contrario, es una imagen plana. La computadora brinda su valor de forma automática en micrómetros
Área del islote: se logra al marcar con cuidado el contorno del islote pancreático hasta rodearlo completamente, es una imagen plana bidimensional. La computadora brinda su valor de forma automática en micrómetros cuadrados
Circularidad del islote: se logra al marcar con cuidado el contorno del islote pancreático hasta rodearlo completamente, es una imagen plana bidimensional. La computadora brinda su valor de forma automática. Describe el grado de circularidad de un objeto, de tal forma que tiene un valor de uno cuando es un círculo perfecto y cero cuando es una línea. A medida que este valor aumenta acercándose a uno indica una forma más circular
Métodos de análisis y procesamiento de la información
Los datos recopilados fueron resumidos y procesados estadísticamente mediante el paquete SPSS versión 20.0 para Windows, que se muestran en tablas y gráficos que posibilitaron la adecuada interpretación de la información acopiada. Para la construcción de estos gráficos se utilizó el paquete de informática Microsoft Office versión 2016. Se emplearon técnicas de estadística descriptiva para la caracterización de la muestra por las diferentes variables estudiadas, así como el empleo de la inferencia estadística para la obtención de los intervalos de confianza y los contrastes entre variables en función de los objetivos planteados, lo que posibilitó obtener el comportamiento puntual poblacional de la media (M)±error estándar de la media (EEM). En el estudio se aplicó la prueba paramétrica (ANOVA de un factor para análisis de varianza) para las comparaciones de los grupos con un nivel de significación de 0,05.
Se realizó la caracterización estadística mediante los estadígrafos descriptivos:
Se utilizó la prueba estadística paramétrica ANOVA de un factor para análisis de varianza. Se consideraron los siguientes valores de significación estadística:
Si p es menor de 0,01 existen diferencias altamente significativas
Si p es mayor e igual a 0,01 y menor que 0,05 existen diferencias significativas
Si p es mayor e igual a 0,05 no existen diferencias significativas.
Se realizó una prueba T para comparación de la media de los diferentes grupos, así como el error estándar de la media en los casos en que se obtuvo significación al realizar la prueba estadística ANOVA de un factor.
RESULTADOS
La Tabla 1 muestra que la media del número de islotes fue menor en el grupo control con 9,88 islotes por lámina, mientras que resultó más alta (14,80) en el grupo control-Zn. Se aplicó la prueba ANOVA y se obtuvo un valor de significación bilateral de 0,380, lo que indica que esta variable no muestra diferencias significativas entre los grupos.
Tabla 1 Distribución de la muestra según el número de islotes pancreáticos por láminas
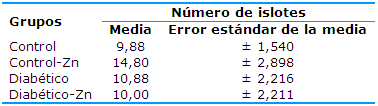
Los datos se presentan como M±EEM. Sin significación estadística ANOVA p>0,05
En el grupo control la media del diámetro mayor de los islotes fue de 205,45 µm. Sobrepasó esta media el grupo diabético-Zn, mientras que en el resto de los grupos resultó menor que en el control. El contraste mediante la prueba ANOVA ofreció un valor de significación de 0,654, lo que indica que esta variable no muestra diferencias significativas entre los grupos (Tabla 2).
Tabla 2 Distribución de la muestra según el diámetro mayor de los islotes pancreáticos

Los datos se presentan como M±EEM. Sin significación estadística ANOVA p>0,05
La media del diámetro menor de los islotes en el grupo control fue de 135,81 µm. Este valor fue superado en el grupo control-Zn y en el resto de los grupos resultó menor que en el control y se encontró la más pequeña de todas en el grupo diabético, con 82,03 µm. El contraste mediante la prueba ANOVA ofreció un valor de significación de 0,000, lo que sugiere en esta variable diferencias altamente significativas entre los grupos (Tabla 3).
Tabla 3 Distribución de la muestra según el diámetro menor de los islotes pancreáticos

Los datos se presentan como M±EEM. ANOVA de un factor p=0,000. Prueba T (*) p<0,05 respecto al grupo control, (**) p<0,05 respecto al grupo control-Zn
Con respecto al área de los islotes pancreáticos la media en el grupo control fue de 19523,55 µm2. Superó esta medida el grupo control-Zn y en los otros dos grupos resultó mucho menor que la del grupo control. Al realizar una prueba de contraste mediante ANOVA se obtuvo un valor de significación bilateral de 0,000, lo que demuestra diferencias altamente significativas entre los grupos (Tabla 4).
Tabla 4 Distribución de la muestra según el área de los islotes pancreáticos

Los datos se presentan como M±EEM. ANOVA de un factor p=0,000. Prueba T (*) p<0,05 respecto al grupo control, (**) p<0,05 respecto al grupo control-Zn
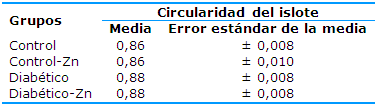
La media de la circularidad de los islotes resultó similar en el grupo control y en el grupo control-Zn con 0,86, superando ligeramente el valor del control en los dos grupos restantes (0,88). La prueba ANOVA arrojó una significación bilateral de 0,176, lo que indica que esta variable no muestra diferencias significativas entre los grupos (Tabla 5).
DISCUSIÓN
En el presente estudio se empleó un modelo animal en el que se utilizó estreptozotocina como agente de inducción de la diabetes y en el que se evidenciaron características del síndrome diabético humano.
Durante el estudio del número de islotes pancreáticos no se apreciaron diferencias significativas entre los grupos para esta variable. Según estos resultados no se evidenció un efecto positivo del suplemento de zinc sobre el número de islotes. El poco efecto de la inducción de diabetes tipo 2 en ratas sobre el número de islotes pancreáticos en los animales diabéticos se diferencia de lo observado en la diabetes tipo 1, en la que si se ha constatado una marcada disminución en el número de islotes. Por ejemplo, en un estudio realizado por Al-Asadi y colaboradores en el año 2016 se analizó la morfometría de los islotes pancreáticos en ratas diabéticas y se informó que el número de islotes fue incluso mayor en el grupo de estudio que en el grupo control;16 sin embargo, otras investigaciones consultadas difieren de los resultados anteriormente expuestos e informan un menor número de islotes en las ratas diabéticas e, incluso, en su descendencia. Un estudio realizado en la Universidad de Ciencias Médicas de Villa Clara en el año 2016 sobre la acción de la estreptozotocina en un modelo experimental de inducción neonatal de la diabetes arrojó una disminución significativa en la media del número de islotes en los grupos de ratas diabéticas.3
Similares resultados se obtuvieron en el año 2016 en estudios que investigaron la acción diabetogénica de la estreptozotocina en un modelo experimental de inducción neonatal.17,18 En un trabajo realizado en ese mismo año se estudió el efecto de un suplemento de zinc en ratas diabéticas y se informó que la diferencia en la media del número de islotes entre los grupos resultó casi imperceptible.13
En cuanto al análisis de la media de los diámetros del islote los resultados más llamativos correspondieron al diámetro menor. Al comparar el grupo diabético contra el grupo control se observó una disminución significativa de este diámetro en el grupo diabético, resultado que coincide con lo esperado en el modelo experimental; sin embargo, también se constató la disminución de este valor en el grupo diabético-Zn respecto al control-Zn, lo que no era el resultado anticipado para el modelo experimental. En ambos casos las diferencias entre los grupos resultaron muy significativas. El diámetro menor también resultó ligeramente mayor en el grupo diabético-Zn que en el diabético, pero esta diferencia no resultó significativa. En el caso del diámetro mayor de los islotes no se encontraron diferencias significativas entre los grupos de estudio.
Igualmente interesante resultó el análisis de la media del área de los islotes pancreáticos. Mediante la comparación del grupo diabético con el grupo control se evidenció que el área de los islotes resultó menor en el grupo diabético, como era lo anticipado en el modelo experimental, puesto que cabe esperar la presencia de islotes más pequeños en los animales diabéticos. Al realizar esta misma comparación entre el grupo diabético-Zn y el control-Zn se observó que la media del grupo diabético-Zn era muy inferior. En ambos casos las diferencias entre los grupos resultaron altamente significativas; sin embargo, no se encontraron diferencias significativas entre el grupo diabético-Zn y el grupo diabético. Como se puede apreciar la inducción de diabetes tipo 2 en las ratas gestantes se correspondió con la disminución del área de los islotes, pero no fue posible observar ninguna influencia del suplemento de zinc sobre este parámetro. Un resultado análogo en cuanto al efecto del zinc sobre el tamaño de los islotes ya había sido informado.13
En un estudio realizado en el año 2016 en la Universidad Al-Nahrain de Iraq analizaron los cambios histomorfométricos inducidos por el embarazo en los islotes pancreáticos y señalaron que la gestación se asociaba al incremento en el área de los islotes.16 En otro estudio no se informaron diferencias significativas en el área de los islotes pancreáticos entre las ratas diabéticas y las sanas.17 En una investigación llevada a cabo en humanos, realizada en el año 2019 en Suecia, tampoco se encontraron diferencias significativas en el área de los islotes de pacientes diabéticos y sanos.19
Con respecto a la variable circularidad de los islotes la media de su valor resultó similar en el grupo control y en el grupo control-Zn, mientras que fue ligeramente superior en el resto de los grupos; no se demostraron diferencias significativas entre los grupos. Teniendo en cuenta que la circularidad permite evaluar la forma de un objeto, estos resultados sugieren que no hubo deformaciones significativas de los islotes en los diferentes grupos de estudio. Este hallazgo parece indicar que la destrucción de las células beta en la diabetes no necesariamente siempre se acompaña de alteraciones visibles en la forma de los islotes. En investigaciones anteriores ya se había informado una pérdida notable de células beta sin alteraciones significativas de la forma de los islotes en ratas diabéticas.20
Un resultado comparable fue ofrecido en otro trabajo en el que tampoco se informaron diferencias significativas en la forma de los islotes pancreáticos de pacientes sanos y con diabetes tipo 2.19
CONCLUSIONES
La presente investigación se propuso describir los efectos de un suplemento de zinc sobre la morfometría de los islotes pancreáticos en ratas Wistar gestantes con diabetes moderada. Durante el estudio no se evidenciaron diferencias significativas en cuanto al número, el diámetro mayor y la circularidad de los islotes pancreáticos entre los grupos de estudio. Tanto el área como el diámetro menor de los islotes resultaron significativamente inferiores en el grupo diabético que en el control. De forma similar se comportaron estos parámetros en el grupo diabético-Zn, respecto al control. En el trabajo no se evidenciaron efectos significativos del suplemento de zinc sobre ninguno de los parámetros morfométricos estudiados.