INTRODUCCIÓN
El estómago humano, órgano que muchos pensaban fuese estéril por su elevado contenido en ácido clorhídrico, puede ser colonizado por Helicobacter pylori (H. pylori), una bacteria gram negativa, que afecta a más del 50 % de la población mundial.1
Este germen, está relacionado con el desarrollo de úlceras gástricas y duodenales, linfoma y cáncer gástrico (CG).2 Sin embargo, no todos los infectados desarrollan enfermedad clínica. Este comportamiento se relaciona con factores genéticos, ambientales y el genotipo de la cepa que coloniza la mucosa gástrica.3
La infección por H. pylori es la principal causa de gastritis crónica,4 en la que evolutivamente, pueden surgir, producto de la inflamación causada en la mucosa gástrica por esta bacteria, la atrofia, la metaplasia intestinal (MI) y la displasia. Precisamente, a través del sistema Operative Link on Gastritis Assessment (OLGA) se puede determinar el riesgo de CG, el cual define la atrofia gástrica (AG) como la lesión típica de progresión de la gastritis crónica2) y está considerada como una lesión precursora de CG.5
En la práctica médica, el diagnóstico de estas lesiones premalignas se dificulta en los pacientes que permanecen asintomáticos o con síntomas inespecíficos de dispepsia. Esto requiere de una historia clínica y estudios endoscópicos del tracto digestivo superior, con la realización de un número suficiente de biopsias gástricas ya que la distribución de las lesiones no es uniforme, como tampoco es la colonización de la mucosa gástrica por la bacteria.6
Resulta vital el diagnóstico precoz de lesiones premalignas gástricas, con el objetivo de brindarle al paciente el seguimiento y tratamiento adecuados. Esto también facilita el diagnóstico precoz o en etapas iniciales del CG. Las etapas avanzadas ofrecen muy pocas opciones de tratamiento curativo al enfermo.7
Se ha demostrado que la bacteria H. pylori cuenta con diversos factores de virulencia que contribuyen al daño de la mucosa. De sus dos tipos de cepas (tipo I y tipo II), el tipo I (que expresa CagA y VacA) es el más virulento. En las cepas tipo II no se expresan estos marcadores.8)
Los pacientes con cepas CagA positivas presentan mayor gravedad de la inflamación en la mucosa gástrica y tienen mayor probabilidad de desarrollar úlcera péptica, gastritis crónica atrófica (GCA) y adenocarcinoma gástrico, que aquellos con cepas CagA negativas.9) En el caso de VacA, este se ha relacionado con el desarrollo de procesos tumorales al inducir la expresión del factor de crecimiento vascular endotelial. VacA está asociada al desarrollo de úlcera y adenocarcinoma gástrico. Se conocen tres tipos de cepas: s1m1, s1m2 y s2m2, de ahí la diversidad genética de VacA. Las dos primeras son muy toxigénicas, a diferencia de las cepas s2m2, que tienen poca citotoxicidad. Las cepas VacA s1m1 están asociadas a una enfermedad más grave.10
Esta investigación se realizó con el objetivo de relacionar los genotipos CagA y VacA del Helicobacter pylori con lesiones precursoras de CG.
MÉTODOS
Se realizó un estudio descriptivo, en el Hospital “Dr. Carlos J. Finlay”. Fueron incluidos 62 pacientes, con biopsias gástricas positivas para H. pylori, con las combinaciones genotípicas CagA/VacA.
Fueron analizadas como variables independientes los genotipos del H. pylori (CagA y VacA) y como variables dependientes los estadios de OLGA (0, I, II, III, IV).
Descripción del estudio: para la determinación del estadio de AG se revisaron las biopsias gástricas realizadas a los pacientes y se estableció, mediante el sistema OLGA, el estadio de atrofia.
Los estadios de AG, según el sistema OLGA, se describen a continuación:5
Estadio 0: sin atrofia en antro, ni en cuerpo.
Estadio I: antro sin atrofia o atrofia leve y cuerpo con atrofia.
Estadio II: antro sin atrofia o atrofia leve y cuerpo con atrofia moderada, antro sin atrofia y atrofia intensa en cuerpo, antro con atrofia moderada y cuerpo sin atrofia o atrofia leve, antro con atrofia intensa y cuerpo sin atrofia.
Estadio III: antro con atrofia intensa y cuerpo sin atrofia o atrofia leve, antro y cuerpo con atrofia o antro con atrofia leve y cuerpo con atrofia intensa.
Estadio IV: antro con atrofia moderada e intensa en cuerpo, antro con atrofia intensa y moderada en cuerpo o antro y cuerpo con atrofia intensa.
Análisis estadístico: se emplearon como medidas de resumen para variables cualitativas la frecuencia absoluta y el porcentaje. Para evaluar la asociación entre variables cualitativas se aplicó el test X2 (ji cuadrado). Se aceptó un nivel de significación estadística p ≤ 0,05. Se calculó el riesgo relativo (RR) entre el genotipo CagA y la citotoxina VacA, así como entre el genotipo CagA y los estadios OLGA, así como entre el genotipo CagA y VacAs1m1 y la AG. Se calcularon los intervalos de confianza (IC) con un nivel de confiabilidad del 95 %.
Consideraciones éticas: la información obtenida en la revisión de las biopsias gástricas solo se utilizó con fines de la investigación, sin revelar la identidad de los pacientes.
RESULTADOS
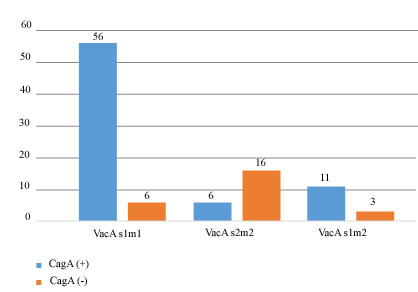
De los 62 pacientes estudiados con H. pylori, 46 (74 %) resultaron CagA positivos, de ellos, el 56 % tenían VacA s1m1, con una significación estadística de p = 0,00002. Solo en el 6 %, se identificaron los genotipos VacA s2m2 y 11 % VacA s1m2.
En la figura 1 se refleja la asociación entre el genotipo CagA y los estadios de OLGA. De los pacientes con CagA, el 6 % (p = 0,2383) se encontraba en estadio 0 (RR = 1,52; IC 95 % = 0,92 - 2,51); 11 % (p = 0,2792; RR = 0,91; IC 95 % = 0,70-1,19) en estadio I; 40 % en estadio II (p = 0,0570; RR = 0,75; IC 95 % = 0,57 - 0,99) y 16 % en estadio III (p = 0,1081; RR = 1,36; IC 95 % = 1,04 - 1,79). Como se aprecia, el mayor por ciento de pacientes con CagA estaban en un estadio de atrofia que no es de alto riesgo para CG (estadio II), pero hay que señalar que aunque no fue significativo estadísticamente, hubo pacientes en estadio III (alto riesgo para CG) y en este caso, los resultados indican que constituyó un factor de riesgo.
Algo similar ocurrió con VacA, como se muestra en la figura 2. El 37 % de los pacientes con VacA s1m1 se ubicaron en el estadio II, con resultados cercanos al grado de significación estadística (p = 0,0650), pero no se comportó como un factor de riesgo (RR = 0,68; IC95 % = 0,46 - 1,00). No se encontraron pacientes en estadio 0 (p = 0,0060) con VacA s1m1, el 6 % (p = 0,3382; RR = 0,74; IC 95 % = 0,36-1,52) se encontró en estadio I y 13 % en estadio III (p = 0,6965; RR = 1,09; IC 95 % = 0,72 - 1,64).
En la figura 3 se relaciona la presencia de CagA y VacA s1m1 con la presencia o no de AG, independientemente del estadio de OLGA. Se observó que el 68 % (p = 0,2736; RR = 1,12; IC 95 % = 0,87-1,45) de los pacientes con AG tenían genotipo CagA y el 55 % (p = 0,6200; RR = 0,95; IC95 % = 0,80 - 1,14) VacA s1m1.
DISCUSIÓN
En los pacientes del estudio, predominó una cepa muy virulenta (CagA +/VacA s1m), que ha sido relacionada con CG, porque puede causar alteraciones histopatológicas más graves, como AG y MI, que implican un mayor riesgo de CG.1 Las combinaciones CagA/VacA s1m1, CagA/VacA s1m1/babA2 positivo, CagA/VacA s1m1/iceA1 determinan la mayor virulencia de las cepas.11 La gravedad de las lesiones histopatológicas se relaciona con la presencia de uno o más de estos genes.
El predominio de la AG en los individuos con genotipo CagA, VacA s1m1 está acorde con lo planteado por la literatura, sobre el surgimiento de este tipo de lesiones y las cepas con mayor virulencia. Resulta necesario recalcar que no todos los pacientes con H. pylori desarrollan CG, pues la carcinogénesis gástrica es un proceso multifactorial en el que también intervienen factores genéticos, nutricionales y ambientales.
La respuesta inflamatoria que causa en la mucosa gástrica esta bacteria puede progresar a gastritis crónica, GCA, MI, displasia y adenocarcinoma gástrico. Este es un proceso lento, que puede durar 15 - 20 años y también está influenciado por el tipo de cepa que causa la infección.11 Esta pudiera ser una probable explicación a la interrogante de por qué existen regiones de alta prevalencia de infección por H. pylori y las tasas de incidencia y prevalencia de CG no se corresponden con la presencia de esta bacteria. Además, la infección por H. pylori se asocia a una compleja interacción de diversos factores5) que explican los diferentes resultados a los que se llega. No todos los pacientes con H. pylori desarrollarán CG. Es lo que se ha dado a conocer como el enigma africano.6
No todas las cepas de H. pylori son patógenas y aunque la presencia de cepas virulentas es necesaria, no es suficiente para el inicio del proceso de carcinogénesis.7 Las cepas CagA, VacA s1m1 son las que tienen mayor probabilidad de desarrollar GCA y CG.9 CagA codifica una proteína inmunogénica, que promueve la activación de vías de señalización celular y desencadena respuestas proinflamatorias y mitogénicas.8
En Cuba, a juicio de los autores también debería plantearse un enigma cubano. Existen reportes de diferentes hospitales y regiones con prevalencias por encima de 60 %.1) Sin embargo, el CG se mantiene en el octavo lugar entre las causas de muerte por cáncer.11) El estudio de los factores de virulencia puede permitir la aplicación de estrategias de trabajo para prevenir enfermedades graves.
Los genotipos CagA y VacA s1m1 de H. pylori fueron los más frecuentes y se relacionaron con la presencia de AG, en más de la mitad de los pacientes. El estadio II de OLGA fue el más frecuente.