INTRODUCCIÓN
Para evitar el riesgo ecológico que supone la diseminación de microorganismos es necesario identificar y rastrear las especies presentes en el interior de las plantas y la rizosfera de las mismas. Es por ello que se busca una correcta identificación de las cepas microbianas a través de técnicas clásicas y de avanzada (Bloemberg y Lugtenberg, 2001).
Azospirillum es el género de rizobacterias de vida libre más estudiado debido al gran interés agrícola existente por su capacidad de fijar nitrógeno biológico y producir fitohormonas (Sangoquiza et al., 2018). El género contiene especies de bacterias muy versátiles, promotoras del crecimiento de las plantas (Cassán et al., 2014), cuyos efectos beneficiosos se debe, además, al incremento de la toma de nutrientes y agua (Ardakani et al., 2011) y la inducción de genes que confieren tolerancia al estrés (Fukami et al., 2017; 2018). Estos mecanismos pueden ser útiles al disminuir el uso de fertilizantes y propiciar la implementación de un desarrollo sostenible y sustentable del suelo (Vital y Mendoza, 2014).
Las técnicas inmunológicas involucran la reacción de afinidad antígeno-anticuerpo. Entre las más empleadas se encuentran la aglutinación, la inmunofluoresencia, la inmunodifusión y los ensayos inmunoabsorbentes (Caballero-Mellado, 2000).
Conjuntamente con las serológicas, las técnicas de biología molecular resultan de gran utilidad en la identificación de las especies de Azospirillum. Entre ellas, el polimorfismo en la longitud de los fragmentos de restricción (RFLP) del operon histidina y las sondas basadas en el gen 16S del ARNr son las más utilizadas por su rapidez, confiabilidad y reproducibilidad (de-Bashan et al., 2007).
Para mejorar la sustentabilidad de la producción de los cultivos, la agricultura ha buscado alternativas biológicas que sean más económicas, mejoren la rentabilidad y eviten el deterioro del medioambiente, por lo cual pueden ser utilizadas para la sustitución parcial o total de fertilizantes químicos (Hernández et al., 2015).
En Cuba se utiliza de forma satisfactoria la cepa 8-INICA de Azospirillum sp. en la biofertilización (Montero et al., 2017). La caracterización morfológica y bioquímica de esta cepa, realizada por Pérez y Casas (2005) indicó que presenta similitudes con las descripciones plasmadas para la especie A. brasilense en el Manual de Clasificación de Bacterias de Berguey. Por la importancia de esta cepa para la continuidad de las labores de biofertilización que se ejecutan en el país, el objetivo del trabajo fue corroborar la identidad de la misma mediante el empleo de técnicas inmunológicas y moleculares.
MATERIALES Y MÉTODOS
Caracterización serológica
Las cepas utilizadas en el estudio proceden de la Colección de Cultivos Microbianos del Instituto de Investigaciones de la Caña de Azúcar (INICA) y fueron aisladas, caracterizadas e identificadas como Azospirillum spp. en estudios previos (Pérez y Casas, 2005). Además, fueron usados los patrones A. brasilense Sp7 (ATCC 29145) y A. lipoferum SpBr17 (ATCC 29709), procedentes del cepario del CNPAB/EMBRAPA de Brasil.
Se realizó la caracterización serológica de la cepa 8-INICA, la más utilizada en Cuba para la elaboración de inoculantes comerciales destinados a la caña de azúcar y otros cultivos económicos, seleccionada por sus significativas posibilidades estimuladoras del crecimiento de las plantas. La cepa fue comparada con los patrones A. brasilense Sp7 y A. lipoferum SpBr17, además de las cepas 79-INICA y 11-INICA (presentes en la Colección del INICA). Cada cepa fue incubada en caldo Okon durante 48 horas, en agitación a 37 °C; posteriormente, las células se colectaron por centrifugación a 10 000 rpm durante 10 minutos y lavaron tres veces con buffer salino fosfato 10 mM, pH 7,4. Finalmente, se resuspendieron en 1 mL del buffer.
Para la obtención de los anticuerpos policlonales a partir de las cepas patrones Sp7 y SpBr17, la biomasa obtenida (utilizada como inmunógeno) se resuspendió en solución salina fisiológica estéril (NaCl 0,85 %), en concentraciones crecientes de densidad óptica (0,4, 0,6, 0,8 y 1,0) medidas en un espectrofotómetro SPEKOL11 (Carl Zeiss Jena, Alemania) y con estas suspensiones se inocularon por vía subcutánea conejos albinos de aproximadamente 2 kg de peso, obtenidos del Centro de Producción de Animales de Laboratorio (CENPALAB), siguiendo el esquema propuesto en la Tabla 1.
Tabla 1 Esquema de inmunización
| Días | 0 | 7 | 14 | 21 | 28 |
|---|---|---|---|---|---|
| D. O. | 0,4* | 0,4 | 0,6 | 0,8 | 1,0 |
D.O. - Densidad Óptica, * Células inactivadas por calor
Los conejos fueron desangrados por punción intracardiaca 10 días después de finalizado el esquema de inmunización y los sueros obtenidos se conservaron a -20 oC. La titulación de los antisueros frente a sus antígenos homólogos se realizó a través de las técnicas de Inmunoprecipitación (IP) e Inmunodifusión doble (IDD). Las relaciones antigénicas entre las cepas patrones y las incluidas se determinaron según la técnica de IDD, en placas de agarosa al 1 % con solución PBS, las cuales difundieron en cámara húmeda a 37 oC durante 48 horas.
Caracterización molecular
Para la caracterización molecular de la cepa cubana 8-INICA se utilizaron las cepas autóctonas de A. brasilense TucH1, TucH2, TucL1, TucL2, TucL3 y la cepa de referencia A. brasilense Az39 (utilizada en Argentina para la formulación de bioproductos, procedente del cepario de la Estación Experimental Agroindustrial Obispo Colombres (EEOC), Tucumán, Argentina).
La extracción del ADN de cada cepa se realizó con el kit de extracción (Accuprep Genomic DNA kit), a partir de 1 mL de cultivo líquido incubado en medio Luria-Bertani por 48 horas. La PCR se realizó con los cebadores específicos 27f (5´ GAGAGTTTGATCCTGGCTCAG 3´) y 149r (5´ CTACGGCTACCTTGTTACGA 3´) que amplifican un fragmento del gen 16S ADNr. La mezcla de reacción para un volumen final de 25 μL fue: 2,5 μL Buffer Taq Pol 10 X, 2 μL MgCl2 25 mM, 1 μL dNTPs 10 mM, 1 μL mezcla de cebadores 27f + 1492r 10 μM, 0,2 μL Taq Polimerasa 500 U (Thermo Scientific), 2 μL ADN molde y 15,3 μL agua miliQ estéril.
Los parámetros para la PCR fueron: un ciclo a 95 °C (5 min), 55 °C (1 min) y 72 °C (2 min); 30 ciclos a 94 °C (45 s), 50 °C (2 min) y 72 °C (50 s) y un ciclo final a 72 °C durante 10 min. Los resultados de la reacción (5 μL) fueron analizados en gel de agarosa 1,5 %, utilizando buffer Tris-ácidobórico-EDTA (TBE) 0,5X como buffer de corrida. Para la visualización de los productos amplificados se agregó 1 μl de GelRed 10.000X (Biotium) por cada 5 μl de muestra. El gel fue visualizado a través de luz UV (320 nm) con un transiluminador Vilber Lourmat TFX-20M. Las imágenes se tomaron con una cámara fotográfica digital (Kodak Digital Science).
El análisis de restricción del ADNr 16S amplificado (ARDRA) se realizó mediante la digestión de los productos amplificados con la enzima de restricción AluI (Thermo Scientific). La mezcla de reacción fue: 10 μL producto PCR, 18 μL de agua miliQ estéril, 2 μL de Buffer Tango 10X y 1 μL Enzima AluI (5 U/μL) (Thermo Scientific). La mezcla se incubó a 37 °C durante 4 h. Transcurrido el tiempo de incubación, la enzima se inactivó por calentamiento a 65 °C durante 20 min. La separación de los fragmentos obtenidos fue mediante electroforesis en gel de agarosa 2 % (p/v) utilizando buffer Tris-ácidobórico-EDTA (TBE) 0.5X, como buffer de corrida. Para la visualización de los productos, se agregó 1 μL de GelRed 10.000X (Biotium) por cada 5 μL de muestra. Una vez finalizada la corrida, el gel fue visualizado y las imágenes según la metodología descrita anteriormente.
RESULTADOS Y DISCUSIÓN
Caracterización serológica
Al enfrentar las diferentes diluciones de los antisueros de las cepas patrones Sp7 y SpBr17 con sus antígenos homólogos mediante la técnica de IP, se obtuvieron títulos de 1:2048 y 1:1024 y con la IDD de 1:64 y 1:8, respectivamente.
La relación cualitativa entre los antisueros (As) de las cepas patrones con los antígenos de las cepas 8-INICA, 11-INICA y 79-INICA, a través de la técnica de IDD (Tabla 2), mostró la formación de bandas de precipitación por la existencia de determinantes antigénicos comunes entre ellas. Esta técnica está basada en el principio de que el antígeno y el anticuerpo difunden a través de un medio semisólido y forman complejos inmunitarios estables, que aparecen como líneas o bandas de precipitación insoluble en el “Punto de Equivalencia”, sitio donde alcanzan las proporciones óptimas (Licea et al., 2016).
Tabla 2 Relación cualitativa del enfrentamiento de los antisueros de A. brasilense Sp7 (ATCC 29145) y A. lipoferum SpBr17 (ATCC 29709) con las de Azospirillum spp. 8-INICA, 11-INICA y 79-INICA
| cepas | ||
|---|---|---|
| Sp7 | +++ | - |
| SpBr17 | - | + |
| 8-INICA | ++ | + |
| 79-INICA | + | ++ |
| 11-INICA | + | - |
AS - antisuero, (+) reacción positiva, (-) ausencia de reacción
Cada signo positivo representa una banda de precipitación
La completa identidad existente entre el Ac Sp7 y su Ag homólogo, se corresponde con la formación de diferentes bandas de precipitación, asociadas a la presencia de un mayor número de determinantes antigénicos. Todos los aislamientos formaron arcos de precipitación comunes con los anticuerpos de las cepas patrones, debido a la existencia entre ellas de determinantes antigénicos de origen genérico, resultado similares al obtenido por Pazos et al. (2000) al realizar una caracterización serológica de cepas de Azospirillum spp. aisladas de arroz.
La experiencia serológica de los estudios con A. brasilense y A. lipoferum arrojaron que los anticuerpos policlonales producidos directamente contra A. brasilense poseen una alta especificidad, con bajos niveles de reacciones cruzadas respecto a otras cepas; sin embargo, reacciones cruzadas aparecen entre los sueros obtenidos para cepas de A. lipoferum (Kirchhof et al., 1997).
La cepa 8-INICA formó dos arcos de precipitación con el antisuero A. brasilense Sp7, lo que indica una mayor proximidad antigénica entre ellas, mientras que 79-INICA compartió un mayor número de determinantes antigénicos con el antisuero A. lipoferum SpBr17. No se observó identidad entre 11-INICA y el antisuero SpBr17. La presencia de distintas bandas de precipitación en el gel de agarosa, cuando se emplea la técnica de IDD, se debe a la divergencia en la velocidad de migración de los diferentes antígenos y anticuerpos en el agar, por lo que, si los microorganismos estudiados poseen varios antígenos comunes, forman diversas bandas de precipitaciones, lo que facilita la determinación de las relaciones antigénicas entre ellos.
La identificación de microorganismos a través del uso de anticuerpos ha sido ampliamente empleada por ser una técnica simple y rápida que se puede automatizar y ser usada para trabajar con varias muestras al mismo tiempo (Rodríguez-Herrera et al., 2009).
Caracterización molecular
Los resultados de la amplificación de un fragmento de 1450 pb del gen ADNr 16S, de la cepa de referencia A. brasilense Az39 (carriles 1 y 7), de los aislamientos autóctonos TucH1, TucH2, TucL1, TucL2 y TucL3 (carriles 2 a 6) y de la cepa 8-INICA (carril 8) se muestran en la Figura 1. El control negativo (carril 9) es la mezcla de reacción sin ADN. No se observó amplificación para las cepas TucH2 y TucL1 lo que puede estar dado a problemas con la muestra de ADN inicial usada como molde en la reacción de PCR.
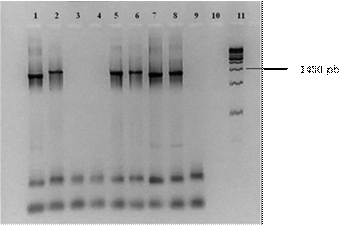 Carriles 1 y 7 - cepa de A. brasilense Az39, carriles 2 al 6 - aislamientos autóctonos TucH1, TucH2, TucL1, TucL2 y TucL3, carril 8 - cepa 8-INICA, carril 9 - control negativo, mezcla de reacción sin ADN, carril 11 - patrón de peso molecular 100 pb Promega
Carriles 1 y 7 - cepa de A. brasilense Az39, carriles 2 al 6 - aislamientos autóctonos TucH1, TucH2, TucL1, TucL2 y TucL3, carril 8 - cepa 8-INICA, carril 9 - control negativo, mezcla de reacción sin ADN, carril 11 - patrón de peso molecular 100 pb PromegaFigura 1 Amplificación de un fragmento de 1450 pb del gen ADNr 16S
El análisis electroforético de los productos amplificados utilizados como molde, usando la endonucleasa AluI, generó un perfil de restricción para 8-INICA que coincide con el control Az39 y los aislamientos de la colección del EEOC pertenecientes a la especie A. brasilense (Figura 2). La similitud entre los diferentes perfiles de restricción permite confirmar que 8-INICA pertenece al género Azospirillum especie brasilense.
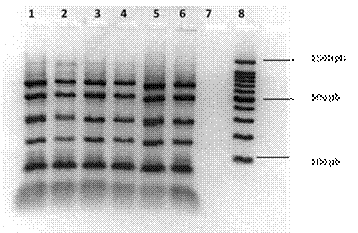 1 (Az39 cepa de referencia), 2, 3, 4 (cepas autóctonas TucH1, TucL2 y TucL3), 5 (Az39), 6 (cepa cubana 8-INICA), 7 (control negativo, mezcla de reacción sin ADN, 8 (patrón de peso molecular 100 pb Promega)
1 (Az39 cepa de referencia), 2, 3, 4 (cepas autóctonas TucH1, TucL2 y TucL3), 5 (Az39), 6 (cepa cubana 8-INICA), 7 (control negativo, mezcla de reacción sin ADN, 8 (patrón de peso molecular 100 pb Promega)Figura 2 Análisis de restricción del ADNr 16S amplificado (ARDRA) de las cepas de Azospirillum
Los estudios moleculares confirmaron los resultados obtenidos por métodos microbiológicos tradicionales y serológicos que ubican a 8-INICA dentro de la especie A. brasilense.
La asignación de las categorías taxonómicas (especie y/o cepa) de microorganismos estuvo durante muchos años basada en la distinción de características bioquímicas y/o antigénicas, y en el mejor de los casos, en aspectos fisiológicos detectables por análisis químicos o bioquímicos; sin embargo, con el desarrollo de las técnicas genómicas, primero se tomaron en cuenta algunas características químicas y fisicoquímicas de los ácidos nucleicos y posteriormente, se llegó a la comparación de secuencias de fragmentos relativamente cortos o un par de genes (Valenzuela et al., 2015). Los métodos de biología molecular se han desarrollado y utilizado ampliamente para la determinación sistemática correcta de cepas de Azospirillum (Pedraza y Díaz, 2000).
El ARNr 16S además de ser conveniente para la detección de bacterias, proporciona información útil y rápida sobre su identificación y filogenia mediante la comparación con bases de datos públicas que contienen un amplio número de secuencias bacterianas (Fernández et al., 2010). El análisis de las secuencias de los genes que codifican para las sub unidades 16S, 23S y 5S del RNAr, en particular los genes del 16S RNAr, se han convertido en una importante herramienta para la identificación de bacterias (Kanimozhi y Panneerselvam, 2010).
CONCLUSIONES
Se corroboró mediante el uso de la técnica inmunológica de Inmunodifusión Doble, las técnicas moleculares de PCR del gen 16S y de análisis de restricción del ADNr 16S que la cepa 8-INICA, de amplio uso en la biofertilización de la caña de azúcar y otros cultivos económicos, pertenece al género Azospirillum especie brasilense














