Introducción
El linfoma primario del tubo digestivo fue inicialmente descrito por Billroth en 1871,1 representando de 1 a 4% de todos los tumores malignos del tracto gastrointestinal,2-5 sin embargo, es el tubo digestivo el sitio más frecuente de linfoma no Hodgkin extraganglionar. (5,6Los órganos gastrointestinales que se afectan en orden de frecuencia son el estómago (60%), intestino delgado (25%) y colon (14%).7 La etiología del linfoma gastrointestinal es desconocida, pero la mayoría de los linfomas se originan del tejido linfoide asociado a mucosa (MALT), aunque para el linfoma gástrico se ha establecido una asociación importante con el Helicobacter pylori.8-10
Los linfomas del tubo digestivo pueden ser primarios o secundarios, lo que definirá el pronóstico tratamiento. Los criterios para determinar que un linfoma es primario del tubo digestivo son morfológicos, pero se incluye el análisis inmunofenotípico e inmunogenotípico. Los criterios más ampliamente usados para determinar que un linfoma es de origen gastrointestinal son los descritos por Dawson.11
Los linfomas no Hodgkin gastrointestinales corresponden de 4 a 20% de todos los linfomas no Hodgkin. El inmunofenotipo B incluye los linfomas de células del manto, que se presentan como poliposis linfomatosa y linfomas de tipo Burkitt y no Burkitt. La enteropatía (enfermedad celiaca) asociada a linfomas de células T es el linfoma gastrointestinal más común.12 La enfermedad de Hodgkin primaria del tubo digestivo es extremadamente poco frecuente.13 Los linfomas de alto grado se han encontrado como los tipos histológicos más frecuentes y tienen un pronóstico menos favorable. El linfoma primario del colon (LPC) es una neoplasia aún menos frecuente, por lo mismo su presentación clínica, manejo y estadificación no han sido estandarizados. Se ha descrito un aumento en la incidencia del LPC, asociándose a diversas patologías, considerándose a estos pacientes como grupos de alto riesgo para presentar LPC, tales como la presencia de colitis ulcerativa crónica inespecífica (CUCI), enfermedad de Crohn, ureterosigmoistomía previa, así como pacientes inmunocomprometidos, como los pacientes trasplantados y los pacientes con SIDA.7,14-17 Los sitios más frecuentes de localización en el colon son el ciego y el recto.8,18,19 En 5% de los pacientes existen lesiones sincrónicas y múltiples pólipos linfomatosos, además de 10 a 25% de los casos pueden estar presentes en distintos segmentos del colon o asociándose a lesiones linfomatosas en intestino delgado y estómago.8,20 El tratamiento de elección para el LPC es la resección quirúrgica.7,14-16,18Para algunos pacientes en que los tumores fueron completamente resecados, la supervivencia se incrementa si se acompaña de tratamiento adicional con quimioterapia y radioterapia postoperatoria.16,21 El objetivo del presente trabajo es el de informar de un caso de linfoma no Hogdkin primario de ciegoi ntervenido quirúrgicamente de urgencia con evolución desfavorable y lamentable deceso.
Presentación de caso
Paciente I.F.M.P, masculino, de 73 años, raza blanca, procedencia urbana, sin antecedentes patológicos personales relevantes. Acudió el pasado 05/07/2019 al servicio de cirugía del Hospital Provincial Carlos Manuel de Céspedes del municipio de Bayamo, Provincia de Granma, Cuba, por presentar un dolor abdominal intenso en hemiabdomen inferior, diarreas ocasionales de características no precisadas, pérdida del apetito y de peso. Es ingresado y luego de realizarse estudios de laboratorio clínico e imagenológicos comienza a manejarse el paciente con el diagnóstico presuntivo de una tumoración del colon derecho. El 08/07/2019es intervenido quirúrgicamente de urgencia con el diagnóstico preoperatorio de tumor de ciego perforado, peritonitis difusa, múltiples abscesos intraabdominales y subfrénico derecho. En el transoperatorio se constata en cavidad abdominal gran cantidad de fibrina gruesa. Se aspiran 150ml de líquido purulento fétido y se advierte la presencia de un tumor de ciego perforado. Se realiza hemicolectomía derecha con cierre del cabo distal, ileostomía y lavado de la cavidad. No se describen accidentes quirúrgicos. Se reporta de grave. Luego de una estadía hospitalaria de nueve días comienza con distención abdominal, signos de peritonitis, y fallece en cuadro de shock séptico y fallo múltiple de órganos.
Anatomía Patológica: biopsia 4602 del año 2019.
Descripción macroscópica: segmento de intestino grueso que incluyó ciego, apéndice cecal y colon ascendente que mide 44 cm de longitud. Serosa deslustrada con presencia de material fibrino-purulento en todo su trayecto. A su total apertura se constata lesión tumoral en el ciego de 10 cm en su diámetro mayor, superficie irregular, color blanquecino, consistencia blanda, que ocluye parcialmente la luz intestinal. A los cortes seriados impresiona comprometer todas las capas de la pared intestinal con sitio de perforación (Fig. 1 y Fig. 2). Bordes de sección quirúrgicos ampliamente libres de tumor. Apéndice cecal con vasos subserosos congestivos. La disección de la grasa mesentérica en torno a la tumoración reveló 18 formaciones nodulares, presumiblemente ganglios linfáticos.

Fig. 2. Lesión tumoral en el ciego de 10 cm de diámetro con sitio de perforación señalado con el dedo pulgar.
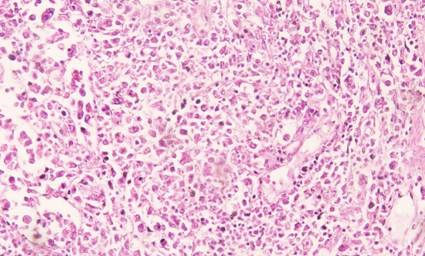
Diagnostico microscópico: linfoma no Hodgkin anaplásico de células grandes del intestino grueso (Ciego), variante común, con numerosas células linfoides malignas con alto grado de anaplasia, con núcleos multilobulados, presencia de células gigantes tumorales multinucleadas, mezcladas con un número variable de células linfoides neoplásicas monomorfas homogéneas con grandes núcleos redondos u ovales, fondo de células hospederas reactivas de linfocitos pequeños, eosinófilos, plasmocitos e histiocitos. Tamaño: de 10cm en su diámetro mayor. Infiltra todas las capas de la pared intestinal formando satelitosis tumorales nodulares en la serosa (Fig. 3). Bordes de sección quirúrgicos libres de infiltración linfomatosa. Se identificaron microscópicamente 18 formaciones ganglionares linfáticas peri cólicas igualmente afectadas por el proceso linfomatoso maligno de alto grado descrito (18 /18). Permeación vascular linfática severa.
Discusión
El LPC es una neoplasia extremadamente rara, sin embargo, es la tercera neoplasia en frecuencia del colon, seguido del adenocarcinoma y tumor carcinoide. Tiene una prevalencia de 0.02 en 100,000 personas de la población general.7Sin embargo, esta prevalencia está aumentando debido al crecimiento de la población inmunocomprometida, ya sea por SIDA o por pacientes trasplantados.7,16,22,23 El paciente en este trabajo no tenía factores de riesgo para la presentación del LPC, ya sea por inmunocompromiso o por encontrarse asociado a una enfermedad inflamatoria del intestino.
El LPC tiene un pico de presentación hacia la sexta década de vida,24 sin embargo, existen reportes en donde se ha presentado desde etapas muy tempranas,25 así como hasta la octava década de vida. Así también se reporta que existe una predilección hacia los hombres con una relación de 2:1,7,24 y es así como se presentó nuestro caso, un paciente masculino de 73 años de edad. La localización anatómica del LPC fue en el ciego, corroborando lo que se describe en la literatura internacional, en donde entre 60 a 74% se presentarán en el ciego,7,21 esto quizá sea explicado a que es en este sitio donde se presenta mayor cantidad de tejido linfoide en condiciones normales del colon y del recto.26
Los síntomas y signos de estas neoplasias son indistinguibles de otras enfermedades colónicas, siendo los más frecuentes el dolor abdominal, pérdida de peso y cambios en los hábitos defecatorios.15,27 En 25% de los casos inician con obstrucción intestinal secundaria a intususcepción o al mismo tumor.25La perforación no es frecuente,14 pero en nuestro paciente masculino se presentó obstrucción de 95% de la luz del ciego con perforación sellada proximal al tumor.
Para el diagnóstico de LPC es imprescindible distinguirlo de una afectación colónica por un linfoma sistémico, ya que el pronóstico y tratamiento son muy diferentes. Por ello en 1961 Dawson estableció los siguientes criterios:8,15,27
Criterios de Dawson:
Ausencia de linfadenopatías periféricas.
Ausencia de linfadenopatías mediastinales en la radiografía de tórax.
Frotis de sangre periférica normal.
Durante la laparotomía el compromiso de sólo esófago, estómago y el intestino o de sólo ganglios regionales.
Ausencia de compromiso hepático y esplénico; excepto por la diseminación directa de la enfermedad a partir de un foco contiguo.
El LPC presenta diversos tipos histológicos, teniendo la gran mayoría expresión para marcadores de superficie para células B con patrón de crecimiento difuso.7,28 Se desarrollan a partir de los linfocitos asociados a mucosas y por lo general son linfomas no Hodgkin. Nuestro caso resultó ser un linfoma no Hodgkin de células grandes de alto grado de malignidad.
La vía de diseminación principal es linfática hacia los ganglios regionales y retroperitoneales, así como la invasión a órganos adyacentes. La diseminación extradominal no es común. Para el pronóstico es importante determinar el compromiso de ganglios regionales mesentéricos y retroperitoneales, porque tienen peor pronóstico cuando están comprometidos por la enfermedad.7,16,26 En nuestro paciente se encontró compromiso linfático posterior al estudio histopatológico en la totalidad de los ganglios linfáticos regionales peri cólicos disecados y estudiados.
El tratamiento óptimo para los linfomas de tubo digestivo es desconocido, debido a que la mayoría de las series son pequeñas. Para los LPC la resección quirúrgica es el tratamiento de elección.14,15,18,19 La colectomía radical puede ser curativa por sí sola con cinco años de supervivencia de 16 a 58% de los casos.14,21,29 Para los tumores etapa I completamente resecados la supervivencia reportada se incrementa de 67 a 87%, si se acompaña de tratamiento adicional con quimioterapia y radioterapia postoperatoria.
La supervivencia a cinco años es de 55%, pero disminuye a 12% cuando se encuentran ganglios linfáticos regionales involucrados. Los pacientes con estadios avanzados de la enfermedad, así como los de alto grado y los linfomas no resecables pueden beneficiarse con quimioterapia y radioterapia.21,30 Los factores pronósticos con mayor significado estadístico son el estadio de la enfermedad (compromiso de los ganglios linfáticos regionales o paraaórticos), el sitio primario de aparición, el grado y tamaño tumoral y, finalmente, la resección completa de la lesión.7,14,19,30
Conclusiones
El LPC es una patología rara que se puede presentar en cualquier edad, y debido a que existe un aumento en los grupos de riesgo relacionados a esta enfermedad (enfermedad inflamatoria del intestino y pacientes inmunocomprometidos), se debe de tener presente para realizar el diagnóstico diferencial de pacientes con dolor abdominal, cambios en los hábitos defecatorios, pérdida de peso y tumor palpable en fosa iliaca derecha. Los criterios de Dawson son de gran ayuda para descartar una afectación colónica por un linfoma sistémico, donde el pronóstico y tratamiento son muy diferentes.