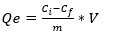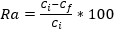INTRODUCCIÓN
Durante el desarrollo de los procesos industriales se producen residuales sólidos, líquidos y gaseosos que contaminan el medio ambiente y contienen en ocasiones elementos de carácter comercial, que pudieran ser recuperados con un adecuado tratamiento (Contreras et al. 2008; Guerrero, Falcón y Martínez 2006).
Los procesos metalúrgicos constituyen uno de los procesos industriales más agresivos para el medio ambiente y la sociedad, por los volúmenes de desechos generados anualmente para la producción de los distintos metales y los reactivos que se manejan en el proceso, además de los recursos minerales, de carácter no renovable (Hernández 2015).
Hoy en día el agotamiento progresivo de las reservas minerales abre un importante espacio para la reflexión acerca de la necesidad del uso racional de los recursos minerales; por tal motivo es de primordial importancia la búsqueda de alternativas que incrementen la eficiencia de los procesos metalúrgicos y a la vez permitan alcanzar los objetivos económicos de la industria minera con menores alteraciones ambientales (Lavaut 2015).
En trabajos recientes se ha demostrado que las lateritas cubanas poseen un contenido apreciable de escandio (Sc) mediante comparación con otros yacimientos del mundo que ya lo están explotando (Carballo et al. 2018). La extracción de este metal, como sub-productos de la industria del níquel, en los países de Australasia se está logrando, en plantas homólogas a Moa-Nickel S.A Comandante “Pedro Sotto Alba” (PSA), localizada en municipio de Moa en la provincia de Holguín, ya que se lixivia fácilmente con ácido sulfúrico en el proceso de lixiviación ácida a alta presión, (HPAL, por sus siglas en inglés.).
Análisis realizados evidencian que una parte importante del Sc presente en el mineral laterítico procesado por la PSA es extraída en el proceso de lixiviación ácida a presión; este metal, ya en forma de solución, atraviesa todas las etapas consiguientes del flujo tecnológico sin ser recuperado, perdiéndose en el residual líquido WL (Mata 2020; Durán 2019).
El Sc es un metal raro y costoso debido a su escasa distribución y dificultades asociadas con su extracción. Presenta aplicaciones muy específicas, como son: la obtención de luces de alta intensidad y calidad, en el craqueo del petróleo y en aleaciones con el aluminio para la industria aeroespacial, de ahí su importancia (Chasseé et al. 2016).
Existen diversos métodos convencionales para eliminar o recuperar metales pesados de aguas residuales (Caviedes et al. 2015; Uçar et al. 2015), pero considerando los aspectos técnico-económicos y la accesibilidad a determinados recursos, la adsorción ha demostrado ser el más conveniente (Peric, Trgo y Medvidovic 2004).
El carbón activado (CA) es un adsorbente muy efectivo en la recuperación de iones metálicos de aguas residuales (Ghasemi et al. 2015), sin embargo, un aspecto influyente en el proceso de adsorción lo constituye la química superficial del material adsorbente (Hernández et al. 2016). La modificación química del CA con diferentes agentes químicos puede modificar sus propiedades físicas y químicas, permitiendo eficiencia en aplicaciones específicas (Hernández 2019; Kano et al. 2017).
Entre la variedad de reactivos químicos utilizados para potenciar la formación de grupos superficiales ácidos en la superficie del CA, fue escogido para esta investigación el ácido fosfórico por su semejanza con el solvente Cyanex 572, que ha aportado buenos resultados en la recuperación de Sc por el método de extracción con solventes, y también como agente oxidante en la modificación química del CA (Nie et al. 2018; Zhou et al. 2008).
Este escenario sugiere la necesidad de evaluar cómo influye la modificación química del CA con soluciones diluidas de ácido fosfórico, en la recuperación del Sc presente en el WL.
MATERIALES Y MÉTODOS
El licor a tratar es el WL, desecho resultante de la Planta de Precipitación de Sulfuros de la PSA. La muestra fue recolectada directamente de la línea de descarga del tanque de licor de desperdicio (194-TK-1). Para garantizar una muestra representativa y homogénea el muestreo se realizó de forma puntual en un día de operación normal de la planta.
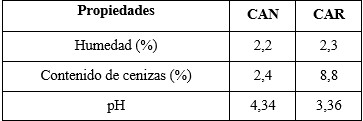
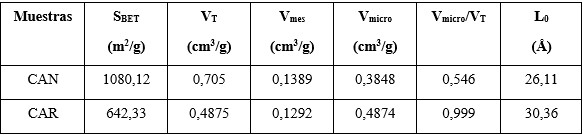
Se evaluaron dos tipos de CA; el primero, un CA granular virgen Norit empleado en el proceso de producción de ron (CAN), y el segundo, ese mismo carbón, pero ya regenerado luego de ser declarado agotado en el proceso de filtración del aguardiente (CAR). Los datos de su caracterización se muestran en la Tabla 1.
Caracterización físico-química del WL
Espectrofotometría por plasma acoplado inductivamente (ICP)
Para determinar la concentración de las especies iónicas de Sc en el WL se utilizó la técnica de ICP que permite la detección de elementos químicos con gran precisión y exactitud.
Espectrometría de Absorción Atómica (EAA)
Además, se analizaron los elementos Ni y Co, por resultar de interés económico para el proceso, mediante el método de EAA en un equipo Modelo contrAA 300 Analytikjena, en el Centro de Investigaciones del Níquel (CEDINIQ).
Adsorción por N2
La caracterización textural de los carbones se realizó por adsorción de N2 utilizando TriStar II 3200 de Micromeritics Instrument Corporation. Antes del análisis, la muestra se desgasificó durante la noche a 300 °C. El área superficial específica (SBET) se estimó por la ecuación BET (Brunauer, Emmett y Teller). La cantidad de N2 adsorbido a la presión relativa de p/p0=0,96 y una temperatura de 77 K, se empleó para determinar el volumen total de poros (VT). El volumen de microporos (Vmicro) se estableció aplicando el método t-plot (Scherdel, Reichenauer y Wiener 2010). El volumen del mesoporo (Vmeso) y la distribución del tamaño de poro de la región del mesoporo se determinaron por el método de Barrett, Joyner y Halenda (BJH) (Gregg 1982) y el análisis de la Teoría Funcional de la Densidad (DFT) (Lastoskie, Gubbins y Quirke 1993) se aplicó a las isotermas de adsorción de nitrógeno para definir la distribución del tamaño de los poros (L0).
Etapa experimental
La primera etapa del experimento consistió en la modificación del CAN y el CAR empleando disoluciones de concentraciones de 1mol/L y 2 mol/L de H3PO4, pues los procedimientos de oxidación provocan una disminución del área superficial del carbón pudiendo afectar su capacidad de adsorción (Tunomukwathi 2015).
Procedimiento para la modificación del CA con H3PO4:
Pesar 6 g de los carbones CAN y CAR en una balanza analítica calibrada y después se vierten cuidadosamente en un Erlenmeyer de 250 mL.
Medir en una probeta 350 mL de disolución de ácido fosfórico (H3PO4) a concentración de 1 mol/L y 2 mol/L.
Verter la disolución de ácido fosfórico en cada uno de los Erlenmeyer que contienen las cantidades de carbón ya pesadas.
Poner en contacto durante dos horas a una temperatura de 100 oC, temperatura que permitió que las fuerzas convectivas ayudaran a la agitación y mezclado entre el material adsorbente y la solución de H3PO4.
Filtrar la solución resultante y lavar el carbón con abundante agua para remover cualquier exceso de ácido existente en el mismo.
Secar los carbones en una estufa a 100 oC durante tres horas.
Los carbones luego de la modificación se codificaron de la siguiente manera:
CAN1: CA Norit oxidado con H3PO4 a una concentración de 1 mol/L.
CAN2: CA Norit oxidado con H3PO4 a una concentración de 2 mol/L.
CAR1: CA Norit regenerado oxidado con H3PO4 a una concentración de 1 mol/L.
CAR2: CA Norit regenerado oxidado con H3PO4 a una concentración de 2 mol/L.
En la segunda etapa se desarrollaron pruebas de adsorción, evaluando cada tipo de CA preparado, para determinar la influencia de la modificación en la selectividad del Sc contenido en el WL. Se procedió de la siguiente manera:
Pesar 1 g de cada uno de los CA y colocarlo en un beaker de 250 mL.
Añadir 50 mL del licor residual ácido (WL).
Dejar en contacto durante 72 horas a temperatura ambiente 25 oC sin agitación para evitar la destrucción y creación de polvo por parte del carbón y sellar con papel Parafilm “M”.
Filtrar y recolectar el filtrado para determinar la concentración final de las especies metálicas.
Los licores luego del tratamiento se codificaron de la siguiente manera:
Ecuaciones empleadas para el cálculo
Al finalizar cada experimento se procedió a determinar la concentración de los iones metálicos de la solución filtrada utilizando EAA o ICP. La capacidad de adsorción del CA por ion metálico se determinó utilizando la ecuación (1) (Manals, Vendrell y Penedo 2015):
Donde:
El porcentaje de remoción de ión metálico (Ra) se calculó a partir de la ecuación (2) (Manals, Vendrell y Penedo 2015):
Donde:
RESULTADOS Y DISCUSIÓN
Caracterización química del WL
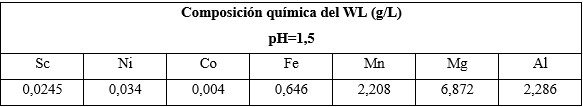
La composición química del WL analizada por ICP para la determinación de Sc y por EAA para el resto de los metales se observa en la Tabla 2.
Como se puede observar las concentraciones de Sc, Ni y Co son muy bajas en comparación con el resto de los metales presentes en el licor.
Teniendo en cuenta el contenido de Sc y tomando como base que se descargan 28 000 m3/día de WL al río Cabañas (Ministerio de Ciencia, Tecnología y Medio Ambiente 2020), se puede estimar una pérdida entre los 369-686 kg/día de Sc en el WL. Basados en estas cantidades, si se calculan las ganancias de su recuperación en función de los precios medios de este metal, en el mercado internacional representan valores aproximados entre 1 000 000 USD y 2 000 000 USD diarios.
Caracterización textural de los carbones empleados
La Tabla 3 presenta los resultados obtenidos para la caracterización textural de los carbones empleados (CAN y CAR), por el método de adsorción de N2. Los valores de área superficial BET del CAN y CAR se encuentran entre 642-1080 m2/g, la disminución del SBET en CAR puede explicarse por el proceso de regeneración al que fue sometido que modifica la estructura porosa del CA (Crespo 2017).
Para estos carbones el diámetro medio de poros está alrededor de 28 Å y el volumen de microporos se encuentra entre 0,38-0,49 cm3/g aproximadamente, lo que refleja un mayor volumen de microporos en el CAR, esto es ventajoso para la adsorción de iones metálicos en fase acuosa (Hernández 2019). Los resultados de los parámetros texturales son comparables con los reportados para carbones activados, obtenidos a partir de residuos lignocelulósicos que pueden alcanzar valores de área superficial de 2 400 m2/g y volúmen de poro de 1,4 cm3/g (Acevedo, Giraldo y Moreno 2017).
Análisis de la influencia de la modificación con H3PO4
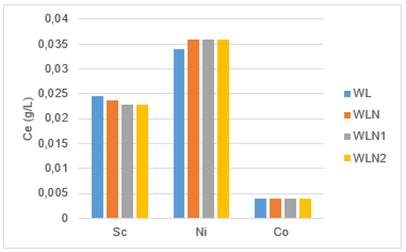
Los resultados de las concentraciones de Sc, Ni y Co presentes en el WL luego del tratamiento con el CA modificado y sin modificar se muestran en la Figura 1.
Se puede apreciar que los mejores resultados los muestran los iones de Sc3+, disminuyendo desde una concentración inicial en el licor WL de 0,0245 g/L hasta 0,0237 g/L, 0,0228 g/L y 0,0229 g/L luego del tratamiento con los carbones CAN, CAN1, CAN2, respectivamente.
En el gráfico se observa que no existió variación en la concentración de Co con ninguno de los CA analizados, por lo que no fue adsorbido por estos. Sin embargo, el Ni incrementó su concentración al final del experimento, lo que podría atribuirse a que este metal está contenido en el CA y ocurre un proceso de desorción.
Resulta evidente que la modificación con H3PO4 influyó en una mejor adsorción de los iones de Sc, no obstante, la modificación del CAN con la disolución a 1mol/L muestra mejores resultados; esto puede estar influenciado por una disminución del área superficial del CA debido a la oxidación a mayor concentración (Hernández 2019).
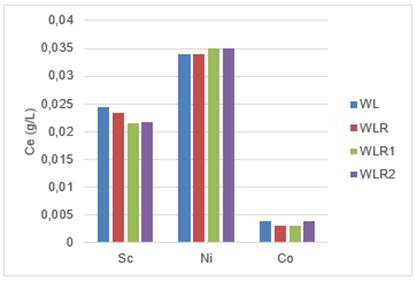
Los resultados observados luego del tratamiento con CAR con y sin modificación con H3PO4 a 1 mol/L y 2 mol/L (CAR, CAR1, CAR2) en la adsorción de Sc, Ni y Co en el WL tratado se muestran en la Figura 2.
Los valores obtenidos de concentración final de iones de Sc3+ en el WL, luego del experimento, muestran una disminución evidente, desde una concentración inicial de 0,0245 g/L hasta 0,0235g/L, 0,0216 g/L y 0,0218 g/L para CAR, CAR1 y CAR2, respectivamente. De igual forma el CAN manifestó el mismo comportamiento, que resultó mejor a la concentración a la oxidación de 1 mol/L.
Además, se evidencia que de manera general el carbón Norit regenerado, tanto modificado con H3PO4, como sin modificar mostró un mejor comportamiento en la adsorción de Sc que el carbón virgen; esto pudiera estar en parte condicionado porque el volumen de microporos disponible en el CAR es mayor que el del CAN, lo que se comprobó con la caracterización textural, que son los poros efectivos en la adsorción de especies ionicas metálicas en fase acuosa.
Para el cobalto se observó un mejor comportamiento por este carbón, que sí logró adsorberlo, disminuyendo su concentración desde 0,004 g/L a 0,003 g/L, tanto para el CAR como para el CAR1, lo que demuestra que en este caso la oxidación no es la causa de la adsorción, sino que puede estar influenciada por el proceso de regeneración al que fue sometido, pues este comportamiento no fue observado para el CAN. Los iones de Ni no fueron adsorbidos por ninguno de los CA analizados, sino que volvió a observarse un incremento en su concentración final.
Resultados de la remoción de escandio con los carbones empleados
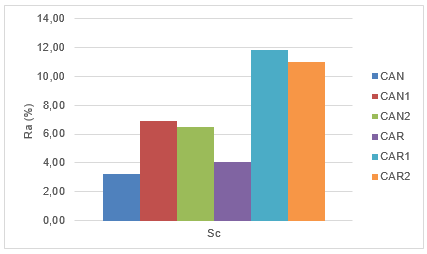
Los porcentajes de remoción calculados para los carbones empleados se muestran en la Figura 3. Los valores de % de remoción que se obtuvieron referidos al Sc fueron de 3,3 %, 6,9 % y 6,5 % para CAN, CAN1 y CAN2, respectivamente, lo que indica que la modificación permitió una mayor remoción de Sc.
Para CAR, CAR1 y CAR2 los valores de porcentaje de remoción que se obtuvieron referidos al Sc fueron de 4,1 %, 11,8 % y 11 %, lo que refleja que la oxidación aumenta su capacidad de adsorción para los iones de Sc y una selectividad superior a CAN, CAN1 y CAN2. Por tanto, se corrobora que los mejores resultados para el Sc los mostró el CA oxidado a 1 mol/L.
Además, se logró una remoción de Co considerable de un 25 % por parte del CAR y CAR1, lo cual no fue posible con el CAN, ni tampoco luego de su modificación, demostrando así un mejor desempeño, al ser este un metal de interés económico.
Se puedo comprobar que la oxidación favorece la adsorción de Sc en el WL. Este comportamiento está influenciado porque los grupos funcionales de oxígeno que se crean mediante la oxidación en la superficie del carbón contienen protones donantes, esto produce un desplazamiento de los iones H+ de la superficie de carbón oxidado, por iones metálicos presentes en el licor que tienen tendencia a formar complejos metálicos con la carga negativa de los grupos ácidos (Álvarez, López y Moreno 2005).
Capacidad de adsorción de CAN, CAN1, CAN2, CAR, CAR1 Y CAR2
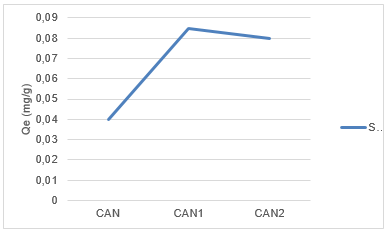
La capacidad de adsorción calculada para el Sc (Fig. 4) fue de 0,04 mg/g, 0,085 mg/g y 0,08 mg/g para CAN, CAN1, CAN2, respectivamente, mostrando el gráfico el mayor pico a la concentración menor a la que fue modificado con H3PO4.
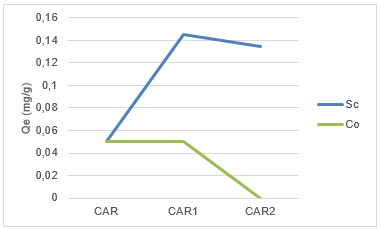
Por otra parte, la capacidad de adsorción para el Sc fue de 0,05 mg/g, 0,145 mg/g y 0,135 mg/g para CAR, CAR1, CAR2, respectivamente, como se observa en la Figura 5. Empleando el CAR1 se logra incrementar la capacidad de adsorción casi el triple que sin la modificación. Para el Co la capacidad de adsorción resulta significativa con un valor de 0,05 mg/g para CAR y CAR1, respectivamente.
CONCLUSIONES
La caracterización textural por adsorción de N2 de los carbones empleados evidencia que son microporosos, con un mayor volumen de microporos que de mesoporos.
Se comprueba que el incremento de los grupos superficiales ácidos en la superficie del CA provoca un aumento de la capacidad de adsorción y porcentajes de remoción de Sc, producto de la creación de interacciones específicas con el material adsorbente.
El CAR modificado con H3PO4 a una concentración de 1 mol/L muestra los mejores resultados en la adsorción de Sc; la oxidación permite una capacidad de adsorción de 0,145 mg/g y un 11,8 % de remoción.