INTRODUCCIÓN
Ipomoea batatas (L.) Lam (boniato) es una planta dicotiledónea que pertenece a la familia Convolvulaceae. Se propaga principalmente de forma vegetativa por esquejes o brotes enraizados (Dugassa y Feyissa, 2011).
Ha sido tradicionalmente visto como un "cultivo de personas pobres" o "cultivo huérfano", y ha atraído una atención limitada en comparación con otros cultivos básicos. Sin embargo, durante la última década, esta percepción ha cambiado, por su alto valor nutricional, rica en carbohidratos, almidón, minerales y vitaminas (Dinu y Soare, 2015) y es ampliamente reconocido que tiene un gran potencial para contribuir al alivio de la desnutrición y el hambre en el mundo en desarrollo (Mwanga et al., 2017). Según FAOSTAT (2016), es el séptimo cultivo en términos de producción a nivel mundial y el cuarto lugar entre los cultivos alimentarios.
En lo referente a las condiciones agroecológicas, I. batatas como especie cultivada y silvestre posee una amplia variabilidad genética que se expresa en la adaptación a condiciones ambientales diversas. Adicionalmente, su manejo agronómico resulta más económico que el de otros cultivos, en términos de menores requerimientos de fertilizantes y plaguicidas (Tique et al., 2009).
Debido al enorme interés comercial en I. batatas, se necesita la conservación del germoplasma de esta especie. La diversidad contenida en un germoplasma debe estar protegida contra las pérdidas. La base de todo mejoramiento genético radica en la diversidad genética, que se refleja en la creación de plantas con resistencia / tolerancia a diversos factores bióticos y abióticos, para asegurar una mayor productividad (Arrigoni-Blank et al., 2014).
Varios autores han establecido métodos para la propagación in vitro de I. batatas y es posible obtener plantas libres de patógenos a partir del cultivo de meristemos y luego multiplicar masivamente estas plantas mediante las técnicas de micropropagación (Salinas, 1990; González et al., 2003; Silva et al., 2003) y la conservación del material vegetal (Jarret et al., 1991; Sigueñas, 1997; Rayas et al., 2016). Estudios realizados han demostrado que las sales minerales y la sacarosa son componentes esenciales para el crecimiento y la supervivencia de plantas de I. batatas in vitro y no deben ser suprimidas en el medio de cultivo de crecimiento (Vettorazzi et al., 2017). Atendiendo a esto, los métodos de conservación deben preservar dichos componentes en el medio de cultivo.
La conservación de los recursos fitogenéticos garantiza su posible utilización como fuente de variación genética potencialmente útil, a la vez que evita la pérdida de diversidad genética en la agricultura, con la consiguiente reducción del material vegetal disponible para el uso de las generaciones presentes y futuras. En el cultivo de I. batatas se desarrollan varios programas que posibilitan la obtención de nuevos cultivares con el objetivo de mejorar la calidad nutricional de esta raíz tuberosa (Morales-Tejón et al., 2016). Así, mediante la vía del policruzamiento de variedades conservadas en el Banco de Germoplasma del INIVIT, Morales-Tejón et al. (2017) obtuvieron las progenies que, en un periodo de seis años de evaluación y selección, dieron origen al primer cultivar cubano de boniato de masa totalmente morada y características agronómicas deseables denominado ‘INIVIT BM-90’, con alto contenido de antocianinas.
El incremento en el número de entradas mantenidas en los bancos de germoplasma impulsa la implementación de técnicas más eficientes para la conservación a mediano y largo plazo. De esta forma, se asegura la disponibilidad de variabilidad genética de las especies y la preservación de la biodiversidad vegetal (Rivero, 2007; Parrado et al., 2013; Monteros-Altamirano et al., 2018). En este proceso se abre el camino a las posibilidades para el desarrollo y evolución de diversas especies. La conservación in vitro se ha perfilado como una alternativa valiosa para la combinación de técnicas de almacenamiento en lugar de depender de una sola.
La conservación in vitro libera las plantas de los riesgos que se producen en el campo, reduce los costos, asegura el mantenimiento de la fidelidad genética y facilita el intercambio de germoplasma. El objetivo de esta práctica es maximizar el período de subcultivo o extenderlo indefinidamente. Para lograrlo, se realizan cambios en el entorno de cultivo (Roca et al., 1994; Arrigoni-Blank et al., 2014).
I. batatas es susceptible a un gran número de enfermedades causadas por hongos, virus y nematodos. También es vulnerable a plagas como insectos y ácaros; por lo tanto, el banco de germoplasma activo en el campo es sensible a la pérdida y, por ende, requiere de conservación in vitro (Arrigoni-Blank et al., 2014).
En el cultivo de I. batatas se han realizado investigaciones para la conservación in vitro del germoplasma (Pennycooke y Towill, 2000; Espinosa et al., 2002; Espinosa et al., 2003; Rayas et al., 2016). Sin embargo, no siempre se consigue disminuir el crecimiento, se obtienen resultados variables unido a que varios autores han referido que la respuesta a la conservación depende del genotipo (Silva et al., 2002; Dugassa y Feyissa, 2011; Arrigoni-Blank et al., 2014). Por ello el objetivo del presente trabajo fue determinar el efecto de manitol y ácido abscísico en la conservación mediante crecimiento mínimo a mediano plazo de cultivares del Banco de germoplasma de I. batatas en el INIVIT.
MATERIALES Y MÉTODOS
La presente investigación se desarrolló en el Laboratorio de Biotecnología Vegetal del Instituto de Investigaciones en Viandas Tropicales (INIVIT), durante el período comprendido de abril de 2016 a marzo del 2017.
Para desarrollar el trabajo se utilizaron los cultivares de boniato ‘Cautillo’ (que se caracteriza por lento crecimiento in vitro) e ‘INIVIT BS - 16 - 2006’ (Cultivar de rápido crecimiento in vitro).
Para el establecimiento in vitro se utilizaron como explantes, meristemos de uno o dos primordios foliares (0.2 - 0.3 mm), procedentes de tubérculos previamente diagnosticados por la técnica de Inmunoensayo Ligado a Enzima a partir del kit Antigen Coated Plate ELISA para el grupo de potivirus (Virus del moteado del boniato, Virus latente del boniato y Virus de moteado suave del boniato), según el procedimiento descrito por Rayas et al. (2016). Se empleó un medio de cultivo que contenía las sales MS (Murashige y Skoog, 1962), tiamina (2.0 mg l-1), 6-bencil aminopurina (6-BAP) (0.3 mg l-1), ácido naftalenacético (ANA) (0.03 mg l-1) y 50.0 g l-1 de sacarosa.
Los explantes fueron incubados a 27 °C y régimen de 16 horas de luz (DFFF de 62-68 µmol m-2s-1) y ocho de oscuridad, durante 35 días.
Posteriormente, se multiplicaron in vitro los cultivares objeto de estudio según metodología descrita por Love et al. (1989), hasta disponer de la cantidad de material vegetal necesario para utilizar como explantes segmentos nodales de plantas in vitro de aproximadamente 2.0 cm de longitud.
Para seleccionar el medio de cultivo de crecimiento mínimo que permitiera la conservación in vitro de I. batatas, se utilizó como medio de cultivo basal (MB) las sales propuestas por Murashige y Skoog (1962) (MS), 100 mg l-1 de mio-inositol, 1 mg l-1 de tiamina y 30 g l-1 de sacarosa. El medio de cultivo basal se combinó con ácido abscísico (ABA) y manitol y se conformaron los siguientes tratamientos:
M0. MB.
M1. MB + ácido abscísico (5 mg l-1)
M2. MB + ácido abscísico (10 mg l-1)
M3. MB + manitol (1.0%)
M4. MB + manitol (1.5%)
M5. MB + manitol (2.0%)
M6. MB + ácido abscísico (10 mg l-1) + manitol (1.0%)
M7. MB + ácido abscísico (10 mg l-1) + manitol (1.5%)
M8. MB + ácido Abscísico (10 mg l-1) + manitol (2.0%)
M9. MB + sorbitol (1.0%) + glucosa (1.0%). (Control)
Todos los medios de cultivo se solidificaron con 4.7 g l-1 de agar E (Biocen) y el pH se ajustó a 5.7 antes de la esterilización en autoclave.
Se utilizaron como controles el tratamiento M0 que contenía solo el medio de cultivo basal y el tratamiento M9, medio de cultivo recomendado por Rayas et al. (2016) por los resultados obtenidos en el cv. ‘Cautillo’.
Se emplearon 30 tubos de ensayo (150 x 25 mm) con 10 ml de medio de cultivo y un explante por tubo y se evaluaron 20 explantes al azar.
Se evaluó a los seis y ocho meses mediante observación visual la supervivencia de los explantes (cálculo de porcentaje a partir del número de explantes vivos), se midió la altura de la plántula (cm), con la ayuda de una regla graduada y se cuantificó el número de hojas activas (hojas verdes).
Una vez seleccionado el medio de cultivo con mejores resultados en la conservación, este se determinó su efecto en 12 cultivares cubanos de boniato, procedentes de la colección de germoplasma de boniato del INIVIT. A los seis meses se evaluó la supervivencia (%), se midió la altura de la planta (cm) y se cuantificó el número de hojas activas y el número de brotes por planta.
Análisis estadístico
Para el procesamiento de los datos se empleó el paquete estadístico SPSS ver. 15.0 para Windows. Puesto que se encontró normalidad y homogeneidad de varianzas, con un nivel de significación de p<0.05, los datos se procesaron mediante análisis de varianza de clasificación simple (completamente al azar) y la comparación múltiple de medias se realizó según la prueba de Tukey.
Para evaluar la influencia del medio de cultivo de crecimiento mínimo en diferentes cultivares se realizó la comparación de medias mediante la prueba de Bonferroni por tener diferentes números de réplicas por cultivar.
RESULTADOS Y DISCUSIÓN
En la conservación in vitro se apreció que en el cv. ‘INIVIT BS - 16 - 2006’ después de seis meses de conservación el mayor porcentaje de supervivencia se observó en los medios de cultivo que contenían manitol (M3, M4, M5). Estos fueron los únicos que a los ocho meses mostraban supervivencia de los explantes superior al 80%. En el cv. ‘Cautillo’ también a los seis meses la supervivencia fue superior en los medios de cultivo con manitol (Tabla 1) (Figura 1).
Se comprobó que el ABA afectó la supervivencia de los explantes. En los medios de cultivo donde se adicionó solo (M2 y M3) se observaron bajos porcentajes de supervivencia de los explantes, los que no lograron superar el 54% a los seis meses y murieron antes de los ocho meses en ambos cultivares. De igual forma, cuando se combinó con manitol no se obtuvieron buenos resultados.
Tabla 1 Supervivencia de explantes de I. batatas cv. ‘INIVIT BS - 16 - 2006’ y ‘Cautillo’ a los seis y ocho meses de conservación in vitro en medios de cultivo de crecimiento mínimo.
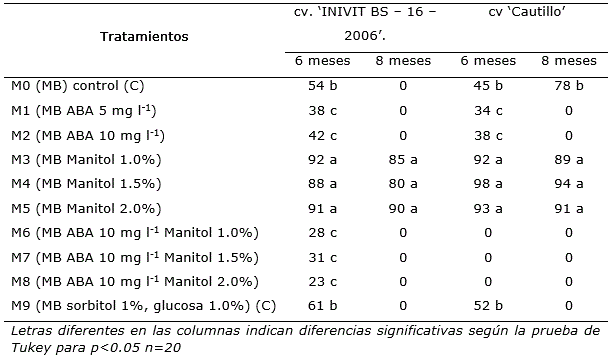

Figura 1 Plantas de Ipomoea batatas cv. ‘Cautillo’ (A) e ‘INIVIT BS - 16 - 2006’ (B) a los ocho meses de conservadas in vitro en medios de cultivo de crecimiento mínimo. M0. Medio de cultivo basal, M3. Medio de cultivo con 1.0% de manitol, M4. Medio de cultivo con 1.5% de manitol, M5. Medio de cultivo con 2.0% de manitol.
Contrario a los resultados en esta investigación, Espinosa et al. (2003) conservaron cuatro cultivares de boniato durante un año en medio de cultivo con 10.0 mg l-1 de ABA con altos porcentajes de supervivencia (≥ 85.5%) y recuperación (≥ 97.5%), entre los que se encontraba el cv. ‘Cautillo’. Sin embargo, Arrigoni-Blank et al. (2014), quienes estudiaron el efecto de concentraciones de ABA en varios cultivares de boniato concluyeron que podrían conservarse durante 180 días con 2.0 mg l-1 de ABA, con una mediana supervivencia (78%). Estos autores sugirieron que este regulador afectaba negativamente la supervivencia de los explantes, lo cual coincide con los resultados de este trabajo donde se emplearon concentraciones superiores. Además, apuntaron que las diferentes respuestas morfogénicas durante la conservación in vitro del boniato podían estar relacionadas con el genotipo debido a que usaron varios cultivares en sus ensayos. Además, las características del material vegetal con se trabaje, el tamaño del explante inicial y las condiciones ambientales de conservación también pueden influir lo cual explicaría las diferencias entre los porcentajes de supervivencia del cultivar ‘Cautillo’ de este trabajo con respecto a los informados por Espinosa et al. (2003) y Rayas et al. (2016).
En cuanto al efecto del manitol se conoce que la limitación del crecimiento por efecto de la concentración del agente osmótico se debe a la reducción de la adsorción de agua y nutrientes del medio de cultivo (García-Águila et al., 2007). Sin embargo, las concentraciones empleadas en este trabajo aunque redujeron el crecimiento no afectaron la supervivencia de las plantas de los dos cultivares aun a los ocho meses de conservadas. Resultados contrarios obtuvieron Díaz et al. (2015) en la conservación in vitro de Dioscorea spp. por crecimiento mínimo con este agente osmótico.
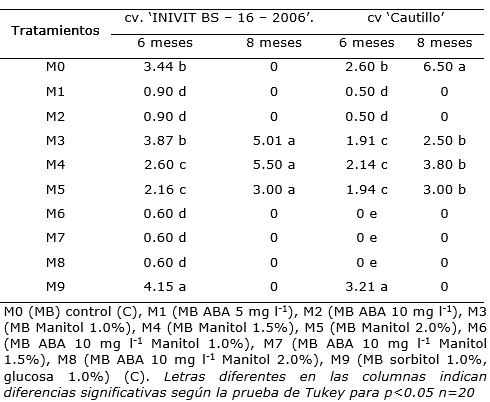
En ambos cultivares se observó que en los medios de cultivo con ABA las plantas no crecieron (0.6 cm) y a los ocho meses ya habían muerto, mientras que, en los medios de cultivo con manitol, sin ABA (M3, M4 y M5) aunque se apreció una reducción en la altura de la planta se mantenían vivas aun después de los ocho meses (Tabla 2).
Tabla 2 Efecto del medio de cultivo sobre la altura (cm) de los explantes en medios de cultivo de crecimiento mínimo a los seis y ocho meses en los cv. ‘INIVIT BS - 16 - 2006’ y ‘Cautillo’.
Los resultados coinciden con informes de otros autores que han referido el uso de manitol para la conservación in vitro de plantas. Al respecto, Fortes y Scherwinski-Pereira (2001) observaron que este agente osmótico produjo una reducción del crecimiento y número de los brotes en papa (Solanum tuberosum, L.) en comparación con la sacarosa. Sin embargo, Borges et al. (2009) al estudiar el efecto del manitol en el crecimiento mínimo del ñame (Dioscorea alata L.) concluyeron que al utilizar concentraciones superiores a 1.5% se afectaba de manera significativa la supervivencia del material vegetal. Por otra parte, Lata et al. (2010) informaron que de 2 a 4% de manitol no es adecuado para la conservación in vitro de la planta medicinal Podophyllum peltatum L.
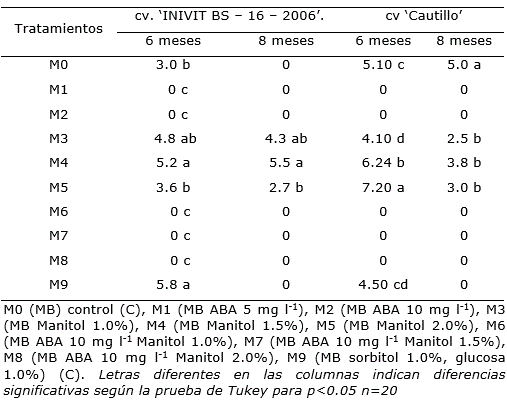
Otro de los efectos negativos de ABA se relacionó con la no formación de hojas en las plantas crecidas en los medios de cultivo que lo contenían. Sin embargo, en presencia de manitol se formaron hojas pequeñas que se mantuvieron verdes por tiempos prolongados (Tabla 3).
Tabla 3 Efecto del medio de cultivo sobre el número de hojas de explantes de Ipomoea batatas cv. ‘INIVIT BS - 16 - 2006’ y ‘Cautillo’ conservados durante seis y ocho meses en medios de cultivo de crecimiento mínimo.
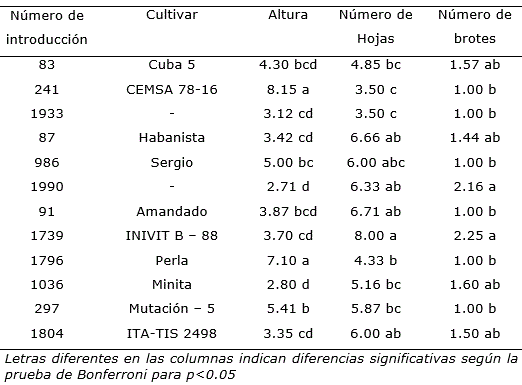
Atendiendo a los resultados se seleccionó el medio de cultivo basal que contenía las sales MS, 2 mg l-1 de tiamina, 100 mg l-1 de mio-inositol y además 1.0% de manitol (Tratamiento M3), para la conservación in vitro de 12 cultivares de la colección de germoplasma. Entre estos se observaron diferencias significativas en cuanto a la altura de la planta obtenida in vitro, el número de hojas y el número de brotes formados después de conservados durante seis meses. Los valores de supervivencia fueron superiores al 80%, sin diferencias significativas entre ellos (Tabla 4, Figura 2). Este resultado evidenció el efecto del genotipo y sugiere la necesidad de clasificar los cultivares para formar grupos según sus hábitos de crecimiento, lo que simplificaría las labores al no subcultivar toda la colección in vitro con la misma frecuencia.
Tabla 4 Respuesta de cultivares de Ipomoea batatas a los seis meses de conservados en el medio de cultivo que contenía 1.0% de manitol.