INTRODUCCIÓN
El petróleo consta de decenas de miles de moléculas orgánicas, desde estructuras tan simples como el metano hasta macromoléculas complejas como los asfaltenos. Entre ellas figuran los llamados biomarcadores, los cuales, en su mayoría se derivan de precursores moleculares que formaban parte de diferentes organismos vivos que habitaban el planeta hace millones de años como bacterias, hongos, algas, plancton, líquenes, musgos, helechos y otras plantas superiores (Peters, K.E., Moldowan, J.W. 1993, 2005).
La cantidad de biomarcadores presentes en este mineral es pequeña y debido a la alta estabilidad de sus estructuras químicas, constituyen testigos arqueológicos del proceso de formación y transformación del mismo. (Peters, K.E., Moldowan, J.W. 1993, 2005, Seifert W.K., Moldowan J.M. 1978). En base a la composición tanto cualitativa como cuantitativa de las moléculas-testigo es posible inferir sobre geo-cronología, el grado de alteración, el ambiente de deposición (terrestre, lacustre, marino ó mezcla) y consecuentemente sobre la materia orgánica involucrada en el proceso. Además, es viable realizar estudios ambientales (contaminación), forenses (derrames) (Wang Z. et al., 2006, 2003, 1994, El-Sabagh, S.M. et al., 2018, Fang, R. et al., 2019) y del comportamiento de los reservorios de hidrocarburos. Según su naturaleza química, dentro de los biomarcadores reportados en la literatura científica, se distinguen alcanos lineales y ramificados, isoprenoides, sesquiterpenos, diterpenoides, terpanos tricíclicos, tetracíclicos y pentacíclicos, esteranos, esteroides, hidrocarburos aromáticos policíclicos y porfirinas, entre otros (Lorenzo, E. et al., 2018, Tao, S. Z. et al., 2015, Walters, C.C. et al., 2018).
La herramienta analítica básica para el análisis de los biomarcadores es la cromatografía de gases acoplada a espectrometría de masas (CG/EM). Consiste en una técnica combinada donde una vez los componentes de una muestra son eluídos en el cromatógrafo, las moléculas volatilizadas del analito son fragmentadas en la cámara de ionización al hacerles incidir un haz de electrones. Los iones así generados son acelerados hacia el analizador másico donde son separados de acuerdo a su relación masa/carga (m/z), y finalmente detectados para generar un espectro de masas característico para cada compuesto. Su empleo permite identificar compuestos desconocidos, cuantificar compuestos conocidos, y elucidar la estructura y propiedades químicas de las moléculas.
En la exploración petrolera, dentro de la fracción de compuestos alifáticos los terpanos y esteranos figuran entre los biomarcadores más utilizados. Las muestras objeto de estudio que no han sido severamente afectadas por procesos de alteración poseen fragmentos iónicos característicos de m/z 191, m/z 217 y 218 (Mei, M. et al., 2018). El objetivo del presente trabajo consiste en desarrollar un procedimiento analítico para obtener la distribución de los biomarcadores saturados terpanos y esteranos mediante la técnica de cromatografía gaseosa acoplada a espectrometría de masas.
MATERIALES Y MÉTODOS
Reactivos
Perfluorotributilamina Mass Spec Std (PFTBA), Alfa Aesar
n-hexano para cromatografía, Merck
n-heptano para cromatografía, Merck
Diclorometano para cromatografía, Merck
Sílica gel 100-200 mesh, Sigma-Aldrich (activado a 200°C por 4 h)
Alúmina, Sigma-Aldrich (activado a 200°C por 4 h)
Sulfato de sodio anhidro, Merck (>99.0 % de pureza)
Papel de filtro para análisis cuantitativo Whatman No.2
Muestras
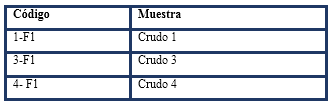
Para el desarrollo de la metodología analítica se seleccionaron 3 muestras de crudos ligeros pertenecientes a la familia II debido a que no presentan alteración y poseen cierto nivel de evolución térmica que posibilita la identificación de todos los picos de interés geoquímico (Domínguez, Z. et al., 2006, 2007, 2008). En la Tabla 1 se muestra la identificación de cada una de ellas.
Preparación de las muestras
Para la precipitación de los asfaltenos se pesó 1 g de crudo en un beaker de 250 mL de capacidad, donde posteriormente se anadió 40 mL de n-heptano. La mezcla se dejó reposar por 24 horas apartado de la luz para promover la precipitación efectiva de la fracción de asfaltenos. Posterior a ello se separó la fracción soluble (maltenos) mediante el proceso filtración con de papel filtro Whatman No. 2. Finalmente, los maltenos disueltos en el disolvente se evaporaron a sequedad.
Una vez obtenidos los maltenos se procedió a la separación de las fracciones de hidrocarburos saturados 1-F1, 3-F1 y 4-F1 a través de la técnica de cromatografía de adsorción en columna. Las pipetas Pasteur que se emplearon fueron de 10 cm de largo por 0,5 cm de ancho y se empacaron con sílice/alúmina en una proporción 1:1. Previo a la siembra de las muestras en el tope de la columna fue necesario disolver 30 mg de las mismas en n-hexano. Las fracciones de saturados 1-F1, 3-F1 y 4-F1 se eluyeron con 2 ml de n-hexano y se transfirieron a viales para su análisis por CG-EM.
Instrumento
Con la finalidad de obtener los biomarcadores, los extractos de hidrocarburos saturados se analizaron por CG/EM. El equipo consiste en un cromatógrafo de gases modelo 7890A acoplado a un espectrómetro de masas modelo 5975C, ambos de la marca Agilent Technologies. El cromatógrafo de gases está equipado con inyector automático modelo G-4513A. La adquisición y el procesamiento de los datos se realizaron con la ayuda del software MSD Productivity ChemStation, versión E.02.02. Para la calibración del espectrómetro de masas se utilizó Perfluorotributilamina (PFTBA). Los iones utilizados fueron m/z 69, 219 y 502 en las zonas de masas pequeña, media y elevada, respectivamente. Los parámetros relativos a la calibración de masas se ajustaron automáticamente (extracción, enfoque, aceleración y detección de los iones) mediante el procedimiento de "autotune" para obtener mayor sensibilidad y una adecuada resolución.
Condiciones experimentales
Las condiciones operacionales fueron las siguientes: columna capilar HP-5MS de 30 m de longitud, 0.25 mm de diámetro interno y 0.25 μm de espesor de película de fase estacionaria. El gas portador utilizado fue Helio y se mantuvo a flujo constante a 1 mL/min. La temperatura del horno se programó desde 60 hasta 300 °C con rampa de calentamiento de 6 °C/min, un tiempo isotérmico inicial de 2 min y final de 15 min. La temperatura del inyector se mantuvo a 300 °C y el volumen de inyección fue de 1 μL en modo "splitless".
El espectrómetro de masas se operó en el modo SCAN (barrido completo de radiofrecuencia en el rango de masas de m/z 50-700) con energía de ionización de 70 eV. Las temperaturas de la fuente de iones y la interface se mantuvieron en 250 °C y 280 °C, respectivamente.
La identificación de los biomarcadores se realizó comparando sus tiempos de retención (tR) y sus espectros de masas con los de la librería NIST soportada en el software y con datos de la literatura especializada (López-Quintero, J. O. et al., 1997, Walters, C.C. et al., 2017). La abundancia relativa de los compuestos terpanos y esteranos en las fracciones F1 se calcularon a partir de la integración de los picos generados en los fragmentogramas de los iones diagnósticos m/z 191, m/z 217 y m/z 218.
Evaluación de los resultados
La precisión del método se evaluó a través de las medidas de dispersión repetibilidad y precisión intermedia. La primera se estimó inyectando la muestra 1-F1 por triplicado en iguales condiciones experimentales, y la segunda de igual manera en días diferentes y por distintos analistas. Los resultados obtenidos se expresaron como desviación estándar relativa (% DER).
RESULTADOS Y DISCUSIÓN
Las fracciones F1 de las muestras 1-F1, 3-F1 y 4-F1 fueron analizadas mediante CG/EM.
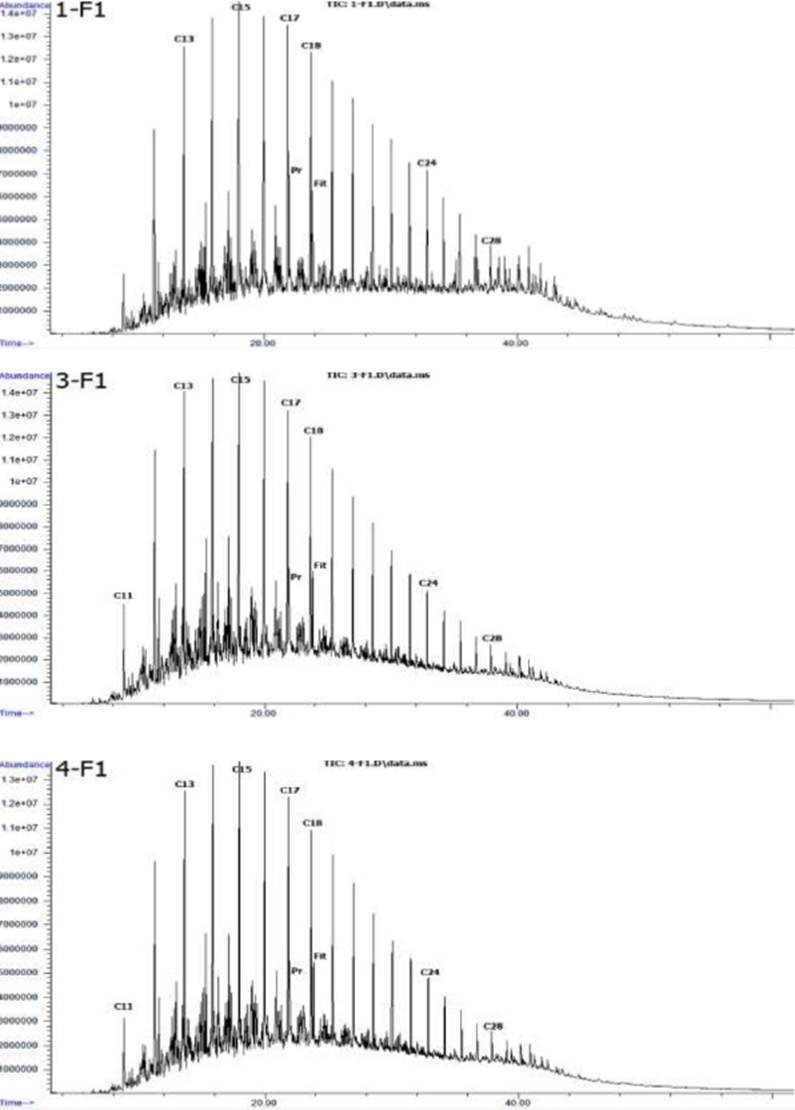
En la figura 1 se presentan los cromatogramas de iones totales (TIC, por sus siglas en inglés) adquiridos en modo SCAN. En ellos se observan los picos cromatográficos correspondientes a la elución de las n-parafinas en el rango de nC11 a nC35, además de los isoprenoides pristano y fitano. Estos cromatogramas de masas le son útiles a los geoquímicos debido a que mediante el predominio par/impar y las relaciones alcano normal/isoprenoide es posible conocer el estado de alteración además del origen de la roca madre (Wang, Z., et al., 2016, Domínguez, Z. et al., 2006, 2007, 2008).
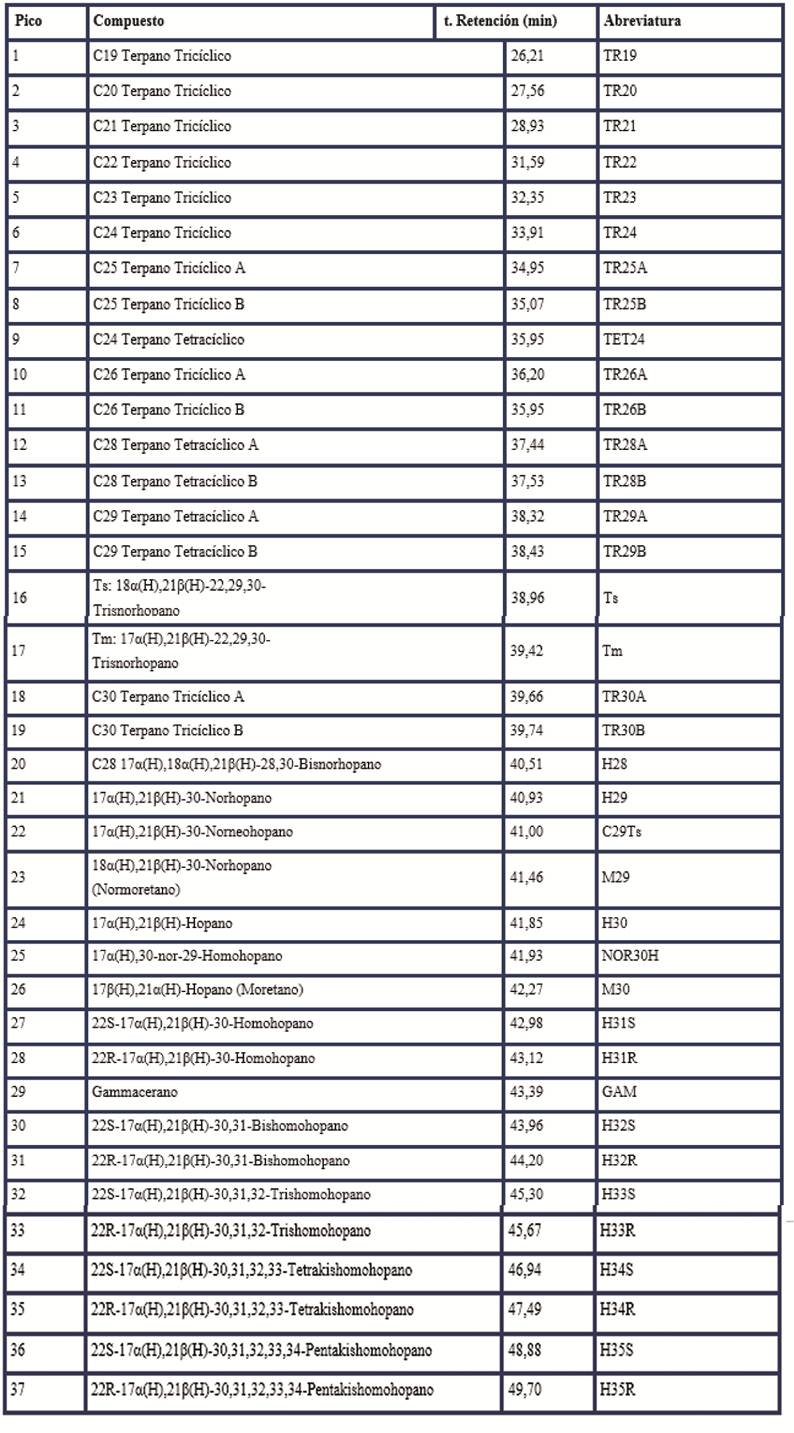
Se identificaron 37 compuestos terpanos y 19 compuestos esteranos que corresponden con los reportados en la literatura especializada (tablas 2 y 3).
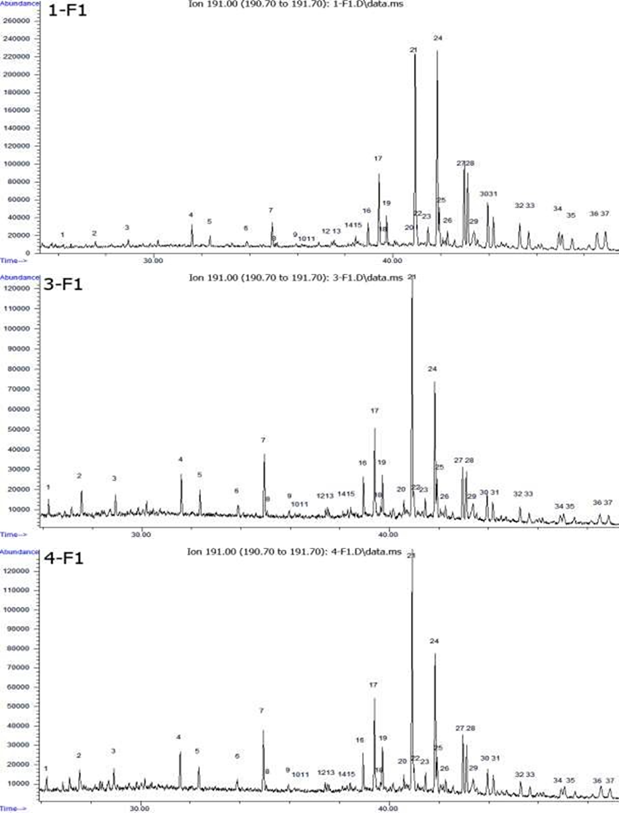
En la figura 2 se presentan los cromatogramas iónicos extraídos a m/z 191 donde se aprecia la distribución de los compuestos terpanos referidos en la tabla 2. Además, se distingue la excelente separación de isómeros de terpanos tricíclicos C26-C30, así como la alta proporción de hopanos extendidos relativo a los terpanos tricíclicos.
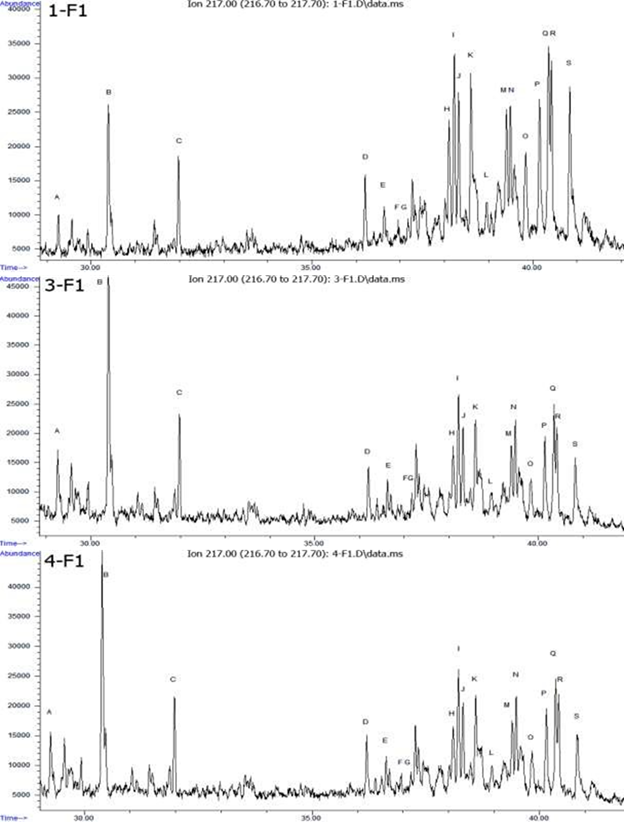
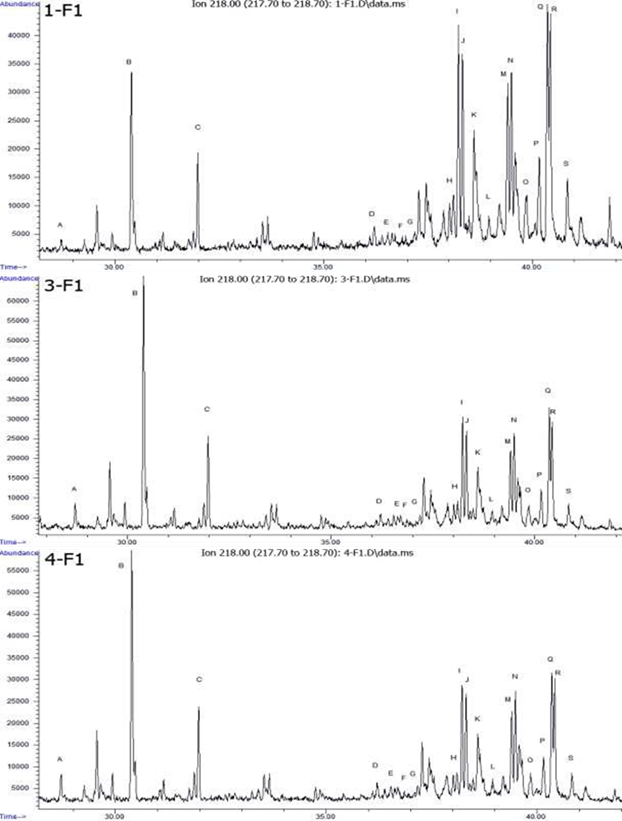
En las figuras 3 y 4 se exhiben los cromatogramas iónicos extraídos a m/z 217 y m/z 218, respectivamente. En ellas se aprecia la distribución de los compuestos entre 29 y 40 min, así como su adecuada separación y predominio de los esteranos regulares C27, C28 y C29 referidos en la tabla 3.
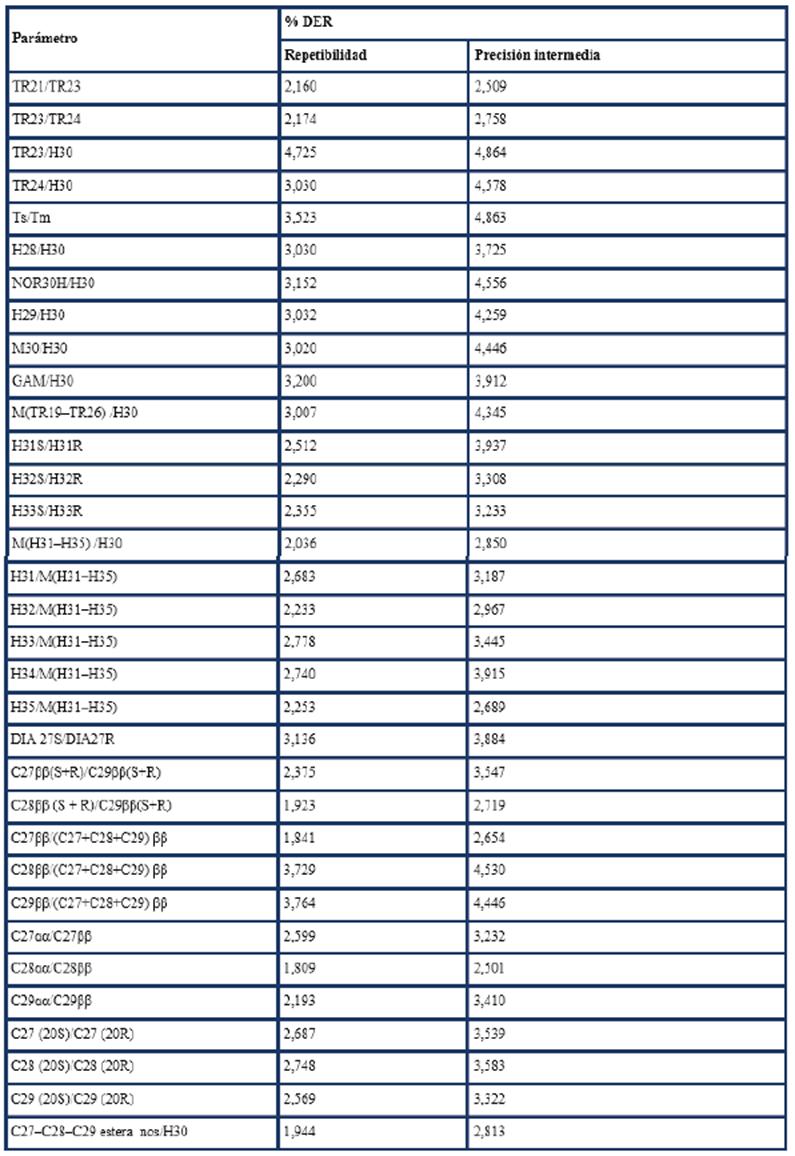
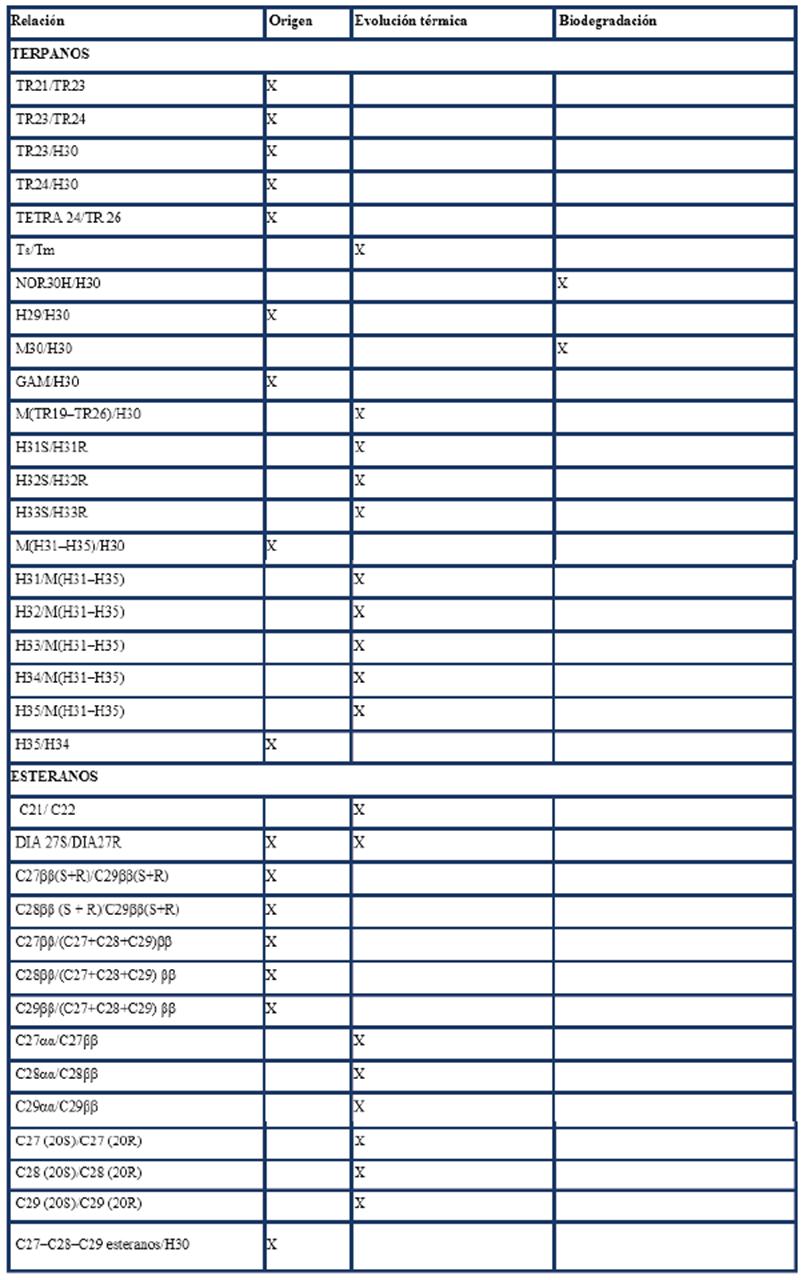
En la tabla 4 se presentan algunos parámetros utilizados frecuentemente en geoquímica orgánica y sus aplicaciones. El cálculo de ellos se efectúa a partir de relaciones de compuestos terpanos y esteranos según sus abundancias relativas (en este caso, medidas de las áreas).
La repetibilidad y precisión intermedia se reportan en la tabla 5. Las desviaciones estándares relativas fueron inferiores al 5% lo que demuestra que los resultados están en concordancia con los criterios de calidad establecidos para métodos cromatográficos análogos en los que se considera hasta un 5 % de variabilidad (Medeiros P.M. et al., 2007, Fernández R. et al., 2010, Cheng, X. et al. 2016).
Tabla 3 Identificación de picos de biomarcadores esteranos (m/z 217 y 218) en el fragmentograma de masas.
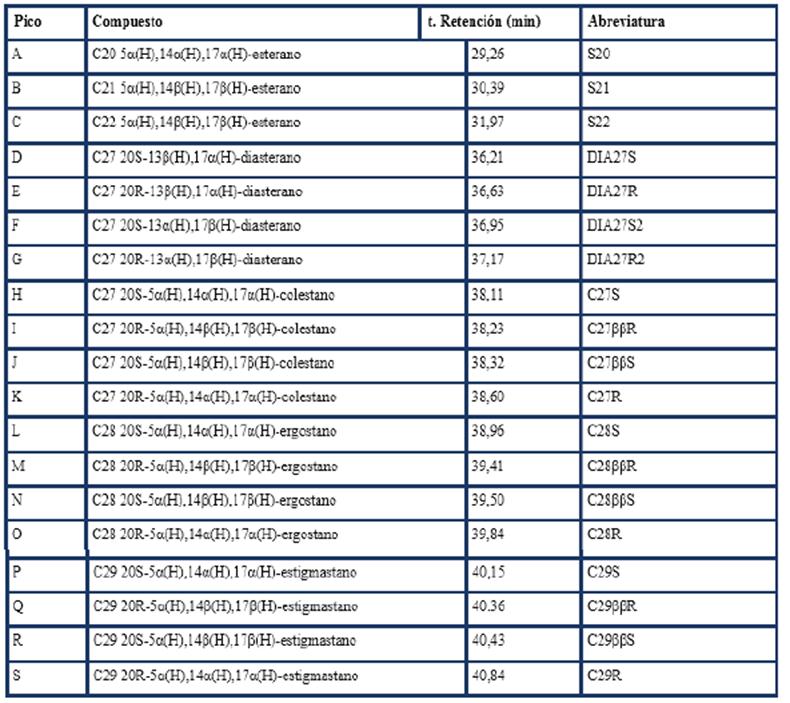
Tabla 4 Parámetros geoquímicos más representativos de la fracción de compuestos alifáticos y sus aplicaciones.
CONCLUSIONES
Se identificaron 37 compuestos del grupo de los terpanos y 19 compuestos del de los esteranos. La distribución de los mismos se obtuvo a través de los iones diagnósticos m/z 191, m/z 217 y m/z 218 de las fracciones de hidrocarburos saturados de las muestras de crudos. La repetibilidad, precisión intermedia y desviaciones estándares relativas fueron inferiores al 5 % lo que demuestra que los resultados están acorde a los criterios de calidad establecidos para métodos cromatográficos análogos. Se desarrolló una metodología analítica para el análisis de biomarcadores mediante la técnica de cromatografía gaseosa acoplada a espectrometría de masas, que puede utilizarse en muestras de crudo para la determinación de parámetros geoquímicos.