INTRODUCCIÓN
La degradación de los suelos posee repercusiones negativas a largo plazo como la pérdida de diversidad genética, menor productividad agrícola y una menor resilencia de los ecosistemas a eventos externos. En este sentido se estima que el avance progresivo de este tipo de afectación para el 2050 puede alcanzar los 900 millones de hectáreas, lo que se manifestará en una disminución de los bienes y servicios que pudiera ofrecer este recurso (BCN, 2019). De ahí la importancia de conservarlo en buenas condiciones para la sociedad.
Diferentes estudios han determinado el efecto de la contaminación por petróleo sobre el ecosistema suelo. Dicha contaminación ocasiona el deterioro de la calidad del ambiente, amenaza a la salud pública, así como daños a las especies vegetales y animales (Greenpeace, 2012). Los suelos contaminados con petróleo afectan el desarrollo de las plantas, y a medida que la contaminación es mayor, la tolerancia de las plantas disminuye (Hernández y col., 2017). En la naturaleza, los hidrocarburos pueden ser eliminados del suelo por cualquiera de los siguientes procesos: biodegradación, emisión, percolación, drenaje superficial u otros. En los últimos años se ha prestado mucha atención a los métodos biológicos y las combinaciones de estos con tratamientos químicos; tanto para la disposición final de residuos industriales como para la recuperación de sitios contaminados. Estos métodos biológicos se conocen genéricamente como procesos de biorremediación y tienen como objetivo el aprovechamiento y optimización de las capacidades biodegradadoras naturales. La biorremediación de suelos contaminados con hidrocarburos es un proceso dinámico en el que contaminante, suelo, clima y actividad biológica interactúan para degradar, transformar e inmovilizar los constituyentes del contaminante (Ponce, 2014).
La evaluación de la ecotoxicidad en procesos de biorremediación de suelos contaminados con hidrocarburos, es de gran importancia. Esto se debe a que en algunos procesos metabólicos asociados a la biodegradación se pueden generar productos de oxidación parcial, que pueden presentar una mayor toxicidad que los productos contaminantes al inicio del biotratamiento. Es importante conocer la evolución de la ecotoxicidad tanto para estudios de riesgo como para la mejora del conocimiento de los procesos de biodegradación. Además de certificar que el proceso de biorremediación ha sido favorable sobre la disminución en la concentración de contaminantes y no existe toxicidad de los productos del metabolismo. Para evaluar la ecotoxicidad de suelos se utilizan ensayos de toxicidad aguda. La toxicidad aguda se analiza mediante bioensayos que involucran los lixiviados del suelo, la inhibición, letalidad y reproducción de los bioindicadores. Estos estudios pueden ser aplicados a los tres tipos de tratamiento en unidades experimentales, microcosmos, mesocosmos y ecosistemas naturales, en cuyos tratamientos se haya logrado la disminución del contaminante.
Para determinar el efecto tóxico de la sustancia o muestra de prueba se calcula la concentración letal media (CL50). Esta variable se refiere a la concentración estimada de la sustancia prueba que produce una mortalidad del 50% de la población de los bioindicadores expuestos durante el periodo de experimentación. El valor de CL50 indica el potencial de peligrosidad de la sustancia de prueba, pero no puede ser usado directamente para predecir los efectos de una descarga de la sustancia de prueba en ambientes naturales. El criterio de toxicidad se establecerá en dependencia de que fracción de la muestra se utilice (fracción sólida suspendida (FSS) o fracción solida acomodada (FSA)).
En muestras sólidas, tales como desechos con hidrocarburos y suelos contaminados, los bioindicadores más comúnmente empleados son lombrices de tierra y plantas. En los bioensayos con plantas se emplean semillas de lechuga, centeno, maíz, berro, trigo, cebada, entre otros (OECD 207, 1984).
El objetivo de esta investigación es aplicar bioensayos de toxicidad aguda para la evaluación eco-toxicológica de suelos tratados contaminados con diésel.
MATERIALES Y MÉTODOS
Se efectuaron ocho tratamientos en microcosmos de suelos contaminados con diésel y a cada uno, se les realizaron bioensayos de toxicidad con semillas de lechuga Latuca Sativa y con la lombriz de tierra Esenia Andrei (Tabla 1), como biomodelos representativos de los ecosistemas terrestres. Ambos bioensayos determinaron el riesgo toxicológico, definido por el criterio de limpieza o remediación de un suelo (Infante y Morales, 2012). La biorremediación con adición de microorganismos (bioaumentación) 1 y 2, consistió en la adición de inóculos en concentraciones de 5 mL/kg y 10 mL/kg respectivamente. Se evaluó en suelos húmedos y secos, la biorremediación con incremento de acondicionadores orgánicos (mejorada) 1 y 2 respectivamente.
Tabla 1 Relación de tratamientos a evaluar
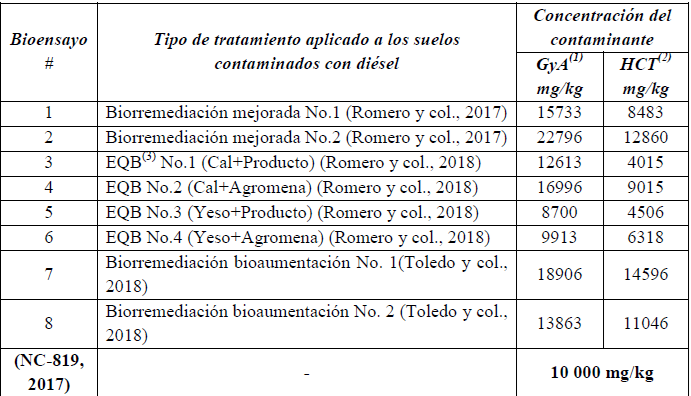
( 1)Grasas y Aceites
(2) Hidrocarburos Totales
(3) Estabilización Química- Biológica
(4)(Romero y col., 2017), (Romero y col., 2018), (Toledo y col., 2018), (NC-819, 2017)
2.1 Bioensayos con semillas de lechuga
La evaluación de la toxicidad de las muestras de estudio se realizó a través del procedimiento para bioensayos con semillas de lechuga según la guía 207 de la OECD (OECD 207, 1984). Los bioensayos se realizaron con papel de filtro No. 20 y se evalúan los efectos fitotóxicos de compuestos de hidrocarburos sobre el efecto letal (inhibición de germinación de la semilla) sobre la estructura y función de las plantas (Cuevas y col., 2012). Las semillas de lechuga (Fig. 1) utilizadas presentan más de un 95% de probabilidad de germinación y certificación aprobada para su uso (Decreto No. 175, 1992).
Preparación de las muestras
200 g de cada uno de los suelos tratados se mezclaron con 800 mL de agua destilada. Se incuban en zaranda reciprocante con agitación de 130 rpm durante 10 min, y se dejan reposar por 12 horas en refrigeración (ASTM E:1391-03, 2014). Con la fracción sólida suspendida (FSS) de la muestra, se preparan diluciones con agua destilada a las concentraciones de 1, 5, 25, 50 y 100 %.
Preparación de los bioensayos
Cada bioensayo se ejecutó en placas Petri, por triplicado incluyendo las réplicas del control. Se añaden cantidades de 0,25, 1,25, 6,25, 12,5 y 25 mL de la solución madre, completando para cada caso con agua destilada a volumen final de 25 mL. De cada solución final se añaden 5 mL al papel de filtro No.201 que contiene cada placa Petri. Para todos los bioensayos se colocan 20 semillas en cada placa cuidadosamente, con la ayuda de una pinza, para asegurar espacio suficiente entre las semillas para permitir la elongación de las raíces sin dificultad. Las placas se incuban envueltas en bolsas plásticas negras para evitar la pérdida de humedad y la entrada de la luz, por un período de 120 horas (5 días).
2.2 Bioensayo con lombriz de tierra
La evaluación de la toxicidad de las muestras de estudio se realizó a través del procedimiento bioensayos con lombrices de tierra (Fig. 2), según la guía 207 de la OECD (OECD 207, 1984). En este bioensayo se midió el efecto letal (mortalidad) de los organismos expuestos por el impacto directo de los hidrocarburos sobre los mismos (Palafox y col., 2012).
El alimento que se utilizó para su mantenimiento, etapa de adaptación y crecimiento por espacio de una semana previo al bioensayo, fue estiércol vacuno. Esta adaptación incluyó condiciones controladas de temperatura +/-220C y humedad del 55%. Para verificar que el estiércol vacuno colectado, se realizó la prueba de la caja. Esta prueba consiste en la selección de 10 lombrices las cuales se introducen en un recipiente con el alimento (estiércol) durante 24 horas. Al día siguiente se cuentan las lombrices y para una supervivencia del 100% se considera adecuado el alimento.
2.2.1. Preparación del bioensayo
Se preparan tres réplicas para cada experimento y el control. Para cada experimento se pesan 250 g de suelo y se depositan en recipientes de vidrio, a los que se añaden 10 lombrices adultas con presencia de clitelo (abultamiento en el cuerpo que constituye la estructura reproductiva). Se incuban por 14 días a 24 ± 2ºC con 8 horas de luz y 16 horas de oscuridad. Las lombrices durante el experimento no se alimentan y se aseguran condiciones de humedad del suelo en un 45% aproximadamente.
2.3 Determinación de la CL50 y criterio de toxicidad
Para determinar el nivel de toxicidad en ambos bioensayos se utiliza un gráfico de dosis-efecto, a partir de los porcentajes de mortalidad y/o no germinación de las concentraciones de la muestra de prueba. De la ecuación de la recta para cada curva obtenida, se calcula la concentración que causa la mortalidad y/o no germinación del 50% de la población (CL50). La toxicidad puede ser expresada como toxicidad aguda o letal, la cual se estima a través de la concentración a la cual se produce más del 50% de inhibición de la germinación y/o mortalidad, debido al efecto tóxico en la muestra que se
esté evaluando (Infante y Morales, 2012). Se establece toxicidad para los suelos a evaluar, cuando el valor de la CL50 esté por debajo del 50% de concentración evaluada para un 100% del bioindicador en las muestras control.
3.1 Resultados de los bioensayos con semillas de lechuga en papel de filtro
Los resultados obtenidos del porcentaje de no germinación, para los bioensayos con semillas en papel de filtro se reflejan desde la Fig. 3, Fig. 4, Fig. 5 hasta la Fig. 6. En los controles hubo una germinación del 100% del bioindicador, por lo que se consideran válidos todos los bioensayos. La Fig. 3 muestra el comportamiento del porcentaje de no germinación del bioindicador de los bioensayos 1 y 2, correspondientes a los suelos tratados por el proceso de biorremediación mejorada No.1 y 2, respectivamente.
Se puede constatar que al 100% de concentración evaluada, existe una no germinación del 42% y 44% respectivamente. Esto indica que no existe toxicidad por parte de estos suelos.
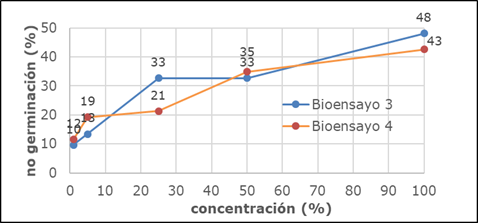
Los resultados correspondientes al bioensayo 3 y 4 (Fig. 4), refieren no toxicidad por parte de los suelos tratados por el proceso EQB No. 1 y 2, al presentarse solo un 48% y 43% de no germinación del bioindicador al 100% de la concentración evaluada.
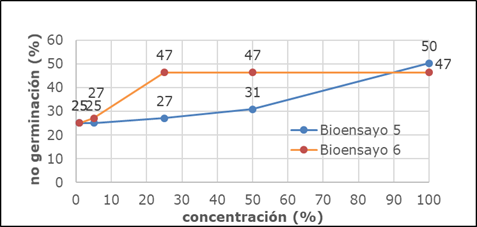
El bioensayo 5 y 6 (Fig. 5), mostraron no toxicidad de los suelos tratados por el proceso de EQB No. 3 y 4, al solo presentarse un 50% y 47% de no germinación del bioindicador al 100% de la concentración evaluada.
La contaminación aún presente en los suelos tratados correspondientes a los bioensayos 1-6 no constituyó un riesgo para el ecosistema terrestre.
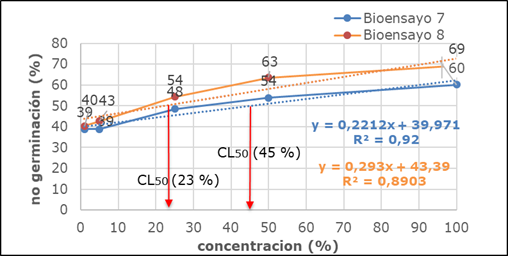
En la Fig. 6 se observan los resultados correspondientes a los bioensayos 7 y 8, de los suelos tratados por el proceso de biorremediación por bioaumentación No. 1 y 2, respectivamente. Al calcular la CL50, se obtiene que: para el bioensayo 7 a una concentración de 45%, existe una no germinación del 50% de las semillas sembradas, lo que demuestra toxicidad del suelo tratado por el proceso de biorremediación por bioaumentación No.1.
Para el bioensayo 8, a 23% de concentración, existe una no germinación de la mitad de la población de las semillas sembradas, siendo superior el nivel de toxicidad de este suelo tratado en el proceso de biorremediación por bioaumentación No.2 en comparación con la bioaumentación No.1. No obstante ambos suelos tratados representan un riesgo para el ecosistema terrestre.
3.2 Resultados de los bioensayos con lombriz de tierra Ensenia Andrei
Se logró la supervivencia y adaptación de las lombrices adultas colectadas. Fue satisfactoria la prueba de caja inicial, al comprobar que todas las lombrices se alimentaron y se mantuvieron con vitalidad. De ahí que el estiércol vacuno resultó ser un alimento adecuado. De la Fig. 7 a la 10 se reflejan los resultados obtenidos del porcentaje de mortalidad para los bioensayos con la lombriz de tierra Ensenia Andrei. En los controles no hubo mortalidad por lo que se considera válido el experimento (Acosta y Romero, 2015).
En la Fig. 7 se reflejan los resultados de los bioensayos 1 y 2. Al calcular la CL50, se obtuvo que, coincidentemente para ambos bioensayos a 26% mueren la mitad de las lombrices expuestas. Este resultado indicó la toxicidad que representan estos suelos.
En la Fig. 8 se reflejan los resultados de los bioensayos 3 y 4. Al calcular la CL50, se obtiene que: para el bioensayo 3 a 55% mueren la mitad de los organismos. Se revela que no existe toxicidad del suelo tratado por el proceso de EQB No.1 y se considera no representa un riesgo para el ecosistema terrestre. Para el bioensayo 4 a 43% de concentración mueren la mitad de la población de los organismos expuestos. Este resultado es un indicador de la toxicidad que presenta el suelo tratado por el proceso de EQB No. 2.
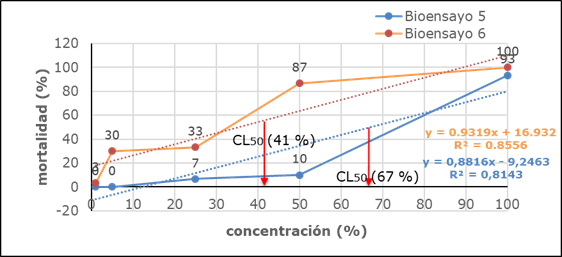
En la Fig. 9 se obtienen los resultados asociados a los bioensayos 5 y 6.
En el bioensayo 5 la CL50 demuestra que a un 67% de concentración mueren la mitad de los organismos expuestos. Esto indica no toxicidad del suelo tratado por el proceso de EQB No. 3. Para el bioensayo 6 la CL50 fue de un 41% por lo que el proceso de EQB No. 4, aún presenta contaminación que resultó ser tóxica.
En la Fig. 10 se observa que para el bioensayo 7 a 55% de concentración mueren la mitad de los organismos expuestos. Esto indica no toxicidad del suelo tratado por el proceso de biorremediación por bioaumentación No.1. Del bioensayo 8 según la CL50 de 43%, se constató toxicidad del suelo tratado por el proceso de biorremediación por bioaumentación No. 2.
Los suelos tratados correspondientes a los bioensayos 1, 2, 4, 6 y 8 constituyen un riesgo para el ecosistema terrestre.
Desde el punto de vista de criterios de remediación de suelos, indiscutiblemente la determinación de la toxicidad es fundamental (Infante y Morales, 2012). Los resultados obtenidos con ambos bioindicadores confirman lo que plantearon Infante y Morales, (2012) sobre la falta de correlación entre la concentración de hidrocarburos en suelos y la toxicidad; ya que una menor o mayor concentración de hidrocarburos no es indicativa de una menor o mayor toxicidad. En la evaluación realizada, los suelos tratados por la EQB con agromena 2 y 4 reportan toxicidad, sin embargo, las concentraciones reportadas de G y A e HCT no difieren en gran medida de las obtenidas para la EQB 1 y 3 con producto. Ambos procesos tuvieron como única diferencia la fertilización aplicada, que en el caso de la agromena pudiera tener un efecto desfavorable en la calidad del suelo por altos aportes de fósforo. En este sentido se informa que el fósforo es poco móvil cuando se produce una alta asimilación de fósforo soluble en un suelo donde no se produce percolación (Fernández, 2011), como en este caso donde la experimentación se realizó en microcosmos. También es conocido que como consecuencia de la biodegradación se forman compuestos carboxílicos más polares y solubles que los hace más biodisponibles que los hidrocarburos originales, por lo que tipo de contaminante y factores ambientales incidirán en la toxicidad durante la evolución de un proceso de biorremediación (Tarache, 2011).
Para ambos tratamientos por bioaumentación se determinó el carácter tóxico que presentaron casi todos los experimentos, atribuible a una menor efectividad del proceso aplicado, cuando persiste contaminación en los mismos. Igual comportamiento mostró la biorremediación mejorada por el efecto letal alcanzado del impacto directo de la contaminación sobre organismos.
CONCLUSIONES
La evaluación eco-toxicológica realizada a los suelos tratados por bioaumentación No. 1 y 2, biorremediación mejorada No.1 y 2 y estabilización químico-biológica No. 2 y 4, evidenció el carácter tóxico que presentan los mismos y el consecuente riesgo para el ecosistema terrestre.
No son tóxicos los suelos tratados por estabilización químico-biológica con producto, sin existir riesgo por su disposición en el medio ambiente.