INTRODUCCIÓN
La Moringa oleífera es un árbol originario del sur del Himalaya que tolera una amplia diversidad de condiciones climáticas y de suelos. Crece principalmente en zonas semi áridas tropicales y subzonas tropicales (Ferrer y col., 2014).
Debido a su alta rentabilidad, productividad y versatilidad frente a las condiciones ambientales para su plantación, autores como González y Francisco, (2018) y Ramírez (2017), mencionan la siembra del cultivo principalmente en regiones tropicales con fines ornamentales, agroforestales y alimenticios para las personas y el ganado.
Sus semillas poseen propiedades oleaginosas permitiendo la extracción de aceite para usos comestibles o industriales. Por su porcentaje en contenido de aceite entre el 30 - 45 % (Gómez y col., 2016), frente al 38 - 44 % de colza, 35 - 42 % de girasol y 10 - 30 % de oliva, ha sido estudiado para usarse en productos cosméticos, alimenticios, Lozano (2018) y para la producción de biodiesel (Rashid et al., 2008).
1.1 Aceites Vegetales
En general todas las semillas y frutos contienen aceite, pero solo las oleaginosas sirven para la producción industrial de aceite. Los aceites vegetales más abundantes en una región se convierten en una fuente de materia prima importante para su aprovechamiento. Una medida de sostenibilidad es evitar su utilización en la producción de biocombustibles afectando la disponibilidad de alimentos, de ahí la importancia de estudios para la producción de biodiesel a partir de aceites no convencionales como el caso del aceite de la Moringa oleífera,Lozano (2018).
1.2 Procesos de extracción de aceites a partir de semillas oleaginosas
A nivel analítico se emplean diversas técnicas, siendo la más usada tradicionalmente la extracción en Soxhlet. Los solventes más empleados son: etanol, metanol, isopropanol, hexano, ciclohexano, tolueno, xileno, éter etílico, éter isopropílico, acetato de etilo, acetona (García y col., 2013). Extracciones con hexano, etanol, agua, han sido realizadas por Penabaz (2016), Águila (2013), (Gómez y col., 2016), a ecotipos de origen cubano con rendimientos entre 30-45%.
1.3 Aceites vegetales como biocombustibles
El aceite vegetal ha sido considerado como un posible combustible para las maquinarias. Su uso podría remontarse a 1893, cuando Rudolf Diesel, inventor del motor que lleva su nombre, corrió su primer modelo en Alemania utilizando aceite de cacahuate como combustible. El uso del aceite vegetal continuó hasta 1920, antes de que el diesel fósil desplazara del mercado a los aceites vegetales. Años más tarde, en 1937 se propuso por primera vez el uso del término “biodiesel”, refiere Saval (2012).
El biodiesel es un biocombustible líquido que se obtiene mediante procesos industriales de esterificación y transesterificación y que se aplica en la preparación de sustitutos totales o parciales del combustible diesel o gasóleo obtenido del petróleo (Mofijur et al., 2015), (Kafuku y Mbarawa, 2010), (Rondón y col., 2017).
Por tanto, el objetivo del trabajo es determinar si las propiedades físico-químicas del aceite de semillas de Moringa oleífera ecotipo Supergenius cumplen con los requisitos que evidencien sus potencialidades energéticas.
MATERIALES Y MÉTODOS
El ecotipo de Moringa oleífera utilizada es Supergenius. procedente del Centro Internacional de Salud La Pradera, Playa, La Habana, Cuba. La metodología investigativa comienza con el secado de las semillas, tal como lo realizó Águila (2013), un estudio granulométrico y luego una extracción sólido - líquido con Soxhlet para obtener el aceite de las semillas. Los disolventes utilizados son: cloroformo y mezcla cloroformo-metanol 1:1. Se plantea un diseño 22 para conocer el comportamiento que tiene el contenido de aceite en las semillas con estos disolventes. Se determinan las propiedades que caracterizan al aceite utilizando métodos físico-químicos de análisis. La determinación de la composición del aceite extraído se realiza utilizando un cromatógrafo de gases 7890A (Agilent, E.E.U.U.), con detector de ionización por llama y una columna capilar BPX-70 (30 m x 0,53 mm, 1 µm Df, SGE, Australia, (Institute for Nutraceutical Advancement). Los análisis se realizaron por triplicado. Los patrones de AG (Sigma, EE.UU.), demás reactivos y disolventes (Merck, Alemania) fueron puros para análisis. Se identificaron los ésteres metílicos de los ácidos grasos para la muestra de ensayo por comparación de los tiempos de retención de cada componente con los tiempos de los ésteres metílicos patrones obtenidos en el mercado.
2.1 Preparación de las semillas de Moringa oleífera ecotipo Supergenius
La semilla se prepara separando primero las cáscaras de los cotiledones ejerciendo presión con las manos sobre las semillas. Se disminuye el tamaño de partícula de los cotiledones hasta valores cercanos a 1·10-3 m según reportes hechos por (Abdulkareem et al., 2011). El tamizado se realiza según la Norma Cubana Minerales-Análisis granulométrico por tamizado (NC 631, 2008). Para la operación se toman muestras representativas de 14 g de semillas trituradas, las cuales deben ser secadas a 105°C durante 24 h en una estufa modelo DHG-9146ª. El juego de tamices que se utiliza pertenece a la escala americana ASTM y sus diámetros (entre 0,125·10-3 y 2·10-3 m) se seleccionan de acuerdo a lo reportado por (Rosabal y Garcell, 2006). Luego de disminuir el tamaño de partículas, las semillas son sometidas a un proceso de secado en una estufa, modelo DHG - 9146A. La determinación de humedad se efectúa por diferencia de pesadas, utilizando una balanza analítica, modelo SARTORIUS BS 124S. La temperatura para el secado se fija por debajo de 60°C para evitar la desnaturalización de las proteínas de las semillas. Se pesa una masa de 10 gramos utilizando una balanza analítica, modelo SARTORIUS BS 124S y se introduce en el Soxhlet. El disolvente se adiciona teniendo en cuenta las relaciones soluto - disolvente 1:6 que se define para la investigación según Águila (2013).
2.2 Diseño de experimento
Para el diseño de experimento se trabaja con el programa estadístico Statgraphics versión 5.1. Este se lleva a cabo teniendo en cuenta 2 variables a 2 niveles con dos réplicas. La primera variable es el tiempo de extracción y la segunda el tipo de solvente empleado al hacer las extracciones manteniendo constante la relación soluto - disolvente en peso-volumen 1:6. Se determinó el contenido de aceite en la extracción como variable dependiente y se realizaron 4 corridas experimentales con dos réplicas para realizar 12 corridas en total.
Variable1: tiempo de extracción (horas). Niveles: 4 y 6 según Águila, (2013).
Variable 2: tipo de solvente. Niveles: cloroformo y mezcla cloroformo-metanol 1:1 según (Lalas y Tsaknis, 2002).
2.3 Caracterización físico-química de los aceites
Existen varios índices que se utilizan para la caracterización físico-química de los aceites Águila, (2013), Penabaz (2016). Entre ellos están: índice de refracción, índice de saponificación, índice de acidez, índice de iodo, índice de peróxido, densidad. La determinación de la composición del aceite extraído se realiza utilizando un cromatógrafo de gases acoplado a un espectrómetro de masas, Águila (2013).
RESULTADOS Y DISCUSIÓN
3.1 Resultados del análisis granulométrico en las semillas
En los análisis granulométricos existe una distribución variada de tamaños de partículas, encontrándose gran parte de la masa en los tamices de mayor abertura. El 76 % de la muestra de semillas trituradas se concentra entre los tamices de mayor abertura (entre 2,0·10-3 y 1,0·10-3 m). Además (Abdulkareem et al., 2011) plantean que a tamaños de partículas menores se incrementa el área de contacto entre el disolvente y el sólido, lo que permite aumentar la velocidad de transferencia del aceite y la tasa de extracción recomendando un intervalo de tamaño pequeño (entre 0,7·10-3 y 0,5·10-3 m) para que cada partícula requiera aproximadamente el mismo tiempo de extracción.
3.2 Resultado del diseño de experimentos 22 realizado a las semillas secas de Moringa ecotipo Supergenius
Los valores del contenido de aceite se muestran en la Tabla 1.
Tabla 1 Porcentaje másico de aceite extraído a partir de semillas secas empleando cloroformo, cloroformo-metanol 1:1
|
|
|
|
|
||
|---|---|---|---|---|---|
| 1 | Cloroformo | 6 | 10,2866 | 3,3610 | 32,67 |
| 2 | Mezcla | 6 | 10,2251 | 3,9551 | 38,68 |
| 3 | Mezcla | 4 | 10,2063 | 3,7896 | 37,13 |
| 4 | Cloroformo | 4 | 10,2198 | 3,1641 | 30,96 |
| 5 | Cloroformo | 6 | 10,2635 | 3,4526 | 33,64 |
| 6 | Mezcla | 4 | 10,2158 | 3,7267 | 36,48 |
| 7 | Cloroformo | 4 | 10,2172 | 2,9998 | 29,36 |
| 8 | Mezcla | 6 | 10,2318 | 3,6661 | 35,83 |
| 9 | Cloroformo | 4 | 10,2231 | 3,1569 | 30,88 |
| 10 | Cloroformo | 6 | 10,2249 | 3,2219 | 31,51 |
| 11 | Mezcla | 6 | 10,1261 | 3,7510 | 37,04 |
| 12 | Mezcla | 4 | 10,2318 | 3,6302 | 35,48 |
Como puede observarse en la Tabla 1, los contenidos de aceite extraídos expresados en % resultan mayoritarios cuando se emplean las mezclas de cloroformo- metanol 1:1, tanto cuando se realiza la extracción a cuatro como a seis horas, y no se aprecia una marcada influencia del tiempo de extracción.
En la Tabla 2 se presenta la matriz ortogonal y en la número 3 (Tabla 3) el análisis de varianza.
Tabla 2 Matriz ortogonal completa
| 1 | 1 | -1 | 1 | 32,67 |
| 2 | 1 | 1 | 1 | 38,68 |
| 3 | 1 | 1 | -1 | 37,13 |
| 4 | 1 | -1 | -1 | 30,96 |
| 5 | 2 | -1 | 1 | 33,64 |
| 6 | 2 | 1 | -1 | 36,48 |
| 7 | 2 | -1 | -1 | 29,36 |
| 8 | 2 | 1 | 1 | 35,83 |
| 9 | 3 | -1 | -1 | 30,80 |
| 10 | 3 | -1 | 1 | 31,51 |
| 11 | 3 | 1 | 1 | 37,04 |
| 12 | 3 | 1 | -1 | 35,48 |
Tabla 3 Análisis de varianza para contenido de aceite
| A: solvente tipo | 83,3187 | 1 | 83,3187 | 80,26 | 0,0001 |
| B: tiempo | 6,87053 | 1 | 6,87053 | 6,62 | 0,0422 |
| AB | 1,44213 | 1 | 1,44213 | 1,39 | 0,2832 |
| bloques | 3,14482 | 2 | 1,57241 | 1,51 | 0,2934 |
| Error Total | 6,22898 | 6 | 1,03816 | - | - |
| Total (corr.) | 101,005 | 11 | - | - | - |
R2- 93,833 %
R2- (ajustado para g.l.)- 91,5204 %
Error Estándar de Est. - 1,0189
Error absoluto de la media -0,625
Estadígrafo Durbin-Watson - 2,38466 (P=0,0875)
Autocorrelación residual lag 1- 0,245041
El diseño experimental y su procesamiento permitieron la obtención de un modelo que explica el comportamiento del contenido de aceite en las semillas, teniendo en cuenta las condiciones experimentales estudiadas. El modelo que se obtiene se representa por la Ecuación 1:
Ca: contenido de aceite extraído en porcentaje, td: tipo de disolvente, ts: tiempo en horas que dura la extracción y td . ts: interacción entre ambos factores.
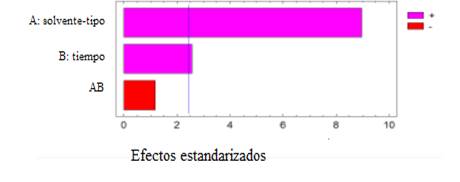
Solo el tipo de disolvente y el tiempo de extracción tienen un valor-P menor que 0,05, indicando que es significativamente diferente de cero para un nivel de confianza del 95%. Ambos factores para los niveles establecidos en el estudio inciden en la variable respuesta. El diagrama de Pareto concuerda con dicho comportamiento. Figura 1
El modelo que se obtiene excluye la interacción de los factores y se representa por la Ecuación 2:
A partir del análisis de varianza para la variable respuesta contenido de aceite se obtiene el valor del coeficiente de Durbin - Watson. Este valor indica si existe independencia de los errores pues es uno de los requerimientos necesarios para la aplicación del método de los mínimos cuadrados. El valor que se desea es en el entorno de 2 y esto ocurre cuando la probabilidad es mayor que 0,05. En el diseño tiene un valor de 2,38466 asociado a una probabilidad de P = 0,0875. No existe correlación alguna en los errores o lo que es equivalente, hay independencia entre los mismos. El modelo obtenido explica la variabilidad del porcentaje del contenido de aceite para las condiciones del estudio.
3.3 Análisis de la caracterización físico-química del aceite
Para la caracterización del aceite se utilizó la muestra obtenida mediante la extracción con la mezcla cloroformo-metanol 1:1, que fue la alternativa donde el porcentaje de extracción de aceite alcanzó su mayor valor. Los resultados se muestran en la Tabla 4.
Tabla 4 Caracterización del aceite de semillas de Moringa oleífera ecotipo Supergenius
|
|
||||
|---|---|---|---|---|
|
|
|
|||
| Contenido de aceite (%) | 40,39 | 34,8 | 38,68 | 41,4 |
| Índice de refracción | 1,4608 | 1,4571 | 1,4651 | 1,4590 |
| Índice de saponificación g KOH/g aceite | 186,67 | 181,4 | 180,90 | 186,32 |
| Índice de Iodo g I2/100g aceite | 69,45 | 68,63 | 65,88 | 65,46 |
| Índice de peróxidos meqg de O2/kg aceite | 1,58 | 1,27 | 1,60 | - |
| Índice de acidez | 0,59 | 1,20 | 1,36 | 1,39 |
| Densidad (g/cm3) | 0,9057 | 0,9032 | 0,9100 | 0,9110 |
| pH | 5,54 | - | 6,0 | 6,0 |
** Lalas y Tsaknis (2002), *(Anwar y Bhanger, 2003), (Anwar y Rashid, 2007)
Los valores obtenidos son similares para la muestra en estudio y los de (Lalas y Tsaknis, 2002), (Anwar y Bhanger, 2003), (Anwar y Rashid, 2007) donde en contenido de aceite hay un intervalo entre 34-41,4 %, similar al planteado por (Falasca y Bernabé, 2009) con valores de 31-47 % de aceite. Para ecotipos cubanos se han obtenido porcentajes entre 30 y 47 %, obtenidos por Águila (2013) y Penabaz (2016). Las diferencias pueden ser debidas a la influencia de medio geográfico, condiciones climáticas, tiempo de almacenamiento, métodos de extracción.
3.4 Resultados de la cromatografía gaseosa
Para conocer la composición de los ácidos grasos del aceite de semillas de Moringa oleífera cubana ecotipo Supergenius se realiza una cromatografía gaseosa acoplada a espectrometría de masa. Se muestra un comportamiento similar a los reportados en la literatura al obtener la señal correspondiente al ácido oleico con un 67,61% comparable con el aceite de oliva y aceites obtenidos de semillas de otras variedades de Moringa oleífera, (Anwar y Rashid, 2007), Penabaz (2016).
El mayor porcentaje corresponde al ácido oleico, monoinsaturado, luego a los ácidos saturados y al éster etílico del ácido linoleico que es diinsaturado, esto se corresponde con los estudios de (Lalas y Tsaknis, 2002), (Anwar y Rashid, 2007) que encontraron que el aceite contiene niveles altos de ácidos grasos insaturados, el oleico (67-75%) fundamentalmente. Los ácidos saturados predominantes fueron el palmítico, el margárico y el behénico que muestra un contenido menor que lo encontrado en la literatura (Anwar y Rashid, 2007). La causa de tal comportamiento pudiera estar asociada a la ocurrencia de reacciones de hidrólisis o transesterificación del aceite en presencia del alcohol durante el proceso de extracción según plantea (Efeovbokhan et al., 2015) o problemas de edad de la planta, zona geográfica, (Anwar y Rashid, 2007), tiempo de almacenamiento de las semillas. Los resultados se muestran en la Tabla 5.
En los últimos tiempos se ha reportado el potencial de la Moringa oleífera para la producción de biodiesel (Mofijur et al., 2014). Existen estudios donde se obtiene biodiesel a partir de aceite de semillas de Moringa oleífera realizados por (Rashid et al., 2008), (Kafufu y Mbarawa, 2010) y (Kivevele et al., 2011) con índices de acidez de 2,9 mg KOH/g de aceite, 1,194 mg KOH/g de aceite y 5 % de índice de acidez, requiriendo pretratamiento para disminuir el índice de acidez en el primer y tercer caso respectivamente. Para que se realice la reacción completa se necesita un porcentaje de ácidos grasos libres, menor al 3 %, según Pedroso (2016); en los tres casos el ácido graso mayoritario es el oleico. El número de cetano (NC) es uno de los indicadores más comúnmente citado de la calidad del diesel. El NC del biodiesel de Moringa oleífera tiene un valor elevado porque se obtiene a partir de un aceite donde predomina un ácido graso insaturado. A partir de la composición de ácidos grasos que posee el portador energético, el número de cetano se encuentra entre 63-67 según apuntan (Kafuku y Mbarawa, 2010), (Kivevele et al., 2011), Pedroso (2016). Esta propiedad ejerce una gran influencia en la calidad de encendido y el rendimiento de un motor diésel (Rashid et al., 2008).
Tabla 5 Resultados de la cromatografía gaseosa
| Ácido oleico | 67,61 | 32,447 |
| Ácido palmítico | 8,98 | 32,347 |
| Linoleato de etilo | 7,23 | 35,787 |
| n-octano + xileno | 5,67 | 4,56 |
| Heptadecanoato de etilo | 2,59 | 36,213 |
| Hexadecanoato de etilo | 1,84 | 31,92 |
| Docosanoato de etilo | 1,84 | 43,33 |
| Ácido eicosanoico | 1,25 | 39,76 |
| Otros | 1,1 | 10,133 |
Se conoce que mientras menor sea el grado de insaturación de un aceite mayor será el NC del biocombustible. Para un aceite transesterificado como el biodiesel, la viscosidad tiene un orden de magnitud más bajo que la del aceite del que fue hecho. La alta viscosidad del aceite explica por qué han sido abandonados como alternativa de diesel. La densidad, viscosidad y el número ácido de los ésteres metílicos de Moringa oleífera ecotipo Criolla cumplen con lo establecido en las normas de los estándares internacionales de calidad para biodiesel, (Díaz y col., 2014), Pedroso (2016). Si se comparan las propiedades físico-químicas del aceite de Moringa oleífera ecotipos Criolla y Supergenius se observa que tienen valores similares, como se exponen en la Tabla 6.
Tabla 6 Propiedades físico-químicas de los ecotipos Criolla y Supergenius
| Supergenius | 1,4623 | 177,47 | 65,58 | 1,58 | 1,40 | 0,9030 | 1,05 |
| Criolla | 1,4600 | 170,8 | 63,0 | 3,15 | 1,41 | 0,9029 | 1,06 |
Índices (IR: Refracción; IS: Saponificación mg KOH/g de aceite; IY: Iodo g de I2/100g de aceite; IP: Peróxidos meq de O2/kg de aceite; IA: Acidez), D: densidad g/cm, GA: grado de acidez; expresado como % ácido oleico.
Las propiedades de los ésteres metílicos del aceite de Moringa oleífera ecotipo Criolla obtenidos durante el estudio realizado por Pedroso (2016) fueron: densidad 0,8650 mg/L, viscosidad dinámica 4,39 mPa*s, viscosidad cinemática 5,07 mm2/s, índice de acidez 0,67 mg de NaOH/g de aceite y un grado de acidez como % de ácido oleico de 0,45. Por tanto, puede suponerse que el aceite de Moringa oleífera ecotipo Supergenius tiene potencialidad para ser evaluado con fines energéticos.
CONCLUSIONES
1) El proceso de extracción aplicado a las semillas de la Moringa oleífera estudiado alcanza de 30 a 39 % en contenido de aceite utilizando el Soxhlet para la extracción.
2) Del diseño factorial 22 se evidencia que el tipo de disolvente y el tiempo de extracción tienen influencia estadística significativa sobre el contenido de aceite extraído para un 95 % de nivel de confianza.
3) El cloroformo y la mezcla cloroformo-metanol son disolventes posibles a utilizar en la extracción del aceite de semillas de Moringa oleífera ecotipo Supergenius cubana.
4) Al analizar los resultados de las propiedades físico-químicas del aceite obtenido utilizando cloroformo-metanol 1:1 se puede asegurar que el aceite tiene potencialidad para ser evaluado con fines energéticos.