INTRODUCCIÓN
La mastitis bovina es una enfermedad compleja y multifactorial, dada por la inflamación del parénquima de las glándulas mamarias y los cambios patológicos que induce en sus tejidos, además de modificaciones biológicas, físicas y químicas en la leche, que ocasionan cambios en su composición y afectación a gran variedad de productos lácteos, además de reducir la producción de leche (Barreiro et al. 2017). Se reconoce como la enfermedad más común y costosa de la lechería a escala global y una de las principales causas de perjuicios a la eficiencia biológica y la fertilidad del ganado de leche (Dalanezi et al., 2020; Fernandes et al., 2021; Singh et al., 2023).
La mastitis también constituye un problema de salud pública, por los riesgos de transmisión a través de la leche de microorganismos zoonóticos y de patógenos con resistencia a los cantimicrobianos, debido a su amplio y/o indebido uso para el control de la enfermedad (Paramasivam et al., 2023).
Entre los patógenos causantes de mastitis se incluyen Staphylococcus aureus, Streptococcus agalactiae, Actinomyces pyogenes, Streptococcus dysgalactiae, Corynebacterium bovis, enterobacterias como Escherichia coli, Klebsiella spp. y Enterobacter spp. y Mycoplasma spp., entre otros (Cameron et al., 2017).
La preocupación por el carácter emergente de Mycoplasma bovis por el aumento de países que reportan su presencia en los últimos años (Citti y Blanchard, 2013; Ruegg, 2017) y el diagnóstico de Mollicutes en leche de tanque de rebaños bovinos (25,8%, 37/143) en la provincia Zamora-Chinchipe, Ecuador, aunque no se confirmó M. bovis (Ramírez et al., 2017), destaca la importancia de profundizar en la etiología bacteriana asociada con vistas al control de la enfermedad en sus rebaños.
MATERIALES Y MÉTODOS
Durante 2015 y 2016 se muestrearon 247 vacas en ordeño de rebaños bovinos lecheros en la provincia Zamora-Chinchipe, seleccionados en los conglomerados definidos en el territorio según sus características ecológicas (Saa et al., 2012).
Prueba de California para mastitis
Luego del despunte del pezón se depositó un pool de 2 ml de leche de todos los cuartos en los pocillos de la paleta indicada para esta prueba, a los que se agregó igual volumen del reactivo para la Prueba California para Mastitis (CMT, de sus siglas en inglés, Lauril sulfato de sodio al 4% Diagnóstico Mastitis Nocar, Medick). Se homogenizó la muestra con movimientos circulares por un tiempo aproximado de 10 a 20 segundos, e inmediatamente se interpretaron los resultados de acuerdo al grado de gelificación observado en la mezcla (Blowey y Edmonson, 2010).
Diagnóstico microbiológico
Después de descartar los primeros chorros de leche de cada pezón, se colectó en tubos estériles un pool de 10mL de leche proveniente de todos los cuartos, previa su limpieza exhaustiva y desinfección con etanol al 70 % (NMC, 2014).
Todas las muestras de leche se refrigeraron (2-8oC) para su traslado al Laboratorio de Sanidad Animal y Zoonosis, de la Universidad Técnica Particular de Loja, donde se conservaron a 4ºC para posteriores análisis microbiológicos.
Diagnóstico de Mycoplasma spp. en muestras de leche
La detección de Mycoplasma spp. se realizó mediante la Reacción en Cadena de la Polimerasa (PCR), en MYCOLAB (Laboratorio Acreditado por la ISO/IEC: 17025, y de Referencia de la Organización Mundial de Salud Animal (OMSA) para el diagnóstico de Mycoplasmas, del Centro Nacional de Sanidad Agropecuaria (CENSA), Cuba.
Para la detección de Mollicutes por PCR se utilizó la pareja de cebadores MGSO y GPO-1, que amplifican un fragmento de 270 pb correspondiente a la región conservada del ARN ribosomal 16S (ARNr 16S) (Van Kuppeveld et al., 1998). Los cebadores se sintetizaron en el Centro de Ingeniería Genética y Biotecnología (CIGB), La Habana, Cuba. Como control positivo se utilizó ADN de Mycoplasma arginini.
Extracción de ADN a partir de muestras de leche
La muestra de leche se centrifugó (3000 rpm por 10 minutos) y el sobrenadante se decantó. Posteriormente se tomaron 50uL del sedimento y se le adicionó 200 µL de buffer de ruptura (Tris HCl, 0,1M, pH 8,5, Tween 20, 0,05% y proteinasa K 0,24mg/mL). La mezcla se incubó durante 1 hora a 60 ºC y luego de ese periodo se incubó a 95ºC durante 15 minutos con el objetivo de lograr la desnaturalización del ADN (Rossetti et al., 2010).
Preparación de la mezcla, condiciones de corrida y visualización de los productos de PCR
La preparación de la mezcla para la amplificación se realizó en un volumen final de 25 μL. Esta mezcla se compuso de 5 µL del ADN de la muestra, 1,5µL de cada cebador (20 pmoles) y 17 μL de Master mix (Promega). Las reacciones se desarrollaron en un equipo Termociclador de ADN REACTOR ThermoHyBaidTM, con el empleo del programa de amplificación específico para cada cebador, según lo descrito por los autores antes mencionados.
Los productos se aplicaron en gel de agarosa al 2 % (v/v). Se utilizó un marcador de peso molecular de 100 pb (Promega, Madison, EE.UU.). El gel se tiñó con Bromuro de Etidio (0,5 μg/mL) durante 15 minutos y los resultados se visualizaron en un transiluminador de luz ultravioleta.
Diagnóstico bacteriológico
La identificación bacteriana en las muestras se realizó mediante la siembra de 15μL de leche y por agotamiento en placas Petri, las que se prepararon previamente con agar MacConkey, Salt Mannitol y Agar Sangre (Becton Dickinson-Difco BBLTM), y Agar chocolate. Todas se incubaron de 24 a 48 horas a 37°C (NMC, 2014).
Además, se realizaron las pruebas de hidrólisis de esculina, hipurato e inulina y crecimiento en cloruro de sodio (NaCl). A los aislados que mostraron bacilos Gram negativos en la tinción de Gram se les realizó la prueba preliminar de lectura inmediata Oxidasa y también se incluyeron las pruebas indol, triple azúcar, urea y citrato (Fernández et al., 2010).
Análisis estadístico
Mediante comparación de proporciones (Castillo y Miranda, 2014) se analizaron los resultados del diagnóstico de Mollicutes y CMT en vacas por cantones y las frecuencias de los diferentes patógenos identificados en las vacas positivas a Mollicutes. A través de Chi Cuadrado se evaluó la relación entre los resultados del diagnóstico de Mollicutes y CMT, así como con los patógenos identificados en el estudio bacteriológico. También mediante regresión logística se comparó la Razón de Prevalencia (RP) de cada patógeno identificado por bacteriología (Corp I, 2012).
RESULTADOS Y DISCUSIÓN
En la investigación a 247 muestras de leche de vacas, resultaron positivas a CMT 201 vacas (81.4%), lo que demuestra la elevada frecuencia de mastitis subclínica (MSC) en los rebaños lecheros de la provincia. También se constató un 33.2% (82/247) de vacas positivas a Mollicutes (Tabla 1).
En Paquisha y Yacuambí no se detectaron vacas positivas a Mollicutes, pero sí a CMT, aunque en ambos cantones se investigó un número inferior de animales con respecto al resto de los cantones ante la reticencia de los productores.
En Sao Paulo se encontró un 16.4% (11/67) de rebaños positivos a Mollicutes; solo uno fue positivo a M. bovis (Manzi et al., 2018), pero se supone la participación de otras especies de micoplasmas que pueden causar mastitis. Si bien M. bovis se considera una de las especies más patógenas y la más frecuentemente aislada a partir de neumonías, artritis y mastitis causadas por ese género en el ganado vacuno, existen otras especies, como M. californicum, M. canadense, M. bovigenitalium, M. alkalescens, M. arginini, M. bovirhinis y M. dispar que pueden causar infecciones en bovinos lecheros (Deeney et al., 2021).
En Zamora-Chinchipe tampoco se identificó M. bovis en leche de tanque positivas a Mollicutes, y también se considera la participación de otras especies de micoplasmas (Ramírez et al., 2017).
La no asociación entre los resultados a CMT y Mollicutes mediante Chi Cuadrado (p(0,05), se puede deber a la evidente participación de otros patógenos en la etiología de la mastitis.
Tabla 1 Resultados del diagnóstico de Prueba de California y Mollicutes en vacas de rebaños lecheros en Zamora-Chinchipe, Ecuador
| Cantones | Prueba California | Total | |||||
| ++ | +++ | Total Pos. | Total Neg. | Pos. | Neg. | ||
| C. del Cóndor | 4 (100,0) | 0 | 4 (100,0)a | 0 | 1 (25,0)d | 3 (75,0) | 4 |
| Paquisha | 6 (75,0) | 0 | 6 (75,0)ab | 2 (25,0) | 0 | 8 (100,0) | 8 |
| Nangaritza | 30 (73,2) | 3 (7,3) | 33 (80,5)b | 8 (19,5) | 21 (51,2)b | 20 (48,8) | 41 |
| Zamora | 20 (62,5) | 4 (12,5) | 24 (75,0)b | 8 (25,0) | 11 (34,4)c | 21 (65,6) | 32 |
| Chinchipe | 1 (33,3) | 0 | 1 (33,3)b | 2 (66,7) | 1 (33,3)d | 2 (66,7) | 3 |
| Yacuambi | 3 (60,0) | 1 (20,0) | 4 (80,0)ab | 1 (20,0) | 0 | 5 (100,0) | 5 |
| Yantzatza | 104 (67,5) | 25 (16,2) | 129 (83,8)b | 25 (16,2) | 48 (31,2)a | 106 (68,8) | 154 |
| Total | 168 (68,0) | 33 (13,4) | 201 (81,4) | 46 (18,6) | 82 (33,2) | 165 (66,8) | 247 |
abcd Letras desiguales en las columnas indican diferencias significativas (p< 0,05).
Así, la investigación bacteriológica detectó Streptococcus spp. (27,2%) y Staphylococcus aureus (S. aureus) (22,6%) con las frecuencias mayores y sin diferencia entre ambas. También se observó infección bacteriana simultánea de diversos agentes bacterianos, un indicador de la participación de algunos patógenos secundarios, como coliformes y Proteus spp. que pueden actuar como predisponentes para la colonización posterior de patógenos mayores. Por ejemplo, coliformes se diagnosticó junto a S. aureus en el 10,5% de las vacas (Tabla 2).
Tabla 2 Resultados bacteriológicos en leche de vacas en ordeño de rebaños lecheros en la provincia Zamora-Chinchipe, Ecuador
| Patógenos | Positivos | % |
|---|---|---|
| 67 | 27,1a | |
| 56 | 22,6a | |
| 26 | 10,5b | |
| Staphylococcus Coagulasa Negativo | 24 | 9,7b |
| Staphylococcus Coagulasa Positivo | 9 | 3,7c |
| 7 | 2,8c | |
|
|
6 | 2,4cd |
| Staphylococcus Coagulasa Negativo y Coliformes | 4 | 1,6cd |
| 3 | 1,2cd | |
| 1 | 0,4d | |
| Negativo | 44 | 18 |
| Total | 247 | 100,0 |
Patógenos tales como Staphylococcus, Streptococcus, y coliformes se señalan como los más comunes asociados a mastitis (Ruegg, 2017).
Los resultados obtenidos coinciden en señalar a S. aureus como uno de los patógenos de mayor ocurrencia e importancia en mastitis (Janus et al., 2023; Heikkilä et al., 2018; Kirkeby et al., 2019; Singh et al., 2023; Woudstra et al., 2023). Aquí se coincide sobre la ocurrencia de S. aureus y diferentes especies de Streptococcus como lo más común.
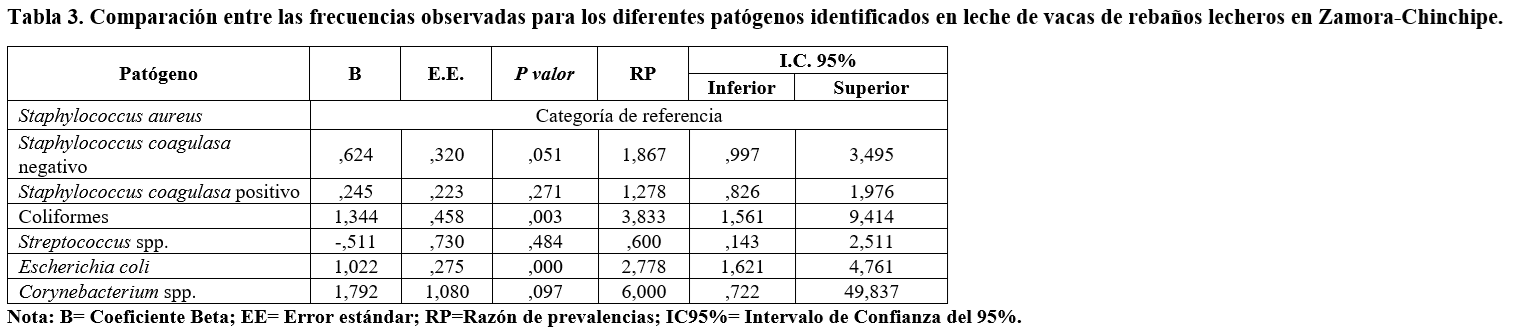
Es importante señalar que la razón de prevalencia (RP) de Staphylococcus coagulasa negativo (SCN) (9,7%) prácticamente no difiere respecto a S. aureus (22,6%) (Tabla 3). El grupo SCN se considera también un emergente mundial de mastitis, y su mayor detección se ha asociado a la disminución de patógenos mayores como Streptococcus agalactiae y S. aureus, aunque no todas las especies del grupo tienen un impacto negativo en el incremento de las células somáticas y la calidad de la leche, ya que otras parece que solo cohabitan la piel de los pezones (Cameron et al., 2017).
En el 2017, un estudio realizado en la provincia El Oro, Ecuador, reveló una prevalencia de 11.6% de mastitis clínica (MC) moderada y 60% de mastitis subclínica (MSC). En los casos de MC se revelaron coliformes (33%), Staphylococcus coagulasa positiva (25,8%), Staphylococcus coagulasa negativa (20,4%), streptococos (9.7%), Bacillus spp. (7.5%) y Klebsiella spp (3.2%). En los casos de MSC, se identificaron staphylococos coagulasa negativa (55.4%), Bacillus spp. (22.1%), streptococos (9.3%), y staphylococos coagulasa positiva (6.1%) (Amer et al., 2018). En contraste, en Zamora-Chinchipe se reveló menor infección por SCN (10%).
Mientras Streptococcus agalactiae (29,8%), Streptococcus pyogenes (11,7%) y Corynebacterium spp. (5,9 %) fueron los patógenos más frecuentes en ganado lechero del norte de Antioquia, Colombia (Ramírez et al., 2018).
No obstante, se entiende que al comparar resultados entre diferentes estudios es necesario tener en cuenta otros muchos factores que influyen en la prevalencia de mastitis, pues el conjunto de los que son propios de cada rebaño probablemente es lo más influyente en la prevalencia de la infección (Dahl et al., 2017), pues la mastitis es una enfermedad multifactorial, vinculada a la triada epidemiológica: animal (huésped), agente etiológico y ambiente (Boas da Silva et al., 2023).
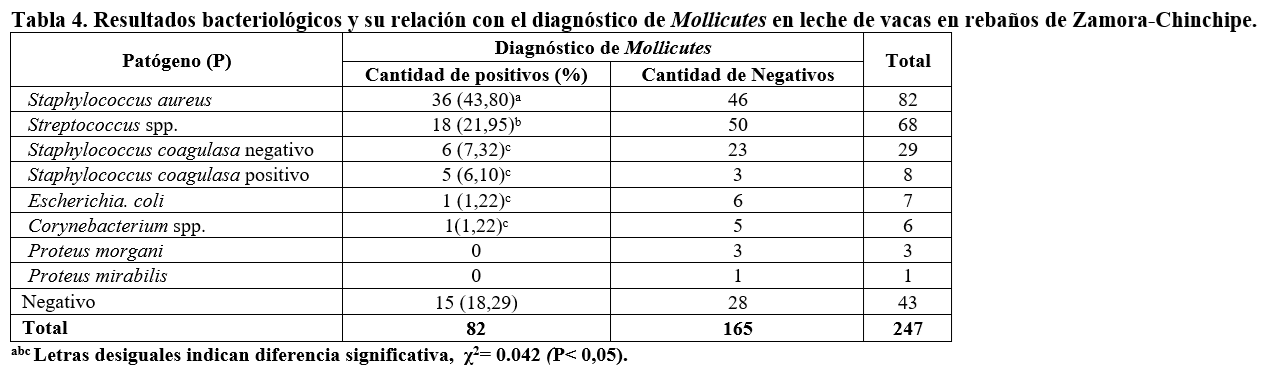
De particular importancia es la relación entre el diagnóstico de Mollicutes y de otros patógenos identificados en los procesos de mastitis (χ2= 0.042). Se comprobó que S. aureus es el patógeno con mayor presencia en coinfección con Mollicutes, seguido por Streptococcus spp., aunque con un margen amplio de diferencia, en tanto el resto de los agentes identificados no difieren entre sí para esa condición (P<0,05) (Tabla 4).
La elevada frecuencia de S. aureus en los cuadros de mastitis no solo constituye una amenaza para la salud animal en la provincia, sino también para la salud pública, pues se conoce su asociación con la emergencia de la resistencia antimicrobiana y su posible carácter zoonótico (Majumder et al., 2023).
La patogénesis de S. aureus es un proceso dinámico que descansa en numerosos factores, como la composición genética y la respuesta inmune del hospedero, las condiciones geográficas, los factores de virulencia y la variabilidad genética de la bacteria (Sivakumar et al., 2023).
La asociación del diagnóstico de Mycoplasma spp. con otros patógenos mayores en los procesos de mastitis en la provincia, y en mayor frecuencia con S. aureus (χ2= 0.042, P<0.05), reviste gran importancia, pues, aunque este patógeno se identificó en el 22,6% de las muestras de leche de las 247 vacas investigadas, en coinfección con Mycoplasma spp. su participación se incrementó al 43,8%.
El rol potencial de Staphylococcus spp. en las mastitis crónicas y recurrentes de difícil pronóstico y difíciles de tratar con antibióticos (Mphahlele et al., 2020; Janus et al., 2023, Walzl et al., 2023) es un factor relevante al analizar su coinfección con Mollicutes en el presente estudio.
Los micoplasmas tienen un patrón de resistencia amplio, pues no son sensibles a los antimicrobianos ß-lactámicos y las sulfonamidas, y solo son generalmente susceptibles a las drogas que interfieren con las proteínas (tetraciclinas, macrólidos, linosamidos y florfenicol) o la síntesis de DNA (fluoroquinolonas) (Maunsell et al., 2011).
A su vez la resistencia de Staphylococcus aureus a los antimicrobianos, combinado con sus factores de virulencia, los mecanismos insuficientes de eliminación de los hospederos y la evasión a la respuesta inmune, inciden en que el patógeno pueda sobrevivir por períodos prolongados de tiempo en los hospederos (Walzl et al., 2023).
Aislados de S. aureus en leche de vacas con mastitis han mostrado elevada incidencia de factores de virulencia con importante papel en la patogénesis de la enfermedad. Así, algunos de esos aislados se observan en rebaños cercanos, y se sugiere su vinculación a través de prácticas de manejo deficientes de los productores, la existencia de patógenos comunes en la misma área, la alimentación y el pastoreo conjunto de animales sanos y enfermos, y el comercio de animales entre rebaños (Singh et al., 2023).
De manera que la coinfección de Mollicutes y S. aureus puede complicar el curso del proceso infeccioso en la ubre, comprometer su recuperación satisfactoria, y por tanto ser uno de los factores no identificados que incida en el curso epidemiológico desfavorable de la enfermedad en los rebaños y los fallos en su control en muchos lugares, como puede ocurrir en Zamora-Chinchipe.
Se reconoce que Mycoplasma spp. puede actuar como agente secundario que exacerba las infecciones preexistentes, pero también se ha señalado como agente primario que facilita la infección posterior con otros patógenos frecuentes en los cuadros de mastitis bovina (Deeney et al., 2021). En este sentido, entre las áreas prioritarias de investigación básica respecto a M. bovis la necesidad de profundizar en la importancia de la coinfección con otros patógenos en relación con la progresión de la enfermedad por ese patógeno (Maunsell et al., 2011).
El control de las mastitis por M. bovis falla regularmente cuando se basa solo en la detección de las infecciones intramamarias y la prevención de la transmisión vaca-vaca en el ordeño, porque a su recurrencia debido a la presencia de portadores asintomáticos, se suman la transmisión y diseminación del patógeno por rutas adicionales a la mamarias, como son los aerosoles y la vía hematógena a partir de otras localizaciones del agente en la anatomía animal (Zadoks et al., 2011). También por su sobrevivencia fuera del animal, porque puede persistir durante largos periodos de tiempo en estiércol, agua, arena y distintos materiales de la cama y convertirlo en un patógeno recurrente (Justice et al., 2011). Es por ello que incluso se recomienda intentar la eliminación de los casos de mastitis por M. bovis mediante el sacrificio (Maunsell et al., 2011).
Es importante destacar que para el sector lechero en su conjunto, la mastitis por S. aureus ocasiona las mayores pérdidas de leche debido a la amplia diseminación del patógeno y las pérdidas moderadas tanto por procesos de mastitis clínica como subclínica (Heikkilä et al., 2018).
Identificar los patógenos asociados a mastitis en los rebaños es relevante para enfrentar su control, y en particular la conducta terapéutica a seguir. Con la intención por disminuir los riesgos de la resistencia antimicrobiana, en la actualidad se insiste en identificar si los patógenos presentes no ocasionan perjuicios productivos y hasta desaparecen en poco tiempo de la glándula mamaria, para solo indicar tratamiento con antibióticos en casos necesarios (Ruegg, 2018). Por lo tanto, es fundamental la detección de los patógenos presentes en cada rebaño, y evaluar su sensibilidad a los antibióticos, como parte de la estrategia de control de las mastitis (Hossain et al., 2017).
La coinfección predominante entre Mycoplasma spp y S. aureus en los casos de mastitis subclínica en los rebaños investigados es evidencia de la repercusión que otros micoplasmas diferentes a M. bovis pueden tener en la manifestación de la enfermedad en los rebaños bovinos lecheros de Zamora-Chinchipe, por lo que se precisan más investigaciones para dilucidar las especies de mollicutes presentes y el papel de su coinfección con otros patógenos en los fallos en el control de la enfermedad.
CONCLUSIONES
La elevada frecuencia en vacas de la coinfección de Mollicutes con Staphylococcus aureus (43,80%) puede ser la causa del comportamiento clínico-epidemiológico desfavorable de la enfermedad en rebaños bovinos lecheros de Zamora-Chinchipe. También constituye una alerta sobre el papel que pueden tener otras especies de micoplasmas diferentes a M. bovis en el control de la mastitis, dada su resistencia reconocida a los antimicrobianos y el incremento de esta en otros patógenos mayores.