INTRODUCCIÓN
La evaluación del conducto (ductus) venoso forma parte de la valoración integral de la salud fetal en la ecografía de las 11-13 semanas de forma rutinaria, pues la presencia de flujo ausente o reverso durante la contracción atrial es un marcador de aneuploidías, cardiopatías o ambas1.
La agenesia de ductus venoso (ADV) es una malformación infrecuente que se asocia con resultados perinatales adversos. Aunque se define como de difícil diagnóstico, algunas series publicadas por grupos muy expertos y en población de alto riesgo la describen en hasta 6/1000 exploraciones2. Se han descrito dos rutas diferentes para el retorno de la vena umbilical en estos fetos: drenaje extrahepático o derivación (shunt) portosistémica, y drenaje intrahepático o derivación umbilico-hepática3.
En este trabajo se muestran las características y la evolución de un feto con diagnóstico de ADV con vena umbilical drenando directamente en la aurícula derecha (AD).
CASO CLÍNICO
Gestante de 30 años de edad (G3P1A1 [provocado]), sin antecedentes patológicos personales ni familiares, con ultrasonido del primer trimestre normal, al igual que el estudio del alfa-fetoproteína y la electroforesis de hemoglobina. Durante el ultrasonido del segundo trimestre, a las 23,4 semanas, se sospechó la presencia de una cardiopatía congénita por dilatación de la AD y se remitió al Cardiocentro Pediátrico William Soler, centro de referencia nacional de las cardiopatías congénitas, donde se le realizó un estudio ecocardiográfico que demostró la presencia de cardiomegalia con predominio de cavidades derechas en la vista transversal de cuatro cámaras (Figura 1) y, al realizar un corte longitudinal del feto con Doppler color superpuesto a la imagen bidimensional, se definió el recorrido de la vena umbilical drenando directamente en la AD (Figura 2). También se encontró la presencia de un foramen oval aneurismático, lo que sugiere la posibilidad de un defecto interatrial en la etapa postnatal.
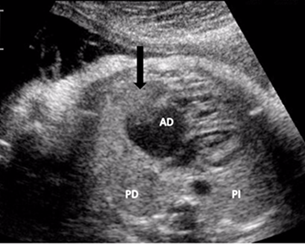
Figura 1 Vista ecocardiográfica de cuatro cámaras donde se evidencia una cardiomegalia moderada a expensa de las cavidades derechas. La flecha señala parte del lóbulo izquierdo del hígado que protruye hacia la cavidad torácica. AD, aurícula derecha; PD, pulmón derecho; PI, pulmón izquierdo.
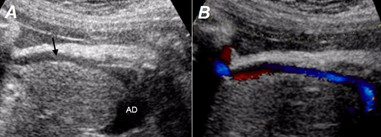
Figura 2 A. Se señala (flecha) la vena umbilical drenando en la aurícula derecha (AD). B. Uso del Doppler color superpuesto a la imagen bidimensional que demuestra tal afirmación.
Se realizó estudio genético por método de FISH (hibridación fluorescente in situ) que resultó normal para los cromosomas 13, 18, 21, y los sexuales. Durante la continuación del embarazo no se presentaron complicaciones ni cambios ultrasongráficos. A las 37,2 semanas se realizó parto por cesárea con recién nacido aparentemente sano, de buen peso y un Apgar de 9/9; a quien se le diagnosticó atresia esofágica con fístula, por lo que trasladado al Hospital Pediátrico William Soler donde fue valorado por un equipo multidisciplinario. Se le realizó un ecocardiograma y se visualizó una estructura extracardíaca adosada a la cara lateral de la AD, de consistencia muy similar a la del hígado, así como la presencia de una pequeña comunicación interauricular de 2 mm, tipo fosa oval, y una persistencia del conducto arterioso con mediciones de 1,7 mm.
Ante la muy infrecuente asociación de una atresia esofágica y la posible hernia diafragmática derecha se decidió realizar un estudio tomográfico donde se constató la presencia de ambos defectos digestivos. El paciente fue operado y se confirmaron ambas alteraciones estructurales, así como la presencia de una hendidura (cleft) traqueo-esofágica. Posteriormente el paciente falleció por complicaciones posquirúrgicas.
Al revisar el video del estudio ecocardiográfico durante la vida fetal, se observó una imagen cerca de la AD, por su cara lateral (Figura 1), que debía corresponder a la porción del lóbulo izquierdo del hígado, demostrado en la etapa posnatal.
COMENTARIO
El ductus venoso es un angosto vaso en forma de trompeta que se origina en el seno umbilical y confluye, después de atravesar el parénquima del hígado, conjuntamente con las venas hepáticas y la cava inferior, en la entrada de la AD; lo que conforma el vestíbulo venoso subdiafragmático4. Su importancia radica en asegurar que una fracción importante (20-30%) de la sangre oxigenada, no se mezcle con el flujo de menor velocidad que transcurre por la vena cava inferior y que procede de la parte inferior del cuerpo, sino que circule de forma preferencial hacia la aurícula izquierda, a través del foramen oval, ayudado por la válvula de Eustaquio. Para ello, dispone de una morfología particular (en forma de cono alargado), de manera que acelera el flujo de sangre cuando lo atraviesa5-6.
Para su identificación durante la exploración fetal, en el corte transversal abdominal, se sigue la vena umbilical en su trayecto hacia el corazón y, antes de llegar, se rota el transductor 30° hacia la zona caudal, donde se identifica una zona de mayor superposición o solapamiento (aliasing) de la señal. Se debe tener la precaución de posibles estructuras que puedan confundir, como son las venas suprahepáticas izquierdas o la vena cava inferior. El perfil típico del flujo en el conducto venoso muestra picos casi idénticos durante la sístole y el principio de la diástole ventricular, con una musca al final de la diástole, que corresponde a la sístole auricular7-8.
Cuando se diagnostica una ADV se pueden presentar dos variantes de drenaje venoso3:
Conexión extrahepática de la vena umbilical directamente a la vena ilíaca, cava inferior, vena renal, AD o, excepcionalmente, a la aurícula izquierda o seno coronario.
Conexión intrahepática de la vena umbilical, sin baipás hepático, al sistema portal; lo que aumenta su flujo.
En el caso que se presenta la variante encontrada fue la extrahepática, con conexión directa a AD y diámetro amplio del cortocircuito o derivación, sistema portal normal y moderada cardiomegalia -a expensa del crecimiento de las cavidades derechas-, sin signos de insuficiencia cardíaca y con estudio genético normal.
Según la literatura, en este tipo de variante, el flujo en el sistema portal y su desarrollo dependerán del diámetro del cortocircuito que, de ser ancho, puede asociarse a hiploplasia o agenesia del sistema portal9. También se asocia a una mayor posibilidad de evolucionar a insuficiencia cardíaca por sobrecarga crónica9-10; por todo esto, es la que tiene peor pronóstico.
Se han descrito tasas de mortalidad de hasta 17%1 y una tasa de malformaciones asociadas muy variable (25-65%), no sólo de cardiopatías, sino en cualquier otra localización; así como aneuploidías y síndromes genéticos como el de Noonan9-10. Dentro de las anomalías cardíacas más frecuentemente asociadas con ADV están los defectos septales auriculares y ventriculares, atresia tricuspídea, doble salida del ventrículo derecho, atresia pulmonar y la transposición de grandes vasos. Otras comúnmente asociadas son las del sistema gastrointestinal (atresia duodenal y fístulas traqueo-esofágicas), genitourinario (hidronefrosis y riñón ectópico), y músculo-esquelético (hemivértebra y anomalías estructurales del radio y el húmero)5-7.
La presencia de atresia esofágica con fístula, la hendidura tráqueo-esofágica y, con menos frecuencia, las hernias diafragmáticas derechas, son de muy difícil diagnóstico durante la vida fetal. Esta última no fue observada por nuestro equipo de trabajo, lo cual atribuimos a un error humano al confundir el lóbulo izquierdo del hígado con tejido pulmonar, y al estar el estómago en una posición normal. Aspectos estos que fueron descubiertos al revisar las grabaciones del caso (Figura 1) una vez realizado el diagnóstico posnatal.
La ADV aislada en ausencia de malformaciones cromosómicas, estructurales o hidropesía, tiene un pronóstico más favorable7. Por ello, nuestra actitud fue expectante, y su evolución estable durante todo el embarazo.














