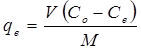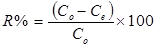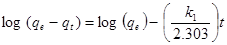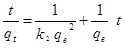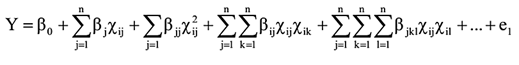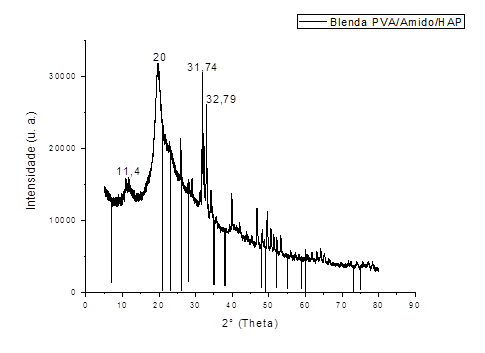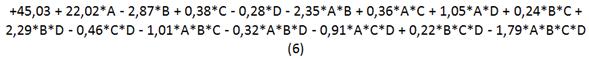Introdução
A liberação desproporcional de metais pesados é uma séria ameaça para a vida biológica em todo o mundo. Esses metais são altamente tóxicos podendo acumular-se dentro dos organismos de plantas e peixes, causando efeitos nocivos a longo prazo para os seres humanos e vida aquática. Entre as industrias que mais geram esses tipos de efluentes destacam-se as de galvanoplastia, processos de acabamento de metal, fabricação de baterias e os processos hidrometalúrgicos.1-3
As principais substâncias tóxicas que se encontram presentes em corpos d'água, mesmo em concentrações muito baixas, são o cádmio, o cromo, o chumbo, o arsênico, o cobalto.1,2,4) Dentre estes, o cádmio é considerado como uma das substâncias mais perigosas que afetam o homem, por causa da baixa eliminação pelo corpo humano. Além disso, o mesmo apresenta toxicidade sinérgica com outros metais, ou seja, há uma potencialização da sua toxicidade. Com isso, o desenvolvimento de métodos que facilitem a remoção desse metal é de grande importância para o tratamento das águas residuais.1,5
Os métodos de tratamento para a remoção de metais pesados mais utilizados, incluem-se a precipitação química, a permuta iônica, a osmose reversa e a separação por membrana.2-5) No entanto, todos estes procedimentos têm desvantagens significativas, como: remoção incompleta e produção de lamas ou resíduos dos produtos tóxicos.6
Um tratamento que vem atraindo atenção entre os pesquisadores é a adsorção, devido à sua simplicidade, economia e eficiência. Este processo oferece flexibilidade na concepção e funcionamento e, em muitos casos irá produzir efluente tratado de alta qualidade. Além disso, a adsorção é por vezes reversível, pois alguns tipos de materiais que são utilizados como adsorventes podem ser regenerados.4,7,8
No presente estudo, optou-se por uma proposta inovadora de aplicação de um sistema de blendas poliméricas para adsorção de íons metálicos, utilizando a hidroxiapatita dispersa neste sistema como material adsorvente, por causa da sua alta capacidade de sorção, baixa solubilidade em água, fácil disponibilidade e baixo custo.9-12)
Estudos de adsorção de cádmio por compósitos de hidroxiapatita utilizando métodos convencionais e clássicos não mostram o efeito combinado de todos os fatores envolvidos. Através da técnica de projeto experimental é possível, usando modelos estatísticos, entender as interações entre os parâmetros que foram otimizados.
Os planejamentos fatoriais são amplamente utilizados para investigar os efeitos de fatores e as interações entre esses fatores em um experimento, ou seja, o efeito de um fator varia com o nível dos outros fatores em uma resposta. As vantagens dos experimentos fatoriais incluem o custo relativamente baixo, um número reduzido de experimentos e maiores possibilidades de avaliar as interações entre as variáveis.13
Os fatoriais são úteis na avaliação da significância estatística dos fatores do experimento. No qual, fornece informações sobre o que acontece quando o fator é alterado e sobre as possíveis interações entre os fatores. Essa interação ocorre quando o efeito de um fator principal depende dos níveis de outro fator (ou fatores).14
O uso da ANOVA no planejamento fatorial garante que o efeito real possa ser diferenciado daqueles decorrentes do erro aleatório. O procedimento leva a um conjunto de estatísticas F e estatísticas P para testar as hipóteses de que cada fator, incluindo as interações.14 Assim, este trabalho teve como objetivo avaliar a interação de vários fatores, pH da solução (2,0<A<6,0), concentração inicial de cádmio em solução (50 <B <150 mg/L), massa adsorvente (0,0 <C<0,06 g) e tempo de processamento (6<D<24 horas), na adsorção de cádmio a partir de solução aquosa pela blenda polimérica Pva/amido/Hap.
Materiais e métodos
Obtenção da blenda polimérica
As blendas poliméricas foram produzidas pela mistura do Álcool Polivinílico (PVA) (Aldrich) e do Amido PA solúvel (C6H10O5)n (IMPEX), através do processo de criogelificação (freezing and thawing).15,16 Esta técnica expõe a blenda polimérica a um ciclo de congelamento (a menos 0°C) e descongelamento à temperatura ambiente em torno de 25°C. Os dois polímeros foram colocados separadamente em dois béqueres de 125mL com 50mL de água em agitação constante a 90°C por uma hora. Em seguida as duas soluções dos polímeros foram misturadas, seguido da adição do material adsorvente, hidroxiapatita ao 1%, sob agitação constante por uma hora. No final a mistura foi vertida em uma placa Petri e colocadas em um ultrafreezer (PANASSONIC - MDF-U56VC) por um período de 18 h para o congelamento da blenda, seguido do descongelamento em temperatura ambiente por 2 h. Após esses ciclos as blendas poliméricas foram secas em estufa (SX 300 DTME Digital) por 24 horas a 37°C. Os equipamentos utilizados nesta etapa pertencem ao laboratório de Engenharia Têxtil da Universidade Federal do Rio Grande do Norte.
A blenda foi caracterizada através das técnicas Termogravimétrica (NETZSCH STA 449F3) em ambiente sintético no intervalo de temperatura 32 a 700 °C e uma razão de aquecimento de 10°C/min, Difração de Raio-X (Shimadzu XRD-7000) utilizando tubo de cobre (radiação Cu Kα1), monocromador de cristal de grafite, voltagem de 40kV, corrente de 30mA e a varredura numa faixa de ângulo 2θ de 5º a 80º, tamanho do passo 0,01 2θ e tempo de exposição por passo de 0,6s. e Potencial Zeta (analisa o grau de carga superficial do material, podendo influenciar na dispersão ou coesão molecular) foi analisado no aparelho modelo zetasizer nanoseries/nanoz-Malvern (suspensões contendo 0,1g da blenda para 50mL de água destilada com diferentes condições de pH (2, 4, 5, 6, 8, 10). Os equipamentos utilizados nesta etapa são vinculados aos laboratórios do Departamento de Engenharia de Materiais e Engenharia Química da Universidade Federal do Rio Grande do Norte.
Estudos cinético da adsorção
Para o estudo cinético da adsorção do íon de cádmio, utilizou-se a blenda Pva/amido/Hap, afim de se analisar a quantidade de metal adsorvido em relação ao tempo de contato. O sistema para realização desta análise foi constituído de 50mL da solução de cádmio (100mg/L), com o pH ajustado para 5,0 utilizando as soluções de ácido sulfúrico (H2SO4) a 0,1M e hidróxido de sódio (NaOH) a 0,1M no medidor de pH de bancada (NOVA INSTRUMENTS- NI PHM) e 0,04g da blenda em um Erlenmeyers de 125mL. O experimento foi realizado em batelada com agitação constante de 150 rpm e em duplicata. Após tempos pré-determinados (1, 2, 5, 10, 20, 40, 80, 120 e 240min.) foram coletadas alíquotas da solução, e armazenadas sob refrigeração para posterior análise de Absorção Atômica.
A capacidade de remoção do metal por grama de biosorvente qe (mg/g) foi calculada através da equação 1.17,14,18
Em que C0 e Ce são a concentração inicial e final da solução de cádmio (mg/L), V o volume da solução em litros (L) e M a massa adsorvente em gramas (g). A determinação da taxa percentual de remoção (R%) do Cd (II) foi calculada pela equação 2.17,14,18
A cinética de adsorção mostra a evolução da capacidade de adsorção com o tempo. Para caracterizar a cinética envolvida no processo de adsorção, foram utilizados os modelos cinéticos de Pseudo-primeira ordem e o de Pseudo-segunda ordem.
Pseudo-primeira ordem representada pela equação 3. 17,14,18
Em que: qe é quantidade de cádmio adsorvida por unidade de massa adsorvente; qt é a quantidade de cádmio adsorvido por unidade de massa adsorvente em um tempo t; K1 é a constante de velocidade da reação.
Pseudo-segunda ordem representada na Eq. 4, como 17,14,18
Em que: K2 é a constante de velocidade de reação de pseudo-segunda ordem (g mg-1 min1); qe é a quantidade de adsorvato retido no sólido no equilíbrio (mg g-1); qt é a quantidade de adsorvato retido no tempo t (mg g-1).
Planejamento Fatorial
O planejamento foi realizado utilizando o “Software Design-Expert 7”, no qual usa-se as variáveis com menores (-) e maiores valores (+), calculando seus pontos médios em um plano fatorial de 24 dos parâmetros pré-estabelecidos. Com isso, é realizada as combinações possíveis entre esses parâmetros, formando uma matriz de variáveis independentes e de respostas. O modelo matemático originado da função de Taylor (5) também é fornecido pelo software, descrita a seguir:19
Em que: j≠k≠1, y é a resposta, xi (i = 1-n) são variáveis não codificadas n = número de variáveis, ẞi, ẞii, ẞij, são os coeficientes de interação linear, quadrático e de segunda ordem e e1 o erro aleatório, que corresponde a outros fatores que não são as variáveis envolvidas, mas estará influenciando na variável resposta.
Para o estudo do percentual de remoção do cádmio, a resposta do experimento, foi gerada no “software” uma matriz com 20 experimentos, no qual utilizou-se os seguintes parâmetros: pH de equilíbrio (A), concentração inicial do cádmio (B), massa adsorvente (Blenda) (C) e o tempo (D), conforme a tabela 1.
Tabela 1 Parâmetros do planejamento para adsorção do cádmio.
| Menor (-1) | Central (0) | Maior (+1) | |
| A - pH de equilíbrio | 2 | 4 | 6 |
| B - Concentração inicial (mg/L) | 50 | 100 | 150 |
| C - Massa adsorvente (g) | 0.02 | 0.04 | 0.06 |
| D - Tempo (h) | 6 | 15 | 24 |
Os experimentos foram realizados utilizando um agitador universal (Certomat MO - B. Braun Biotech Int.) a 150 rpm, em uma temperatura de 25°C. Primeiro pesou-se a blenda Pva/amido/Hap (0,02, 0,04 e 0,06g) utilizando balança analítica (SHIMADZU- AUY220), em seguida foram colocados em um Erlenmeyer contendo a solução de cádmio de 50, 100 e 150mg/L variando o pH em 2, 4 e 6. Uma alíquota de 1mL da solução foi diluída com água desidratada e filtrada utilizando papel filtro. Para o cálculo do percentual de remoção foi utilizada a equação 2, mencionada anteriormente.
Resultados e discussões
Caracterização da Blenda
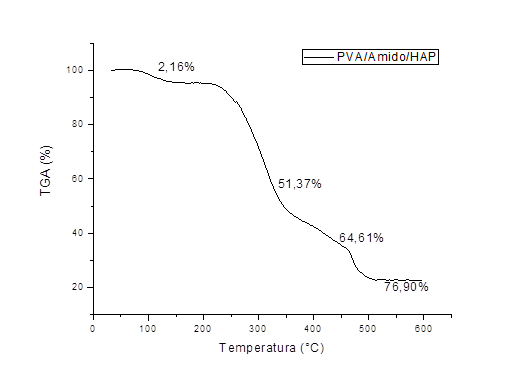
A curva da TGA (figura 1) revelou quatro etapas de degradação térmica da blenda Pva/amido/Hap: A primeira na faixa de temperatura de 80-150°C onde ocorre uma perda de água em torno de 2,16%. Na segunda faixa de transição 150-300°C com perda total de 51,37% que está relacionada a degradação do polímero de PVA. A faixa entre 350-480°C representa a carbonatação do PVA com uma perda de 64,61% a partir de 500°C ocorre a perda máxima de 76,90%.
A análise estrutural por DRX (figura 2) foi aplicada a blendas empregadas neste estudo. Segundo Yang20 o PVA puro apresenta uma estrutura semicristalina com dois picos bem distintos a 2θ=19-20 e outro em 39-40, como pode ser observado no DRX. Esses picos encontram-se presente na blenda polimérica PVA/Amido/HAP, mas com menor intensidade. O pico referente ao amido polimorfo (11,4) também pode ser visualizado, bem como os principais picos encontradas na hidroxiapatita (2θ=31 e 32).
A última análise do material adsorvente foi pelo potencial zeta, sendo observado em pH 2,0, um potencial de - 1,07mV e pH 6,0 apresentou potencial de - 3,92mV. Desta forma demonstra-se que em função do aumento do pH, as cargas superficiais deste material tornam-se mais negativas.
Percentual de remoção
O sistema para realização desta etapa foi constituído de 50mL da solução de cádmio (100mg/L). A taxa de remoção do cádmio, em função do tempo, ocorreu nos primeiros 5 min, evidenciando a eficiência da blenda Pva/amido/Hap na adsorção do Cd2+ (figura 3). O percentual de remoção nos primeiros 20 minutos ficou em torno de 87 %. Após esse período a captação do cádmio pela blenda atinge o equilíbrio de adsorção.
Observou-se uma rápida remoção do Cd2+, nos primeiros minutos de contato, sendo semelhante ao observado por Poinern et al.,21 e Dutta et al.,7, onde este fenômeno pode ser justificado segundo os autores por haver grande disponibilidade de sítios ativos no material adsorvente, acarretando equilíbrio do sistema em menos de 5 minutos.
Cinética de adsorção
O estudo da adsorção foi realizado em função do tempo, a fim de caracterizar a cinética envolvida no processo, foram analisados dois modelos cinéticos a pseudo-primeira ordem (figura 4) e a pseudo-segunda ordem (figura 5) para adsorção de Cd (II) pela blenda Pva/amido/Hap. O sistema para realização desta etapa foi constituído de 50mL da solução de cádmio (100mg/L). Observou-se um melhor ajuste nas condições experimentais para o modelo de Pseudo-segunda ordem (R2=0,999 9; qe = 1,05 e K2 = 0,008 83), em comparação com o modelo de Pseudo-primeira ordem.
O presente resultado foi semelhante ao observado por Dutta et al7 onde observou que o modelo cinético de pseudo-segunda ordem se aplicou melhor a remoção do cádmio, que é explicada pela ocorrência da quimiossorção na qual as interações entre o adsorvente e o adsorvato ocorrem mediante ligações químicas. Envolvendo as forças de valência através partilhas e troca de elétrons entre o cádmio (adsorvato) e a blenda Pva/amido/Hap (adsorvente).
Análise estatística
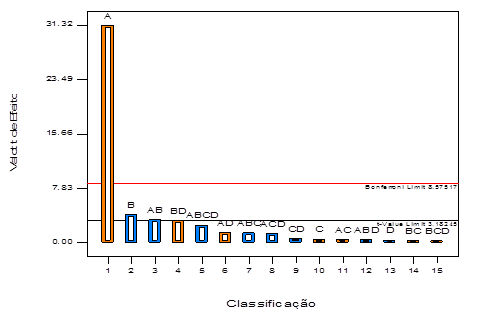
A percentagem de remoção de cádmio depende da variável individual e das combinações dessas variáveis no ensaio. A análise do gráfico de Pareto (figura 6) mostra os efeitos das variáveis independentes e suas interações sobre a variável dependente. A cor laranja representa os fatores que tiveram uma influência positiva no processo e a cor azul uma influência negativa.
A relação empírica entre remoção de íons de cádmio (%) e as quatro variáveis (pH, concentração inicial, massa e tempo) em valores codificados obtidos pela aplicação de metodologia de superfície de resposta é dada pela equação 6
Os resultados do modelo de superfície de resposta de segunda ordem na forma de análise de variância (ANOVA) são mostrados na tabela 2. A significância estatística da equação do modelo foi determinada a partir dos valores de F e P. E a qualidade do modelo desenvolvido foi avaliada com base no coeficiente de determinação (R2) A aplicação da ANOVA é a forma mais confiável para a avaliação da qualidade do modelo ajustado.
Tabela 2 Análise de variância (ANOVA) para o percentual de remoção de Cd (PVA/Amido/HAP).
| Fonte | Soma de quadrados | Quadrados Médios | F-Valor | P- Valor Prob - F |
| Modelo | 8 174,96 | 545,00 | ,,68,90 | 0,002 5 |
| A | 7 760,50 | 7 760,50 | 981,14 | < 0,000 1 |
| B | 131,37 | 131,37 | 16,61 | 0,026,7 |
| AB | 88,39 | 88,39 | 11,17 | 0,044 3 |
| BD | 83,56 | 83,56 | 10,56 | 0,047 5 |
| Erro Puro | 23,73 | 7,91 | ||
| Total corrigido | 9 481,95 | |||
A análise de variância mostrou que existe uma estatística significância no modelo quadrático com um F-Valor de 68,90 e P 0.0025. De acordo a ANOVA, os valores F maiores e os valores P menores (P <0,05) indicam efeitos de significância dos coeficientes correspondentes.22 Os valores de P foram usados para verificar a significância de cada coeficiente, o que, por sua vez, poderia indicar o padrão das interações entre as variáveis. Quanto menor o valor de P, mais significativo foi o coeficiente correspondente. Neste caso, A, B, AB, BD são termos significativos no modelo pois os valores de P são menores que <0,05. A precisão adequada que mede a relação sinal/ruído foi de 22,36, demonstrando que o modelo é significativo para o processo de adsorção de Cd (II), já que a relação maior que 4 é desejável. Além disso, um valor relativamente baixo do coeficiente de variação (CV = 5,74) indica boa precisão e confiabilidade dos experimentos que foram realizados.23,24
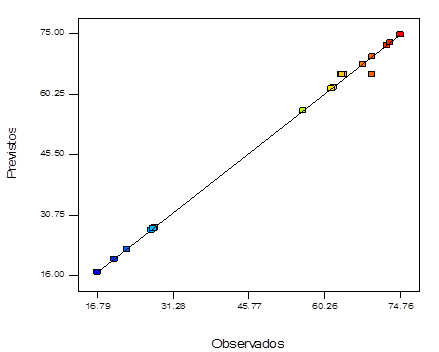
A figura 7 apresenta os valores observados no eixo horizontal e os valores previstos no eixo vertical utilizados para determinar se um modelo é ou não satisfatório para a blenda polimérica PVA/Amido/HAP. O resultado mostra que o valores previstos da resposta (% remoção) estão em concordância com valores observados sobre o intervalo selecionado de variáveis independentes. A maioria dos pontos de resposta estão localizados em faixas estreitas com valores residuais desprezíveis. A concordância entre os valores previstos e observados indicou que o planejamento fatorial foi empregado com sucesso como uma ferramenta eficaz e confiável para avaliar o comportamento de adsorção de Cd (II) e para otimizar as condições de adsorção.24 Além disso, os valores de R-quadrado e R-ajustado são próximos a 1, indicando uma alta correlação entre os valores observados e os previstos, para a blenda polimérica PVA/Amido/HAP (R²= 0,997 1 e adj. R²= 0,982 6).
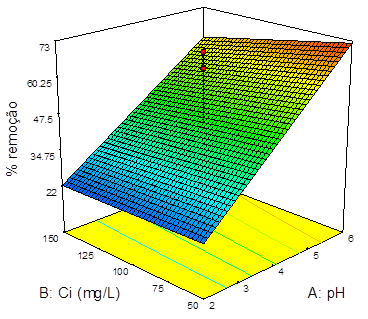
A figura 8 do gráfico de superfície de resposta 3D mostra o efeito simultâneo do pH e a concentração inicial de Cd (II) na solução aquosa, na eficiência de remoção de cádmio. Um aumento na remoção do íon cádmio com aumento no pH na faixa de 2-6 foi observado a valores de concentração iniciais baixos. A remoção máxima de Cd (II) (74,76%) foi obtida em um pH de solução de 6. Segundo RAO et al.25 na concentração inicial mais baixa, a percentagem de cádmio aumentaria à medida que mais locais ativos de ligação de cádmio estariam disponíveis para menos número de íons. Outros pesquisadores também investigaram o efeito do pH e da concentração de íons cádmio na adsorção de cádmio, usando diferentes tipos de adsorventes e encontraram resultados similares com este estudo. Amini et al22 utilizaram Aspergillus niger e observaram que a absorção Cd2+ aumentou com o acréscimo do pH com uma remoção máxima de 99,41% em um pH de 6,12.
Conclusão
Neste trabalho a blenda polimérica PVA/Amido/Hap foi demonstrada como um novo sistema para adsorção de íons cádmio em solução aquosa. As influências de pH, massa adsorvente, tempo de contato e concentração inicial na adsorção do íon de cádmio e suas interações foram investigadas por uma metodologia de superfície de resposta. O resultado mostrou que o pH da solução é o principal fator que afeta o comportamento de adsorção de cádmio. O planejamento experimental mostrou um bom ajuste do modelo em relação as interações dos fatores e a resposta, com um R²= 0,9826. A adsorção de íons estudados foi rápida com um percentual de remoção em torno de 87%. O estudo cinético foi realizado com base nas equações de pseudo-primeira ordem e pseudo-segunda ordem. Os resultados mostram que a adsorção segue o modelo de pseudo-segunda ordem