Introducción
La lepra es una enfermedad infecciosa, contagiosa, causada por el bacilo Mycobacterium leprae y lepromatosis. Este microorganismo fue descubierto por el Dr. Gerhard Hansen, y la enfermedad fue bautizada como EH. Durante mucho tiempo, se pensó que la EH era hereditaria, una maldición o un castigo de Dios. La enfermedad afecta la piel y los nervios y puede causar daños severos. Debido a sus efectos destructivos, la lepra ha causado miedo, segregación y prejuicio en todas las sociedades desde los tiempos bíblicos. Los pacientes con la EH no han sido tratados con humanidad en todo el mundo a lo largo de los siglos.1)
Enfermedad de Hansen
Se trata de una paciente femenina, mestiza de 20 años, universitaria que cursa el segundo año de medicina, procedente de la provincia de Guantánamo y con antecedentes de la COVID-19 en agosto de 2021, hace 5 meses comienza con lesión cutánea a nivel de la mejilla derecha de más menos 2 cm, eritematosa, de bordes bien delimitadas, no pruriginosa. Simultáneamente dolor e inflamación de articulaciones de las manos que evolucionaron de manera progresiva hasta tomar rodillas, tobillos y pies, y que se acompañaba de rubor, aumento de volumen y cambios de la temperatura en dichas articulaciones.
Hace 3 meses presenta un empeoramiento de su clínica, con exacerbación de las manifestaciones cutáneas, aparecieron nuevas lesiones de características similares a las descritas en la región peribucal, hombro, espalda y miembros superiores e inferiores, acompañado de aumento de volumen de hemicara derecha que comprometía el ojo y la región frontal del mismo lado, además de un eritema y dolor de ambos pabellones auriculares, asociado a elevación de la temperatura corporal de predominio vespertino, decaimiento, pérdida del cabello, parestesias en miembros inferiores y adenopatías pequeñas en región cervical. Acude a nuestra consulta de reumatología con exámenes complementarios dentro los parámetros normales, ANA negativo y con biopsia de piel realizada por dermatología, por lo que se decide su ingreso para realizarle estudio y tratamiento bajo el diagnóstico de conectivopatía sospechada.
Examen físico (positivo)
Signos vitales: temperatura 36,5 °C; frecuencia cardíaca 70 latidos por min; presión sanguínea 120/70 mmHg; frecuencia respiratoria 18 respiraciones por min; saturación de oxígeno 100 % con respiración aire ambiental.
Apariencia general: bien nutrido, ligeramente decaída; talla 1, 50 cm; peso 46 kg; IMC: 20,4 kg/m2 (normopeso).
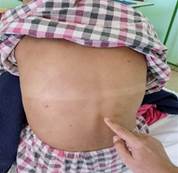
Piel: placas eritematosas infiltradas de bordes bien delimitados sin escama, algunas con hiperestesia mayormente en espalda, en miembros superiores e inferiores (fig 1).
Placa en la mejilla derecha que toma ojo derecho y ambos pabellones auriculares (fig. 2).
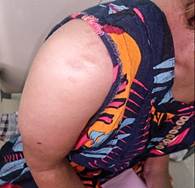
En hombro derecho lesión eritematosa descamativas delimitada, sobre elevada. Además de presentar una piel áspera y gruesa (fig. 3).
Hemolinfopoyético: presencia de adenopatías cervicales, móviles no dolorosas, de aspecto inflamatorio, no supraclaviculares ni axilares palpables.
Tejido celular subcutáneo: ligero edema en tobillo izquierdo.
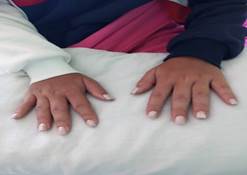
Sistema musculoesquelético: aumento de volumen de carpos y dolor a la palpación. Test de Squeeze positivo bilateral. Falanges: aumento de volumen y dolor a la palpación de todas las interfalángicas proximales y distales (fig. 4).
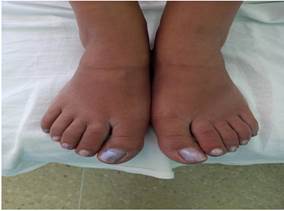
Rodillas: dolor a la palpación en la interlinea articular interna y externa, no peloteo. Tobillos: aumento de volumen de tobillo izquierdo, dolor a la palpación de ambos tobillos. Pies: test de Poullosson positivo, aumento de volumen de todas las falanges proximales y distales (fig. 5).
Sistema nervioso central (SNC): consiente, orientado en tiempo, espacio y persona. hiperreflexia osteotendinosos generalizada, sobre todo rotuliana, simétrica. Parestesia de las manos.
Resultados de laboratorio
En el ingreso la paciente es valorada por dermatología por las lesiones cutáneas donde se plantea una posible EH versus lupus eritematoso sistémico (LES) por las características de las lesiones y por presentar erosión y cogestión del tabique nasal derecho, además de un engrosamiento del nervio cubital y mediano izquierdo, motivo por lo que se indica una baciloscopía nasal, auricular y de ambos codos, junto a estudios encaminados a buscar una enfermedad del tejido conectivo.
En los estudios realizados se encontró que el coagulograma completo: normal, EKG: sin alteraciones, electroneuromiografía: compatible con una polineuropatía axonal severa, anticuerpos de actividad para LES: anti-histona: 1 U/mL V.R: 0 - 18 U/m, anti-DNA (IgG) cualitativo: negativo, anti P-ribosomales (Rib-P): 10 U/mL V.R: 0 - 18 U/m. Anticuerpos antinucleares totales (ANA): negativo, anti-DNAdc (IgG): negativo. ANCA (cribado Anti-PR3 y MPO): negativo, antígeno de superficie: negativo, serología para la hepatitis C: negativo, anticuerpos para HIV: negativo. VDRL: no reactiva, prueba de Coombs: negativo, urocultivo: negativo, exudado vaginal simple: negativo, ultrasonidos: U/S abdominal: normal, U/S de rodillas: normal, rastreo ganglionar: pequeños linfonodos en ambas regiones inguinales, ecocardiograma: normal. Rx tórax: normal, Rx miembros superiores e inferiores: normal; aunque en los Rx no se reportaron alteraciones se discutieron en colectivo y se pudo constatar osteopenia yuxtaarticular y numerosas geodas, I/C neurología: por la polineuropatía axonal severa de posible origen infeccioso y la presencia de las alteraciones neurológicas se decidió empezar tratamiento con gabapentina (300 mg) 1 cápsula en la noche, antipéptidos citrulinado: 1 U/mL V.R: 0 - 17,9 U/m, factor reumatoide (aglutinación látex): negativo, biopsia diagnóstica de piel: lepra lepromatosis, baciloscopía para Hansen (M. leprae): codificación 2.
Discusión
La prevalencia de la lepra varía notablemente en todo el mundo y entre pacientes de un mismo país. La gran mayoría de los casos se encuentran en países en desarrollo, principalmente en India y Brasil. La lepra ha disminuido en Cuba en las últimas décadas. Por lo que los médicos se han vuelto menos conscientes de hacer un diagnóstico de lepra. Por ello, el caso es relevante para demostrar que este problema aún puede existir en nuestro país.
La lepra es una enfermedad granulomatosa crónica causada por el complejo mycobacterium leprae; prevalece en algunos países del mundo, de los cuales la India tiene los números más altos. Las manifestaciones reumáticas incluyen poliartritis inflamatoria, síndrome de manos y pies hinchados, tenosinovitis, policondritis, paniculitis, diversas erupciones cutáneas, úlceras y gangrena. Además, puede conducir a niveles elevados de autoanticuerpos, ANA y factor reumatoide, debido a la hiperglobulinemia policlonal que acompaña a esta enfermedad. La lepra debe ser considerada como una posibilidad en el contexto de fiebre, dolor en las articulaciones y afectación de la piel como nódulos, úlceras, o placas.2
Es causada por bacilos acidorresistentes (BAAR) del complejo mycobacterium leprae, que incluye m. leprae y m. lepromatosis. La bacteria en forma de bastón m. leprae, perteneciente al género mycobacterium, fue descrita por primera vez por el médico noruego Gerhard Armauer Hansen.3 El agente etiológico es un organismo resistente a los ácidos y de crecimiento lento que muestra predilección por replicarse en macrófagos, células endoteliales y células de Schwann. Los bacilos pueden agruparse en tejidos para formar globos que contienen cientos de bacilos. m. leprae y m. lepromatosis son organismos intracelulares obligados que se replican lentamente, crecen idealmente en temperaturas que oscilan entre 27,8 oC a 33,8 oC, y no se puede cultivar en medios artificiales.4
En 1966 Ridley y Jopling clasificaron la lepra en cinco grupos diferentes según la respuesta inmunológica del paciente: lepra tuberculoide (TT), grupo borderline (BT: borderline tuberculoide; BB: borderline-borderline; BL: borderline lepromatous) y lepra lepromatosa (LL). Los casos límite tienen una respuesta inmunitaria de células T intermedia.5
En 1997, la Organización Mundial de la Salud creó una división para facilitar la clasificación y el tratamiento de la lepra en áreas endémicas y la dividió en tres grupos: (1) paucibacilar con una sola lesión cutánea, (2) paucibacilar con dos a cinco lesiones cutáneas y (3) multibacilar (con más de cinco lesiones cutáneas). Esta división se realizó independientemente del tamaño o las características histológicas. La lepra multibacilar (MB) incluye BB, BL y LL.6
Después de las dermatológicas y neurológicas, las afectaciones musculoesqueléticas son la tercera manifestación más frecuente. Las manifestaciones sistémicas (eritema malar, nódulos, ulceraciones, púrpura, necrosis isquémica, fenómeno de Raynaud, polineuropatía, mononeuritis múltiple, debilidad muscular, adenopatías generalizadas, hepatoesplenomegalia y glomerulonefritis) se observan principalmente en la lepra multibacilar y son secundarias a la infiltración y proliferación directa del bacilo en el órgano afectado.7,8
No es raro que la lepra se confunda con otras enfermedades de la piel. Al igual que la lepra, las manifestaciones cutáneas en el LES pueden ser heterogéneas. Las similitudes entre las placas infiltradas en la lepra límite y el lupus tumidus pueden representar un desafío diagnóstico, como es nuestro caso. La falta de un alto índice de sospecha puede conducir a un diagnóstico erróneo. Texeira y otros,9,10,11 informaron una frecuencia del 9 % de lesiones discoides en pacientes con lepra que pueden explicarse por un diagnóstico erróneo. Aunque su presentación clínica puede ser similar a la del lupus eritematoso cutáneo crónico (LECC), ciertas características de la lepra deben alertar al médico, tales como: lesiones cutáneas anestésicas, agrandamiento de los nervios y sensibilidad nerviosa. Las lesiones pueden afectar a los nervios periféricos cutáneos, principalmente al nervio tibial posterior, cubital, mediano y poplíteo lateral.
La presentación clínica de la lepra varía mucho y depende de la respuesta inmunológica del individuo a la infección. La piel, el sistema nervioso periférico y el sistema reticuloendotelial están principalmente afectados; sin embargo, otros como el tracto respiratorio superior, los huesos, articulaciones, los ojos, los testículos y las glándulas suprarrenales también pueden verse afectado.12
La EH siempre debe ser considerada entre los diagnósticos diferenciales de las artritis en regiones endémicas. En la literatura existen descripciones de pacientes con EH que fueron diagnosticados de LES, AR, dermatomiositis/polimiositis y vasculitis sistémicas.13
Ribeiro y otros14 en sus estudios publicado en el 2015 demostró que mycobacterium leprae no solo puede determinar síntomas que simulan brotes de lupus, incluida la producción de autoanticuerpos, sino que también podría actuar como desencadenante de la reactivación del lupus.14
Según Pernambuco y otros,15) la poliartritis puede ser un síntoma inicial de la EH y las manifestaciones articulares que ocurren durante los episodios reaccionales en la EH la asemejan a las colagenosis.15
La EH a pesar de ser eliminada por la OMS en el año 2000, hoy en día constituye un azote para las naciones en desarrollo, y Cuba no queda exenta de tal enfermedad, aun cuando existe un Programa Nacional de Lepra que lleva la Atención Primaria de Salud, en todo el país, es una enfermedad subdiagnosticada por su similitud a múltiples enfermedades.
La paciente en la actualidad se encuentra atendida en su provincia natal por el área de salud con buena respuesta al tratamiento.