INTRODUCCIÓN
Uno de los problemas de salud más frecuentes de países en vías de desarrollo en el período de embarazo, y responsable de altas tasas de morbilidad y mortalidad materno infantil, es el relacionado con la hipertensión, 1 siendo la hipertensión crónica y la preeclampsia los más complejos debido a que involucran a la madre y el feto poniendo en peligro la vida de los dos. 2
La preeclampsia se determina como un trastorno del embarazo que se caracteriza por presentar hipertensión arterial y proteinuria principalmente, 3 y en ocasiones edema en las piernas y retención de líquido.
Epidemiológicamente, según información de la Organización Mundial de la Salud (OMS) cada 3 min. fallece una mujer en el mundo por causa de la preeclampsia lo que suma un total de casi 50 000 al año, esto la convierte en la primera causa de atención en emergencia de hospitales, 2 y en Ecuador es la primera causa de morbilidad perinatal con el 8.3 % de incidencia y responsable del 14 % de mortalidad infantil. 4
En un estudio realizado por Tejera E, et al. se determina que, geográficamente hablando, la incidencia de preeclampsia en Ecuador es mayor en habitantes de la sierra debido a la altura y la escasez de oxígeno, 5 asimismo se observa un incremento de casos de preeclampsia con síntomas de severidad de 8961 en 2015 a 11609 en 2018, en tanto que sin síntomas de severidad disminuyó de 1870 a 1739, en el mismo período de tiempo.
La preeclampsia suele presentarse entre la semana 20 hasta 2 semanas luego del parto con presión arterial de 140/90 mmHg asociada a proteinuria de más de 30 mg en muestra única o más de 300 mg en muestra de 24 h. 6
Puede ser leve en caso de presión arterial mayor o igual que 140/90 mmHg y proteinuria cualitativa desde 1; o severa presión arterial mayor o igual a 160/110 mmHg; proteinuria cualitativa de 2 a 3+, además de otros síntomas como oliguria, elevación de creatinina sérica, edema pulmonar, disfunción hepática, trastorno de la coagulación, ascitis. 7 El origen de la enfermedad es incierto, por lo que su detección y manejo es complicado, se conoce que es multifactorial; se han establecido probables factores predisponentes que podrían ser predictores tempranos 8 como: genéticos, medioambientales, inmunológicos, la mayoría de los factores de riesgo cardiovascular como dislipidemia, 9 hipertensión, obesidad, diabetes mellitus y otras afectaciones orgánicas como lupus eritematoso sistémico, trombofilias, nefropatías. 10
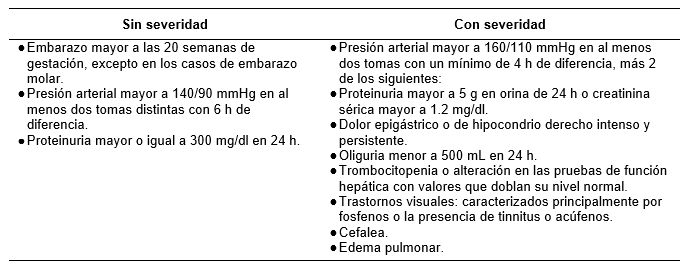
De acuerdo con el nivel de hipertensión, la preeclampsia puede ser con criterios de severidad o sin criterios de severidad, la tabla 1 resume los criterios de clasificación.
En el tratamiento de la preeclampsia en el Ecuador basa su acción terapéutica en los criterios de la Guía de Práctica Clínica 12 en la que se recomienda el uso de labetalol y nifedipino en los trastornos hipertensivos del embarazo como medicamentos de primera línea, como se detalla en la tabla 2.
Tabla 2 Medicamentos para el tratamiento farmacológico de los trastornos hipertensivos del embarazo.

El objetivo de esta revisión es analizar la efectividad de labetalol y nifedipino como tratamiento antihipertensivo en la preeclampsia.
DESARROLLO
Metodología de búsqueda y selección de resultados
El presente estudio es una revisión sistemática que busca el análisis crítico y la síntesis del empleo de labetalol o nifedipino en el tratamiento de la preeclampsia.
Búsqueda y selección de la evidencia
La búsqueda de información se realizó mediante palabras clave como preeclampsia, hipertensión, labetalol, nifedipino, en bases de datos como Pubmed, Medes, Elsevier y Google Scholar y gestores de búsqueda especializados.
Las referencias tomadas en cuenta se limitaron a los 5 últimos años, es decir entre 2018 y 2022. Para su selección se empezó por considerar el título, el resumen y las conclusiones con el fin de determinar su elegibilidad, posteriormente se sometieron los recursos encontrados a los criterios siguientes:
Criterios de inclusión:
Se incluyeron revisiones sistemáticas, estudios clínicos, de casos, guías de manejo clínico y metaanálisis 5 años o menos a la fecha, que se encuentren disponibles, completos y acordes con la pregunta de investigación, tanto en español, inglés o portugués.
Criterios de exclusión:
Revisiones narrativas, artículos de opinión, estudios no concluyentes, artículos mayores a 5 años, estudios incompletos o sobre otros tipos de tratamiento y en otros idiomas distintos a los mencionados.
Extracción de datos
Para la selección de datos se empleó la matriz de caracterización de estudios incluidos la misma que contiene: autor y año, tipo de estudio, muestra, fármaco empleado, dosis, efecto y magnitud del estudio.
La pregunta de investigación planteada hace referencia a la metodología PICO (paciente, intervención, comparación y resultados).
P (Pacientes): Mujeres embarazadas con diagnóstico de preeclampsia.
I (Intervención): Prescripción de labetalol o nifedipino como tratamiento farmacológico.
C (Comparación): Efectividad de los dos n medicamentos prescritos.
(Resultados) Outcomes: Control de la preeclamsia.
Los resultados se describen en el anexo 1, tomando en cuenta que las referencias se gestionaron mediante Mendeley.
Evaluación del riesgo de sesgo y calidad de la evidencia encontrada
Con el fin de determinar el grado de riesgo de sesgo de la información y la calidad de los estudios se empleó la escala de Jadad, la misma que asigna un puntaje entre 0 a 7 de acuerdo con las siguientes preguntas:
¿Es un estudio aleatorizado?
¿Se describe el método utilizado para generar la secuencia de aleatorización y este método es adecuado?
¿Es adecuado el método utilizado para generar la secuencia de aleatorización?
¿El estudio se describe como doble ciego?
¿Se describe el método de enmascaramiento (o cegamiento) y este método es adecuado?
¿Es adecuado el método de enmascaramiento (o cegamiento)?
¿Hay una descripción de las pérdidas de seguimiento y los abandonos?
Cada pregunta se puntúa con 0 o 1 y se suma al final el total de las preguntas. Para la evaluación de los estudios es necesario que obtenga una puntuación superior a 4, por lo que los estudios con puntaje menor a 3 se consideran débiles y de pobre calidad investigativa.
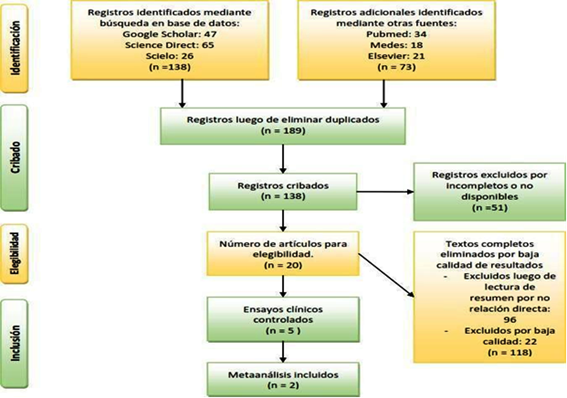
Se encontraron 211 fuentes de estudio de las cuales se excluyeron 22 por encontrarse duplicadas, 51 estudios fueron excluidos por no estar disponibles o estar incompletos y 107 retirados por baja calidad investigativa de acuerdo con la escala JADAD aplicada, quedando al final 31 fuentes de investigación, de las cuales 7 son las principales para establecer una comparación entre los fármacos estudiados.
La selección de estudios se puede verificar en el gráfico 1 que presenta el flujograma bajo el modelo PRISMA.
El tratamiento, dependiendo de la clasificación, indica que, en casos de severidad con más de 34 a 37 semanas, 13 la indicación es de un parto prematuro que solucionaría los síntomas presentados, en menos de 34 semanas se busca alargar el tiempo de gestación con la prescripción de corticosteroides prenatales. 14
Sin criterios de severidad se busca mantener el mayor largo de vida gestacional mediante la hospitalización con una dosis mayor de corticosteroides más sulfato de magnesio por vía intravenosa. 15
Se observa en el anexo 2 el tratamiento prescrito según la clasificación, entre los cuales se consideran de primera línea el labetalol y el nifedipino. 16
Labetalol
Labetalol es un fármaco antihipertensivo único de tercera generación que opera acciones antagonistas β- adrenérgicas no selectivas y antagonistas α1- adrenérgicas selectivas, con efecto vasodilatador y antihipertensivo, siendo un antagonista reversible de los adrenoceptores con una mezcla de cuatro isómeros con dos pares de isómeros quirales (dos centros de asimetría). 17
Los dos isómeros son relativamente inactivos, mientras que el tercero y el cuarto son un potente bloqueador α y un potente bloqueador β, respectivamente. El labetalol tiene una proporción de 3:1 de antagonismo β:α después de la dosificación oral. 18
El bloqueo alfa lleva a la reducción de la resistencia vascular sistémica, lo que reduce la presión arterial sin afectar significativamente el gasto cardíaco y la frecuencia cardíaca.
La dosis oral diaria recomendada varía entre 200 a 2400 mg/día según los requerimientos de los pacientes, en casos graves se puede necesitar 1200 a 2400 mg de labetalol al día (con o sin diuréticos tiazídicos), en tanto que en emergencias hipertensivas la dosis recomendada es de 20 mg por inyección intravenosa administrada durante 2 min., seguida de 40-80 mg durante 10 min. hasta un máximo de 300 mg en total. 19
Entre los efectos secundarios del labetalol se encuentran: cosquilleo, mareos, cansancio excesivo, cefalea, malestar estomacal y congestión nasal; si estos síntomas se hacen severos o aparecen disnea, inflamación de piernas y pies, aumento súbito de peso y dolor en el tórax, es necesario evaluar el beneficio del medicamento. 20
Nifedipino
El nifedipino es un fármaco antagonista del calcio perteneciente a la familia de las 1.4-dihidropiridinas, cuyo efecto es vasodilatador y aumenta el flujo coronario sin afectar la conducción auriculoventricular debido a que se une a los canales de calcio en un lugar diferente que se demuestra con un buen perfil especialmente por su administración por vía oral y su bajo costo. 21
Como antagonista del calcio, el nifedipino impide el ingreso de este mineral en las células musculares lisas vasculares bloqueando el poro del canal del calcio e inhibiendo el mecanismo contráctil de las células vasculares con la consiguiente vasodilatación, tanto de las arterias coronarias como de los vasos periféricos. 22
Esta vasodilatación coronaria con el correspondiente aumento del flujo, incrementa la llegada de oxígeno a los tejidos del miocardio, al mismo tiempo que la vasodilatación periférica reduce las resistencias periféricas, la presión arterial sistémica y la poscarga. 23
A su vez, la reducción de la poscarga disminuye la presión en las paredes del miocardio y menora su demanda de oxígeno.
El nifedipino se recomienda generalmente cuando fracasan antihipertensivos beta agonistas-beta adrenérgicos o el sulfato de magnesio en ambiente hospitalario evitando el desenlace de parto prematuro. 24
En casos de preeclampsia se recomienda dosis de 10 mg de nifedipino estándar cada 4-8 h o dosis de 20 mg cada 6-8 h. La administración de nifedipino durante 48 h o menos es capaz de retardar el parto varios días. No se recomiendan tratamientos más prolongados, ni se debe utilizar al mismo tiempo sulfato de magnesio. 25
Los efectos secundarios presentados generalmente en bajo nivel son: dolor de cabeza, náuseas, mareos o aturdimiento, rubor, acidez estomacal, latidos cardíacos rápidos, calambres musculares, estreñimiento, tos y disminución en la capacidad sexual; se consideran manifestaciones adversas de gravedad: inflamación de la cara, los ojos, los labios, la lengua, las manos, los brazos, los pies, los tobillos o las pantorrillas, dificultad para respirar o tragar, desvanecimiento, sarpullido, coloración amarillenta en la piel o los ojos, aumento de la frecuencia o intensidad del dolor en el pecho (angina). 26
Labetalol vs nifedipino
Se identificó un estudio realizado en 593 mujeres embarazadas diagnosticadas con preeclampsia a las que se les dividió en dos grupos, 298 tratadas con nifedipino y 295 con labetalol. 27
En promedio, la presión arterial de los dos grupos fue similar y se estableció en arterial sistólica de ≥160 mm Hg o una medición de la presión arterial diastólica de ≥110 mm Hg, interviniéndose con dosis de 10 mg de nifedipino oral después de 1 h, se podría administrar una dosis adicional de 10 mg cada h para dos dosis adicionales (hasta un total de 30 mg) y 200 mg de labetalol oral si su presión arterial sistólica superaba los 155 mm Hg o su presión arterial diastólica superaba los 105 mm Hg después de 1 h, se podía administrar una dosis adicional de 200 mg cada h para dos dosis adicionales (hasta un total de 600 mg). Los resultados arrojaron que en un lapso de 6 h y sin resultados adversos el control de presión arterial fue más significativo en el uso de nifedipino (85 %) frente a labetalol (78 %), debiendo notarse que el 44 % de pacientes tratadas con nifedipino requirió una segunda dosis frente al 48 % de pacientes tratadas con labetalol. El estudio concluye que existe una diferencia pequeña en la efectividad a favor del nifedipino frente al labetalol, considerando que, en los aspectos de control, administración de fármacos y otros elementos no existió variaciones significativas en ambos casos.
Otro estudio analizó el tratamiento de preeclampsia en 363 mujeres divididas en dos grupos, tratadas con nifedipino y con labetalol. 28) Las dosis empleadas fueron similares al estudio anterior y los resultados arrojaron mayor eficacia del nifedipino para controlar la presión arterial ligada a la preeclampsia en casos sin complicación, aunque en casos más severos, no se demostró un mejor desempeño de uno u otro fármaco.
Esta investigación concluye que, si bien no existen diferencias significativas entre ambos fármacos en cuanto al tratamiento de preeclampsia, sí se encuentra respecto al costo y disponibilidad del producto en países en vías de desarrollo.
El estudio realizado por Zulfeen M, et al., en 120 mujeres diagnosticadas con preeclampsia y con presión arterial promedio de ≥ 160/110 mm Hg, dosificó el tratamiento con labetalol recibió inicialmente 20 mg seguidos de dosis crecientes de 40 mg, 80 mg, 80 mg y 80 mg (5 dosis) cada 15 min. hasta un máximo de 300 mg. El grupo de nifedipino recibió inicialmente 10 mg seguidos de dosis repetidas de 20 mg cada 15 min. (5 dosis en total) hasta un máximo de 90 mg. 29
El análisis que realiza este estudio fue en función del tiempo de control de la hipertensión como meta básica para el tratamiento de preeclampsia, determinándose que en el caso de nifedipino el tiempo de control fue menor en 36.75 min.
Corroborando lo anterior observamos en un estudio prospectivo en el que se compara la efectividad del labetalol intravenoso con nifedipino oral, realizado este en 16 mujeres embarazadas de entre 24 y 42 semanas de gestación con hipertensión severa reflejada en una presión arterial sistólica ≥160 mmHg y/o presión arterial diastólica ≥110 mmHg. Se le administró 20 mg de labetalol intravenoso al primer grupo y 10 mg por vía oral al segundo grupo, obteniendo como resultado luego de 30 min. de medicación una disminución significativa en la presión sistólica, presión arterial media y presión de perfusión cerebral en quienes tomaron nifedipino oral, aunque no se notaron diferencias significativas en la presión diastólica el cambio en la velocidad de la arteria cerebral media por Doppler transcraneal. 30) Esta investigación concluye que el nifedipino por vía oral presentó un mejor perfil de efectividad en la disminución de la presión de perfusión cerebral impulsada por la disminución de la presión arterial periférica más que la disminución del flujo sanguíneo cerebral, frente al labetalol por vía intravenosa.
De manera individual, el labetalol resulta con mejor perfil terapéutico que otros medicamentos como alfa- metildopa, el estudio de Morales-Avendaño V, et al., establece que, en 250 casos investigados de mujeres con preeclampsia, tratados con labetalol y alfa-metildopa, se observaron valores significativamente más bajos en el primer caso en cuanto a la presión arterial sistólica, diastólica y media. 31
CONCLUSIONES
A pesar de no obtener una diferencia significativa desde el punto de vista estadístico, después del análisis podemos deducir que, el uso de nifedipino es más conveniente que el labetalol por diferentes aspectos en los que se destacan la eficacia en los casos sin complicación, el menor uso de segundas dosis para controlar la preeclampsia, la reducción del tiempo de control de la hipertensión y su costo.