INTRODUCCIÓN
En la isla de Cuba, se desarrollan cuatro especies endémicas de pino: Pinus tropicalis Morelet, Pinus caribaea Morelet var. caribaea Barret y Golfari, Pinus cubensis Griseb y Pinus maestrensis Bisse, de ellas dos en la zona occidental y las dos últimas en la oriental. Estas especies son de suma importancia, económica y ecológica, pues ocupan grandes extensiones de tierra en el archipiélago y por tanto en los bosques de pinos cubanos se puede encontrar una gran cantidad de recursos madereros y no madereros y una gran variedad de especies animales y vegetales.
Pinus caribaea var caribaea, se distribuye geográficamente en la provincia de Pinar del Río e Isla de la Juventud (López-Almirall, 1987; Geada-López et al., 2021). En gran parte este se asocia simpátricamente con el Pinus tropicalis Morelet o en rodales puros solamente en la meseta de Cajálbana. Desde el punto de vista evolutivo es una especie joven y que reporta un comportamiento invasor (Camacho et al., 2018; Gallien et al., 2015).
Las variaciones anatómicas y morfológicas en plantas son respuestas a la variabilidad ambiental, procesos como la adaptación y la aclimatación se derivan o se asocian a estas variaciones. Por esto el estudio de la variabilidad en la anatomía foliar entre poblaciones que ocupan ecótopos con diferentes condiciones edafoclimáticas son de gran importancia para la conservación y manejo del genofondo de la especie, sobre todo para el uso de procedencias para la reforestación.
Las acículas juegan un rol importante en el proceso de aclimatación o adaptación, al ser el órgano responsable de la fotosíntesis, la asimilación del CO2 atmosférico y el intercambio de gases. De ahí que modifiquen la estructura anatómica de la acícula, para soportar ambientes desfavorables como respuesta diferencial a estos, lo cual a largo plazo afectará la supervivencia y el crecimiento de la planta (Grill et al., 2004, López et al., 2010, Huang et al., 2016, Geada López et al., 2021).
Los factores ambientales tienen una influencia directa en la estructura de los tejidos de la acícula, en el patrón y posición de los estomas, el número y tamaño de los conductos de resina, en especial para las especies de Pinus(Twari et al., 2013; Ghimire et al., 2014; Meng et al., 2018), el grosor de parénquima de transfusión y área del mesófilo (Meng et al., 2018; Köbölkuti et al., 2017, Huang et al., 2016). Por lo que, la anatomía puede variar entre poblaciones y especies, en especial, dentro de aquellas con amplios rangos de distribución continental (Jasiñska et al., 2014; Boratyñska et al., 2015; Zhang et al., 2017).
Hasta el momento se han llevado a cabo diversos estudios relacionados con el tema, por ejemplo: (Pérez-del Valle et al., 2016) demostraron cierta variación atómica en la acícula de Pinus caribaea var, caribaea en seis localidades de Pinar del Río. Más adelante (Pérez-del Valle et al., 2020) encontró diferencias en la anatomía de la acícula de Pinus caribaea var. caribaea en tres ecótopos de la especie donde habita en simpátria con Pinus tropicalis. Recientemente se demostraron diferencias anatómicas foliares en poblaciones naturales de Pinus caribaea var. caribaea (Pinaceae) en Pinar del Río y Artemisa, Cuba (Geada-López et al., 2021).
En general, las acículas de Pinus caribaea var. caribaea presentan 13,6 ± 1,0 cm de largo y 1,3 ± 0,3 mm de ancho. La estructura anatómica equifacial, en forma de abanico, muestra la epidermis uniestratificada. Las estomas se distribuyen en ambas superficies de la acícula, el número promedio de hileras de estomas por acícula es 17 y estos se encuentran hundidos en la hipodermis. La hipodermis posee tres a cinco capas de células, de tipo multiforme y con esclereidas. El parénquima clorofílico tiene como promedio tres capas de células de bordes replegados, seguido de varias capas de células del tejido parénquima de transfusión. El tipo de canal resinífero es endonales dentro del parénquima clorofílico, en ocasiones llega al parénquima de transfusión (Pérez-del Valle et al., 2020).
Para P. caribaea hasta el momento el factor de estudio que ha prevalecido es la influencia del ecótopo sobre la anatomía foliar (Pérez-del Valle et al., 2020, Geada-López et al., 2021), la posición en el árbol no se ha abordado y la variabilidad bajo este factor puede ser indicador de la madures del individuo, del rodal y las potencialidades de producción de resina. El estudio se plantea como hipótesis que la altura a la que se desarrolla la acícula en el árbol influye en sus características anatómicas y morfológicas. Teniendo en cuenta que en otras especies del género Pinus se ha demostrado esta variabilidad se plantea como objetivo de este trabajo caracterizar la variación anatómica de las acículas de Pinus caribaea var. caribaea en función su posición altitudinal en el árbol.
MATERIALES Y MÉTODOS
Muestreo
Las muestras fueron tomadas de 30 árboles de un rodal de P. caribaea ubicado en áreas de la estación experimental de Viñales, provincia Pinar del Río, Cuba. Se recolectaron acículas en la parte inferior, media y alta de individuos jóvenes de aproximadamente tres metros de altura.
Variables
Para las mediciones anatómicas se realizaron cortes transversales en la parte media de la acícula. Se midieron con un aumento de 100x las siguientes estructuras: el grosor del parénquima clorofílico (GPc), el grosor del parénquima de transfusión (GPt), la altura del tejido de conducción (ATC) y el ancho del tejido de conducción (LTC), el número de estomas (NE) y el número de canales (NC); y con aumento de 400x: el grosor de la cutícula (GC), el grosor de epidermis (GEp), el grosor de hipodermis (GHp) y el número de capas de células de la hipodermis (NCHp),
Análisis estadístico
Se determina el efecto del factor posición de la acícula en la copa, con tres niveles: alto (A tercio superior de la copa), bajo (B, tercio inferior) y medio (M la parte central de la copa). Para esto se realizó un análisis de varianza por rangos de Kruskal-Wallis (α = 0,05) y una prueba de comparación múltiple de pares entre las medias de los rangos de los tratamientos, según lo descrito en Conover (1999), ya que los datos no se ajustaron a una distribución normal.
Se empleó el análisis de discriminantes en el que se asume como grupos a priori las tres zonas donde se colectaron las acículas alto (A), medio (M) y bajo (B) con el objetivo maximizar las diferencias de la anatomía foliar, así como distinguir las variables que más contribuyen a diferenciación. El análisis estadístico se realizó con el programa InfoStat v.2015.
RESULTADOS
Caracterización anatómica de las acículas según su posición en la copa
En la Tabla 1, se presentan los valores medios de la variable anatómica y su desviación estándar de acuerdo a la posición en la copa. Este factor tiene efecto significativo, según la prueba de Kruskal-Wallis (P<0,05), sobre las variables número de estomas, el número de células de la hipodermis, el grosor del parénquima de transfusión y el largo del tejido de conducción (Tabla 1).
Tabla 1. - Valores medios y desviación estándar de las variables anatómicas evaluadas de Pinus caribaea en tres posiciones del árbol
| Variable | A | M | B | H | P | ||||||
| NC | 2,17 | ± | 0,53 | 2,03 | ± | 0,18 | 2 | ± | 0 | 0,47 | 0,16 |
| NE | 15,43 | ± | 2,87B | 13,13 | ± | 2,24A | 12,27 | ± | 2,02A | 18,6 | 0,00 |
| GC | 0,73 | ± | 0,33 | 0,73 | ± | 0,33 | 0,78 | ± | 0,3 | 0,68 | 0,71 |
| GEp | 15,48 | ± | 2,68 | 15,11 | ± | 3 | 14,48 | ± | 1,99 | 2,08 | 0,35 |
| GHp | 41,35 | ± | 10,47 | 39,59 | ± | 7,9 | 37,98 | ± | 9,63 | 2,17 | 0,33 |
| NCHp | 2,63 | ± | 0,72B | 2,1 | ± | 0,76A | 1,93 | ± | 0,87A | 10,28 | 0,00 |
| GPc | 109,67 | ± | 15,34 | 105,74 | ± | 18,09 | 105,53 | ± | 18,04 | 1,73 | 0,42 |
| GPt | 129 | ± | 19,26B | 121,35 | ± | 14,19AB | 112,44 | ± | 19,15A | 9,62 | 0,00 |
| ATC | 248,55 | ± | 49,64 | 252,13 | ± | 52,11 | 238,68 | ± | 59,74 | 1,52 | 0,46 |
| LTC | 506,71 | ± | 69,42B | 480,14 | ± | 81,8AB | 439,28 | ± | 87,18A | 10,78 | 0,00 |
NC: Número de canales, NE: Número de estomas, GC. Grosor de cutícula, GEp: Grosor de epidermis, GHp: Grosor de hipodermis, NCHp: Número de células de la hipodermis, GPc: Grosor del parénquima clorofílico, GPt: Grosor del parénquima de transfusión, ATC: Ancho del tejido de conducción, LTC: Largo del tejido de conducción. Posición A-alta, B-bajo, M-medio
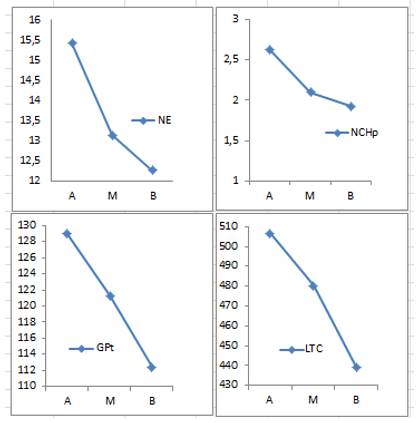
En la Figura 1, se representa la tendencia del comportamiento en las variables en las que la posición de la acícula en la copa tuvo un efecto significativo para un a< 0,05 en la prueba de Kruskal Wallis (Figura 1).
Diferenciación anatómica entre las posiciones de las acículas en el árbol
En la Tabla 2, se presentan los resultados del análisis de discriminante, las dos funciones que se obtienen del análisis permitieron explicar el 100 % de las variaciones entre los tres grupos definidos a priori(Tabla 2).
Tabla 2. - Resultado del análisis de discriminante, coeficientes estandarizados de cada variable y centroides de las tres posiciones de P. caribaea en las dos funciones discriminantes
| Función | |||
|---|---|---|---|
| 1 | 2 | ||
| Autovalores | 0,57 | 0,05 | |
| % | 91,34 | 8,66 | |
| % acumulado | 91,34 | 100 | |
| Variables | Coeficientes estandarizados | ||
| Número de canales | 0 | 0,26 | |
| Número de estomas | -0,78 | 0,35 | |
| Grosor de cutícula | 0,31 | 0,02 | |
| Grosor de epidermis | -0,02 | -0,39 | |
| Grosor de hipodermis | 0,17 | -0,32 | |
| Número de células de la hipodermis | -0,63 | 0,61 | |
| Grosor del parénquima clorofílico | 0,27 | 0,46 | |
| Grosor del parénquima de transfusión | -0,15 | -0,72 | |
| Ancho del tejido de conducción | 0,08 | -0,39 | |
| Largo del tejido de conducción | -0,17 | -0,41 | |
| Centroides | |||
| Grupo (Posición en la copa) | Eje 1 | Eje 2 | |
| Tercio superior (A) | -1 | 0,1 | |
| Tercio inferior (B) | 0,79 | 0,21 | |
| Parte central (M) | 0,21 | -0,32 | |
De acuerdo a los coeficientes estandarizados las variables más importantes en la discriminación entre las tres posiciones son, en la primera función el número de estomas y número de células de la hipodermis. En la segunda el grosor de epidermis y el grosor del parénquima de transfusión.
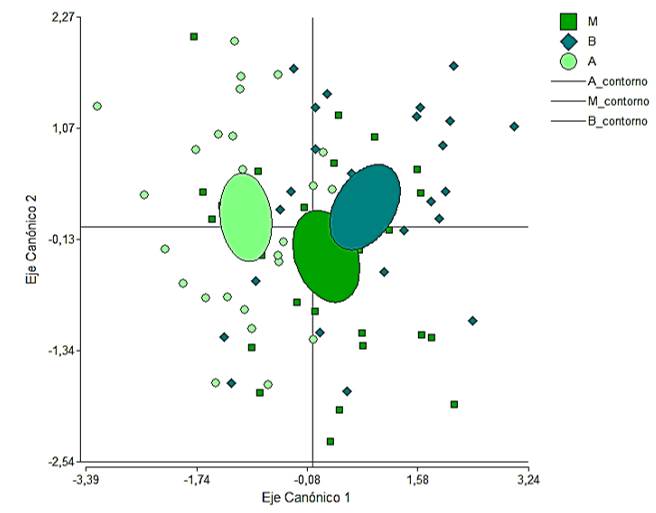
De acuerdo a los valores de los centroides y la ubicación en el plano definido por las dos funciones discriminantes (Figura 2), hay mayor diferenciación en la anatomía de las acículas colectadas en la parte superior de la copa con respectos a las otras dos, que, aunque bien definidas tienen cierto grado de solapamiento.
 NC: Número de canales, NE: Número de estomas, GC. Grosor de cutícula, GEp: Grosor de epidermis, GHp: Grosor de hipodermis, NCHp: Número de células de la hipodermis, GPc: Grosor del parénquima clorofílico, GPt: Grosor del parénquima de transfusión, ATC: Ancho del tejido de conducción, LTC: Largo del tejido de conducción.
NC: Número de canales, NE: Número de estomas, GC. Grosor de cutícula, GEp: Grosor de epidermis, GHp: Grosor de hipodermis, NCHp: Número de células de la hipodermis, GPc: Grosor del parénquima clorofílico, GPt: Grosor del parénquima de transfusión, ATC: Ancho del tejido de conducción, LTC: Largo del tejido de conducción.Fig. 2. - Agrupación de las posiciones en las dos primeras funciones discriminantes, basado en variables anatómicas de Pinus caribaea representadas en tres grupos a priori. Los contornos corresponden a elipses de predicción al 95 % de probabilidades
Lo anterior se confirma en la Tabla 3, donde se presenta la clasificación de cada caso según las funciones discriminantes obtenidas. Se muestra que hay mayor indefinición en cuanto a las diferencias anatómicas (error 60 %) de las acículas entre la parte media, sobre todo con respecto a la parte inferior de la copa (Tabla 3).
DISCUSIÓN
Variación anatómica de las acículas de acuerdo a la posición en la copa
La variabilidad anatómico morfológica que se observan en una especie pueden estar determinadas por variaciones geográficas, climáticas, de sitio, entre árboles de un mismo sitio y hasta variaciones dentro de un mismo árbol (Cattuse 1991).
La variación anatómica de las acículas en las tres posiciones en la copa del árbol que se estudiaron se ve reflejada principalmente por cuatro variables: número de estomas, número de células de la hipodermis, grosor del parénquima de transfusión y largo del tejido de conducción, todas vinculadas a procesos de regulación hídrica y sostén como es el caso del tejido de conducción.
Geada-López et al. (2022) reporta que la especie P. caribaea en comparación con Pinus tropicalis puede desarrollar mayor número de estomas, mayor número de células de la hipodermis y mayor grosor del tejido de transfusión como respuesta a diferencias en las condiciones ambientales.
En este estudio se confirma en las cuatro variables de la anatomía de la acícula en que se comprobó efecto estadístico significativo de la posición en la copa, un ligero aumento de sus valores hacia la parte superior, que es la más expuesta al efecto desecante del viento y a la luz, estas características ayudan a evitar el colapso de los elementos del haz vascular en condiciones de pérdida de turgencia (Larcher 2003, Grill et al., 2004) , comportamiento comprobado en la anatomía de P. canariensis cuando se somete a ensayos de sequía (Grill et al., 2004) y entre pruebas de procedencias establecidas en lugares secos y xéricos (López-Rodríguez 2009). Sin embargo, Dörken y Stützel (2012) plantean que comúnmente se asume que los representantes de Pinus subg. Diploxylon tienen dos haces vasculares, cuando estos en realidad son un único haz separado por bandas de células de parénquima que pueden ser más o menos numerosas y lignificadas o no. Cambios en el tamaño de esta estructura parecen estar relacionados con la disponibilidad de agua en el suelo (Boratyñska et al., 2011, 2015b, Ghimire et al., 2014).
En el estudio se comprobó que en la parte alta de la copa además de aumentar el número de células de la hipodermis también hay un pequeño incremento en el grosor de hipodermis (Tabla 1), aunque es necesario aclarar que el aumento del grosor de la hipodermis no siempre está acompañado con un mayor número de capas de célula de la hipodermis, aunque ambas características, regulan las pérdidas de agua, en especial si se acompaña de esclereidas como elemento del tejido de sostén (Grill et al., 2004). Nikoliæ et al., (2014 y Nikoliæ et al., 2019) en estudios de las poblaciones naturales de Pinus heldreichii en los Balcanes reportaron que, hacia sitios más secos, debido a la pendiente y el sustrato, el grosor de la hipodermis y cutícula eran mayores, pero con un menor número de capas de la hipodermis.
El parénquima de transfusión tiene sus valores más altos en la parte alta, donde es necesaria una mayor reserva de agua, pues estas acículas van a estar más expuestas a la radiación solar. López et al. (2010) plantean que este comportamiento es común donde es necesario almacenar gran cantidad de agua junto a materiales de reserva, pues representa un ahorro en la síntesis de compuestos y almacén de metabolismos bajo estas condiciones (López-Rodríguez 2009, Esteban et. al. 2010). Esta característica es ventajosa para plantas que experimentan períodos prolongados de estrés hídrico ya que permite mantener vivos los tejidos de la hoja ante prolongadas sequías (López et al., 2010, Hodžiæ et al. 2020).
Existe además muy poca variación respecto al número de canales, solamente se observa un pequeño aumento hacia la parte alta, la cual se comporta como la parte más seca debido a las fuertes exposiciones al sol y al viento. En estudios preliminares se ha detectado que la mayor densidad de canales se asocia a áreas de menor disponibilidad de humedad (Jankowski et al. 2017, Jankowski et al. 2019) y su incremento en número y tamaño está correlacionado en Pinus yunnanensis con disminuciones de la precipitación y aumento de la temperatura, que contribuyen a reducir la influencia de la extrema sequía y el calor (Huang et al. 2016).
En la Figura 2, resultado del análisis de discriminantes, se puede observar que las acículas de la parte alta de la copa se distinguen de las colectadas en las otras dos posiciones, dicha disyunción está dada por la influencia de las variables ambientales a las que están sometidas las acículas según su posición, pues los factores ambientales tienen una influencia directa en la estructura de los tejidos de la acícula, en el patrón y posición de los estomas, el número y tamaño de los conductos de resina, en especial para las especies del género Pinus(Twari et al., 2013, Ghimire et al., 2014, (Meng et al., 2018, el grosor de parénquima de transfusión y área del mesófilo (Meng et al., 2018, Huang et al., 2016, Köbölkuti et al., 2017).
El análisis de discriminante destaca en la primera función las variables número de estomas y número de células de la hipodermis como las variables más importantes, desviándose hacia el cuadrante negativo de la Figura 2, cuyas acículas se desarrollan en un ambiente de más alta intensidad lumínica y menor humedad relativa.
Dörken y Stützel (2012) y Grill et al., (2004) describen que las especies de Pinus que se desarrollan en ambientes extremos, generalmente desarrollan una cutícula prominente, gruesa y una hipodermis conformada por varias capas de células gruesas de forma circular. Sin embargo, P. caribaea desarrolla mayor número de capas y grosor de la hipodermis (tipo multiforme) como adaptación a iguales condiciones. Kivimäenpää et al., 2017 plantea que una especie adaptada a hábitats soleados puede tener un tejido del mesófilo más grueso y una mayor densidad estomática para alcanzar mayores rendimientos fotosintéticos. Esto también explica las diferencias enmarcadas entre la posición Alta con respecto a la Baja y la posición Medio.
Con respecto a la segunda función de discriminante la mayor importancia corresponde al parénquima de transfusión, cuyo tejido está presente solo en las coníferas, en especial en el género Pinus(Canny 1993 y Liesche et al., 2011) cuya función es almacenar gran cantidad de agua, pero que además tiene un complejo mecanismo de funcionamiento post-xylema, pre-floema que transporta agua, nutrientes minerales junto a fotoasimilatos simples (Canny 1993, Liesche et al., 2011) que en caso de ser necesario emplean una vía simplástica para llevar energía al tejido de asimilación.
Al respecto López et al., (2010) y Liesche et al., (2011) plantean que en condiciones ecológicas de sequía o xéricas el desarrollo de un tejido de transfusión grueso significaría, además, una ventaja con el almacenamiento de agua y un ahorro en la síntesis de compuestos (López et al., 2010, Esteban et al., 2010, Hodžiæ et al., 2020).
Implicaciones en la silvicultura
Hasta el momento muchos de los estudios desarrollados están dirigidas principalmente hacia la selección de árboles con capacidades superiores en producción, e identifican el número adecuado de individuos con la suficiente variabilidad genética (Barrett, 1980). La caracterización de la variabilidad anatómica a lo largo del fuste del árbol de P. caribaea puede ser un indicador de las potencialidades para la producción de resina. Sin embargo, son pocos los estudios que han abordado las relaciones entre la producción de resina y los aspectos ecológicos y climáticos donde crecen los árboles (Reyes-Ramos et al., 2019, Abdillah et al., 2020, Rodríguez-García et al., 2015).
Este estudio no va dirigido directamente a la producción de resina, independientemente de que la especie P. caribaea se encuentra dentro los planes de resinación del país, sino que se enfoca hacia la importancia de conocer el sitio dentro del árbol donde cabría encontrar la mayor cantidad de canales. Para esto el conocimiento de la variación anatómica de la acícula facilita diagnosticar la capacidad de producción neta de la especie conociendo que el número y tamaño de canales resiníferos están relacionados con el flujo de resina (Westbrook et al., 2015). Por ejemplo, Reyes-Ramos et al., (2019) demostraron la relación entre la temperatura y la producción de resina en P. oocarpa, entonces las acículas en la parte superior de la copa están expuestas a mayor radiación solar y temperatura, por ende, la producción de resina tendría a ser mayor. En este sentido, identificar la existencia de diferencias en los canales y de dimensiones en los tejidos es crucial, para estimar la producción de resina.
La característica anatómica foliar es un punto a tener en cuenta no solo a la hora de obtener grandes resultados en la producción con fines económico sino también en la selección del material de propagación, de modo que la variación en cuanto a dimensiones de las variables estudiadas, pudiese estar vinculado a estrategias del sistema de defensa de las coníferas para hacer frente a distintas perturbaciones bióticas y abióticas, que integran una respuesta compleja de defensa a corto y largo plazo.
CONCLUSIONES
En la especie Pinus caribaea var caribaea existe variación en la anatomía de la acícula determinada por la posición de la misma en la copa, se manifiesta un aumento del grosor de los tejidos de protección hacia la parte superior. Las variables que más contribuyen a diferenciar las acículas según la posición en el árbol son el número de estomas y el número de células de la hipodermis.











 texto em
texto em