Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Cirugía
versión On-line ISSN 1561-2945
Rev Cubana Cir v.47 n.3 Ciudad de la Habana sep.-dic. 2008
ORIGINAL
Valoración manométrica del esófago de pacientes operados de acalasia mediante cirugía laparoscópica
Manometric assessment of the esophagus in patients operated on of achalasia by laparoscopic surgery
Daisy Naranjo Hernández,I I. García Freyre,II A. Fernández Zulueta,III V. Anido Escobar,IV F. Verdecia Fernández,V B. Pascau IllasVI
I Especialista de II Grado en Fisiología Normal y Patológica. Investigadora Auxiliar. Instituto de Gastroenterología. Centro de Cirugía Endoscópica. Hospital «Calixto García». La Habana, Cuba.
II Doctora en Ciencias Médicas. Especialista de II Grado en Fisiología Normal y Patológica. Profesora Consultante. Instituto de Gastroenterología. Centro de Cirugía Endoscópica. Hospital «Calixto García». La Habana, Cuba.
III Especialista de II Grado en Cirugía Laparoscópica. Instituto de Gastroenterología. Centro de Cirugía Endoscópica. Hospital «Calixto García». La Habana, Cuba.
IV Especialista de II Grado en Gastroenterología. Instituto de Gastroenterología. Centro de Cirugía Endoscópica. Hospital «Calixto García». La Habana, Cuba.
V Doctor en Ciencias Médicas Especialista de II Grado en Higiene y Administración de Salud Pública. Profesor Titular. Instituto de Gastroenterología. Centro de Cirugía Endoscópica. Hospital «Calixto García». La Habana, Cuba.
VI Licenciada en Enfermería. Instituto de Gastroenterología. Centro de Cirugía Endoscópica. Hospital «Calixto García». La Habana, Cuba.
RESUMEN
INTRODUCCIÓN. La acalasia esofágica es un trastorno motor primario con ausencia de peristaltismo e incapacidad de relajación del esfínter esofágico inferior. El presente estudio tuvo como objetivo comparar la evolución clínica y las características manométricas del esófago de pacientes con acalasia esofágica, antes y después cirugía laparoscópica.
MÉTODOS. Se realizó un estudio prospectivo descriptivo con 17 pacientes (6 del sexo masculino y 11 del femenino), con edad comprendida entre 38 y 70 años y diagnóstico radiológico y endoscópico de acalasia esofágica, confirmado por estudio manométrico. Posteriormente, estos pacientes fueron sometidos a tratamiento quirúrgico, mediante esofagocardiomiotomía de Heller con funduplicatura antirreflujo de Dor o Toupet, por videolaparoscopia de forma aleatoria. A todos se les realizó manometría esofágica evolutiva entre los 6 y 18 meses después de la operación.
RESULTADOS. Se encontró notable mejoría clínica en todos los pacientes, aunque persistió una disfagia ocasional mínima a sólidos en el 64,7 % y dolor retroesternal ligero en el 47 %. La presión del esfínter esofágico inferior disminuyó de X= 47,7 mm Hg a X= 17,5 mm Hg (p < 0,01). La relajación del esfínter esofágico inferior aumentó de X= 59 % a X= 75,5 %. (p < 0,01). La presión intraesofágica se normalizó en el 70,6% de los casos, (p < 0,05). Persistió el aperistaltismo en los pacientes operados y asimetría del esfínter esofágico inferior en el 82,4%.
CONCLUSIONES. Tras la valoración clínica y manométrica, se consideraron satisfactorios los resultados de la cirugía laparoscópica en el grupo estudiado.
Palabras clave: Nanometría, esófago, cirugía laparoscópica.
ABSTRACT
INTRODUCTION. Esophageal achalasia is a primary motor disorder with abscence of peristaltism and incapacity for relaxation of the lower esophageal sphincter. The present study was aimed at comparing the clinical evolution and manommetric characteristics of the esophagus of patients with esophageal achalasia before and after laparoscopic surgery.
METHODS. A prospective descriptive study was conducted in 17 patients (6 males and 11 females) aged 38-70 with radiological and endoscopic diagnosis of esophageal achalasia confirmed by manometric study. Later on, these patients underwent surgical treatment by Heller esophagocardiogram with Toupet or Dor's antireflux funduplication by randomized video-assisted laparoscopy. Evolutive esophageal manometry was performed in all of them between 6 and 18 months after surgery.
RESULTS. A marked clinical improvement was found in all the patients, although a minimal occasional dysphagia to solids persisted in 64.7 %, and mild retrosternal pain in 47 %. The pressure of the lower esophageal sphincter decreased from X= 47.7 mm Hg to X= 17.5 mm Hg (p < 0.01).The relaxation of the lower esophageal sphincter increased from X= 59 % to X= 75.5 %. (p < 0.01).The intraesophageal pressure was normal in 70.6 % of the cases, (p < 0.05). Aperistaltism persisted in the operated on patients and the asymmetry of the esophageal sphincter in 82.4.
CONCLUSIONS. The results of laparoscopic surgery in the studied group were considered satisfactory after the clinical and manometric assessment..
Key words: Nanometry, esophagus, laparoscopic surgery.
INTRODUCCIÓN
La acalasia esofágica es un trastorno primario de la motilidad, caracterizado por ausencia de peristaltismo del cuerpo esofágico e incapacidad del esfínter esofágico inferior (EEI) para relajarse en respuesta a la deglución. Todo esto conlleva a la retención de alimentos en la luz del esófago y a la progresiva dilatación de este, lo cual ocasiona la mayor parte de los síntomas y complicaciones.
Los síntomas más frecuentes son la disfagia, regurgitaciones, dolor retroesternal, pérdida de peso y en algunas ocasiones complicaciones pulmonares y aumento de secreciones esofágicas espesas o espumosas, producidas por la fermentación de la comida retenida en el esófago.1,2
Aunque se han descrito lesiones en el tallo cerebral y en el nervio vago de los pacientes con acalasia, la hipótesis actual sobre su patogenia plantea que existe una pérdida selectiva de las neuronas inhibidoras acompañada de un infiltrado inflamatorio; se trata de una «neuronitis nitrinérgica» del plexo mientérico, con predominio de la excitación selectiva mediada por los nervios colinérgicos. El resultado neto es que el esfínter no se relaja, está hipertónico y esta función alterada del EEI es el rasgo cardinal de la acalasia.2-6 Además, existen evidencias que sugieren etiología viral, autoinmunitaria o hereditaria.7
El diagnóstico se puede sospechar por la sintomatología, pero generalmente se requieren pruebas complementarias que lo confirmen. La confirmación suele hacerse por manometría esofágica, que es la técnica de elección para el estudio de la acalasia, ya que hace el diagnóstico incluso en estadios precoces y es imprescindible en el diagnóstico diferencial de los trastornos motores del esófago.8
Los criterios manométricos en la acalasia son:
· Presión de reposo del EEI normal o elevada.
· Relajaciones del EEI incompletas (< 80 %) o ausentes.
· Presión basal del cuerpo esofágico elevada (igual o superior a la intragástrica).
· Aperistaltismo del cuerpo esofágico.
· Presencia de contracciones vigorosas no peristálticas en caso de acalasia vigorosa.
Las alternativas de tratamiento disponibles en la actualidad incluyen: tratamiento farmacológico, dilataciones, métodos nuevos mediante endoscopia y cirugía, todos encaminados a disminuir la presión de reposo del EEI.7,10-12
La sección quirúrgica de las fibras musculares del EEI (esofagocardiomiotomía) es el método más directo de tratar la acalasia. Esta técnica mediante laparoscopia o videolaparoscopia es muy utilizada actualmente, y ofrece buenos resultados en manos expertas y ventajas sobre la cirugía convencional: es menos invasora, requiere menor tiempo de hospitalización y de recuperación, produce menos incomodidad y menos complicaciones para el paciente.13-16
A pesar de que tradicionalmente la cirugía había sido reservada para los pacientes con disfagia residual, después de dilatación neumática, en la actualidad la mayoría de los expertos consideran a la cirugía como el tratamiento primario en esta enfermedad.13
En los últimos años diferentes autores han reportado resultados exitosos con el empleo de la cirugía laparoscópica (técnica de Heller y funduplicatura antirreflujo) en pacientes con acalasia esofágica.7,17-19
La manometría intra y posoperatoria en la acalasia aporta detalles sobre la motilidad del esófago y, en los pacientes en que los síntomas persisten, se encontrarán las alteraciones del EEI, lo que permite valorar los resultados de la técnica quirúrgica y el pronóstico en cada caso.20-22
El objetivo general del presente estudio fue comparar la evolución clínica y las características manométricas del esófago, en pacientes con acalasia esofágica antes y después de ser sometidos a cirugía laparoscópica. Específicamente se buscó evaluar los cambios producidos en el EEI y el cuerpo esofágico en estos mismos pacientes, después de la esofagocardiomiotomía de Heller con funduplicatura antirreflujo, y compararlos con los resultados reportados en la literatura médica.
MÉTODOS
Se realizó un estudio prospectivo descriptivo con 17 pacientes, 6 del sexo masculino y 11 del sexo femenino, con edad comprendida entre 38 y 70 años (X = 51,7), los cuales acudieron a nuestra Sección de Motilidad Digestiva con diagnóstico radiológico y endoscópico de acalasia esofágica, que fue confirmado por estudio manométrico en todos los casos.
Antes de la realización de la prueba, todos los pacientes fueron entrevistados, y se recogieron sus datos generales, los resultados de la radiografía esofágica de la endoscopia superior y se exploraron cuidadosamente los síntomas clínicos de cada uno de ellos.
Posteriormente, estos pacientes se sometieron a tratamiento quirúrgico, mediante esofagocardiomiotomía de Heller con funduplicatura antirreflujo de Dor o Toupet, por videolaparoscopia de forma aleatoria.
A todos se les hizo manometría esofágica evolutiva entre los 6 y 18 meses después de la operación. El día de este estudio fueron nuevamente interrogados sobre sus síntomas clínicos y el grado de bienestar experimentado en cada caso.
Las pruebas manométricas se realizaron mediante un sistema de perfusión continua de agua destilada, acoplado a transductores externos, empleando un catéter de registro con 4 orificios orientados radialmente, el cual transmite las variaciones de presión intraesofágica hacia los transductores. Este sistema está conectado a un polígrafo (PC Polygraf HR), el cual procesa y transforma las señales que son enviadas hacia una computadora con programa de análisis para manometría esofágica.
Se valoraron la motilidad esofágica y las presiones esfinterianas, tanto en reposo, como en respuesta a la deglución de volúmenes de 5 mL de agua a temperatura ambiente y en intervalos de 30 s. Las variables manométricas estudiadas en cada paciente, antes y después del tratamiento quirúrgico, fueron las siguientes:
· Presión de reposo del EEI.
· Presión residual y porcentaje de relajación del EEI en respuesta a la deglución.
· Simetría del EEI (presión detectable en los 4 canales de registro).
· Porcentaje de peristaltismo normal en el cuerpo esofágico.
· Características de la presión intraesofágica.
· Presión de reposo y residual del esfínter esofágico superior (EES).
Nuestros resultados se expresaron en tablas y gráficos, y se utilizaron las pruebas estadísticas t de Student para variables cuantitativas y Mc Nemar para análisis de variables cualitativas.
RESULTADOS
Los síntomas más frecuentes que presentaron nuestros pacientes con acalasia fueron: disfagia mixta grave, presente en los 17 casos, hipersecreción esofágica en 14 casos y regurgitaciones y pirosis referidas en 11 pacientes.
Después de la miotomía de Heller con funduplicatura persistió sólo disfagia ligera a sólidos en 11 casos (64,7 %). La hipersecreción esofágica al igual que la pirosis y regurgitaciones fueron observadas en sólo 1 paciente. El dolor retroesternal referido en 9 pacientes, se manifestó en 8 casos (47 %) después de la cirugía. Todos los pacientes recobraron su peso habitual (tabla 1).
Tabla 1. Síntomas clínicos (n = 17)
| Síntomas | Antes de la cirugía | Después de la cirugía | ||
| Disfagia | 17 (mixta) | 100% | 11 (a sólidos) | 64,70% |
| Hipersecreción esofágica | 14 | 82,4% | 1 | 5,9% |
| Regurgitaciones y pirosis | 11 | 64,7% | 1 | 5,9% |
| Dolor retroesternal | 9 | 53,0% | 8 | 47,0% |
| Vómitos | 9 | 53,0% | 1 | 5,9% |
| Pérdida de peso | 5 | 29,4% | 0 | 0% |
Al analizar los estudios manométricos en los casos realizados, encontramos que la presión de reposo del EEI que era de X= 47,7 ± 19,3 mm Hg, disminuyó de forma significativa a X = 17,5 ± 6,9 mm Hg para (p < 0,01) después de la operación.
La presión residual del EEI en respuesta a la deglución de un valor de X= 22,2 ± 13,8 mm Hg, disminuyó después del tratamiento quirúrgico a X= 7,4 ± 4,7 (p < 0,01). Ocurrió lo mismo con el porcentaje de relajación, el cual antes del tratamiento tenía un valor X = 58,9 ± 13,1 % y mejoró después de la cirugía a X = 75,7 ± 16,8 %, (p < 0,01) (tabla 2 y figuras 1 y 2).
Tabla 2. Variables manométricas estudiadas del esfínter esofágico inferior (n = 17)
| Presión de reposo | Presión residual | % de relajación | |
| Antes de la cirugía | 47,78 ± 19,32 | 22,27 ± 13,18 | 58,99 ± 13,11 |
| Después de la cirugía | 17,55 ± 6,90 | 7,47 ± 4,71 | 75,72 ± 16,86 |

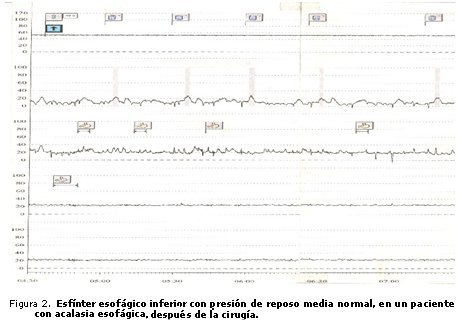
Las variables cuantitativas que se estudiaron del EES, presión de reposo y presión residual no presentaron variación, antes o después de la operación (tabla 3). Los resultados de las variables manométricas cualitativas estudiadas (tabla 4) fueron los siguientes:
· Antes del tratamiento quirúrgico, 10 pacientes (58,8 %) tenían el EEI simétrico, después de la cardiomiotomía se demostró simetría esfinteriana en sólo 3 casos (17,7 %) para una (p < 0,05).
· La presión intraesofágica antes de la cirugía estaba elevada en 14 pacientes (82,4 %) y normal solamente en 3 (17,7 %). Después del tratamiento quirúrgico, 12 pacientes (70,6 %) mostraron presión intraesofágica normal y en 5 de ellos (29,4 %) se mantuvo elevada (p < 0,05).
Tabla 3. Variables manométricas estudiadas del esfínter
esofágico superior (n = 17)
| Presión de reposo | Presión residual | |
| Antes de la cirugía | 62,11 ± 32,49 | - 2,23 ± 5 |
| Después de la cirugía | 52,98 ± 27,61 | -2,86 ± 4,3 |
Tabla 4. Variables manométricas cualitativas estudiadas (n = 17)
| Simetría del EEI | Presión intraesofáagica | Peristaltismo | ||||
| Simétricos | Asimétricos | Normal | Elevada | Ausente | Presente | |
| Antes de la cirugía | 10 | 7 | 3 | 14 | 17 | 0 % |
| Después de la cirugía | 3 | 14 | 12 | 3 | 14 | 3 |
En todos los pacientes estudiados (100 %) el peristaltismo esofágico estaba ausente antes del tratamiento quirúrgico (figura 3) y después de este se observó la recuperación de menos del 8 % de peristalsis normal en 3 casos; persistió el aperistaltismo en la mayoría (14 pacientes operados; 82,4 %).

DISCUSIÓN
En la revisión de la literatura se señala que la disfagia mejora en aproximadamente el 90 % de los pacientes después de la cirugía laparoscópica. Sin embargo, muchos autores han reportado en sus series quirúrgicas, la persistencia de disfagia que puede ser grave o ligera y plantean como posibles causas de esta disfagia residual ocasional, una miotomía incompleta, de corta longitud o una funduplicatura apretada.23-26
Otros argumentan que la persistencia de la disfagia puede ser mayor en aquellos pacientes con disfagia preoperatoria grave.27 Esto último es lo que sucedía a nuestros pacientes, quienes padecían una acalasia clásica, con disfagia a sólidos y líquidos, persistente y de grave intensidad, lo que podría explicar en parte, la ocurrencia de este síntoma de forma ocasional en nuestros casos operados. Por otra parte, no podemos olvidar que el aperistaltismo esofágico se mantiene, con lo cual persiste por tanto un grave daño a la capacidad de propulsión del alimento a través del cuerpo esofágico.
Los síntomas de reflujo gastroesofágico (RGE), tales como las regurgitaciones y la pirosis, se manifestaron en 1 solo paciente después de la cirugía, lo que representa una mejoría significativa, que se explica por la disminución de los alimentos retenidos en el esófago y la efectividad de la técnica antirreflujo empleada en estos pacientes. Este hecho coincide con lo señalado por algunos autores, que plantean además que no existe relación directa con el tipo de funduplicatura utilizada. Incluso algunos obtienen un bajo riesgo de padecer RGE si en el acto quirúrgico no se emplea un método contra el reflujo.20,28,29
Se considera que los síntomas principales de la acalasia, antes de la gran dilatación del esófago, son la disfagia y el dolor retroesternal. Por cierto, cuando además existe pirosis, este último en ocasiones hace sospechar la existencia de una enfermedad por reflujo (ERGE), lo cual retarda el diagnóstico de acalasia y permanece no muy clara la etiología de los síntomas.30
El dolor retroesternal persistió en 8 operados (47 %), 3 de los cuales presentaban algunas contracciones esporádicas en el cuerpo esofágico, algo intensas, cuando se realizó la manometría posquirúrgica. Este hecho pudiera explicar el dolor torácico de tipo espasmódico que ellos padecieron. Sin embargo, no se puede explicar tal persistencia en los otros 5 pacientes con igual sintomatología.
De la misma forma, otros trabajos, como el de Perretta y otros1 reportan la persistencia del dolor torácico en sus pacientes operados (11 %) y afirman que el efecto de la miotomía de Heller sobre este síntoma es desconocido. En otras casuísticas, se reporta la existencia de dolor torácico en algunos casos después de cirugía laparoscópica, sin asociación con RGE anormal.31
Como es conocido, desde el siglo XVII cuando Sir Thomas Willis32 utilizó un hueso de ballena para dilatar el esófago en un paciente con acalasia, todos los esfuerzos terapéuticos se han centrado en el EEI, mediante dilataciones, fármacos o cirugía, con el objetivo fundamental de disminuir la presión de reposo esfinteriana, facilitar el vaciamiento esofágico y de este modo reducir los síntomas ocasionados por la retención de alimentos y la dilatación del cuerpo esofágico.
En nuestros pacientes se comprobó que la presión media de reposo del EEI descendió significativamente después de la cirugía a un valor de 17,55 mm Hg, considerado como normal. Este resultado coincide con lo encontrado por la mayoría de los autores en sus casos sometidos a miotomía con proceder antirreflujo o sin él, en los cuales ha disminuido la presión del EEI. Se plantea que para considerar la cirugía como exitosa, esta disminución debe estar dentro del rango normal para el EEI (14 a 35 mm Hg), como sucedió en nuestro casos.26
Otros como Sharp y colaboradores23 sostienen que la presión del esfínter debe caer a menos de 18 mm Hg para lograr un mejor alivio de la disfagia. Por otra parte, algunos criterios indican que en los pacientes operados con presión del EEI con valores por debajo de 10 mm Hg, la peor complicación es el RGE, en más de la mitad de los casos, en los primeros 10 años después de la miotomía y que la incidencia disminuye cuando se realiza técnica antirreflujo.6
También se plantea que los mejores resultados se obtienen cuando se logra llevar la presión del EEI a este valor, realizando miotomía gástrica extendida unos 2 a 3 cm por debajo de la UGE.21,22,27 De ello se puede deducir que los valores bajos de presión de reposo del EEI después de la cirugía aseguran un mejor alivio de la disfagia posoperatoria, pero a su vez constituyen un índice de peor pronóstico a largo plazo para la aparición del RGE patológico.
La presión residual y el porcentaje de relajación del EEI en nuestros operados mejoraron de forma significativa, al igual que reportan otras series quirúrgicas.14 Sin embargo, los valores no llegaron a los normales, ya que el tratamiento quirúrgico no puede restablecer el déficit de neurotransmisores inhibitorios (VIP, óxido nítrico) que existe en la acalasia y que intervienen en la fase relajatoria de la musculatura lisa.
Analizando las variables cualitativas, encontramos que después de la miotomía, el EEI resultó asimétrico en 14 casos (82,4 %), 7 de los cuales tenían su esfínter asimétrico antes y 4 habían sido dilatados previamente mediante dilatación forzada de Stara. Esta maniobra puede conllevar a un mayor daño de las fibras musculares del esfínter, antes de la miotomía, y trae como consecuencia una mayor asimetría posquirúrgica.
De acuerdo con los resultados manométricos, en 12 pacientes operados la presión intraesofágica retornó a valores normales. La literatura médica señala que en la mayoría de los sujetos sometidos a miotomía por acalasia, la presión del esófago disminuye, lo cual indica la desaparición del obstáculo mecánico al flujo esofágico de los alimentos.
Consideramos que no es significativa la escasa recuperación del peristaltismo de menos de un 8 % observada en 3 de nuestros pacientes, a pesar de que este hallazgo ha sido descrito por algunos autores, los cuales explican que estas contracciones probablemente ya existían antes de la cirugía y no eran detectadas en el estudio manométrico, debido a la dilatación del esófago. Estos autores concluyen que el mecanismo de producción de este posible fenómeno de recuperación de la peristalsis en algunos casos aislados es desconocido.33,34
El estudio manométrico del EES no mostró datos de interés, al no encontrarse cambios en las variables estudiadas antes y después de la cirugía, tampoco se relacionaron con los hallazgos clínicos encontrados en nuestros pacientes.
La mayoría de los autores coinciden en señalar, que la miotomía de Heller con funduplicatura antirreflujo por vía laparoscópica, supone una incomodidad considerablemente menor para el paciente; disminuye la morbilidad, el dolor posoperatorio y los períodos prolongados de hospitalización. Es una técnica menos invasora, con reducción de la mortalidad inmediata, por lo que se considera en la actualidad el tratamiento primario y de elección para la acalasia esofágica y queda atrás el criterio de que debía ser empleada en los pacientes con disfagia residual después de dilatación neumática.
REFERENCIAS BIBLIOGRÁFICAS
1. Perretta S. Achalasia and chest pain: effect of laparoscopic Heller myotomy. J.Gastrointest Surg. 2003. Jul-Aug;7(5 ):595-8.
2. Pasricha P.J. Algoritmo terapéutico actual en la acalasia del cardias. Curso de Posgrado. 2000.
3. Aggestrup S, Uddman R, Sundler F. Lack of vasoactive intestinal polypeptide nerves in esophageal achalasia. Gastroenterology. 1983;84:924-7.
4. Watanabe V, Audo H, Seo T, Katsuno S, Marui V. Attenuated nitrinerging inhibitory neurotransmission to intersticial cells of Cajal in esophageal Achalasia in children. Pediatr. Int . 2002;44:145-8.
5. Moses PL, Ellis LM, Anees MR. Antinueuronal antibodies in idiopathic Achalasia and gastro-esophageal reflux disease. Gut 2003;52:629-36.
6. Mearin F, Mourelle M, Guarner F. Patients with Achalasia lack nitric oxide synthase in gastro-esophageal junction. Eur J Clin. Invest. 1993;23:724-8.
7. Cacchione RN, Tran D N, Rhoden DH. Laparoscopic Heller myotomy for Achalasia. Am.J. Surg. 2005 Aug; 190(2):191-5.
8. Diaz Rubio M. Trastornos motores del aparato digestivo. Cap 24. México: Editorial Médica Panamericana; 1996. Pp. 69-70.
9. Stendal Ch. Clinical Procedures in Achalasia. Practical Guide to Gastrointestinal Function Testing . 1997;173-4.
10. Pasricha PJ. Achalasia. Are we wining the war or loosing peace? Endoscopy 1997; 28:574-5.
11. Cowgil SM, Villadolid DU, Al Saddi S, Rosemurgy AS. Difficult myotomy is not determined by preoperative therapy and does not impact outcome. J.S.L.S. 2007 Jul-Sept; 11(3 ):336.
12. Zaninotto G, Annese V, Costantini M, Del Genio A, Epifeni M. Randomized controlled of botulinum toxin versus laparoscopic Heller myotomy for esophageal Achalasia. Gastroenterology 2004 Dec; 127(6):1850-2.
13. Kostic S, KjellinA, Ruth M, Johnson E, Anderson M. Pneumatic dilatation or laparoscopic cardiomyotomy in the management in idiophatic achalasia. World J. Surg. 2007 Mar; 31(3):471-8.
14. Chen LQ, Chungtai T, Sideris L, Nastos D, Ferrari P. Long term effects of myotomy and partial fundoplication for Achalasia. Dis Esophagus. 2002;15(2):171-9.
15. Suarez J, Mearin F, Zanon V, Armengol JR, Pradell J, Bermejo B. Laparoscopic myotomy vs endoscopic dilatation in the treatment of Achalasia. Surg Endosc. 2002 Jan;16(1):75-7.
16. Blomston M, Boyce A, Manel J, Albrink M, Murr M, Durkin M. Videoscopic Heller myotomy results beyond short term follow up. J. Surg. Res. 2000;92(2):150-56.
17. Peillon C, Fromont G, Awray S, Serisec F. Achalasia. The case for primary laparoscopic treatment. Surg. Laparosc. Endosc. Percutan. Tech. 2001;11(2):21-5.
18. Patti MG, Molena D, Fisichella PM, Whang K, Yamada H, Perretta S. Laparoscopic Heller myotomy and Dor fundoplication for Achalasia: analysis of successes and failures. Arch Surg 2001 Aug;136(8):870-7.
19. Ferulano GP, Dilillo S, D Ambra M, Lionetti R, Brunacino R. Short and long term results of the laparoscopic Heller-Dor myotomy. Surg. Endosc. 2007. Nov;21(11):2017-23.
20. Oelschlager BK, Chovy L, Pellegrini CA. Improved outcome after extended gastric myotomy for Achalasia. Arch. Surg. 2003;138(5):490-5.
21. Di Martino N, Monaco L, Izzo G, Cozenza A, Torelli F. The effect of esophageal myotomy and myotomy on the lower esophageal sphincter pressure profile: Intraoperative computerized manometric study. Dis. Esophagus. 2005;18(3):160-5.
22. Nussbaum MS, Jones MP, Pritts TA, Fischer DR, Borde J. Intraoperative manometry to assess the esophagogastric junction during laparoscopic fundoplication and myotomy. Surg. Laparosc. Endosc. Percutan Tech 2001;11(5):294-96.
23. Sharp KW, Khaitan L, Scholz S, Holgman MD, Richard WQ. 100 consecutive minimally invasive Heller myotomy: lessons learned. Am. Surg. 2002;235(5):631-8.
24. Zaninotto G, Costantini M, Portale G, Bathaglia G, Molena D. Etiology diagnosis and treatment of failures after laparoscopic Heller myotomy for Achalasia. Am. Surg. 2002;235(2):186-92.
25. Grotenhuis BA, Winhoven BP, Myers JC, Jamienson GG, Devitt PG. Reoperation for dysphagia after cardiomyotomy for Achalasia. Am J Surg. 2007;194(5):678-82.
26. Jeansonne L.O, White B.C, Pilger K.E, Shone M.D, Zagorski S, Davis S.S. Ten years follow-up of laparoscopic Heller myotomy for Achalasia shows durability. Surg Endosc. 2007;21(9):1498-502.
27. Khajanchec YS, Kanmegonti S, Leatherwood AE, Honan PD. Laparoscopic Heller myotomy with Toupet fundoplication: outcomes predictors in 121 consecutive patients. Arch Surg. 2005;140(9):827-33.
28. Villegas L, Rege RV, Jones DB. Laparoscopic Heller myotomy with bolstering partial posterior fundoplication for Achalasia J. Laparoendosc. Adv. Surg Tech A. 2003;13(1):1-4.
29. Diamantis T, Pikoulis E, Felekouras E, Tsigris C, Bastouris E. Laparoscopic esophagomyotomy for Achalasia without a complementary antireflux procedure. J. Laparoendosc. Adv. Surg Tech A. 2006;16(4):345-9.
30. Spiess AE, Karhilas PJ. Treating Achalasia from whalebone to laparoscope. JAMA. 1998;280(7):638-42.
31. Omura N, Kashivvagi H, Tsuboi K, Ishubashi Y, Kawasaki N. Therapeutic effects of laparoscopic Heller myotomy and Dor fundoplication on the chest pain associated with Achalasia. Surg Today. 2006;36(3):235-40.
32. Willis T. Pharmaceutice Rationalis Sive Diatribe de Medicamentorum Operationibus in Human Corpore. England: Hagae Comitis; 1674.
33. Zaninotto G, Costantin M, Anselmino M. Onset of esophageal peristalsis after surgery for idiopathic achalasia. Br. J. Surg. 1995;82(11):1532-4.
34. Parrilla P, Martínez de Haro, Ortiz A. Factors involved in the return of peristalsis in patients with achalasia of the cardias after Heller's myotomy. Am J Gastroenterol. 1995;90(5):713-7.
Recibido: 16 de febrero de 2008.
Aprobado: 26 de abril de 2008.
Daisy Naranjo Hernández. Calle 25 núm. 503, entre H e I, El Vedado. La Habana, Cuba. Correo electrónico:dnaranjo@infomed.sld.cu














