Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Cirugía
versión On-line ISSN 1561-2945
Rev Cubana Cir v.49 n.1 Ciudad de la Habana ene.-mar. 2010
Cirugía torácica videoasistida en la terapia de resincronización cardíaca
Video-assisted thoracic surgery used in the cardiac re-synchronizartion therapy
Edelberto Fuentes Valdés,I Guillermo Mojena Morfa,II Miguel Martín González,III Roberto Zayas Molina,IV Marleny Cruz Cardentey,V Juliette Pérez López,VI Pedro Nodal Leyva VII
IDoctor en Ciencias Médicas. Especialista de II Grado en Cirugía General. Profesor Titular. Servicio de Cirugía General, Hospital «Hermanos Ameijeiras». La Habana, Cuba.
IIEspecialista de I Grado en Cirugía General y Cirugía Cardiovascular. Instructor. Instituto de Cardiología y Cirugía Cardiovascular. La Habana, Cuba.
IIIEspecialista de II Grado en Cirugía General. Instructor. Hospital «Hermanos Ameijeiras». La Habana, Cuba.
IVEspecialista de II Grado en Cardiología. Profesor Auxiliar. Servicio de Electrofisiología y Marcapasos, Instituto de Cardiología y Cirugía Cardiovascular. La Habana, Cuba.
VEspecialista de I Grado en Cardiología. Instructor. Servicio de Electrofisiología y Marcapasos, Hospital «Hermanos Ameijeiras». La Habana, Cuba.
VIEspecialista de I Grado en Anestesiología y Reanimación. Cardiocentro, Hospital «Hermanos Ameijeiras». La Habana, Cuba.
VIIEspecialista de I Grado en Anestesiología y Reanimación. Instituto de Cardiología y Cirugía Cardiovascular. La Habana, Cuba.
RESUMEN
Se presenta el primer caso de terapia de resincronización cardíaca (TRC) intervenido en el Hospital «Hermanos Ameijeiras» mediante técnica de cirugía torácica videoasistida. El paciente es un hombre de 67 años de edad, que presenta una miocardiopatía dilatada con disfunción sistólica ventricular izquierda grave. Al ingreso presentaba cuadro clínico de insuficiencia cardíaca avanzada, por lo que se consideró la indicación de TRC. Tras el fallo de la técnica percutánea para la colocación de un electrodo en una vena epicárdica del ventrículo izquierdo, se decidió el acceso quirúrgico de mínima invasión. El implante del electrodo epicárdico mediante cirugía torácica videoasistida fue un procedimiento seguro sin complicaciones transoperatorias ni posoperatorias. Hasta donde conocemos, esta es la primera ocasión en que se utiliza la videotoracoscopia en Cirugía Cardiovascular en Cuba.
Palabras clave: Insuficiencia cardíaca, resincronización ventricular, cirugía torácica videoasistida, electrodo epicárdico de marcapaso.
ABSTRACT
This is the first case of cardiac re-synchronization therapy (CRT) operated on the "Hermanos Ameijeiras" Clinical Surgical Hospital using video-assisted thoracic surgery. Patient is a man aged 67 presenting with a dilated myocardiopathy with severe left ventricular systolic dysfunction. At admission he showed a clinical picture of advanced cardiac insufficiency, thus, we considered the prescription of a CRT. After the failure of the percutaneous therapy for placing a electrode in a epicardiac vein of left ventricle, we decide the minimal invasive surgical approach. The epicardiac electrode implantation by thoracic surgery was a safe procedure without transoperative and postoperative complications. We have knowledge that this is the first time that a video-thoracoscopy in Cardiovascular Surgery is performed in Cuba.
Key words: Cardiac insufficiency, ventricular re-synchronization, video-assisted thoracic surgery, pacemaker ipicardic electrode.
INTRODUCCIÓN
Las enfermedades cardiovasculares son la causa más importante de muerte en el mundo. No obstante, se ha observado un descenso de las muertes por cardiopatía isquémica y enfermedad cerebrovascular, al tiempo que se produce un aumento de la prevalencia, morbilidad y mortalidad por insuficiencia cardíaca (IC).1
Los pacientes con IC avanzada presentan trastornos de la conducción interventricular e intraventricular que determinan una pérdida de la sincronía mecánica ventricular.2 El bloqueo de la rama izquierda del haz de Hiss (BRIHH) también contribuye a la pérdida de la coordinación en la contracción y la relajación del ventrículo izquierdo (VI) en relación con el derecho, retraso de la contracción de la pared libre del VI con respecto al septo interventricular, contribución auricular inefectiva al llenado y aumento de la insuficiencia mitral protodiastólica. Todo ello conduce a un mayor deterioro de las funciones sistólica y diastólica ventricular izquierda de un corazón ya afectado.1,3
El pronóstico de la IC es globalmente malo. El desarrollo del desfibrilador automático implantable (DAI) significó un aporte importante para la disminución de la muerte súbita, pero no modifica la evolución de la enfermedad. El trasplante cardíaco surgió como el tratamiento capaz de cambiar el pronóstico de aquella, con mejoría de la sobrevida, de la capacidad funcional y de la calidad de vida, pero, desafortunadamente, el número de enfermos que necesitan este tratamiento sobrepasa por mucho la disponibilidad de donantes.4
La estimulación eléctrica con marcapaso del VI o en múltiples sitios (auriculobiventricular) puede recuperar la sincronía mecánica ventricular y resultar en una mejoría hemodinámica y sintomática para el enfermo; dicha estimulación se ha denominado terapia de resincronización cardíaca (TRC).4 Con esta técnica se produce una mejoría de la clase funcional, de la tolerancia al ejercicio y de la fracción de eyección del VI, así como una reducción de los volúmenes ventriculares, de la insuficiencia mitral y del número de ingresos hospitalarios por descompensación de la enfermedad.3
Corrientemente la estimulación del VI se logra al colocar, por vía percutánea, un electrodo endocárdico de marcapaso en una de las venas epicárdicas del corazón. El procedimiento es laborioso y con larga curva de aprendizaje, con una tasa de fracasos de alrededor del 8 %.2 Una técnica alternativa ha sido la toracotomía,5 y en los últimos años la cirugía torácica videoasistida (CTVA), con ayuda robótica o sin ella.6,7
La colocación de un electrodo en el VI logra su estimulación y mejora la sincronía ventricular. Los primeros electrodos diseñados a este efecto se implantaban directamente en la superficie epicárdica del VI, mediante toracotomía, con el fin de realizar la estimulación biventricular.3 Más tarde, se desarrolló la técnica intravascular de inserción del electrodo a través del seno coronario, para hacerlo progresar hasta una vena epicárdica del VI, motivo por el cual el acceso quirúrgico pasó a segundo plano, por su elevada morbilidad y mortalidad perioperatoria y parámetros de estimulación inapropiados.3
El propósito del presente trabajo es presentar el primer enfermo a quien se le realizó TRC mediante CTVA en el Hospital «Hermanos Ameijeiras» y, hasta donde conocemos, el primer caso de cirugía cardiovascular en Cuba intervenido mediante cirugía torácica videoasistida.
PRESENTACIÓN DEL CASO
Se presenta el caso de un paciente del sexo masculino, de 67 años de edad, con índice de masa corporal (IMC) de 29,3 kg/m² y antecedentes de hipertensión arterial sistémica, diabetes mellitus de tipo II, alcoholismo y miocardiopatía dilatada con disfunción sistólica ventricular izquierda grave. Al ingreso en noviembre de 2007 presentaba cuadro clínico de insuficiencia cardíaca avanzada (clase funcional de la New York Heart Association III-IV), latido de la punta desplazado hacia el 6to-7mo espacio intercostal izquierdo y soplo sistólico de insuficiencia mitral de grado III-IV/VI, bien audible en el ápex.
Los resultados de los exámenes de laboratorio clínico realizados al ingreso fueron normales. El electrocardiograma basal de 12 derivaciones fue compatible con una fibrilación auricular (FA) con respuesta ventricular normal y bloqueo de rama izquierda del haz de Hiss (BRIHH) (QRS > 130 ms). El telecardiograma demostró la presencia de cardiomegalia grave y signos de congestión vascular pulmonar. El ecocardiograma transtorácico (modo M, bidimensional y Doppler) informó marcado aumento de los diámetros y volúmenes telediastólico y telesistólico del VI (DTDVI: 94 mm, DTSVI: 87 mm, VTDVI: 363 mL, VTSVI: 308 mL), crecimiento de aurícula izquierda (diámetro longitudinal de 72 mm y transversal de 57 mm) y tiempos diastólicos variables; disfunción sistólica ventricular izquierda grave con marcada reducción de la fracción de eyección del VI (FEVI = 16 % por el método de Teich y FEVI = 15 % por el método de área-longitud), signos de insuficiencia mitral sistólica y diastólica, signos de hipertensión arterial venocapilar pulmonar ligera, y presencia de asincronía de la contracción auriculoventricular, interventricular e intraventricular con zona de mayor retardo de la contracción de la pared libre lateral basal del VI con respecto al septo interventricular. La coronariografía mostró arterias coronarias epicárdicas sin lesiones angiográficas significativas.
El paciente estaba recibiendo tratamiento farmacológico con diuréticos, digitálicos, inhibidores de la enzima de conversión de la angiotensina II y betabloqueadores, en dosis aceptadas como «máximo óptimo».
Por los hallazgos antes descritos se consideró que cumplía los criterios para TRC.8 Primero se intentó el implante de los electrodos por vía percutánea intravenosa. Se colocó un electrodo endocárdico bipolar (Biotronik) en la aurícula y ventrículo derechos bajo control fluoroscópico, el cual se conectó a un generador tricameral de la misma marca, para obtener una estimulación auriculobiventricular con programación variable de la conducción del impulso eléctrico. Después se intentó insertar un electrodo endocárdico de marcapaso a través del seno coronario y se hizo avanzar hacia una de las venas epicárdicas del VI. El fallo de este procedimiento, al parecer causado por la variación de la anatomía del sistema venoso, secundaria al crecimiento ventricular izquierdo, hizo necesaria la evaluación del implante quirúrgico del electrodo, directamente en la superficie epicárdica del VI mediante videotoracoscopia.
La intervención se realizó con anestesia general e intubación endotraqueal mediante tubo de doble luz para garantizar ventilación pulmonar selectiva y colapso del pulmón izquierdo con el objetivo de facilitar las maniobras quirúrgicas.
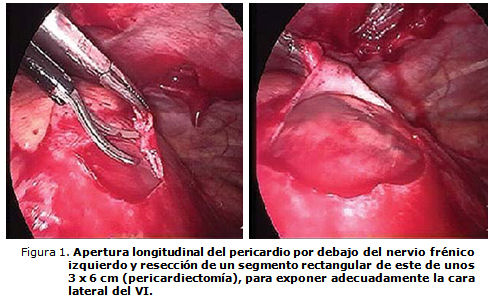
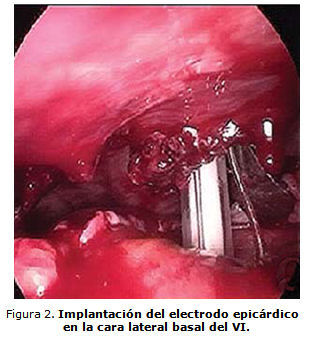
El paciente fue colocado en decúbito lateral derecho y, con la preparación adecuada de la piel y una vez colocados los paños de campo, se realizaron 3 incisiones de 10 y 12 mm de longitud a nivel del 5to. EICI línea axilar media, 3er. EICI línea axilar posterior y 7mo. EICI línea axilar posterior, dispuestas a modo de los vértices de un triángulo, a través de las cuales se colocaron los trocares para la introducción de los instrumentos de trabajo. El telescopio se introdujo a través del canal colocado en 5to. EICI y se identificó el pericardio parietal. Se realizó incisión longitudinal de pericardiotomía por detrás del nervio frénico izquierdo y se resecó un segmento rectangular de unos 3 x 6 cm que permitió la exposición adecuada de la cara lateral del VI (figura 1). A través del trocar situado en el 5to. EICI, línea axilar media (el telescopio se desplazó al puerto del 7mo. EICI), se implantó, mediante dispositivo de tornillo, el electrodo unipolar epicárdico en una zona relativamente avascular, previamente identificada como la zona de mayor retraso (figura 2). Se realizaron mediciones del umbral de estimulación del electrodo y se introdujo dentro de la cavidad torácica un segmento de éste, de unos 10-15 cm, para evitar que los movimientos de expansión pulmonar pudieran desinsertarlo. El extremo libre se hizo avanzar por el tejido celular subcutáneo, con la ayuda de una guía rígida, hasta la región pectoral izquierda donde se conectó al generador de marcapaso.
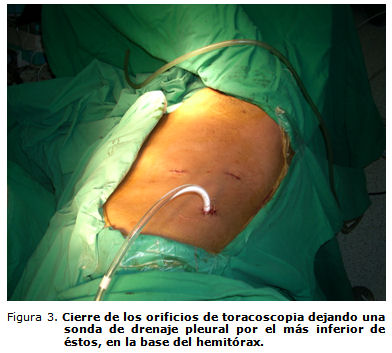
Con la colocación de una sonda de drenaje pleural en la base del hemitórax, conectada a un sistema de drenaje irreversible con sello de agua, se dio por terminada la intervención (figura 3). El período posoperatorio inmediato transcurrió en la Unidad de Cuidados Intensivos Quirúrgicos Cardiovasculares, en la cual el paciente permaneció hasta lograr la estabilidad hemodinámica y s retirara la sonda de drenaje torácico.
Antes del alta hospitalaria se practicó un nuevo ecocardiograma transtorácico para ajustar definitivamente el retraso de la conducción eléctrica interventricular. El seguimiento posoperatorio fue realizado por consulta externa ambulatoria con evaluaciones clínicas, radiológicas y electrocardiográficas mensuales.
Resultados
El tiempo quirúrgico fue de 105 min. El colapso pulmonar izquierdo fue bien tolerado desde el punto de vista gasométrico y hemodinámico. Se pudo colocar con éxito el electrodo epicárdico en la zona identificada con mayor retraso de la contracción del VI (lateral basal) y se obtuvieron parámetros de estimulación intraoperatorios adecuados con umbral aproximado de 0,6 mV. El paciente permaneció 24 h en la Unidad de Cuidados Intensivos. Fue necesario apoyar la contractilidad cardíaca con dobutamina para mantener la estabilidad hemodinámica. No hubo complicaciones transoperatorias ni posoperatorias. En el período posoperatorio inmediato se reinstituyó el tratamiento de base. La evolución satisfactoria hizo posible el egreso hospitalario al séptimo día.
El ecocardiograma transtorácico realizado antes del alta permitió resincronizar en forma óptima la actividad eléctrica y mecánica del corazón, con la programación de la conducción del impulso eléctrico con un adelanto de unos 20 ms en la estimulación del VI en relación con la del VD con lo que se logró mejoría de la sincronía de la contracción inter, intra y auriculoventricular, disminución de la magnitud de la insuficiencia mitral tanto sistólica como diastólica y mejoría moderada de la función sistólica del VI (FEVI = 21 % por el método de Teich y FEVI = 19 % por el método de área-longitud).
Seis meses después de la operación se mantiene la mejoría clínica significativa, con disminución de los síntomas de IC, lo que lo ubica al paciente en una clase funcional II de la NYHA. No se ha observado desplazamiento ni fallo de estimulación del electrodo ventricular izquierdo y los parámetros de estimulación durante el seguimiento no han experimentado cambios con respecto a los valores observados durante la intervención quirúrgica.
DISCUSIÓN
Aproximadamente el 15 % de los pacientes con insuficiencia cardíaca presentan retraso de la conducción interventricular o intraventricular.1 En los sujetos con insuficiencia cardíaca moderada a grave, este retraso ocurre hasta en un tercio de los casos.2 Los pacientes con insuficiencia cardíaca y descenso de la fracción de eyección que, además, presentan bloqueo completo de rama izquierda presentan un descenso aún mayor de la contractilidad por diversos motivos, como la ausencia de coordinación en la contractilidad del VI, la contracción anómala del septo, la alteración del llenado ventricular y el aumento de la insuficiencia mitral, lo que hace que se incremente la mortalidad.1
La TRC mejora la función del ventrículo izquierdo, la tolerancia al ejercicio, la calidad de vida y reduce la mortalidad en pacientes con NYHA de clase III y IV y en los que presentan una fracción de eyección del ventrículo izquierdo menor del 35 %.9-12
El procedimiento percutáneo es laborioso, requiere entrenamiento y no está exento de complicaciones.1 Por otro lado, un grupo de enfermos no se beneficiarán de esta técnica porque no puede implantarse el electrodo por la gran variabilidad anatómica de la anatomía venosa del corazón.1,3 El fracaso del procedimiento percutáneo obliga a la práctica de una técnica de rescate. La CTVA constituye una alternativa a la cirugía torácica convencional por su menor morbilidad y mortalidad, además de favorecer una recuperación más rápida y menos molestias posoperatorias.2,13
Entre las ventajas de la CTVA sobre la técnica percutánea de implante del electrodo epicárdico tenemos:14 la visión directa permite elegir la zona más apropiada al evitar la grasa epicárdica y las áreas de fibrosis, que pueden producir artefactos sobre los parámetros de estimulación; facilita la fijación segura del electrodo mediante dispositivo de tornillo y la tasa de fracaso del implante es menor que con la técnica percutánea.14 En nuestra experiencia, y en la de otros,3,14 no hubo desplazamiento posoperatorio del electrodo.
Como desventajas se citan el uso de anestesia general, la colocación del paciente en decúbito lateral con un pulmón colapsado y mantener la ventilación unipulmonar durante un período considerable. En nuestro caso no hubo complicaciones ventilatorias ni hemodinámicas importantes durante el procedimiento.
El implante del electrodo por videotoracoscopia es una técnica compleja.14,15 La adquisición de experiencia reduce significativamente los tiempos quirúrgicos15 y, lo que es más importante, minimiza la posibilidad de accidentes, como desgarros del epicardio14 por la manipulación de los instrumentos o al insertar el electrodo.
En resumen, el implante de electrodos epicárdicos en el VI mediante videotoracoscopia es considerado un procedimiento seguro y eficaz, con una tasa reducida de complicaciones posoperatorias.
REFERENCIAS BIBLIOGRÁFICAS
1. Hernández A, Escobar C, Blanco B, Marín I, Moya JL, Moro C. Resincronización cardíaca en la insuficiencia cardíaca: bases, métodos, indicaciones y resultados. Rev Esp Cardiol 2004;57(7):680-93.
2. Farwell D, Patel NR, Hall A, Ralph S, Sulke AN. How many people with heart failure are appropriate for biventricular resynchronization? Eur Heart J 2000;21:1246-50.
3. Fernández AL, García-Bengochea JB, Ledo R, Vega M, Amaro A, Alvarez J, et al. Implante de electrodos epicárdicos en el ventrículo izquierdo para resincronización mediante cirugía mínimamente invasiva asistida por videotoracoscopia. Rev Esp Cardiol 2004;57(4):313-19.
4. Asenjo R, Zapata M, Aramburu I, Morris R, Cereceda M, Brugere S, et al. Resultados clínicos de la resincronización ventricular en pacientes con insuficiencia cardíaca severa. Rev Med Chile 2003;131:1101-10.
5. Izutani H, Quan KJ, Biblo LA, Gill IS. Biventricular pacing for congestive heart failure: early experience in surgical epicardial versus coronary sinus lead placement. Heart Surg Forum 2002;6:E1-6.
6. Jansens JL, Jottrand M, Preumont N, Stoupel E, Cannière D. Robotic- enhanced biventricular resynchronization: an alternative to endovenous cardiac resynchronization therapy in chronic heart failure. Ann Thorac Surg 2003;76:413-7.
7. García-Bengochea JB, Fernández González AL, Vega Fernández M, Amaro Cendón A, Álvarez J, Rubio J, et al. Implante de electrodos en ventrículo izquierdo para resincronización. Ventajas de la videotoracoscopia frente a la técnica percutánea. Rev Esp Cardiol 2003;56(Supl 2):29.
8. Aranda JM, Woo GW, Schofield RS. Management of heart failure after cardiac resynchronization therapy: Integrating advanced heart failure treatment with optimal device function. J Am Coll Cardiol 2005;46:2193-98.
9. Préda I. Survival in cardiac resynchronization therapy. What do we know? Anadolu Kardiyol Derg. 2007;7(Suppl 1):57-9.
10. Eldadah ZA, Rosen B, Hay I, Edvardsen T, Jayam V, Dickfeld T, et al. The benefit of upgrading chronically right ventricle-paced heart failure patients to resynchronization therapy demonstrated by strain rate imaging. Heart Rhythm. 2006;3(4):435-42.
11. Gepner K, Sterliñski M, Przybylski A, Maciag A, Ko³sut P, Szwed H. From implantable cardioverter-defibrillator to cardiac resynchronization therapy with the use of epicardial left ventricular lead. The evolution of the treatment of post inflammatory heart failure—a case report. Kardiol Pol. 2006;64(10):1113-7.
12. Chen J, Garcia EV, Henneman MM, Bax JJ, Boogers MJ, Trimble MA, Borges-Neto S, Velazquez EJ, Iskandrian AE. Measuring left ventricular mechanical dyssynchrony from ECG-gated SPECT myocardial perfusion imaging. Minerva Cardioangiol. 2008;56(2):227-35.
13. Kaseda S, Aoki T, Hangai N, Shimizu K. Better pulmonary function and prognosis with video-assisted thoracic surgery than thoracotomy. Ann Thorac Surg 2000;70:1644-46.
14. Jansens JL, Jottrand M, Preumont N, Stoupel E, Cannière D. Robotic- enhanced biventricular resynchronization: an alternative to endovenous cardiac resynchronization therapy in chronic heart failure. Ann Thorac Surg 2003;76:413-17.
15. DeRose JJ, Ashton RC, Belsley S, Swistel DG, Vloka M, Ehlert F, et al. Robotically assisted left ventricular epicardial lead implantation for biventricular pacing. J Am Coll Cardiol 2003;41:1414-19.
Recibido: 19 de enero de 2009.
Aprobado: 26 de abril de 2009.
Edelberto Fuentes Valdés. Hospital Clinicoquirúrgico «Hermanos Ameijeiras». Calle Padre Varela y San Lázaro, Centro Habana. La Habana, Cuba.
Correo electrónico: efuentes@infomed.sld.cu