Introducción
La periodontitis se manifiesta como una respuesta inflamatoria mediada por la susceptibilidad inmunitaria del hospedero y asociada a microorganismos. Es una enfermedad crónica y progresiva que destruye el sistema de soporte periodontal. La fisiopatología de la periodontitis incluye vías moleculares que conducen a la activación de las proteinasas del hospedero, lo que produce la degeneración de las fibras marginales del ligamento periodontal, la migración apical del epitelio de la unión y la propagación apical de la biopelícula bacteriana a lo largo de la superficie de la raíz.1,2
Una infección focal localizada, como la periodontal, podría conducir a una inflamación sistémica de bajo grado, con resultados adversos para enfermedades sistémicas crónicas, como la diabetes mellitus y enfermedad coronaria, resultados adversos del embarazo, etc.3
La disfunción endotelial vascular se asocia con una variedad de enfermedades y factores de riesgo para la aterosclerosis, que incluyen la edad, hipertensión arterial, dislipidemias, diabetes, tabaquismo, enfermedades cardiovasculares específicas como arteriopatía coronaria, cerebral y periférica, y procesos infecciosos e inflamatorios como enfermedad periodontal.4 La disfunción endotelial conduce a cambios en la microvasculatura con un tono vasoconstrictor predominante y perjudicial.5
La dilatación mediada por flujo (DMF) es un marcador de la función endotelial de la arteria braquial.6) Para la evaluación de la función endotelial también existen otros métodos de prueba no invasivos con diferentes metodologías para medir la función endotelial, como son: infusión intracoronaria de acetilcolina, pletismografía de antebrazo, pletismografía de pulso-dedo (ENDO-PAT) y análisis de curva de pulso.7
Un metaanálisis de estudios descriptivos encontró una asociación entre el grosor de la íntima media carotideo y la dilatación mediada de flujo con la periodontitis.8) Por otro lado, ensayos clínicos reportan los efectos del tratamiento periodontal no quirúrgico sobre la función endotelial.9,10,11) Por este motivo, la presente revisión tuvo por objetivo actualizar los conocimientos sobre los efectos del tratamiento periodontal no quirúrgico en la función endotelial de los pacientes con periodontitis crónica.
Métodos
Esta revisión de la literatura se elaboró utilizando la base de datos de la Biblioteca Nacional de Medicina, Washington D. C. (Medline-PubMed).
Criterios de inclusión
Los artículos que se incluyeron en esta revisión, cumplen los siguientes criterios de inclusión:
Población: pacientes con periodontitis
Intervención: tratamiento no quirúrgico estándar en 4 sesiones (desbridamiento supragingival y subgingival) o tratamiento no quirúrgico en una sesión.
Comparación: tratamiento periodontal diferido (después de terminado el estudio) o solo tratamiento de raspado y pulido supragingival.
Resultados: evaluación de la función endotelial mediante cambios en la dilatación mediada por flujo de la arteria braquial o de la arteria carótida y cambios en la pletismografía de pulso-dedo (ENDOPAT).
Diseño de estudio: ensayos clínicos aleatorizados (ECAs).
Búsqueda electrónica
Como estrategia de búsqueda primaria se realizó una planificación de una búsqueda (I, II y III) utilizando el PubMed Advanced Search Builder el 5 de julio de 2019. Se utilizaron palabras tomadas del lenguaje natural en una combinación de vocabulario, términos controlados de texto libre y frases exactas, las que fueron discriminadas a través operadores booleanos u operadores de limitación con el motor de búsqueda de libre acceso PubMed, que permite consultar mayoritariamente los contenidos de la base de datos MEDLINE.
“endothelial” or “endothelium” or “endothelial dysfunction” or “blood vessels” or “vessels” or “vascular” or “vascular endothelial” or “intima media thickness”
“periodontal” or “periodontal treatment” or “periodontal disease” or “periodontal disease risk” or “treatment periodontal disease” or “periodontal bacteria”
I AND II
El resultado de (I AND II) fue: ((“endothelial” or “endothelium” or “endothelial dysfunction” or “blood vessels” or “vessels” or “vascular” or “vascular endothelial” or “intima media thickness”)) AND (“Periodontal” or “periodontal treatment” or “periodontal disease” or “periodontal disease risk” or “treatment periodontal disease” or “periodontal bacteria”).
Como estrategia de búsqueda secundaria se revisaron las referencias contenidas en los artículos seleccionados. Los resultados de la búsqueda fueron 2214 artículos, de los cuales se consideraron 3 artículos que cumplían con los criterios de inclusión para formar parte de la revisión.
Selección de artículos y extracción de datos
Dos revisores examinaron los títulos, resúmenes y textos completos de los artículos que fueron identificados, para, con posterioridad, extraer los datos. La confiabilidad entre los revisores se calibró a partir del cálculo de las concordancias mediante el coeficiente Kappa (K: 0,8).
Evaluación de la calidad
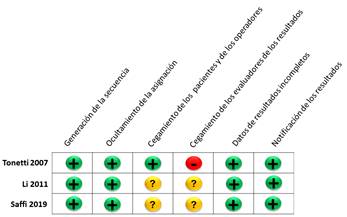
Se realizó el riesgo de sesgo de los ECAs incluidos siguiendo el manual de Cochrane para intervenciones de revisiones sistemáticas versión 5.1.0.12 Se evaluaron seis criterios principales de calidad: generación de la secuencia, ocultamiento de la información, cegamiento de los participantes y del personal, cegamiento de los evaluadores de los resultados, datos de resultados incompletos, reporte selectivo y otros sesgos. Estos criterios se calificaron como bajo (verde), no claro (amarillo) y alto riesgo de sesgo (rojo), según la descripción dada para cada campo individual (Fig. 1).
Análisis e integración de la información
Se seleccionaron 29 artículos de un total de 2214, por ser estudios en humanos donde se encontraban relacionadas las variables de estudio. Del 100 % de los artículos seleccionados se encontró que el 37,9 % correspondían a estudios de casos y controles, el 31 % correspondían a estudios transversales, el 10,34 % a estudios de cohorte y solo 20,6 % fueros ensayos clínicos, de los cuales solo 3 artículos (10 %) se eligieron para esta revisión, porque cumplían con los criterios de inclusión. Los ensayos clínicos aleatorizados seleccionados en la revisión según autor, evaluación de la disfunción endotelial, intervenciones realizadas en el grupo control y en el grupo experimental, seguimiento y población están descritos en la tabla 1.
Tabla 1 Estudios seleccionados
| Autor/año | Diseño | Población /país | Intervención | Comparación | Resultados | Seguimiento |
|---|---|---|---|---|---|---|
| Mauricio Tonetti (2007)9 | ECAs: grupos paralelos | 120 sujetos sanos con periodontitis (59 grupo control y 61 grupo experimental) País: Inglaterra | Tratamiento intensivo de raspado y alisado subgingival | Solo tratamiento de raspado y pulido supragingival | Dilatación media por flujo en la arteria braquial | 1, 7, 30, 60 y 180 días |
| Xiao Li (2011)11 | ECAs: grupos paralelos | 50 sujetos sanos con periodontitis (25 grupo control y 25 grupo experimental) País: China | Tratamiento periodontal inmediato | Tratamiento periodontal no quirúrgico diferido (después de los 3 meses del estudio) | Pletismografía de pulso-dedo (ENDOPAT) | 3 meses (90 días) |
| Marco Aurelio L. Saffi (2019)10 | ECAs: grupos paralelos | 76 sujetos con enfermedad arterial coronaria estable y con periodontitis (40 grupo control y 36 grupo experimental) País: Brasil | Tratamiento no quirúrgico estándar en 4 sesiones (supragingival y subgingival) | Tratamiento periodontal no quirúrgico diferido (después de los 3 meses del estudio) | Dilatación media por flujo de la arteria braquial | 3 meses (90 días) |
Tabla 2 Resumen de las conclusiones presentadas de los ensayos clínicos aleatorizados incluidos
| Autor | Título | Conclusiones |
|---|---|---|
| (2007) Mauricio Tonetti9 | Treatment of Periodontitis and Endothelial Function. | “El tratamiento periodontal intensivo dio como resultado una inflamación sistémica aguda a corto plazo, así como persistencia de la disfunción endotelial. Sin embargo, a los 6 meses después de la terapia periodontal, los beneficios en la salud oral se asociaron con una mejoría en la función endotelial”. |
| (2011)Xiao Li11 | Effect of periodontal treatment on circulating CD34+ cells and peripheral vascular endothelial function: a randomized controlled trial. | “El presente ensayo clínico aleatorizado a corto plazo muestra que el tratamiento de la periodontitis disminuye significativamente el recuento de células CD34+ circulantes, mientras que tiene efectos neutros en la función endotelial vascular periférica”. |
| (2019)Marco Aurelio L. Saffi10 | Periodontal therapy and endothelial function in coronary artery disease: a randomized controlled trial. | “El tratamiento periodontal no quirúrgico no proporcionó una mejor vasodilatación en pacientes con enfermedad coronaria en un periodo de seguimiento a corto plazo (3 meses). Se observaron pequeños beneficios después del tratamiento periodontal no quirúrgico con respecto a los marcadores sanguíneos de vasodilatación en términos de mantenimiento de niveles estables a lo largo del tiempo”. |
Periodontitis
La formación de biopelículas bacterianas inicia la inflamación gingival; sin embargo, la iniciación y la progresión de la periodontitis dependen de los cambios ecológicos disbióticos en el microbioma y los productos de degradación del tejido que enriquecen algunas especies bacterianas, así como los mecanismos antibacterianos que intentan contener los microbios dentro del surco gingival una vez que se ha iniciado la inflamación.1,2 La alteración de los sistemas inmunes innato y adaptativo puede desempeñar un papel importante en el inicio de la enfermedad periodontal.2 Se ha señalado que la periodontitis conduce a una inflamación sistémica en bajo grado, que puede influir negativamente en los resultados de enfermedades sistémicas crónicas como diabetes mellitus, enfermedad coronaria, resultados adversos del embarazo, etc.2,3,8
Desde el año 1977, la clasificación de la periodontitis se ha modificado en un intento de alinearla con la evidencia científica emergente. En el 2017, la Academia Americana de Periodoncia (AAP) y la Federación Europea de Periodoncia (EFP) llevaron a cabo un taller mundial cuyo producto fue una nueva clasificación de la enfermedad periodontal. La nueva conceptualización consideró dentro del grupo de periodontitis: 1) periodontitis necrotizante; 2) periodontitis como manifestación de una enfermedad sistémica y la categoría; 3) “periodontitis”, en la cual se unificaron las formas conocidas en la clasificación anterior como periodontitis “crónica” y “agresiva”. En esta última clasificación se introducen los términos de estadificación y graduación en los procedimientos diagnósticos. La estadificación clínica es la forma de describir la extensión de una lesión y la graduación es la forma para determinar el grado de progresión.1
Las cuatro categorías de la estadificación para la periodontitis están determinadas por un número de variables fisiopatológicas (pérdida de inserción clínica, cantidad y el porcentaje de pérdida ósea, la profundidad de sondaje, presencia y la extensión de los defectos óseos angulares y afección de defectos intraradiculares en molares, movilidad dental y pérdida dentaria por periodontitis). Las categorías van desde la etapa I (menos grave), hasta la etapa IV (la más grave progresión, grado C). El nuevo sistema de clasificación permite al profesional desarrollar una estrategia completa de tratamiento en función de las necesidades específicas para cada paciente.13) La descripción de la clasificación de la periodontitis según las etapas de gravedad (según el nivel de pérdida de inserción clínica interdental, pérdida ósea radiográfica y pérdida de dientes), complejidad, extensión y distribución se describen en la tabla 3.
Tabla 3 Clasificación de la periodontitis.13
| Estadio de la periodontitis | Estadio I | Estadio II | Estadio III | Estadio IV | |
|---|---|---|---|---|---|
| Severidad | Nivel de adherencia clínica (NAC) en el sitio de mayor pérdida | NAC 1-2 mm | NAC 3-4 mm | NAC ≥ 5mm | NAC ≥ 5mm |
| Pérdida ósea radiográfica | Tercio coronal (< 15 %) | Tercio coronal (15-33 %) | Extensión hacia la mitad o hacia el tercio apical de la raíz | Extensión hacia la mitad o hacia el tercio apical de la raíz | |
| Pérdida de dientes | No hay pérdida de dientes debido a la periodontitis | Pérdida dental debido a la periodontitis ≤ 4 dientes | Pérdida dental debido a la periodontitis ≥ 5 dientes | ||
| Complejidad | Local | Profundidad máxima de sondaje ≤ 4 mm Comúnmente pérdida ósea horizontal | Profundidad máxima de sondaje ≤ 5 mm Comúnmente pérdida ósea horizontal | En adicional a la complejidad del estadio II: Profundidad del sondaje ≥ 6mm Pérdida ósea vertical ≥ 3mm. Involucra furca: clase I o clase II - Defecto de reborde moderado | En adicional a la complejidad del estadio III la necesidad de rehabilitación compleja debido a: Disfunción masticatoria Trauma oclusal secundario (movilidad dentaria ≥ 2) Defecto alveolar avanzado Colapso de mordida Abanicamiento, migraciones dentarias - Menos de 20 dientes residuales |
| Extensión y distribución | Adherir al estadio como el descriptor | Por cada estadio, describir la extensión como localizada (< 30 % de los dientes envueltos), generalizada (≥ 30 % de los dientes envueltos) o patrón molar e incisivo | |||
Disfunción endotelial
El endotelio desempeña funciones importantes en la modulación del tono vascular, ya que sintetizando prostaglandinas vasodilatadoras, óxido nítrico (ON) e hiperpolarización dependiente del endotelio, así como factores contractuales derivados del endotelio. Dichos mecanismos son ventajosos para garantizar el mantenimiento adecuado del tono vascular en condiciones donde una de las respuestas mediadas por el factor vasoactivo está comprometida y favorece un estado vasoconstrictor, protrombótico y proinflamatorio.14
El endotelio vascular saludable tiene una acción antiinflamatoria, puede detectar cambios en las fuerzas hemodinámicas y reaccionar sintetizando y liberando sustancias vasoactivas como el óxido nítrico o la prostaciclina (PGI2). Sin embargo, cuando el endotelio se enferma, la producción de moléculas antiinflamatorias disminuye, mientras que la expresión de moléculas proinflamatorias y protrombóticas aumenta. El endotelio dañado se caracteriza por un desequilibrio entre la biodisponibilidad de los vasodilatadores y los factores de contratación derivados del endotelio.15
La disfunción endotelial es causada principalmente por la reducción de la producción o la acción de los factores relajantes derivados del endotelio y podría ser un paso inicial hacia la enfermedad cardiovascular.14,15
Una de las características de la disfunción endotelial es una respuesta reducida a los estímulos dependientes del endotelio, como la acetilcolina. La acetilcolina estimula el óxido nítrico sintasa endotelial (NOS-3) para generar ON, que se difunde a las células musculares lisas subyacentes, induciendo la relajación al aumentar la producción de guanosínmonofosfato cíclico (cGMP), lo que lleva a una reducción transitoria de la presión arterial in vivo.16,17 Por lo tanto, la disfunción endotelial se define ampliamente como un deterioro en la relajación vascular, debido a la disminución de la producción de ON por el endotelio o al aumento de la inactivación de ON. Además de ser un vasodilatador potente, el ON tiene propiedades antitrombóticas, antiinflamatorias y antimitogénicas, lo que explica por qué la reducción de los niveles de ON se asocia con un mayor riesgo de enfermedad cardiovascular.18
Existen abundantes técnicas no invasivas para la evaluación de la función endotelial, que pueden proporcionar información crucial sobre el riesgo, el progreso y la aplicación terapéutica de cada paciente en la medicina vascular. A saber:7
Evaluación de la función endotelial microvascular:
Vasodilatación mediada por flujo
Vaso constricción mediada por bajo-flujo
Plestismografía de oclusión venosa
Cambios en la forma de onda del pulso arterial periférico
Cambios en la velocidad de la onda del pulso arterial
Evaluación de la función endotelial macrovascular:
Relación entre periodontitis y disfunción endotelial
Según el consenso del 2009, los editores del American Journal of Cardiology (Revista Americana de Cardiología) y Journal of Periodontology (Revista de Periodoncia), declararon en la American Heart Association (Asociación Americana del Corazón) en el 2012, que existe un nivel suficiente de evidencias que apoyan una asociación entre la enfermedad vascular aterosclerótica con la enfermedad periodontal, sin embargo, no pueden clasificarse como causales.19
Se cree que los productos de la inflamación, como la proteína C reactiva (PCR), interleucina (IL) -1α, IL-1β, IL-6, factor de necrosis tumoral (TNF-α), prostaglandinas (PGE2) y metaloproteinasas de matriz (MPM), expresadas en la periodontitis, son liberadas en la circulación sistémica y pueden estimular las células endoteliales para producir otros marcadores inflamatorios que inducen o exacerban la disfunción endotelial.20-22,23
Entre los mecanismos que asocian periodontitis con disfunción endotelial, también se cree que los marcadores inflamatorios, como TNF-α e IL-6, que se expresan y aumentan en la periodontitis, pueden reducir la producción o la biodisponibilidad del ON, con un impacto negativo en la función de endotelio vascular y vasodilatación dependiente del endotelio.16
Se han propuesto varias vías biológicas directas e indirectas de asociación entre la enfermedad periodontal y la enfermedad vascular aterosclerótica. Las vías indirectas incluyen una vía fundamentalmente inflamatoria basada en el conocimiento de que se han establecido procesos aterogénicos y la disfunción endotelial, los que pueden conducir a enfermedades cardiovasculares como resultado de la actividad inflamatoria elevada.17
Con respecto a la relación entre la periodontitis y la disfunción endotelial se han presentado tres teorías: bacteriológica, inflamatoria e inmunológica16
Teoría bacteriológica
Indica el rol de los patógenos periodontales principalmente de la Porphyromonas gingivalis (Pg) y del Aggregatibacter actinomycetemcomitans (Aa). La Pg es un patógeno periodontal que presenta características invasivas necesarias para la progresión y patogénesis de la periodontitis, con potencial de efectos sistémicos. La naturaleza invasiva y persistente de la Pg es crucial para la inducción de disfunción endotelial. Aumenta la producción de mediadores proinflamatorios y moléculas de adhesión, incrementa la adhesión de leucocitos a la pared vascular. Por lo tanto, la Pg es capaz de transmitir una respuesta proaterogénica en las células endoteliales vasculares.16
Por otro lado, la Aa es una bacteria gram negativa que expresa una toxina que afecta selectivamente a los leucocitos, la que, además de matarlos, activa una respuesta proinflamatoria sustancial en estas células.18 La Aa también produce la leucotoxina (LtxA), una sustancia que induce la apoptosis en los glóbulos blancos en los humanos así como también en las células endoteliales microvasculares humanas.22
Teoría inflamatoria
Las células gingivales expresan productos inflamatorios (IL, TNF-a, CRP, MMP y prostanoides) que se liberan en la circulación sistémica. Estos productos inflamatorios estimulan a las células endoteliales, ya que producen otros mediadores inflamatorios como MCP-1, factor estimulante de colonias de macrófagos (MCSF), ICAM, VCAM, P-selectina y E-selectina. El MCP-1 es responsable del reclutamiento de monocitos y el M-CSF transforma los monocitos en macrófagos. Los macrófagos se transforman en células espumosas (foamcells) e inducen la producción de citoquinas proinflamatorias, lo que lleva así a la disfunción endotelial.16
Teoría inmunológica
Esta teoría defiende la idea de que el huésped puede tener un fenotipo de monocitos hiperinflamatorios. Este fenotipo da como resultado la liberación de una cantidad anormalmente alta de mediadores proinflamatorios, cuando son provocados por el lipopolisacárido de bacterias gram negativas. Los individuos con este tipo de fenotipo tienen un mayor riesgo de desarrollar periodontitis y la sobreexpresión de mediadores proinflamatorios fortalece aún más el riesgo de disfunción eréctil. La Pg puede activar respuestas inmunes innatas del hospedador relacionado con la disfunción endotelial. Se observa que en la respuesta inflamatoria la Pg podría agravar la inflamación vascular como resultado de la expresión de citoquinas, lo que orquesta la disfunción endotelial.16
Efecto de la terapia periodontal sobre la disfunción endotelial
En la revisión sistemática realizada por Teeuw et.al,19) en la que se evaluó si la terapia periodontal afecta el perfil de riesgo cardiovascular en pacientes con periodontitis, se menciona que el tratamiento periodontal reduce los biomarcadores de la enfermedad aterosclerótica y podría mejorar la función endotelial. Con respecto a la evidencia del tratamiento periodontal sobre la función vascular, se clasificó en un nivel moderado de evidencia.19
En los ensayos clínicos aleatorizados y controlados que formaron parte de la presente revisión, aparecen un grupo experimental (tratamiento periodontal no quirúrgico convencional o en una sola sesión) en comparación con un grupo de control (tratamiento periodontal solo supragingival o tratamiento periodontal retrasado).9,10,11 Sobre la base de los datos obtenidos (Tabla 1 y 2) la terapia periodontal no presenta un efecto sobre la función endotelial en un periodo de 3 meses. Sin embargo, según el estudio de Tonetti y otros9, a los 6 meses después de la terapia periodontal, se asocia con una mejoría en la dilatación media por flujo en la arteria braquial, que es un método para evaluar la función endotelial.
En los trabajos revisados se encontró que el tratamiento de la periodontitis disminuye significativamente el recuento de CD34+ (marcado de células madre hematopoyéticas primitivas), así como también beneficios después del tratamiento periodontal no quirúrgico con respecto a los marcadores sanguíneos de vasodilatación.
Conclusiones
La literatura incluida en esta revisión permite concluir que la terapia periodontal no quirúrgica puede mejorar la función endotelial vascular. No se encontraron efectos significativos sobre la función endotelial en pacientes con enfermedad periodontal después de tres meses de la terapia periodontal no quirúrgica. Sin embargo, si se encontró mejoría significativa en la función endotelial en pacientes con enfermedad periodontal después de seis meses de la terapia periodontal no quirúrgica. Por lo que se requiere mayor número de ensayos clínicos aleatorizados para afirmar la efectividad del tratamiento periodontal no quirúrgico a corto y a largo plazo.