Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Farmacia
versión On-line ISSN 1561-2988
Rev Cubana Farm v.31 n.3 Ciudad de la Habana sep.-dic. 1997
Determinación de un polimorfo de la cimetidina mediante la calorimetría diferencial de barrido
Luis Martínez Álvarez,1 Rolando Fernández Sierra2 y Yacqueline Gutiérrez31 Licenciado en Química. Especialista A.
2 Licenciado en Ciencias Farmacéuticas. Investigador Agregado.
3 Técnico Medio en Química.
RESUMEN
Se estableció la diferencia entre 2 sustancias de masa molecular similar -la cimetidina A y la B-, pero de estructuras internas distintas, mediante el empleo de la técnica de calorimetría diferencial de barrido donde solamente una de ellas, la cimetidina B, posee la actividad farmacológica requerida, es decir, cumple con las especificaciones de la farmacopea.Descriptores DeCS: RASTREO DIFERENCIAL EN CALORIMETRIA/métodos; CIMETIDINA/química; QUIMICA FARMACEUTICA.
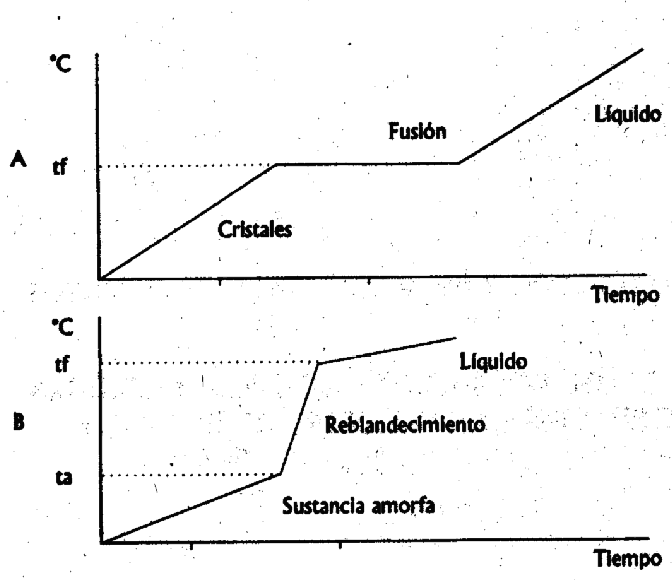
Se conocen muchos casos en que una sustancia existe con diferentes formas cristalinas, es decir, se diferencian entre sí por su estructura interna, además las propiedades físico-químicas son diferentes. A este tipo de fenómeno se le denomina polimorfismo.1 Las distintas formas polimórficas están caracterizadas por tener diferentes puntos de fusión, constante física que permite identificarlas y que a su vez es de gran utilidad para evaluar la pureza de éstas.2 Las sustancias cristalinas tienen la particularidad de fundir de una manera brusca a una temperatura constante; sin embargo, las sustancias amorfas se caracterizan generalmente, por tener previo a la transición al estado líquido, un intervalo de reblandecimiento, y esto trae como consecuencia un cambio continuo de sus propiedades.1
El conocimiento de las distintas formas polimórficas de una sustancia es de gran utilidad para la Industria Farmacéutica, pues esto permite eliminar aquella sustancia que bien puede ser inestable o que sus propiedades físico-químicas se alteren, ya bien sea por influencia del tiempo, como por las condiciones de temperatura y humedad, pero que además desde el punto de vista terapéutico no cumplan su objetivo.
La sustancia objeto de estudio es la cimetidina, principio activo ampliamente utilizado en la industria farmacéutica en la preparación de tabletas destinadas para el tratamiento de enfermedades tales como: úlcera duodenal, gástrica, esofagitis péptica, síndrome de Zollinger, y otras.3
MÉTODOS
El equipo empleado para la determinación del punto de fusión y el calor de fusión fue el TA 3000/DSC 20, además se utilizó como complemento de esta técnica para la identificación de los grupos funcionales de las sustancias estudiadas la espectroscopia infrarroja empleando el equipo FTIR Mattson- Unicam 1020.Se utilizaron 2 cimetidinas de distintos proveedores, así como también un patrón internacional y una mezcla de las 2 cimetidinas antes mencionadas.
En la experiencia se pesaron con presición y exactitud las cantidades de muestras siguientes:
Cimetidina A: 3,997 mg
Cimetidina B: 4,112 mg
Cimetidina patrón: 3,960 mg
Mezcla de A y B: 7,218 mg
La velocidad de calentamiento utilizada fue de 5E/min y el intervalo de temperatura evaluado entre 35 y 200E/min; se emplearon como porta-muestras crisoles de aluminio.
RESULTADOS
Las curvas térmicas registradas por DSC para las cimetidinas A y B, la mezcla de ambas y el patrón internacional objetos de estudio se observan en la figura 2. Como resultado de este análisis realizado a una velocidad de calentamiento de 5E/min, se registraron cada una de las transiciones endotérmicas características de la fusión de cada sustancia. Teniendo en cuenta el valor del rango de fusión reportado en literatura (140-144 EC), solamente la cimetidina A no cumplió con este parámetro.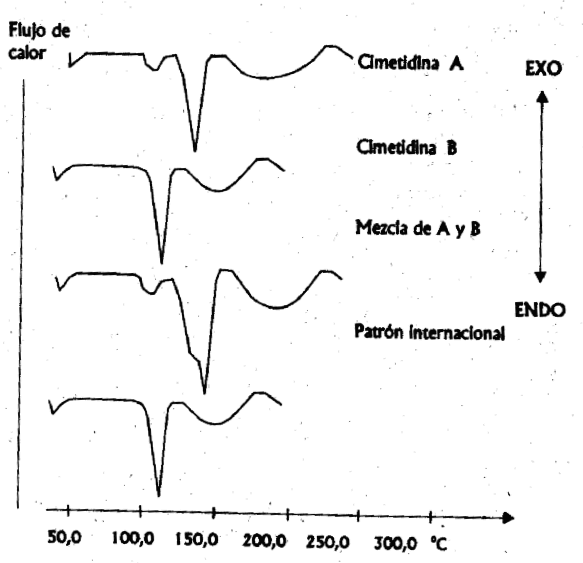
Los resultados numéricos de los valores de fusión registrados se relacionan en la tabla, así como también los valores del calor de fusión y los de la determinación de pureza por DSC. El porcentaje de pureza que presentó la cimetidina A estuvo por debajo del esperado.
| Sustancia | | | |
| Cimetidina A | | | |
| Cimetidina B | | | |
| Patrón internacional | | | |
| Mezcla A y B | | |
DISCUSIÓN
La cimetidina A tal y como se observó en la figura 2, presentó una pequeña transición endotérmica a una temperatura de 120 EC, seguida de un pico endotérmico de fusión a 148,4 EC, la pureza calculada por DSC fue de 96,07 %. El pico de fusión de la cimetidina B se detecta a una temperatura de 142,6 EC y la pureza de 98,96 %. El patrón internacional presentó un comportamiento similar que la cimetidina B, con un 99,20 % de pureza y un pico endotérmico a 142,0 EC. Entre los puntos de fusión de la cimetidina A y B existe una diferencia significativa, lo que demuestra que las estructuras internas de ambas sustancias son diferentes, tal y como se comprobó con los espectros infrarrojos y la técnica termoanalítica DSC, la cual resultó ser una herramienta muy fuerte y eficaz para los estudios de polimorfismo. El valor del calor de fusión calculado para la cimetidina A es de 567 mJ, para la B de 845,01 mJ, esto hace aun más notoria la diferencia entre la cimetidina A y la B, no siendo así entre la B y el patrón que fue para este de 834,29 mJ.El punto de fusión de la cimetidina B se corresponde con el rango de fusión reportado en la literatura consultada,4-7 en cambio para la cimetidina A no fue este el resultado esperado.
La mezcla de ambas cimetidinas, en una relación 1:1 originó aparentemente una nueva forma polimórfica que fundió a una temperatura de 144,5 EC y un calor igual a 1 369,8 mJ. Esto demuestra que entre ambas cimetidinas hubo una interacción que originó la formación de una nueva sustancia dado los valores obtenidos.
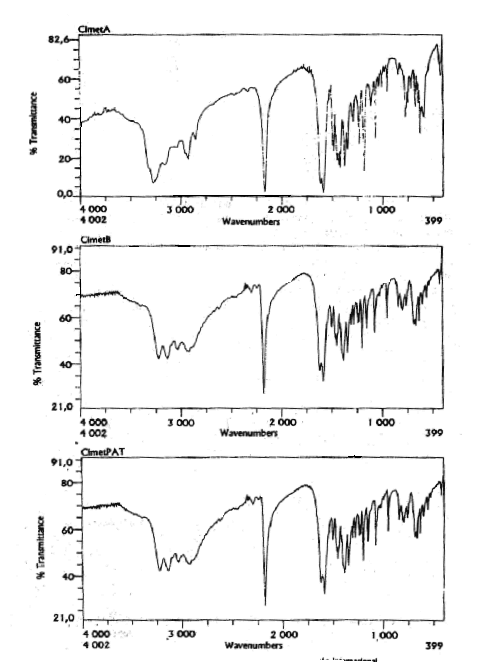
Solamente presentaron estructuras semejantes dado los espectros infrarrojos obtenidos, la cimetidina B y el patrón internacional. El espectro de la cimetidina A no se corresponde ni con el espectro del patrón, ni con la muestra B. Los picos principales reportados7 son: 1 620(a), 1 208(b), 1 082(c), 1 160(d) y 1 503(e).
SUMMARY
The difference between two substances of similar mollecular mass but of different internal structuras -cimetidine A and B- was established by using the differential scanning calorimetry. It was proved that only one of them, cimetidine B, has the required pharmacological activity, which means that it fulfills the pharmacopoeia specifications.Subject headings: CALORIMETRY, DIFFERENTIAL SCANNING/methods; CIMETIDINE/chemistry; CHEMISTRY, PHARMACEUTICAL.
REFERENCIAS BIBLIOGRÁFICAS
- Karapetiants MJ. Estructura de las sustancias. 2 ed. Moscú: Editorial Mir, 1979:328.
- Medicamenta. Guía teórico-práctica para farmacéuticos y médicos. 6 ed. Barcelona: Editorial Labor, 1962:381-2.
- Wendlant W. Thermal methods of analysis. 2 ed. New York: Inter Science Publishere, 1974:193-7.
- The Merck Index. 9 ed. Ranway: Merck, 1976:1.
- The United States Pharmacopoeia. 29 ed. London: The Pharmaceutical Press, 1985:1711.
- Martindale W. The extra pharmacopoeia. 29 ed. London: Pharmaceutical Press, 1990:1300-5.
- Clarke EG. Clarke's isolation and identification of drugs. 2 ed. London: The Pharmaceutical Press, 1986:467.
Lic. Luis Martínez Álvarez. Centro de Investigación y Desarrollo de Medicamentos. Ave 26 No. 1605 entre Rancho Boyeros y Calzada del Cerro, municipio Plaza de la Revolución, Ciudad de La Habana, Cuba.














