Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Farmacia
versión On-line ISSN 1561-2988
Rev Cubana Farm v.40 n.1 Ciudad de la Habana ene.-abr. 2006
Artículos originales
Centro para el Desarrollo de la Farmacoepidemiología
El Sistema Cubano de Farmacovigilancia, seis años de experiencia en la detección de efectos adversos
Giset Jiménez López,1 Francisco Debesa García,2 Blanca González Delgado,3 Jenny Ávila Pérez3 y Julián Pérez Peña4
Resumen
El Centro para el Desarrollo de la Farmacoepidemiología cuenta entre sus principales líneas de trabajo con la investigación, docencia, información de medicamentos, consulta terapéutica, Programa para el Uso Racional de los Medicamentos (PURMED) y la farmacovigilancia con su Unidad Nacional Coordinadora. El objetivo de este trabajo es exponer los principales resultados de trabajo en 6 años de creado este sistema de vigilancia. Se realizó un estudio descriptivo retrospectivo para caracterizar los reportes de sospechas de reacciones adversas recibidas en la Unidad Coordinadora Nacional de Farmacovigilancia. Se recibieron en este periodo un total de 89 540 notificaciones de reacciones adversas medicamentosas, lo que da un promedio 17 908 sospechas de notificación/año, y una tasa de reporte de más de 1 000 notificaciones por millón de habitantes. Con estos resultados queda identificado un comportamiento regular en algunos de estos indicadores, como es el predominio de efectos adversos en el sexo femenino, la afectación de la piel y el sistema digestivo entre las reacciones más reportadas y el predominio en todos los años de los antimicrobianos, antiinflamatorios no esteroideos y los antihipertensivos como grupos farmacológicos; de igual modo han aumentado las reacciones adversas de baja frecuencia de aparición y se han seguido los efectos adversos graves. La farmacovigilancia en el mundo sigue siendo una disciplina científica y clínica muy dinámica, la cual resulta imprescindible para afrontar los problemas que pueda plantear un arsenal de medicamentos que no deja de crecer en variedad y potencia. Por ello es tan necesario que, en cuanto surjan efectos adversos o toxicidad –sobre todo si aún no están descritos–, se notifique y analice el episodio y se comunique adecuadamente su importancia a los profesionales sanitarios.
Palabras clave: Farmacovigilancia, reacciones adversas a medicamentos, Sistema Cubano de Farmacovigilancia, efectos adversos.
La estrategia de la farmacoepidemiología comienza a desarrollarse en Cuba en el año 1996, ya que era necesario contar con una disciplina nueva que abarcara todos los aspectos relacionados con el medicamento durante su tránsito, desde la producción hasta el consumo; para ello se definió como centro rector el Centro para el Desarrollo de la Farmacoepidemiología (CDF), creado en junio de ese año, cuya estructura descansa en una red nacional formada por 175 centros municipales de Farmacoepidemiología, ubicados en una farmacia seleccionada en cada municipio y que a partir de ese momento se conoce como farmacia principal municipal (FPM).1
Regida metodológicamente por el CDF, en esta farmacia radica la presidencia del Comité Farmacoterapéutico Municipal, órgano multidisciplinario de evaluación y control del uso racional de los medicamentos en el territorio, este comité esta dirigido por un médico especialista en Medicina General Integral, entrenado en Farmacoepidemiología.1
El CDF cuenta entre sus principales líneas de trabajo con la investigación, docencia, información de medicamentos, consulta terapéutica, Programa para el Uso Racional de los Medicamentos (PURMED) y la farmacovigilancia con su Unidad Nacional Coordinadora.
Esta última se decidió ubicar dentro del CDF en el año 1999, con el objetivo de impulsar dicha actividad en el país, sus principales funciones se exponen a continuación:2
- Coordinar la actividad de los centros provinciales de farmacovigilancia, unificar criterios sobre el método de trabajo y prestar el debido soporte en lo que respecta a la codificación, tratamiento, emisión y evaluación de información sobre sospechas de reacciones adversas a medicamentos.
- Definir, diseñar y desarrollar los sistemas de tratamientos de la información y administrar la base de datos nacional.
- Recibir, valorar, procesar y emitir información sobre sospechas de reacción adversa medicamentosa (RAM) o cualquier otro problema relacionado con su eficacia durante su aplicación clínica.
- Prestar apoyo científico-técnico a todos los organismos del Ministerio de Salud Publica (MINSAP) y del Estado, que así lo requieran en la evaluación de los acontecimientos ocurridos en la fase IV de los ensayos clínicos.
- Realizar y coordinar estudios científicos sobre la seguridad de los medicamentos y elaborar informes para las autoridades sanitarias y sistema de salud.
- Intercambiar información con organismos internacionales en materia de farmacovigilancia y representar a Cuba ante ellos.
- Formar personal en materia de farmacovigilancia en colaboración con universidades, facultades de Ciencias Médicas y otras entidades.
- Efectuar balances de beneficio-riesgo de los medicamentos que están en el mercado.
Como primer paso se definen y discuten con las provincias cuales serian las tareas a realizar y los objetivos a alcanzar a corto, mediano y largo plazo, comienza así la consolidación de trabajo de este sistema. A partir de 1era Reunión Nacional de Farmacovigilancia, efectuada en el CDF en septiembre de 2000, surgen los indicadores para medir el trabajo, se definen conceptos necesarios como el de RAM importante y medicamentos a seguir de forma intensiva, y se le da una primera formación a los responsables provinciales. El mecanismo creado comenzó a dar sus frutos y el año 2000 cierra con resultados muy buenos; se destaca la calidad de las notificaciones recibidas en la Unidad Coordinadora Nacional de Farmacovigilancia (UNCFV), sobre todo en el ultimo trimestre de este año.1-4
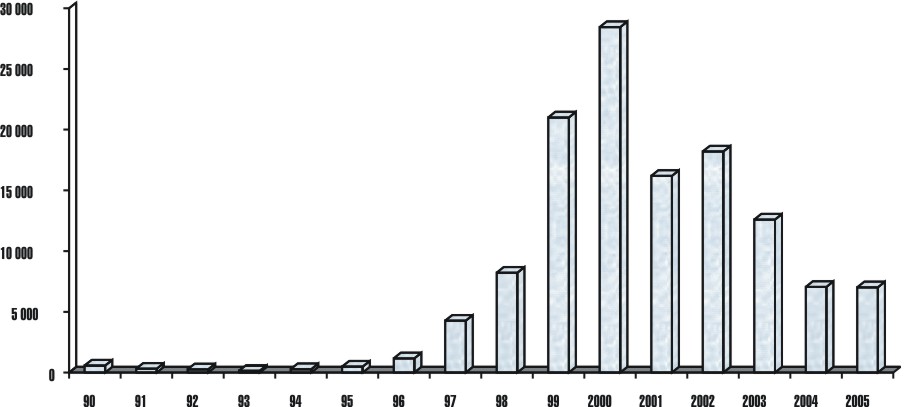
Como resultado del trabajo desarrollado y la acción desplegada por los farmacoepidemiólogos de la red; en los últimos años se ha sobrepasado la cifra de 7 000 notificaciones, que si se compara con las recibidas hasta el año 1995, muestra claramente el impacto que ha tenido la red de Farmacoepidemiología en esta actividad (fig.).1,2
Métodos
Se realizó un estudio descriptivo y retrospectivo de farmacovigilancia en el que se revisaron las notificaciones recibidas en la UNCFV en un período de 6 años; de manera que se caracterizó el reporte por variables demográficas, grupos farmacológicos, sistemas de órganos, severidad, causalidad y frecuencia de las reacciones adversas.
Fig. Número de notificaciones recibidas en el Centro Nacional
de Vigilancia Farmacológica de Cuba. 1990-2005.
Resultados
En los 6 años de trabajo de esta UNCFV, como brazo ejecutor del CDF para velar por la seguridad de los medicamentos los principales resultados son los siguientes:5-7
Se reciben en este período un total de 89 540 notificaciones de RAM, lo que da un promedio de notificación por año de 17 908 sospecha de notificación/año, y una tasa de reporte de más de 1 000 notificaciones por millón de habitantes. La tabla 1 evidencia los principales resultados en el período 2000-2005.
Tabla 1. Principales resultados de farmacovigilancia. Años 2000-2005
| Parámetro | Año 2000 | Año 2001 | Año 2002 | Año 2003 | Año 2004 | Año 2005 |
| No. de notificaciones | 28 450 | 16 195 | 18 206 | 12 601 | 7 063 | 7 025 |
| RAM importantes* | 40,3 % | 68,8 % | 36,0% | 35,9 % | 45,1 % | 50,8 % |
| No útiles | 0 | 0,2 % | 0,2% | 0,5 % | 0,5 % | 0,1 % |
| Asociaciones fámaco-RAM de baja frecuencia | 27 | 228 | 418 | 1 290 | 1 989 | 2 568 |
| Sexo predominante | Femenino | Femenino | Femenino | Femenino | Femenino | Femenino |
| Severidad | Leves Moderadas Graves Mortales | Leves Moderadas (52,7%) Graves Mortales | Leves Moderadas Graves Mortales | Leves Moderadas Graves Mortales | Leves Moderadas Graves Mortales | Leves Moderadas Graves Mortales |
| Notificación por nivel de atención | APS (89,9 %) AS (6,7 %) Otros (1-2 %) | APS (83,2 %) AS (16,8 %)
| APS (79,4 %) AS (16,9 %) Otros (2,0 %) | APS (83,5 %) AS (16,2 %) Otros (0,3 %) | APS (85,0 %) AS (14,9 %) AT (0,1 %) | APS (86,7 %) AS (13,2 %) AT (0,01 %) |
| RAM más frecuentes | Rash (9,0 %) Vómito Náuseas | Rash (10,2 %) Vómitos Náuseas | Rash (9,9 %) Vómitos Náuseas | Rash (16,0 %) Vómitos Epigastralgia (4,2 %) | Rash (18,4 %) Vómitos Epigastralgia (3,9 %) | Rash (18,8 %) Vómitos Cefalea |
| Grupo farmacológico más frecuente | Antimicrobianos (21,0 %) AINES Anti-HTA | Antimicrobianos (27,4 %) AINES Anti-HTA | Antimirobianos (27,3 %) AINES Anti-HTA | Antimirobianos (31,9 %) AINES Anti-HTA | Antimicrobianos (32,9 %) Anti-HTA | Antimicrobianos (31,2 %) AINES Anti-HTA |
* Según criterios para definir una RAM importante de la UNCFV.
Con estos resultados queda identificado un comportamiento regular en algunos de estos indicadores, como es el predominio de efectos adversos en el sexo femenino, un mejor trabajo en la atención primaria de salud en cuanto a reporte de sospechas de RAM, la afectación de la piel y el sistema digestivo entre las reacciones más reportadas y el predominio en todos los años de los antimicrobianos, antiinflamatorios no esteroideos y los antihipertensivos como grupos farmacológicos.
La tabla 2 muestra algunas asociaciones fármaco-RAM de baja frecuencia de aparición detectadas en este período, entre las que se destacan el abombamiento de fontanela por ácido nalidíxico y la necrólisis tóxica epidérmica por antiinflamatorios no esteroideos.
Tabla 2. Ejemplos de asociaciones fármaco-RAM de baja frecuencia de aparición detectadas por el Sistema de Farmacovigilancia Cubano. Años 2000-2005
| Años | Asociación fármaco-RAM de baja frecuencia de aparición |
| 2000 | Ceguera por morfina |
| 2001 | Abombamiento de fontanela por ácido nalidíxico |
| 2002 | Trombocitopenia y leucopenia por carbamazepina |
| 2003 | Aplasia medular por dipirona |
| 2004 | Rash por dipirona |
| 2005 | Convulsiones por ciprofloxacina |
Fuente: Unidad Nacional Coordinadora de Farmacovigilancia.
En estos años se han realizado análisis como el seguimiento de los fármacos más reportados según severidad, y estos prácticamente no varían de un año a otro, se destacan en este grupo de los más reportados el captopril, con más del 70 % de sus efectos adversos leves, y le siguen las penicilinas (rapilenta y cristalina) con más del 50 % de sus notificaciones moderadas y graves, entre los más reportados se encuentran el cotrimoxazol, la dipirona y la ciprofloxacina, con predominio de reacciones moderadas.
La valoración de causalidad es otra característica que se ha mantenido, teniendo el sistema siempre más del 70 % de las sospechas de RAM clasificadas como probables.
Discusión
En los primeros años (1999 al 2000), se trabajó duro en el sentido de aumentar el número de notificaciones, creando hábitos en los notificadores potenciales (médicos, farmacéuticos, enfermeras y otros profesionales); a partir de la definición del concepto de RAM importante en septiembre del 2000 se comenzó a ver una tendencia a disminuir la notificación de reacciones leves y aumentar las de moderadas, graves y mortales, y se produce un fenómeno importante en el sentido del aumento de la calidad de los reportes enviados por las provincias.
A partir del año 2004 se observa una disminución importante del número de reportes, ocasionado por cambios en el personal de la red, a la cual se incorporan nuevos profesionales, por lo que se consideró necesario establecer nuevas estrategias de capacitación; sin embargo, la calidad de los reportes en estos ha aumentado notablemente, a partir de la introducción de una evaluación de calidad de los reportes, de los evaluadores y de la introducción de los datos en la base de datos central, así como la detección de reacciones adversas de baja frecuencia de aparición.
Desde el año 2001 se comenzó a discutir y estudiar las reacciones de baja frecuencia de aparición, con lo cual se ha demostrado la cultura de reporte alcanzada por el sistema y la focalización de la búsqueda hacia problemas más importantes. Otro logro en este año fue la creación de grupos de expertos a nivel provincial y nacional, los cuales están constituidos por profesionales de diferentes especialidades, que discuten en su marco científico las sospechas de reacciones adversas mortales, graves que lo ameriten y de baja frecuencia de aparición.5-7
En estos años el sistema ha continuado trabajando en perfeccionar los filtros de revisión de notificaciones a nivel municipal y provincial, en afianzar los grupos de trabajo multidisciplinarios y en desarrollar nuevos métodos de análisis como el método bayesiano de generación de señales, así como en el mantenimiento de la capacitación, investigaciones, publicaciones y retroalimentación a su red.5-7
Se observa también con el paso de los años un aumento en la notificación de RAM importante para el sistema y en la detección de efectos adversos de baja frecuencia.
La retroalimentación del sistema y la comunicación del riesgo llega hasta los notificadores y profesionales sanitarios en general, expresión de esto ha sido la detección de casos de hipertensión endocraneana asociada al ácido nalidíxico en niños menores de un año, serie de casos que se siguió desde el año 2001 en que aparecen los primeros casos, hasta el 2003 donde se culminan las investigaciones y se redacta una nota informativa a profesionales sanitarios que dio a conocer las características del problema y las recomendaciones para la prevención de este efecto indeseable.8
Otro ejemplo fue la detección de reacciones graves seguidas a la administración de cefalosporinas en pacientes con antecedentes de alergia a las penicilinas, lo cual culminó con una nota informativa a profesionales sanitarios que advertía las consecuencias de este efecto adverso. Igualmente cada año se realizan alrededor de 6 investigaciones basadas en los datos que recoge el sistema y estas se han extendido a nivel provincial.
Por último se debe señalar que la Unidad Coordinadora Nacional ha mantenido estrechas relaciones con el Centro Internacional de Monitoreo de RAM en Uppsala, Suecia, y a partir del año 2004 se logra crear un programa para enviar todos los reportes del país a la base de datos internacional de farmacovigilancia, envío este que se mantiene con periodicidad semestral.
Además la información de la base de datos nacional ha sido fuente de información de investigaciones, tesis de diplomado, especialidad y publicaciones nacionales e internacionales.
La farmacovigilancia en el mundo sigue siendo una disciplina científica y clínica muy dinámica, por lo cual resulta imprescindible para afrontar los problemas que pueda plantear un arsenal de medicamentos que no deja de crecer en variedad y potencia. Por ello es tan necesario que, en cuanto surjan efectos adversos o toxicidad (sobre todo si aún no están descritos), se notifique y analice el episodio y se comunique adecuadamente su importancia a los profesionales sanitarios.
Es nuestra tarea continuar trabajando y transformar la farmacovigilancia en una búsqueda activa de potenciales efectos adversos, para lograr una adecuada valoración beneficio-riesgo de los fármacos de que se disponen en el mercado cubano.
Summary
The Cuban system of drug surveillance: six years of experience in detecting adverse effects
The Center for the Development of Pharmacological Epidemiology has several working lines such as research, teaching, drug information, therapeutic consultation, program for the rational utilization of drugs (PURMED) and drug surveillance with the National Coordinating Unit. The objective of this paper was to present the main working results achieved in 6 years after the creation of this drug surveillance system. A retrospective descriptive study was performed to characterize the reports of suspected adverse reactions from the National Coordinating Unit of Drug Surveillance. In the period, 89 540 notifications of adverse drug reactions were received for an average of 17 908 notifications per year, and a report rate of more than 1000 notifications per 1 million inhabitants. These results reflected a regular behaviour in some of these indicators like the predominance of adverse effects in females, affected skin and digestive system as the most reported reactions and the prevalence of antimicrobials, non-steroidal antinflammatory drugs and antihypertensive drugs as the pharmacological groups with more reactions. Similarly, the number of less frequent adverse drug reactions has increased and serious adverse effects have been followed-up. Drug surveillance continue to be a very dynamic scientific and clinical discipline worldwide, being indispensable to face the possible problems of an armory of drugs that does not cease to grow in potency and variety. Therefore, it is necessary that, as soon as adverse effects or toxicity signs occur – mainly if they have not been yet classified – they must be notified and analyzed, and then the importance of the episode should be adequately reported to corresponding health professionals.
Key words: Drug surveillance, adverse reactions to drugs, Cuban Drug Surveillance System, adverse effects.
Referencias Bibliográficas
1. Debesa F, Jiménez G, Pérez J. Vigilancia farmacológica en Cuba. Situación actual. Bol Fármacos. 2001;4(1). Disponible en: www.boletinfarmacos.org
2. Debesa F, Jiménez G, Pérez J, Avila J. La estrategia de Farmacoepidemiología en Cuba. Características y papel de la Unidad Coordinadora de Farmacovigilancia en Cuba. Bol Fármacos. 2001;4(2). Disponible en: www.boletinfarmacos.org
3. Debesa F, Jiménez G, Bastanzuri T, Avila J, Rosell A, Portuondo C, Yera I. La Unidad Coordinadora Nacional de Farmacovigilancia, principales funciones y resultados. Rev Cubana de Farm. 2002;36(Suplemento Especial No. 2):214.
4. Debesa F, Jiménez G, Figueras A, Diogenes E, Pérez J, Avila J, Laporte JR. Spontaneous reporting of adverse drug reactions in Cuba: integrating continuous education, training and research in a network approach. Br J Clin Pharmacol. 2002;54:333-6.
5. Anónimo. Cuba-Story behind the success. Uppsala Reports. 2002 October;(20) 6-7.
6. Debesa F, Jiménez G, Pérez J, Avila J. Principales resultados del sistema cubano de farmacovigilancia en el año 2002. Bol Fármacos. 2003;6(3). Disponible en: www.boletinfarmacos.org
7. Jiménez G, Debesa F. Medicamentos y riesgos. Rev Cubana Farm. 2002;36 (Suplemento Especial No. 2):217.
8. Página Web del Centro para el Desarrollo de la Farmacoepidemiología. Boletines de Farmacovigilancia. Disponible en: http://www.cdf.sld.cu
Recibido: 8 de noviembre de 2005. Aprobado: 9 de diciembre de 2005.
Dra. Giset Jiménez López . Centro para el Desarrollo de la Farmacoepidemiología (CDF). Calle 44 No. 502 esq. 5ta Ave, municipio Playa, Miramar , Ciudad de La Habana. Correo electrónico: giset@mcdf.sld.cu
1Especialista de II Grado en Farmacología.
2Vicedirector del Centro para el Desarrollo de la Farmacoepidemiología.
3Especialista Unidad Nacional Coordinadora de Farmacovigilancia.
4Director del Centro para el Desarrollo de la Farmacoepidemiología.