Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Medicina
versión On-line ISSN 1561-302X
Rev cubana med v.47 n.1 Ciudad de la Habana ene.-mar. 2008
TRABAJOS ORIGINALES
Estudio descriptivo de respuesta a quimioterapia en pacientes con carcinoma de células no pequeñas de pulmón inoperable
Descriptive study of response to chemotherapy in patients with inoperable non-small cell lung carcinoma
Elia Nenínger VinagerasI; Concepción del Castillo CarrilloII; Rebeca Barbán SuárezII; Carmen ViadaIII; Reimer Febles CabreraIV; Joaquín González GonzálezII; Mayté Lima PérezII; Jorge Luis Soriano GarcíaI
IEspecialista de II Grado en Oncología. Hospital Clinicoquirúrgico "Hermanos Ameijeiras". La Habana, Cuba.
IIEspecialista de I Grado en Oncología. Hospital Clinicoquirúrgico "Hermanos Ameijeiras". La Habana, Cuba.
IIIMaster en Ciencias Bioestadísticas. Centro Inmunología Molecular. Hospital Clinicoquirúrgico "Hermanos Ameijeiras". La Habana, Cuba.
IVEspecialista de I Grado en Medicina Interna. Hospital Clinicoquirúrgico "Hermanos Ameijeiras". La Habana, Cuba.
RESUMEN
Se reportaron los resultados de un estudio descriptivo y retrospectivo basado en la estandarización terapéutica de los pacientes con cáncer de pulmón de células no pequeñas, no operables, que recibieron quimioterapia de combinación cisplatino-vinblastina para determinar su supervivencia. Se observó que 185 recibieron tratamiento (cisplatino 100 mg/m2 y vinblastina 6 mg/m2) endovenoso el día 1 y, posteriormente, cada 21 d; 125 (78 %) recibieron entre 4 y 6 ciclos de tratamiento. Se halló que la supervivencia global de todos los pacientes fue de 11,82 meses (mediana 8,43), mientras que en los estadios IIIB y IV fue de 9,11 (mediana 7,60) y 8,96 meses (mediana 5,80), respectivamente. En estos estadios se obtuvo 48 % de control de la enfermedad considerada como respuesta objetiva más estabilización. La toxicidad fue fundamentalmente digestiva, renal y hematológica. Se observó tendencia a una mayor supervivencia en el sexo femenino. No se encontraron diferencias en la supervivencia entre los estadios IIIB y IV, sin embargo, en aquellos pacientes en los cuales se obtuvo control de la enfermedad, la supervivencia fue significativamente mayor. Se halló que los pacientes en estadios IIIB y IV con buen estado general tuvieron mayor supervivencia al igual que los que presentaron una sola comorbilidad.
Palabras clave: Carcinoma de células no pequeñas, cisplatino, quimioterapia.
ABSTRACT
The results of a descriptive and retrospective study based on the therapeutic standardization of the patients with inoperable non-small cell lung cancer that received cisplatin-vinblastine combined chemotherapy were reported to determine their survival. It was observed that 185 were administered endovenous treatment (cisplatin 100 mg/m2 and vinblastine 6 mg/m2) the first day and, later, every 21 days; 125 (78 %) received between 4 and 6 treatment cycles. It was found that the global survival of all the patients was 11.82 months (mean 8.43), whereas in the stages IIIB and IV it was 9.11 (mean 7.60) and 8.96 months (mean 5.80), respectively. In these stages, it was obtained 48 % of control of the disease considered as an objective response plus stabilization. Toxicity was mainly digestive, renal and haematological. A trend towards survival was observed among females. No differences were detected in the survival between the stages IIIB and IV. However, in those patients among whom a control of the disease was attained, the survival was significantly higher. It was concluded that the patients in stages IIIB and IV with a good general condition had a greater survival, as well as those that presented only one comorbidity.
Key words: Non-small cell carcinoma, cisplatin, chemotherapy.
INTRODUCCIÓN
Aproximadamente, la tercera parte de todas las muertes por cáncer son ocasionadas por el cáncer de pulmón. Esta entidad ocasiona más muertes que el cáncer de mama, próstata y colon juntos.1 En Cuba constituye la primera causa de mortalidad por tumores malignos.2
La quimioterapia para el cáncer de pulmón de células no pequeñas es a menudo considerada inefectiva o excesivamente tóxica; sin embargo, estudios de meta-análisis han demostrado que, cuando se compara con el tratamiento de soporte, significa un pequeño incremento en la supervivencia de este tipo de pacientes.3 También se ha demostrado que reduce síntomas y mejora la calidad de vida de los enfermos.4 La combinación de cisplatino-vindesina o cisplatino-vinblastina ha logrado una respuesta objetiva de 25 %.5 Otros estudios en los que a esa combinación han añadido el mitomycin han reportado respuestas hasta del 30 %. Al comparar la combinación cisplatino-vinblastina vs. cisplatino-vinblastina-mitomycin se obtuvo respuesta mayor con el segundo régimen, pero con mayor deterioro de la calidad de vida y con supervivencia media similar para ambos grupos (8,4 meses).5
En este trabajo se reportan los resultados del tratamiento de pacientes con cáncer de pulmón de células no pequeñas, no suceptibles de tratamiento quirúrgico.
MÉTODOS
Selección de los pacientes
Fueron incluidos todos los pacientes a quienes se les diagnosticó carcinoma de pulmón de células no pequeñas estadios IIb y IIIA no suceptibles de recibir tratamiento quirúrgico así como los de estadios IIIB y IV (según Sistema TNM de la UICC). Estos pacientes fueron tratados en el Hospital "Hermanos Ameijeiras," en el período comprendido desde marzo del 2000 a junio del 2004.
La población del estudio estuvo constituida por 185 pacientes con diagnóstico confirmado por biopsia y/o citología, con edades no menores de 18 años, funciones de médula ósea, renal, hepática y cardíaca dentro de límites normales y que no hubieran recibido quimioterapia previa.
El tratamiento con radiaciones se administró según el criterio de los investigadores. Todos los pacientes recibieron el régimen de cisplatino (100 mg/m2) en el día 1 por infusión endovenosa de 1 h con prehidratación y posthidratación así como diuresis con manitol y vinblastina, 6 mg/m2 en el día 1. Los cursos se repiten cada 21 d durante 4 a 6 ciclos.
Previo al comienzo del tratamiento, a cada paciente le fue realizado examen físico, radiografía simple de tórax, ultrasonido abdominal, tomografía axial computadorizada de tórax y de cerebro, así como estudios hematológicos y química analítica. Antes de cada ciclo de tratamiento se realizó examen físico, exámenes de sangre completos y radiografías en dependencia de los requerimientos del paciente. Una vez finalizado el tratamiento, los pacientes fueron evaluados para respuesta 4 sem después del último ciclo, luego pasaron a consulta de seguimiento con control trimestral.
Diseño del estudio
Los datos fueron obtenidos por revisión de las historias clínicas, registro de información de tumores, registro de Anatomía Patológica e informes de imagenología así como los registros de seguimiento de tumores de pulmón del Servicio de Oncología. Los datos incluyeron características de los pacientes como, edad, raza, sexo, fecha de diagnóstico, hábito de fumar, estadio de la enfermedad al diagnóstico, estado general (PS), localización del tumor, número de ciclos recibidos, respuesta al tratamiento, fecha de progresión, fecha de fallecimiento y toxicidad al tratamiento.
Análisis estadístico
Las características demográficas y médicas de los pacientes fueron analizadas utilizando métodos de estadística descriptiva. La supervivencia global fue estimada usando el método de Kaplan-Meier. La distribución de la supervivencia fue comparada mediante el test de log-rank.
RESULTADOS
La edad media fue de 58 años (rango 35 a 77) con 124 pacientes (67 %) del sexo masculino y una proporción hombre/mujer 2:1. El 74 % fueron de la raza blanca. El 94,1 % de la muestra eran fumadores (174 pacientes); de ellos, el 44,3 % durante más de 30 años. La mayor proporción de los pacientes tuvieron estado general entre 1 (paciente ambulatorio capaz de llevar cabo un trabajo ligero) y 2 (paciente ambulatorio incapaz de realizar ningún trabajo, capaz de realizar sus cuidados personales), con 50,8 y 47,6 %, respectivamente. Con respecto a las comorbilidades, se observó que 85 pacientes padecían otras enfermedades, de ellos el 82,3 % estaban aquejados de más de una enfermedad concomitante (tabla 1).

La distribución de los pacientes según el estadio de la enfermedad señala que la mayoría fue diagnosticada en estadios IIIB y IV (tabla 2). Hubo 32 pacientes en estadios IA-IIIA que no fueron operados por las razones siguientes: negativa del paciente (n= 3), enfermedad concomitante que contraindicaba la cirugía (n= 15) estado general no adecuado (ECOG 2/3) (n= 14).

Adhesión al tratamiento
Todos los pacientes recibieron el mismo esquema terapéutico (cisplatino/vinblastina); de ellos 60 (32,4 %) recibieron entre 1 y 3 ciclos de tratamiento y 125 (67,5 %), entre 4 y 6.
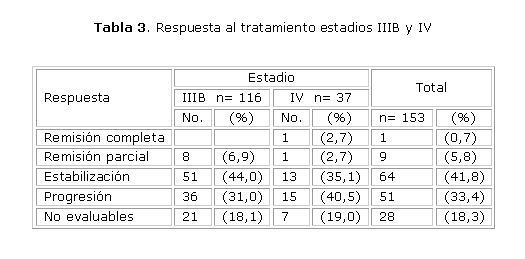
La respuesta al tratamiento de los estadios IIIB y IV se refleja en la tabla 3. Diez pacientes presentaron respuesta objetiva, es decir, remisión completa y parcial de la enfermedad (9 y 1 pacientes, respectivamente). La mayor proporción de pacientes presentó estabilización de la enfermedad. Considerando aquellos que presentaron respuesta objetiva conjuntamente con los que estabilizaron se observó 48 % de pacientes con control de la enfermedad.
La toxicidad se manifestó fundamentalmente con náuseas, vómitos, leucopenia y elevación de los valores de creatinina y en la mayoría de los pacientes fue considerada grados I-II, es decir ligera a moderada según CTC. Solamente 5 pacientes interrumpieron el tratamiento por toxicidad grado 3/4.
Análisis de la supervivencia
La mediana de supervivencia fue de 8,43 meses (IC 7,34; 8,79) y la supervivencia media, de 11,8 meses (IC 9,58; 12,98), considerada desde el diagnóstico (fig. a) mientras que, desde el fin de la quimioterapia, la supervivencia media fue de 8,52 meses (IC 6,90; 10,14).
Teniendo en cuenta la edad promedio de nuestros pacientes, se establecieron 2 grupos de edades: menores de 60 años y mayores de esa edad. La supervivencia media encontrada en ambos grupos fue de 10,30 vs. 7,60 meses (p= 0,606), respectivamente, diferencia que no fue estadísticamente significativa.
Se observó tendencia a una mayor supervivencia en las mujeres (12,35 meses vs. 10,08 meses (p= 0,28). No hubo diferencia significativa en la supervivencia entre los distintos grupos raciales (p= 0 ,3129).
La supervivencia alcanzada en el estadio IA, fue de 15,93 meses (1 solo caso) y en el IIB y IIIA fue 22,41 meses (IC 15,37; 29,45) y 16,03 meses (IC 11,65; 20,40), respectivamente. En el estadio IIIB, la mediana de supervivencia fue de 7,60 meses (IC 6,60; 8,60) y la media, de 9,11meses (IC 7,90; 10) y en el estadio IV la mediana fue de 5,60 meses (IC 4,99; 6,61) con una media de 8,96 meses (IC 4,95; 12,97) , considerada desde el diagnóstico. Considerando la supervivencia en estos 2 estadios desde el fin de la quimioterapia se observa en el estadio IIIB una mediana de 4,93 meses (IC 3,86; 6,01) y una media de 6,37 meses (IC 5,37; 7,38), mientras que en el estadio IV, la mediana de supervivencia fue de 3,17 meses (IC 2,47; 3,86) mientras la media fue de 6,12 (2,37; 9,88) p = 0,13 (tabla 4). No hubo diferencia significativa (fig. b) y hay 4 pacientes vivos en el momento de este reporte (2 de cada grupo) (tabla 4).
De acuerdo con el estado general (PS), encontramos diferencias significativas de supervivencia entre los pacientes que presentaban un PS 1 cuya supervivencia fue de 10,9 meses (IC 8,20 13,60) y los de PS 2 que fue de 5,61(IC 4,20 6,72) p= 0, 0030 (fig. c).
En los sujetos de los estadios IIIB y IV que obtuvieron control de la enfermedad se observó que los que alcanzaron respuesta objetiva tuvieron una supervivencia de 9,79 meses (IC 4,71; 14,87), mientras que los de enfermedad estable fue de 4,61 meses (3,77; 5,45) (p= 0, 027) lo que resulta estadísticamente significativo (fig. d).
Al analizar la supervivencia con respecto al hábito de fumar encontramos que 52 pacientes expuestos al tabaco durante más de 30 años tuvieron una supervivencia de 11,66 meses (IC 9,62; 13,7) en comparación con los de menor exposición que fue de 9,18 (IC 7,39; 10,97), diferencia esta que no resulta significativa.
En relación con las enfermedades comórbidas, observamos que los pacientes que no presentaban ninguna enfermedad o aquejados de una sola, sobrevivieron 10,78 meses (IC 8,96; 12,61) mientras que los que padecían más de una presentaron una supervivencia de 7,12 meses (IC 5,22; 9,01) diferencia que resulta significativa (p= 0,02).
Para los pacientes en estadio IV se estudió la correlación entre el número de sitios metastáticos y la supervivencia; los enfermos que presentaron un solo sitio metastático (n= 25) tuvieron una supervivencia media de 10,63 meses (IC 5,16; 16,10) mientras que los que tenían más de un sitio metastático sobrevivieron 5,38 meses (IC 3,98; 6,77).
DISCUSIÓN
La atención terapéutico de los pacientes con cáncer de pulmón metastático, localmente avanzado o en estadios tempranos inoperables permanece aún controversial por el bajo índice de respuesta alcanzada, aunque al compararse la quimioterapia con el tratamiento de soporte se aprecia mejora en los índices de respuesta y, lo que es más importante, en la supervivencia.1
Por lo general, estos pacientes reciben tratamiento con quimioterapia de régimen de platino, lo que constituye la piedra angular del tratamiento actual de esta entidad.
En nuestro estudio, la mayoría de los pacientes recibieron como promedio 4 ciclos de tratamiento, de acuerdo con los criterios actuales acerca de la quimioterapia.6
Al evaluar los aspectos demográficos en los pacientes estudiados no se encontraron diferencias en la distribución por grupos de edades o raza. En relación con el sexo, en nuestro estudio también se apreció tendencia a un discreto incremento en la supervivencia del sexo femenino, lo cual concuerda con lo reportado por algunos autores.7
Teniendo en cuenta el vínculo irrefutable entre cáncer de pulmón y hábito de fumar encontramos que el 44 % de los pacientes de nuestra serie fumaron durante más de 30 años; sin embargo, no observamos diferencias en la supervivencia entre los fumadores según el tiempo de exposición.
En los pacientes en estadio IIIB y IV se observó un porcentaje de respuesta objetiva a la quimioterapia de 5,8 y 0,6 %, que resulta bajo en comparación con la reportada en la literatura más actual en la cual se informa desde 20 % de respuesta parcial, con la combinación de carboplatino-taxol, hasta 43,6 % con el triplete carboplatino-taxol-gemcitabina.8
Treat y otros9 reportaron los resultados de un estudio fase III donde se comparaba paclitaxel y carboplatino (PC) con gemcitabina y carboplatino (GC) o gemcitabina y paclitaxel (GP). Encontraron en 929 pacientes con carcinoma de células no pequeñas en estadio avanzado, no tratados previamente, una supervivencia global de 7,7 meses y al año, de 33 %, por grupos fue: para PC 7,9, para GC 7,6 y para GP 8,4 meses, respectivamente. La supervivencia para el régimen que no incluyó platino fue similar a los regímenes de platino. En nuestra serie, de los 153 pacientes diagnosticados en estadios IIIB y IV, la supervivencia media encontrada de 9 y 8,96 meses, respectivamente no dista de lo reportado por otros autores.
Considerando los factores que pueden influir en la supervivencia de los pacientes con cáncer de pulmón de células no pequeñas, es importante identificar aquellos que no se benefician con la quimioterapia. Hasta el momento se considera como uno de los factores más importantes el estado general (PS). Sweeney y otros10 encontraron una mediana de supervivencia de 4,1 meses mientras sólo el 19 % de los pacientes con PS, 2 supervivieron 1 año. En nuestro estudio, el haber encontrado una supervivencia de 14,20 y 7,79 meses, respectivamente, en los pacientes con PS 1 y 2 enfatiza que debe realizarse un análisis minucioso de los pacientes con mayor compromiso del estado general, ya que son más propensos a presentar mayor toxicidad a la quimioterapia y por tanto, puede ser que se beneficien menos con este tratamiento.
Resultados similares condujeron a que en las guías de tratamiento de la Sociedad Americana de Oncología de 1997 se estableciera que la quimioterapia en el estadio IV prolonga la supervivencia siendo más apropiada para individuos con buen estado general.11
El número de sitios metastáticos también puede influir en el pronóstico. Pacientes con la enfermedad confinada a los pulmones suelen presentar mejor evolución; estudios aleatorizados han sugerido que pacientes con un solo sitio metastático pueden presentar mejor evolución ante terapéuticas agresivas. Los pacientes con múltiples metástasis (hígado, cerebro y hueso) presentan peor evolución. En nuestra serie se observó tendencia a una mayor supervivencia en los pacientes con un solo sitio metastático.
En conclusión, esta evaluación retrospectiva confirma que la quimioterapia con régimen de platino aporta beneficios a los pacientes con cáncer de pulmón avanzado. No obstante, los resultados terapéuticos siguen siendo pequeños, por lo que este tipo de paciente puede beneficiarse de su inclusión más activa en protocolos de ensayos clínicos de nuevos productos antitumorales.
AGRADECIMIENTOS
Los autores agradecen a los doctores Gisela González y Agustín Lage del Centro de Inmunología Molecular por la revisión de este trabajo.
REFERENCIAS BIBLIOGRÁFICAS
1. Schiller JH, Harrington D, Velan CP, Langer C, Sandler A, Krook J et al. Comparison of tour chemotherapy regimens for advanced non-small-cell lung cancer. NEJM. 2002;346(2):92-8.
2. Cuba. Ministerio de Salud Pública. Dirección Nacional de Estadísticas. Anuario Estadístico 2003. Ciudad de La Habana, 2004.
3. Marino P, Pampalona S, Preatoni A, Cantoni A, Invernizzi F. Chemotherapy versus supportive care in advanced non-small-cell lung cancer: results of a meta-análisis of the literatura. Chest. 1994;106:861-5.
4. Culle M, Billingham J, Woodrafe C. Mitomycin, ifosfamide, and cisplatin in unresectable non-small-cell lung cancer: effects on survival and quality of life. J Clin Oncol. 1999;17:3188-94.
5. Kosmidis P, Mylonakis N, Sharlos DV, Samantas E, Beer M, Theocharis D et al. A comparative study of cisplatin and vinblastine versus ifosfamide, cisplatin and vinblastine in non-operable non-small-cell lung cancer. Ann Oncol. 1994;5:159-62.
6. Socinsky M, Schell MJ, Peterman A, Bakri K, Yates S, Gitten R et al. Phase III Trial comparing defined duration of Therapy versus continuous therapy followed by second-line therapy in advanced stage IIIB/IV Non-Small-Cell Lung Cancer. J Clin Oncol. 2002;5:1335-43.
7. Fu JB, Kau TJ, Severson RK, Kalemkerian GP. Lung cancer in women. CHEST. 2005;127(3):768-77.
8. Paccagnella A, Oniga F, Bearz A, Favoretto A, Clerici M, Barbieri F et al. Adding Gemcitabine to Paclitaxel/Carboplatin Combination increases Survival in Advanced Non-Small-Cell Lung Cancer: Results os a Phase II-III Study: J Clin Oncol. 2006;24:681-7.
9. Treat J, Belani CP, Edelman NJ. A randomized phase III trial of Gemcitabine (G) in combination with Carboplatin (C) or Paclitaxel (P) versus paclitaxel and carboplatin (PC) in advanced (Stage IIIB, IV) non-small-cell lung cancer (NSCLC): Update of the Alpha Oncology trial (A1 99002L. Proc Am Soc Clin Oncol. 2005;23:2926-32.
10. Sweeney CJ, Zhu J, Sandler AB. Outcome of patients with a performance status of 2 in Eastern Cooperative Oncology Group Study E1594: a Phase II trial in patients with metastatic non-small cell lung carcinoma. Cancer. 2001;92:2639-47.
11. Barclay L. New ASCO Guidelines for management of unresectable non-small cell lung cancer. J Clin Oncol. 2004;22:330-53.
Recibido: 15 de enero de 2007.
Aprobado: 29 de junio de 2007.
Dra. Elia Nenínger Vinageras. Hospital Clinicoquirúrgico "Hermanos Ameijeiras", San Lázaro No. 701 entre Belascoaín y Marqués González, Centro Habana, Ciudad de La Habana, Cuba. Habana 3, CP 10300. E-mail: nenin@infomed.sld.cu














