Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Medicina
versión On-line ISSN 1561-302X
Rev cubana med v.47 n.4 Ciudad de la Habana oct.-dic. 2008
TRABAJOS ORIGINALES
Tratamiento del carcinoma de células pequeñas del pulmón y supervivencia a 5 años
Treatment of small cell lung carcinoma. Survival at 5 years
Elia Neninger VinagerasI; Concepción del Castillo CarrilloII; Carmen ViadaIII; Rebeca Barbán SuárezII; Carlos Gassiot NuñoIV; Joaquín González GonzálezIV
IEspecialista de II Grado en Oncología. La Habana, Cuba.
IIEspecialista de I Grado en Oncología. La Habana, Cuba.
IIIMaster en Ciencias. Licenciada en Bioestadística. Centro Inmunología Molecular. La Habana, Cuba.
IVEspecialista de II Grado en Neumología. La Habana, Cuba.
RESUMEN
Se reportaron los resultados de un estudio retrospectivo de pacientes con carcinoma de células pequeñas de pulmón en todos los estadios de la enfermedad, diagnosticado por citología y/o biopsia de la lesión. Métodos: Se estudiaron 68 enfermos que padecían un carcinoma de células pequeñas de pulmón en todos los estadios y recibieron tratamiento de primera línea con cisplatino-etopósido y de segunda línea, con ciclofosfamida, doxorubicina y vincristina. Los pacientes de enfermedad limitada fueron evaluados al final del primer ciclo para planificar el tratamiento con radiaciones; los de enfermedad extendida recibieron radiaciones sobre sitios metastáticos o para mejorar algún síntoma. Resultados: La respuesta al tratamiento fue: 25 % de respuesta objetiva (RC y RP) y 56 % de control de la enfermedad. La mediana de supervivencia global fue 10,10 meses. En el sexo femenino se observó tendencia a un incremento de la supervivencia en relación con el masculino (10,23 vs. 9,33 meses). La supervivencia en la enfermedad limitada fue de 12,5 meses y en la enfermedad extendida, de 6,57 meses lo cual fue estadísticamente significativo (p = 0,004).
Palabras clave: Carcinoma de células pequeñas.
ABSTRACT
The results of a retrospective study of patients with small cell lung carcinoma in all the stages of the disease diagnosed by cytology and/or biopsy of the lesion were reported.
Methods: 68 patients that suffered from a small cell lung carcinoma in all the stages that received first-line treatment with cisplatin-etoposide, and second line treatment with cyclophosphamide, doxorubicin and vincristine were studied. The patients with limited disease were evaluated at the end of the first cycle to plan the treatment with radiations; those with extended disease received radiations on metastic sites or to improve some symptom.
Results: The response to the treatment was as follows: 25 % of objective response (CR and PR) and 56 % of control of the disease. The global mean survival was 10.10 months. Among females, it was observed a trend towards an increase of survival compared with males (10.23 vs. 9.33 months). The survival of the limited disease was 12.5 months, whereas in the extended disease it was 6.57 months, which was statistically significant (p = 0,004).
Key words: Small cell carcinoma.
INTRODUCCIÓN
El carcinoma de células pequeñas de pulmón es una entidad clínica e histológica dentro del rango de los cánceres de pulmón. Sus elementos patológicos fueron reconocidos por primera vez por Barnard, en 1926.1 Watson y Berg describieron más tarde los elementos clínicos de la enfermedad en detalle, y notaron su localización central preferente en la radiografía de tórax, la tendencia a la diseminación precoz, la alta frecuencia de metástasis encontradas en la autopsia, y la alta tasa de respuesta a la quimioterapia.2 El carcinoma de células pequeñas de pulmón es el subtipo más agresivo. Aunque la mayoría responde a la quimioterapia, más del 95 % de los pacientes fallece por la enfermedad. Esta entidad tiene una incidencia aproximada del 14 % de los nuevos casos diagnosticados de cáncer de pulmón. Su aparición se encuentra relacionada, en el 95 % de los casos, con el consumo de tabaco,3 es muy raro que se presente lo suficientemente localizada como para que sea posible su resección.
En este trabajo se reportan los resultados del tratamiento de pacientes con cáncer de pulmón de células pequeñas que recibieron tratamiento convencional en el servicio de Oncología Clínica del Hospital "Hermanos Ameijeiras".
MÉTODOS
Selección de los pacientes
Fueron incluidos todos los pacientes a quienes se les diagnosticó un carcinoma de pulmón de células pequeñas que recibieron tratamiento en el Servicio de Oncología del Hospital Clinicoquirúrgico "Hermanos Ameijeiras", en el periodo comprendido desde marzo del año 2000 hasta junio del 2004.
La población de estudio comprendió 68 pacientes a los que les fue realizado el diagnóstico por citología y/o biopsia de un carcinoma de células no pequeñas del pulmón, con edades no menores de 18 años, funciones de médula ósea, hepática, cardiaca y renal dentro de límites normales, según los parámetros de Laboratorio Clínico del centro, que no hubieran recibido quimioterapia previa.
El tratamiento con radiaciones se realizó según lo establecido en las Guías de Practica Clínica del servicio y las Normas Nacionales de Oncología. Los pacientes con enfermedad limitada (EL), una vez finalizado el primer ciclo de quimioterapia, fueron evaluados para la planificación del tratamiento con radiaciones; los pacientes con enfermedad extendida (EE) recibieron tratamiento con radiaciones de acuerdo con el criterio de los investigadores: de forma individualizada sobre sitios de metástasis o con la intención de mejorar síntomas.
Todos los pacientes recibieron quimioterapia de primera línea, régimen de cisplatino (80 mg/m2) en el día 1, por infusión endovenosa de 1 h con prehidratación y poshidratación, así como diuresis forzada con manitol más etoposido (vepesid) 100 mg/m2 días 1 al 3.
Los cursos se repiten cada 21 d durante 6 ciclos. Veintidós pacientes recibieron tratamiento de segunda cuyo esquema consiste en 750 mg/m2 de ciclofosfamida, 50 mg/m2 de doxorrubicina y 1,4 mg/m2 de vincristina, de administración endovenosa directa en el día 1 de cada ciclo cada 21 d, durante 6 ciclos.
Previo al comienzo del tratamiento, a cada paciente le fue realizado examen físico, radiografía simple de tórax, ultrasonido abdominal, tomografía axial computarizada (TAC) de tórax, abdomen y cerebro, biopsia de médula ósea, ante la sospecha clínica de infiltración a ese nivel, así como estudios hematológicos y química analítica.
Antes de cada ciclo de tratamiento, a cada paciente le fue realizado examen físico, exámenes de laboratorio clínico (hematología y química), radiografía de tórax después del segundo ciclo. Una vez finalizado el tratamiento, los pacientes fueron evaluados para respuesta. Aquellos que presentaron estabilización de la enfermedad o que mostraron ser refractarios al régimen de platino recibieron la segunda línea de tratamiento, si mantenían un índice de estado general adecuado (PS 0-1), perfil hematológico y químico, normales al igual que la función cardiaca.
Diseño del estudio
Los datos fueron obtenidos por revisión de las historias clínicas, registro de información de tumores, registro de Anatomía Patológica e informes de Imagenología así como los registros de seguimiento de tumores de pulmón del Servicio de Oncología Clínica. Los datos incluyeron características demográficas de los pacientes como edad, sexo, raza, fecha de diagnóstico, hábito de fumar, estadio de la enfermedad al diagnóstico, estado general (PS), localización del tumor, número de ciclos recibidos (primera o segunda línea), toxicidad al tratamiento, respuesta a la quimioterapia, fecha de progresión y fecha de fallecimiento. La supervivencia se consideró desde el diagnóstico hasta el fallecimiento.
Análisis estadístico
Se utilizaron métodos de estadística descriptiva para el análisis de las características demográficas y médicas de los pacientes. La supervivencia global fue estimada usando el método de Kaplan-Meier. La distribución de supervivencia fue comparada usando el método de log-rank.
RESULTADOS
Fueron incluidos 68 pacientes que reunieron los criterios de inclusión en el protocolo de tratamiento específico para el carcinoma de células pequeñas establecido en el Servicio de Oncología Clínica. La edad media fue de 56 años (rango 37-76 años), con 31 pacientes del sexo femenino y 37 del masculino, con una proporción hombre/mujer de 1.2:1. La mayoría de los pacientes eran fumadores (96 %), de los cuales el 53 % fumó menos de 30 años y el 47 % lo hizo durante más de ese tiempo (tabla 1). La mayoría de los pacientes tuvieron estado general 1 (performance status o PS).
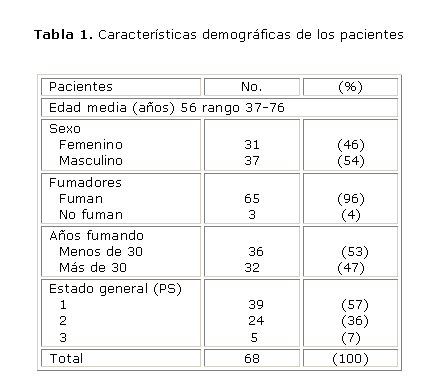
El 68 % de los pacientes se encontraba en estadio de enfermedad limitada, mientras que el 32 % se presentó al diagnóstico con la enfermedad extendida (EE), es decir, en fase de diseminación. La localización anatómica de los tumores fue fundamentalmente hacia los lóbulos superiores; 32 pacientes en el lóbulo superior derecho y 25 en el lóbulo superior izquierdo, todos en posición central. En 2 de los pacientes la lesión se ubicaba anatómicamente en el mediastino (tabla 2).

La mayoría de los pacientes eran polisintomáticos. Los síntomas fundamentales fueron disnea, dolor toráxico, tos, disfonía, astenia, hemoptisis, fiebre, cefalea y dolor óseo. Dos pacientes presentaron tromboflebitis migratriz y en 2 se observó trombosis venosa profunda de miembros inferiores. La duración media del cortejo sintomático fue de 2,3 meses antes de acudir a este centro donde les fue aplicado el protocolo de diagnóstico y tratamiento de la enfermedad.
Todos los pacientes recibieron primera línea de tratamiento con esquema de cisplatino-vepesid, de ellos 59 pacientes (87 %) recibieron entre 4 y 6 ciclos. Once pacientes interrumpieron el tratamiento tras recibir menos de 3 ciclos del mismo; 9 de esos pacientes presentaban enfermedad extendida, los cuales presentaron: toxicidad inaceptable (4 pacientes) y deterioro del estado general (5 pacientes). Veintidós pacientes recibieron tratamiento de segunda línea (tabla 3), de ellos 18 recibieron entre 4 y 6 ciclos; 4 interrumpieron el tratamiento, de ellos 3 por progresión de la enfermedad y 1 por toxicidad cardiovascular (grado 3/4). El tratamiento con radiaciones aparece reflejado en la tabla 3, la mayoría de los pacientes recibió irradiación torácica.
La toxicidad presentada por el resto de los pacientes se manifestó fundamentalmente por náuseas, vómitos, leucopenia, fatiga y elevación de la creatinina sérica.
Respuesta al tratamiento
La respuesta al tratamiento aparece reflejada en al tabla 4. Se obtuvo respuesta objetiva en 15 pacientes (4 completa y 11 parcial) lo que equivale a un 25 %. De ellos, 12 presentaban estadio de enfermedad limitada y 3, de enfermedad extendida. Diecisiete pacientes presentaron estabilización de la enfermedad lo que equivale al 30 %. Al considerar a los que presentaron respuesta objetiva conjuntamente con los que lograron la estabilización se observó un 56 % de control de la enfermedad.

Análisis de la supervivencia
La mediana de supervivencia global de nuestros pacientes fue de 10,10 meses (IC 7,17 13,03) con una media de 21,61 meses (IC 14,67 28,54), figura 1.
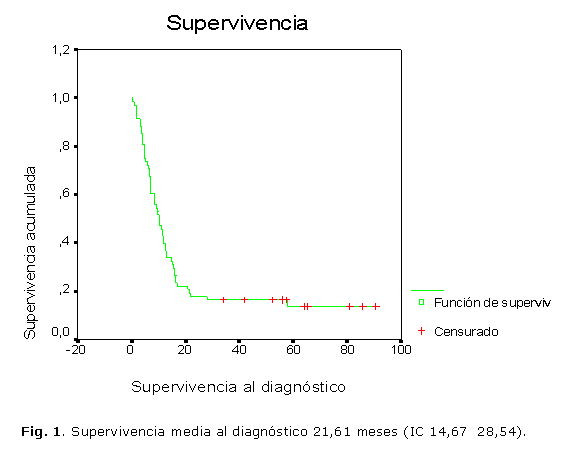
Se establecieron 2 grupos de edades: menores de 60 años y mayores de esa edad. La mediana de supervivencia encontrada en ambos grupos fue de 10,23 meses (IC 8,31 12,16) y 8,33 meses (IC 4,69 11,98), (p = 0,39) diferencia que no fue estadísticamente significativa.
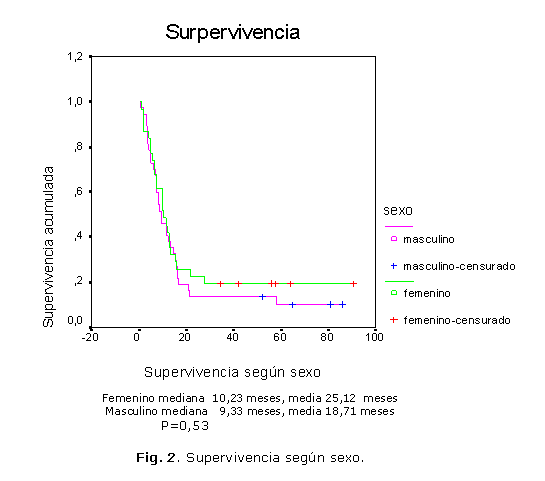
Teniendo en cuenta el sexo, se encontró una mediana de supervivencia en las mujeres de 10,23 meses (IC 8,20 12,27) y en los hombres, de 9,33 meses (IC 5,39 13,27) p =0,53 lo que muestra una tendencia a una mayor supervivencia en el sexo femenino (fig. 2).
Según el estadio, la mediana de supervivencia hallada en la enfermedad limitada fue de 12,50 meses (IC 9,39 15,61) y en la enfermedad extendida, 6,57 meses (IC 2,61 10,53) p =0,00 lo que resulta estadísticamente significativo (fig. 3).

Al momento de este reporte se encuentran vivos 5 pacientes, 4 de EL y 1 de EE, todos fueron respondedores al tratamiento y se encuentran dentro de los que se logró control de la enfermedad. La supervivencia de ellos se encuentra entre los 15 y 44 meses.
En la EE se considera la supervivencia relacionada con el número de sitios metastáticos; los pacientes con un solo sitio metastático presentan una mediana de supervivencia de 10,17 meses (IC 7,37 12,96) mientras que en los de mas de uno fue de 6,37 meses (IC 3,78 8,95) p =0,098.
DISCUSIÓN
La quimioterapia combinada continúa siendo la piedra angular en el tratamiento del carcinoma de células pequeñas, para ambos estadios. En general, la administración de etoposido y cisplatino mas irradiación torácica en aquellos pacientes que se presentan con buen estado general al diagnóstico y estadio de EL debe producir un índice de respuesta de 80 % o mayor, con una mediana de supervivencia que puede llegar a exceder los 17 meses y una supervivencia libre de enfermedad a 5 años de 12-25 %. Los pacientes con EE que reciban el tratamiento de quimioterapia deben presentar un índice de respuesta completa de alrededor de 20 % y supervivencia por encima de los 7 meses.4
Al considerar los aspectos demográficos de los pacientes estudiados se encontró que hubo predominio del sexo masculino, con una relación hombre/mujer igual 1,2:1; la mayoría de ellos eran fumadores, lo que se encuentra en concordancia con lo reportado en la literatura.5 Existen características previas al tratamiento en los pacientes con carcinoma de células pequeñas, que, al igual que en el carcinoma de células no pequeñas, han sido asociados con diferencias en la supervivencia.6 En este estudio solo se encontró tendencia a una mayor supervivencia en las mujeres.
Más de la mitad de los pacientes presentaban buen estado general al diagnóstico.
En los casos estudiados se encontró que el 68 % fueron estadiados como EL, lo que no guarda relación con lo reportado internacionalmente, ya que las dos terceras partes de este tipo de tumor son diagnosticados en estadio de EE.7 La localización fue principalmente hacia los lóbulos superiores con un predominio del pulmón derecho.
En los pacientes que resultaron evaluables se observó un índice de respuesta objetiva (respuesta completa más parcial) del 26 % lo que resulta bajo en relación con lo que se reporta en la literatura actual; sin embargo, al considerar aquellos pacientes que presentaron estabilización de la enfermedad se observa que hubo un 56 % de control.
Sundstrom y otros, en un gran ensayo clínico randomizado, en el cual comparaban el régimen de cisplatino/etoposido vs. ciclofosfamida, doxorrubicina y vincristina CAV,8 encontraron una mediana de supervivencia en la enfermedad limitada de 14,5 meses para aquellos que recibieron la combinación de platino y 9,7 meses para aquellos asignados al esquema CAV. Todos nuestros pacientes recibieron este esquema terapéutico, sin embargo, nuestros resultados distan de lo reportado por estos autores. Cuarenta y cuatro de nuestros pacientes recibieron quimioterapia concurrente con irradiación torácica. Considerando los factores que pueden influir en la supervivencia del carcinoma de células pequeñas en estadio de enfermedad limitada resulta interesante evaluar si la radioterapia pudiera contribuir a mejorar la eficacia del tratamiento sistémico. En cuanto a la enfermedad extendida, la mediana de supervivencia exhibida al nivel mundial es de 7 a 9 meses aun con las combinaciones terapéuticas más actuales. En el presente estudio, la mediana de supervivencia alcanzada en este estadio no dista de lo que señalan otros autores.5,6,9
En conclusión, en este estudio retrospectivo se encontró un índice de control de la enfermedad de más del 50 % de los pacientes tratados, lo que refleja el beneficio aportado a la supervivencia y la calidad de vida; sin embargo, estos resultados deben mejorarse.
Existen varios productos antitumorales que resultan novedosos y están siendo investigados en el carcinoma de pulmón de células pequeñas, dentro de los cuales se incluyen c-kit,10 matriz metalloproteinasa11 y vacunas de gangliósidos,12 por lo que se considera que estos pacientes podrían beneficiarse más al incluirlos en protocolos de investigación con estos nuevos productos.
REFERENCIAS BIBLIOGRAFICAS
1. Barnard W. The nature of the "oat-celled sarcoma" of the mediastinum. J Pathol. 1926;29:241-4.
2. Jackman MD, Jonson BE. Small-cell lung cancer. Lancet. 2005;366:1385-96.
3. Watson WL, Berg JW. Oat cell lung cancer. Cancer. 1962;15:759-68.
4. Janne PA, Friedlin B, Saxman S. Twenty-five years of clinical research for patients with limites stage small-cell lung carcinoma in North America. Cancer. 2002;95:1528-38.
5. Khuder SA, Mutgi AB. Effect of smoking cessation on major histologic types of lung cancer. Chest. 2001;120:1577-83.
6. Paesman M, Sculier JP, Lecomte J. Prognostic factors for patients with small-cell lung carcinoma: analysis of a series of 763 patients included in 4 consecutive prospective trials with a minimum follow-up of 5 years. Cancer. 2000;89:523-33.
7. Johnson DH, Einnhorn LH, Birch R. Randomizaed comparison of high dose vs conventional dose cyclophosphamide, doxorubicin, and vincristine for extensive stage small cell lung cancer: a phase III trial of the southeastern Cancer Study Group. J Clin Oncol. 1994;5:1737-8.
8. Sundstrom S, Bremnes RM, Kaasa Sl. Cisplatine and Etoposide regime is superior to cyclophosphamide, Epirubicin and vincristine regime in small-cell lung cancer: results from a randomized phase III tril with with five years follow-up. J Clin Oncol. 2002;20:4665-72.
9. Spiegelman D, Maurer LH, Ware JH . Prognostic factors in small-cell carcinoma of the lung: an analysis of a series of 1521 patients. J Clin Oncol. 1999;7:344-54.
10. Johnson BE, Fischer T, Fischer B. Phase II study of Imatinib in patients with small-cell lung cancer. Clin Cancer Res. 2003;9:5880-7.
11. Eckardt JR, von Pawel J, Manikas G. Comparable activity with oral Topotecan/cisplatin (TC) and IV Etoposide/Cisplatin(PE) as treatment for chemotherapy naive patients with extensive disease small-cell lung cancer (ED-SCLC): final results of a randomized phase III trial. Proc Am Soc Clin Oncol. 2005.LBA 70003.
12. Neninger E, Diaz RM, De la Torre A, Vazquez AM. Active immunotherapy with an Anti-idiotipe Vaccine in Patients with Small Cell Lung Cancer. Report of a Phase I trial. Cancer Biology and Therapy. 2007;6:1721-27.
Recibido: 26 de agosto de 2008.
Aprobado: 17 de noviembre de 2008.
Dra. Elia Neninger Vinageras. Hospital Clinicoquirúgico "Hermanos Ameijeiras" San Lázaro No. 701 entre Belascoaín y Marqués González, Centro Habana, Ciudad de La Habana, Cuba.














