Introducción
El Linfoma de Hodgkin (LH) constituye el 0,5 % de todas las neoplasias y el 10 % de las hemopatías malignas.1 Las estrategias terapéuticas actuales de primera línea incluyen la poliquimioterapia, el uso racional de la radioterapia (RT) (en combinación o no con la quimioterapia) y el empleo de un tratamiento ajustado al riesgo del paciente.2,3,4,5,6,7 En consecuencia, se logran alcanzar, por lo general, altas tasas de remisión completa (80-90 %).
A pesar de los éxitos alcanzados en el manejo del LH, un grupo de pacientes no logra un control efectivo de la enfermedad con el tratamiento de inducción, (también conocido como fallo de inducción) o recaen después de haber alcanzado la remisión completa. Es en estas situaciones en las que se realiza el trasplante autólogo de progenitores hematopoyéticos (TAPH).8,9
Este es un procedimiento complejo y de participación multidisciplinaria. Se aplican altas dosis de quimioterapia y/o radioterapia (RT) (conocido como tratamiento acondicionante [TA]) con posterior rescate hematológico dado por la infusión de progenitores hematopoyéticos. El TAPH tiene como principal objetivo eliminar todos aquellos elementos tumorales residuales que puedan persistir y permita prolongar la supervivencia y eventual cura de los pacientes.10
Representa un procedimiento agresivo, por lo que muchas investigaciones se han centrado en la evaluación de la mortalidad relacionada con el trasplante (MRT), especialmente la temprana (antes de los 100 dίas pos-TAPH), la que traduce calidad y seguridad del trasplante.11
En el Servicio de Hematología del Hospital Clínico Quirúrgico “Hermanos Ameijeiras” el TAPH se inició en el año 1985. En el presente estudio se evaluó la respuesta al trasplante autólogo de progenitores hematopoyéticos en los pacientes con LH.
Métodos
Se realizó un estudio explicativo con carácter retrospectivo de los pacientes con diagnóstico de LH, a quienes se les realizó TAPH en el Hospital Clínico Quirúrgico “Hermanos Ameijeiras”, durante el período comprendido entre enero de 1991 y noviembre de 2018.
De un total de 63 casos se seleccionaron 60 para el estudio de acuerdo a los siguientes criterios de inclusión: tener entre 17 y 60 años de edad y haber presentado fallo de inducción o recaída quimio-sensible. Los criterios de exclusión fueron los pacientes con sepsis activa, pacientes refractarios a tratamiento (quimio-resistentes) y los pacientes con datos incompletos para los efectos de la presente investigación.
El diagnóstico histológico se basó en la clasificación de la OMS del 201612 y la estadía de los casos siguió las recomendaciones de Ann Arbor.13
La evaluación del estado de la enfermedad se hizo de acuerdo a los criterios del Consenso del subcomité de revisión de los criterios de respuesta de 2007.14
A todos los pacientes se les realizó una exhaustiva evaluación pre-trasplante, debiendo constatarse la presencia de funciones cardíaca, hepática, renal y pulmonar normales, además de la ausencia de focos sépticos.
A todos los casos se le aplicó el TA, que consistió en la aplicación de muy altas dosis de quimioterapia acompañado o no de RT tipo irradiación corporal total. Las drogas empleadas estuvieron de acuerdo a la condición clínica individual de cada caso y a la disponibilidad del fármaco en cuestión al momento del TAPH.
En todos los pacientes, se utilizaron células progenitoras hematopoyéticas (CPH), ya sea de médula ósea o de sangre periférica, conservadas a 4ºC, sin criopreservación. La técnica de extracción e infusión de médula ósea no criopreservada fue la descrita desde la década de los años 8015 y en los trasplantes cuyas CPH se obtuvieron de sangre periférica, se empleó el método comunicado por Ruiz-Argüelles y otros.16
En todos los casos, el día de la infusión de las CPH se consideró el día cero. Posterior a ello a los pacientes se les inició un aislamiento protector en cuartos simples, con filtro de aire de alta eficiencia y con una alimentación estéril. De acuerdo a la disponibilidad, después del trasplante se empleó el factor estimulante de colonias granulocíticas para acortar el período de neutropenia. La antibioticoterapia de amplio espectro se utilizó cuando los pacientes presentaron una neutropenia febril. Se mantuvo un apoyo racional con hemocomponentes (concentrado de hematíes y de plaquetas) de acuerdo a la condición clínica de los casos. La recuperación hematológica estuvo determinada por un conteo absoluto de neutrófilos mayor a 500 x mm3 durante tres días consecutivos.
Los resultados pos-TAPH fueron evaluados a través del análisis del estado de la enfermedad (remisión completa vs enfermedad activa) al cabo de los tres meses. La supervivencia global se consideró desde la fecha de diagnóstico hasta la fecha de fallecimiento o última consulta y la sobrevida libre de enfermedad desde el día cero del trasplante hasta la recaída, muerte o fecha de última consulta. Ambas fueron estimadas a los 5 años. La MRT a los 100 días se consideró la muerte dentro de este período relacionada directa o indirectamente con los tratamientos y/o procederes recibidos por el paciente durante el TAPH.
Para el análisis estadístico, se empleó la información de las historias clínicas de los pacientes y se utilizó una base de datos en Excel. Primero se describió la muestra de pacientes evaluados a través de todas las variables demográficas y clínicas estudiadas mostrando los resultados en tablas resúmenes. Para las variables continuas se calculó la media con la desviación estándar y se presentaron los valores mínimo y máximo. En caso de las variables categóricas se calculó la frecuencia absoluta y el porcentaje por cada categoría descrita.
Para determinar la tasa de respuesta se describió el número y porcentaje de sujetos en cada categoría con la variable estado de la enfermedad previo al trasplante y a los tres meses de la intervención. Para este análisis se incluyeron a los pacientes que tenían un mínimo de tres meses de seguimiento.
Para evaluar la supervivencia se construyeron curvas por el método de Kaplan-Meier.17 Se especificó la tasa de SG a los cinco años y de SLE en ese mismo tiempo. Para estos análisis, se utilizó el paquete estadístico SPSS versión 18.0 y el programa EPIDAT versión 3.0.
La revisión de historias clínicas y el procesamiento de datos tuvo un carácter científico, anónimo y sin implicar perjuicio a los pacientes.
Resultados
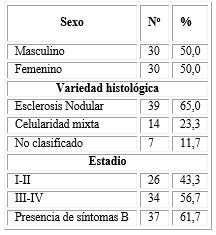
La variante histológica más frecuente resultó la esclerosis nodular (65,0 %), siguiéndole en orden de frecuencia la celularidad mixta (23,3 %). En un pequeño grupo de pacientes, la enfermedad no se pudo clasificar (11,7 %). Predominaron los casos que debutaron en estadios avanzados (56,7 %) y con síntomas B (61,7 %) (tabla 1).
La edad promedio de los casos trasplantados fue de 31,5 años. La mayoría de los casos se trasplantaron con una enfermedad aún activa 31 (51,7 %) y con una remisión completa de 29 (48,3). El porcentaje de la desviación estándar se calculó en base al total de pacientes (n=60).
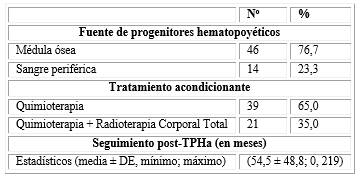
La fuente de progenitores hematopoyéticos más empleada fue la médula ósea con 76,7 % de pacientes, los TA más utilizados resultaron aquellos que solo incluían quimioterapia (65,0 %) y hubo un seguimiento posterior al TAPH como promedio de 54,5 meses (tabla 2).
Al evaluarse la respuesta al TAPH al cabo de los tres meses (tabla 3), se comprobó que la cifra inicial de 29 pacientes con enfermedad en actividad (50,9 %) se redujo a solo cinco casos (8,8 %), lo que representa una tasa de respuesta en este grupo de pacientes de un 82,7 %. Todos los que tenían respuesta completa en el momento de la intervención se mantuvieron con esa respuesta a los tres meses.
Tabla 3 Estado de la enfermedad antes del TAPH y a los tres meses de su realización

*Se excluyen tres casos que fallecieron antes de los tres meses posteriores al trasplante
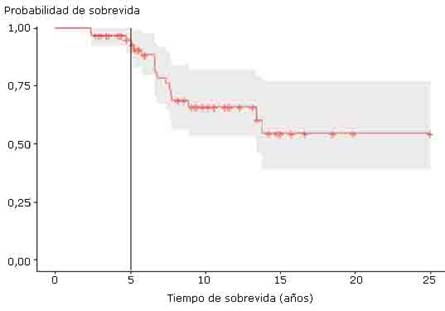
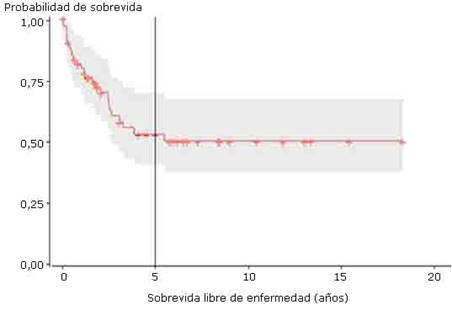
Las figuras 1 y 2 muestran los estimados de SG y SLE posterior al trasplante en la cohorte estudiada, observándose que a los cinco años estas son de un 94,7 % y un 51,7 %, respectivamente.
Solo tres casos fallecieron en el período inmediato pos-TAPH, dos a consecuencia de infecciones bacterianas y uno por enfermedad veno-oclusiva hepática, por la que la MRT a los 100 días fue de un 5 %.
Discusión
Evaluar los resultados de procedimientos terapéuticos resulta de gran importancia en general, pero es de particular relevancia cuando se trata de modalidades de tratamiento agresivas como resulta el TAPH.
El subtipo histológico más frecuente resultó la esclerosis nodular, lo que coincide con ser la variedad histológica más frecuente entre todos los pacientes diagnosticados con LH en general.18
Dentro de la cohorte estudiada predominaron los pacientes con estadios avanzados y con síntomas B, lo que está en relación con que sean estos los tipos de casos que con mayor asiduidad tienen recaídas tributarias de incluir al TAPH en la estrategia de tratamiento.
Al analizar los datos relacionados con la edad, nos percatamos que como promedio los casos trasplantados fueron pacientes jóvenes, sin superar ninguno los 55 años, lo que se debe a que este tipo de tratamiento puede tener potenciales consecuencias fatales, de manera que solo se haya aplicado a pacientes en los que no existían comorbilidades ni deterioro orgánico que impidiera su empleo, hecho que ha limitado su empleo en poblaciones de pacientes ancianos. También hay que tener en cuenta que esta enfermedad es más frecuente entre los pacientes jóvenes, lo que contribuye a la realización del TAPH con mayor.19
Un número importante de pacientes se trasplantaron con enfermedad en actividad, indicador de una enfermedad de difícil control y que constituye uno de los criterios en los que se puede recomendar el TAPH como alternativa terapéutica que pueda solucionar la enfermedad en estas situaciones.
En una mayor cantidad de pacientes, se empleó la médula ósea como fuente de progenitores hematopoyéticos, lo que está condicionado porque esta fue la fuente primordial utilizada al inicio de la práctica del procedimiento, hasta que surgió la posibilidad de obtenerlos de sangre periférica; no obstante, la insuficiente disponibilidad de las máquinas de aféresis y los accesorios necesarios para llevarlas a cabo también han influido en el mayor uso de la médula ósea en nuestro medio.
En relación con los TA utilizados, predominaron los que solo contemplaron el empleo de la quimioterapia. La RT se vio limitada en su uso por el hecho de que muchos casos habían estado irradiados antes como parte de los protocolos de tratamiento combinados que habitualmente se emplean en los estadios iniciales de la enfermedad, además en los últimos años, ha sido desplazada progresivamente por TA con quimioterapia más óptimos y que evitan las conocidas toxicidades que a mediano y largo plazo ocasiona la RT (toxicidad a órganos y tejidos [fibrosis pulmonar, cardiotoxicidad e hipotiroidismo entre otros], segundas neoplasias e infertilidad). El seguimiento postrasplante de 54,5 meses como promedio, permitió obtener valoraciones útiles en términos de supervivencia.
En la cohorte evaluada se apreció que más de la mitad de los casos llegaron al TAPH con una enfermedad aún presente; sin embargo, este grupo se redujo considerablemente en la primera evaluación sobre el estado de la enfermedad realizada a los tres meses pos-TAPH, quedando en un 8,8 % (solo cinco pacientes), lo que representa una elevada tasa de respuesta de un 82,7 %. Esta situación también traduce un alto nivel de efectividad y de control de la enfermedad del TA empleado, lo que en última instancia es el propósito inmediato que se persigue al realizar un TAPH. Todos los casos trasplantados con enfermedad en remisión completa mantuvieron este estatus al llegar a los tres meses como era esperado. En los resultados comunicados por Sirohi y otros,20 en su estudio sobre 195 casos trasplantados, obtuvieron una tasa de respuesta de un 61 %, inferior a la aquí observada, y que pudo estar influenciado por el hecho de haber incluido en su serie 45 casos con enfermedad refractaria; hecho que también pone de relieve la importancia del estado de la enfermedad previo al trasplante.
En una publicación reciente, investigadores brasileños en una serie de 107 casos, comunicaron una respuesta pos-TAPH de un 84,1 %, semejante a la alcanzada en el presente estudio.21
Los análisis de supervivencia arrojaron una SG y SLE a los cinco años de un 94,7 % y un 51,7 % respectivamente, los que representan resultados satisfactorios. Estudios anteriores con resultados similares a los de este estudio son los que han apoyado que en la actualidad se mantenga como estándar de tratamiento la realización del TAPH en los pacientes con LH en fallo de inducción o en recaídas quimiosensibles, aún en el contexto actual de aplicación de novedosas drogas (anticuerpos monoclonales anti CD30 y anti PD-1).22
En este sentido cabe señalar dos trabajos de referencia realizados en esta área, por investigadores británicos y alemanes en 1993 y 2002, respectivamente,23,24 que resultaron los primeros en demostrar la superioridad del TAPH con relación a la quimioterapia convencional.
Sin embargo, estos estudios no lograron demostrar un beneficio claro en términos de SG, pero posteriormente Lavoie y otros desde Canadá,25 sí lograron evidenciar una mejoría en la SG, en su investigación realizada sobre los primeros 100 casos trasplantados en Vancouver, dando a conocer un 54 % de SG, estimación hecha incluso a los 15 años.
En otra investigación desarrollada por Smith y otros26 sobre los resultados en dos centros norteamericanos (Memorial Sloan-Kettering Cancer Center y Cleveland Clinic Taussig Cancer Institute) en 214 casos trasplantados, dieron a conocer una SG y SLE estimada a los seis años de 61 %/55 % y 47 %/35 %, respectivamente para cada centro, siendo estos últimos muy inferiores a lo alcanzado en el presente estudio.
Pereira Cortez y otros27 desde Brasil, informaron en 2011 los resultados de su investigación sobre la aplicación del TAPH en 106 pacientes con LH, ellos comunican estimaciones en términos de SG y SLE al cabo de cinco años de 86 % y 60 % respectivamente, valores que difieren ligeramente a los obtenidos en el presente estudio.
Estudios más recientes también han evaluado estos aspectos. Investigadores del sur de Alemania estudiaron una cohorte de pacientes muy similar a la presente (66 pacientes, desde 1996 y hasta 2017), en los que observaron una SG de 59,5 % y una sobrevida libre de progresión (SLP) de 46,1 % a los cinco años.28 En tanto, Fatobene y otros21 comunicaron una SLP y SG a los cinco años de 59,9 y 74 % respectivamente.
En relación con la MRT a los 100 días, se comprobó que fue de solo un 5 %, con un total de tres fallecimientos en este período, dos a causa de sepsis bacterianas y otro a consecuencia de un síndrome de obstrucción sinusoidal. Estudios iniciales realizados al respecto, reportaron en la década de los años 90 una MRT de un 13 %29 resultado insatisfactorio a la luz de los actuales estándares de calidad asociados al TAPH. Otro estudio similar y que incluyó casos de hasta 63 años de edad, reportó un 9 % de MRT temprana.30
En un análisis muy reciente que comprendió decenas de miles de casos trasplantados en Europa desde 1980 y donde se evalúa este aspecto, los investigadores determinaron una MRT a los 100 días de un 7,34 % y 3,67 % de acuerdo a si el TAPH era antes o después del 2001, respectivamente.31
Un estudio similar realizado en Finlandia, donde se analizó la MRT en igual período, en 1482 casos sometidos a TAPH en diversas hemopatίas malignas y que incluyó a 86 casos con LH, comunican un excelente resultado de solo un 1,2 % de MRT. Las principales causas que señalan dentro de estas son las infecciones seguido de la toxicidad orgánica.11
En el estudio ya citado anteriormente de Pereira Cortez y otros,27 se reseña una MRT temprana de un 3,74 %, con cuatro pacientes fallecidos, tres de ellos fueron a causa de infecciones, y el otro a causa de un daño orgánico, en su caso a nivel pulmonar; similar a lo ocurrido en la presente serie, donde predominaron las infecciones seguida del daño irreversible a órganos (localizado esta vez en el hígado). En este sentido, investigadores estadounidenses también han dado a conocer resultados favorables, con una MRT a los 100 días de un 4 %.26
No obstante, lo obtenido en el presente estudio representa también una proporción baja de casos con desenlace fatal, teniendo en cuenta que nuestra cohorte es más pequeña y que incluyó pacientes desde la década de los años 90, en la que los tratamientos de soporte no estaban tan desarrollados como en la actualidad.
En el presente trabajo se confirma al TAPH como una alternativa terapéutica válida para aquellos casos con LH e indicación de este, logrando tasas de respuesta a los 3 meses y estimaciones de supervivencia a los cinco años de SG y SLE similares a lo comunicado en la literatura internacional; con una MRT a los 100 días baja para un recurso terapéutico de características agresivas como lo es el TAPH, lo que implica que su aplicación se ha realizado con un perfil de seguridad satisfactorio.