Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Pediatría
versión impresa ISSN 0034-7531
Rev Cubana Pediatr vol.86 no.2 Ciudad de la Habana abr.-jun. 2014
Revista Cubana de Pediatría. 2014; 86(2)
ARTÍCULO ORIGINAL
Experiencia en el tratamiento de los hemangiomas infantiles con propranolol de producción nacional
Experiences in treating infantile hemangiomas with Cuban-made propranolol
MSc. Dra. Edelisa Moredo Romo, MSc. Dra. Fernanda María Pastrana Fundora
Hospital Pediátrico "Juan Manuel Márquez". La Habana, Cuba.
RESUMEN
Introducción: los hemangiomas infantiles son los tumores más frecuentes de la infancia. Aunque son de naturaleza benigna, su rápido crecimiento los puede tornar destructivos, incluso con riesgo vital, en alrededor de 1 % de los casos. En la actualidad han sido utilizados los betabloqueadores, como el propranolol oral, con muy buenos resultados.
Objetivo: evaluar el efecto y seguridad del propranolol de producción nacional para el tratamiento de hemangiomas infantiles en fase proliferativa.
Métodos: estudio descriptivo y aplicado -efectuado desde el 1 de diciembre de 2010 hasta el 31 de junio de 2012- de una serie de 21 pacientes con 26 hemangiomas infantiles en fase proliferativa, atendidos en la Consulta de Dermatología del Hospital Pediátrico Docente "Juan Manuel Márquez", y tratados con propranolol de producción nacional por vía oral a 2 mg/kg/día en 2 subdosis. Los pacientes fueron evaluados en consulta quincenal hasta el tercer mes de tratamiento, y después, mensualmente, hasta los 6 meses de duración de este. Se realizó un registro de los efectos adversos.
Resultados: en todos los casos, en los primeros días después de comenzado el tratamiento, su efecto positivo (cambios favorables en la coloración o tamaño) fue evidente. Los efectos adversos fueron leves y autolimitados. Se alcanzó respuesta excelente o buena en el 99 % de los pacientes a los 6 meses de tratamiento.
Conclusiones: el esquema de tratamiento utilizado con el propranolol oral de producción nacional induce una mejoría rápida de los pacientes con hemangiomas infantiles, acortando considerablemente la evolución natural de estos tumores, con escasos efectos secundarios.
Palabras clave: hemangiomas, angiomas, propranolol, betabloqueadores, infancia.
ABSTRACT
Introduction: infantile hemangiomas are the most frequent tumors in children. Although they are generally benign, its fast growth may turn them into life-threatening destructive tumors in roughly 1 % of cases. At present, betablockers such as oral propranolol have been used with very good results.
Objectives: to evaluate the effects and safety of Cuban-made propranolol for the treatment of infantile hemangiomas in proliferation phase.
Methods: descriptive applied study of 21 patients with 26 infantile hemangiomas in proliferation phase. It was conducted from December 1st 2010 through June 31st 2012. The patients had been seen at the dermatology department of "Juan Manuel Márquez" teaching pediatric hospital and treated with Cuban-made orally administered propranolol at 2 mg/kg/day divided into 2 sub-doses. They were evaluated every 15 days up to the third month of treatment and monthly up to the 6 months of treatment. Adverse effects were recorded.
Results: few days after the beginning of the treatment, the positive effect was evident in all the cases (favorable changes in staining or size). The adverse effects were slight and self-limited. The response to treatment was good or excellent in 99 % of patients after 6 months of treatment.
Conclusions: the treatment with Cuban-made orally administered propranolol induces rapid improvement of infantile hemangiomas in these children, considerably shortening the natural evolution of these tumors with low secondary effects.
Keywords: hemangiomas, angiomas, propranolol, betablockers, childhood.
INTRODUCCIÓN
Los hemangiomas infantiles (HI) son los tumores benignos más comunes de la infancia, y consisten en neoplasias vasculares que crecen por una rápida proliferación celular a partir de las células endoteliales.1
Los HI durante su evolución natural cursan por 3 etapas o fases: una fase de proliferación rápida, en la cual el tumor está en constante crecimiento; seguido de una fase de involución prolongada; y una tercera fase residual fibrótica. Algunos autores plantean que el 50 % de los HI se resuelven a los 5 años, 70 % a los 7 y 90 % a los 10 años.2,3
Aproximadamente 20 % de los hemangiomas en el transcurso de su fase de crecimiento dan lugar a complicaciones, generalmente locales, con compresión u obstrucción de estructuras importantes (ojos, nariz, boca, vía aérea, etc.) y con deformidad estética.2
Los hemangiomas superficiales suelen llegar a su tamaño más grande en un período de 6-8 meses, pero los hemangiomas profundos pueden presentar un crecimiento de 12 a 14 meses, e incluso, de hasta 2 años. Aproximadamente un 20-40 % de los hemangiomas dejarán pequeñas lesiones cicatriciales. Los hemangiomas localizados en la nariz, labios y área parotídea tienen una fase involutiva más lenta.4
Los hemangiomas faciales de gran tamaño pueden distorsionar las estructuras anatómicas de forma irreversible. Aunque es conocida la reducción progresiva a partir de una determinada edad, es aconsejable tratar los hemangiomas de gran tamaño o con complicaciones.5
La frecuencia cada vez mayor con la que se registran casos en niños, está haciendo que avance la investigación en la materia, y aunque se desconozca su causa, se ha comprobado que son más frecuentes en las personas de piel blanca, y puede influir, además de la prematuridad del bebé y el bajo peso al nacer, la edad de la madre y algún factor genético.3,6
Han sido utilizados diferentes esquemas de tratamiento para los HI. Los corticoides intralesionales, o por vía oral, han sido casi una elección clásica hasta el momento; también han sido utilizados el interferón, la vincristina y el imoquimod para estos fines. En los últimos años han aparecido algunas publicaciones sobre el uso del propranolol en el tratamiento del HI.5,7
El propranolol, como opción terapéutica para los HI, fue propuesto por la doctora CristhineLéauté-Labréze, en un trabajo presentado en la Jornada Dermatológica de París, en Diciembre de 2007,8 y posteriormente, en el 17o Workshop on Vascular Anomalies, realizado en Boston en junio de 2008, donde se presentó una serie de 18 pacientes que fueron tratados con propranolol a 2 mg/kg/d, y se observó en todos cambios en el color y tamaño a las 24 h de tratamiento.9
Otros trabajos presentados con series muy pequeñas de casos han demostrado los beneficios de este medicamento en el tratamiento del HI,5,10,11 y, aunque su utilidad terapéutica fue hallada de manera accidental al administrar este medicamento a pacientes afectados de trastornos cardiovasculares pero que presentaban HI, no se conoce con claridad qué hace el propranolol para evitar el crecimiento de este tipo de tumores. La hipótesis es que esta droga favorecería la apoptosis de las células endoteliales capilares y la disminución de la expresión del factor de crecimiento vascular endotelial y del factor básico de crecimiento de fibroblastos.11 También tiene un rol selectivo en la inhibición de la expresión de la matalo-proteinasa 9 (MMP-9), por lo que aumenta sus propiedades antiangiogénicas.12,13
En nuestro centro, desde el año 2009, se ha aplicado esta opción terapéutica en un grupo de pacientes con excelentes resultados,14,15 por lo que es de interés mostrar nuestra experiencia, aunque sea en una serie pequeña de pacientes, si se tiene en cuenta que en el mundo no hay reportes con series importantes de casos.
El objetivo propuesto en este estudio es evaluar el efecto del propranolol de producción nacional en el tratamiento de los HI de los pacientes, así como su seguridad, y precisar los efectos adversos que pudieran presentarse durante su administración.
MÉTODOS
Se realizó un corte de una investigación prospectiva y longitudinal en desarrollo: Hemangiomas infantiles. Opción terapéutica con Propranolol, en un Centro de Referencia Nacional, donde acuden pacientes de todas las provincias del país.
Se seleccionaron pacientes de ambos sexos, menores de 2 años de edad, residentes en Cuba, diagnosticados clínicamente con HI, en consulta ambulatoria del Hospital Pediátrico Docente "Juan Manuel Márquez", de La Habana. En el periodo analizado: 1º de diciembre de 2010 al 31 de diciembre de 2011, se diagnosticaron 32 pacientes con HI, pero solo 21 necesitaban de tratamiento sistémico. Estos 21 pacientes cumplieron además con los criterios de inclusión y de exclusión siguientes, y en consecuencia, integraron la muestra estudiada. A ellos se les administró propranolol sistémico, y se evaluaron quincenalmente hasta el tercer mes de tratamiento, y mensualmente hasta los 6 meses. Previamente fue firmado el consentimiento informado por los padres o tutores. Se realizó un registro gráfico del paciente en cada control.
Criterios de inclusión:
- Pacientes con HI.
- Tener una edad máxima de 2 años.
- Consentimiento informado firmado por el padre, madre o tutor.
Criterios de exclusión:
- Pacientes que presenten manifestaciones de hipersensibilidad al propranolol.
- Pacientes que presenten una enfermedad de base para la cual esté contraindicado el propranolol.
- Familiar responsable poco cooperativo.
Criterios de diagnóstico:
Consistió fundamentalmente en un examen físico, en el cual se observó un aumento de volumen con coloración rojiza, un halo telangiectásico, o una lesión que simulaba un hematoma. La evolución natural de la enfermedad referida por los padres fue un componente importante del diagnóstico.
A todos los pacientes se les realizó ecografía doppler de la lesión, ultrasonido abdominal o transfontanelar en caso necesario, y valoración por cardiología.
Clasificación de los hemangiomas:
Los hemangiomas fueron clasificados, según su ubicación en los planos de la piel, en:
Superficial: se ubica en la dermis superficial. Se presenta como un solevantamiento o pápula, o bien como placa o nódulo rojo brillante, bien delimitada, firme, de superficie lisa o irregular.
Profundo: se localiza en la dermis profunda y/o tejido subcutáneo. Corresponde a una masa o nódulo blando, mal delimitado, de color piel o tinte azulado.
Mixto: combinación de las formas anteriores.
Efecto clínico del tratamiento:
Para medir el efecto clínico del tratamiento se tuvo en cuenta el tamaño del hemangioma (medido en cm), la consistencia (clasificada en dura, semiblanda o blanda), y el color de la lesión (catalogado como rojo intenso o violáceo, rosado intenso, rosado apagado, o blanqueamiento de la lesión).
Respuesta al tratamiento:
La característica de la respuesta al tratamiento se definió de acuerdo con los criterios siguientes:
- Excelente: desaparición de la lesión.
- Buena: atenuación marcada de las lesiones en tamaño, consistencia y coloración, con una disminución evidente igual o mayor del 50 %.
- Regular: disminución moderada de las lesiones en tamaño, consistencia y coloración, con una disminución evidente menor del 50 %.
- Mal: cuadro clínico inicial de la lesión mantenido sin variación o empeorado.
Vía y dosis de administración del propranolol:
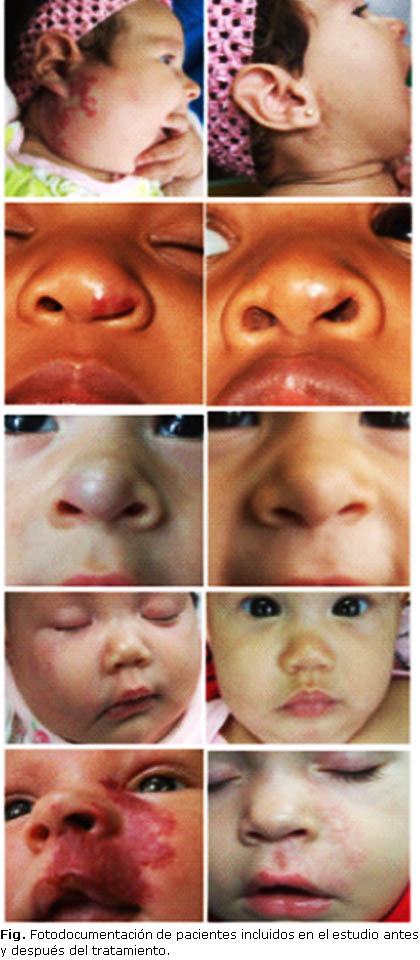
A cada paciente se le administró una dosis inicial de 1,5 mg/kg/día. A los 15 días esta dosis se elevó, y se mantuvo a 2 mg/kg/día por vía oral, dividida en 2 suddosis, durante un periodo de 6 meses, o bien hasta la desaparición de las lesiones en aquellos casos donde desaparecieron antes de los 6 meses, en quienes se redujo gradualmente la dosis hasta su supresión. A todos los pacientes se les tomó imagen gráfica antes y después del tratamiento, así como ecografía doppler evolutiva al final de este.
Para el procesamiento de la información, se creó una base de datos automatizada con la hoja de cálculo electrónica Excel 2007. Los datos primarios se procesaron con los programas informáticos STATISTICA 6.1, InStat 3.1 y CIA 4.2. Las variables cualitativas y la edad, llevadas a escala ordinal, se describieron estadísticamente mediante cifras frecuenciales y porcentuales (frecuencias absolutas y relativas). La investigación de la asociación de variables se llevó a efecto con la prueba homónima sustentada en la distribución X2. Se aplicó el test X2 de tendencia, para decidir si existía o no una tendencia lineal estadísticamente significativa, en el conjunto de determinadas categorías ordenadas en una tabla de contingencia. En todas las pruebas estadísticas inferenciales, se empleó el nivel de significación 0,05.
Para los porcentajes de interés, se calculó el intervalo de confianza con el 95 % de confiabilidad (IC al 95 % para proporciones), dado por sus cotas inferior y superior, el cual aporta el rango esperado de valores, donde se puede encontrar el por ciento correspondiente con ese nivel de confianza, en cualquier estudio que se pueda realizar con características similares al presente.
RESULTADOS
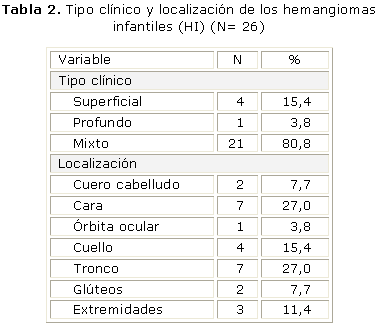
Se trataron 26 HI en 21 pacientes, ya que 3 de estos presentaron más de una lesión; en ninguno de los casos se presentó hemangiomatosis visceral. Existió un predominio numérico del sexo femenino con relación al masculino (relación de 3 a 1); la piel blanca fue la más frecuente. La edad media de los pacientes fue de 3 meses (tabla 1).
Las localizaciones más frecuentes de los HI fueron la facial y el tronco, seguidas del cuello y las extremidades. En cuanto a la variedad clínica, los HI mixtos fueron los más numerosos, seguidos de los hemangiomas superficiales; se presentó 1 solo caso de hemangioma profundo (tabla 2).
La tabla 3 se destinó a presentar la asociación entre la coloración del HI y el momento del tratamiento. Entre las cifras que llaman la atención, se encuentra la anulación de los porcentajes de coloración rojo intenso o violáceo, a partir del tercer mes de la terapéutica establecida, así como la modificación de las cifras de blanqueamiento, las que parten de la nulidad como es lógico, y llegan a alcanzar a casi las dos quintas partes de los pacientes. El vínculo entre la coloración del HI y el momento del tratamiento se reveló estadísticamente significativo (c2 de asociación= 19,3, gl= 2, p= 0,0001); además, se puso de manifiesto una tendencia significativa al aumento de los porcentajes de blanqueamiento de las lesiones angiomatosas con el decursar del tratamiento (c2 de tendencia= 15,9, gl= 1, p= 0,0001). En todos los HI, desde las primeras semanas, se empezó a notar un ablandamiento de la lesión, la cual, progresivamente, se hacía suave y reductible, sobre todo en los HI mixtos (los más voluminosos).
En la tabla 4 se registraron los datos pertinentes a la reducción del tamaño de los HI en función del momento del tratamiento. Las categorías utilizadas para plasmar la reducción fueron definidas por las autoras del presente trabajo, al mismo tiempo que, los momentos del tratamiento seleccionados para el examen de los datos, constituyen parte del método estipulado en la sección correspondiente. Llama la atención que, casi las tres quintas partes de los pacientes experimentaron una reducción completa de la lesión. El nexo entre las variables Reducción del tamaño del HI y Momento del tratamiento, fue estadísticamente significativo (c2 de asociación= 83,5, gl= 6, p= 0,0001). Ahora bien, si con propósitos de análisis se efectúa la fusión de las filas Completa e Incompleta por un lado, y de las filas Parcial y Nula por otro, se mantiene la significación estadística entre las mencionadas variables (c2 de asociación= 59,8, gl= 2, p= 0,0001), y se destaca, además, una tendencia significativa al incremento de los porcentajes de la primera de estas combinaciones (c2 de tendencia= 50,2, gl= 1, p= 0,0001).
Al evaluar integralmente la evolución de los hemangiomas, salta a la vista que, casi las tres quintas partes de estos exhibieron la respuesta calificada de excelente, con un IC que se extiende aproximadamente desde más de un tercio hasta una proporción que rebasa las tres cuartas partes, y son estos los valores que cabe esperar en estudios que puedan llevarse a efecto con un diseño semejante al actual (fig.). Este enfoque de los intervalos de confianza sirve para abstenerse de la formulación de pronósticos imprudentes, pues ellos permiten disponer de la justa medida de resultados posibles. En relación con los restantes intervalos, existen líneas de razonamiento totalmente similares; así, digamos, en otra investigación con el mismo perfil de la presente, la respuesta Buena puede lograrse solamente en una quinta parte de la casuística, pero también pudiera alcanzarse en prácticamente tres quintas partes de los pacientes sometidos al tratamiento de referencia (tabla 5).
En lo concerniente a las reacciones adversas en los casos tratados, las madres de 5 pacientes (23,8 %) refirieron sueño intranquilo en las primeras semanas de tratamiento, en 2 casos (9,5 %) se reportó disminución del apetito, y en ninguno se presentó hipotensión, bradicardia, hiperreactividad bronquial, hipoglicemia, u otros efectos adversos descritos en la literatura.
DISCUSIÓN
En los HI, cuando se completa su fase involutiva, solo el 7,3 % de los casos recobran su aspecto normal, porcentaje que coincide mayormente con los HI profundos, pero los HI superficiales y mixtos suelen alterar más la textura cutánea, y pueden dejar una zona de piel atrófica, hipoelástica, hipopigmentada o hiperpigmentada.16 Por esta razón, es necesaria una terapéutica cada vez más temprana, la cual puede evitar deformidades y mejorar la calidad de vida de los pacientes, debido al hecho que, un por ciento importante de estos tumores, se localizan en áreas visibles.
En nuestro estudio predominó porcentualmente el sexo femenino, lo cual coincide con lo reportado en otros estudios, en los que se plantea una relación, incluso mayor, de 3:1.17,18 A pesar de que en la literatura no se encontraron reportes en los que se asociara la presencia de los HI con el color de la piel, en la mayoría de las publicaciones en las que aparecen imágenes se aprecian niños de piel blanca, y esta característica sí se aviene con nuestro estudio. Resultaría interesante indagar en investigaciones futuras por qué es más frecuente esta afección en los pacientes de piel blanca.
La literatura reporta que, la mayoría de los HI se localizan en la región facial y el cuello,19-23 hallazgos que guardan analogía con los nuestros, con el detalle que, en nuestros casos, los HI del tronco fueron más frecuentes que los del cuello, y además, el 50 % de los pacientes con HI en esta localización tenían más de una lesión.
En este trabajo se constataron cambios relevantes desde las primeras semanas de tratamiento en relación con la coloración, la consistencia, y la reducción del tamaño de la lesión, llegando a desaparecer totalmente la lesión, o reducirse a discretamente perceptible en más del 80 % de los casos, resultados muy similares a los reportados por varios autores, quienes abogan por el uso del propranolol como primera línea de tratamiento de los HI.8,17,21-23
En el apartado de los efectos adversos, solo se encontraron sueños intranquilos, que cedieron después de la tercera semana de tratamiento, y no fueron necesarias la suspensión ni la reducción de la dosis del fármaco utilizado, lo cual apunta en la misma dirección que Bagazgoitia y otros,24 quienes reportan 10 casos con trastornos del sueño en una serie de 71 pacientes tratados con propranolol. Otro síntoma referido por 2 madres fue la inapetencia transitoria, elemento subjetivo del que no es posible precisar la relación directa con el empleo del medicamento, por no limitarse solo al tiempo de tratamiento. En definitiva, en este trabajo las reacciones adversas halladas fueron leves y cedieron espontáneamente, hecho que puede guardar relación con la adaptación al medicamento por los pacientes, sin ser necesaria la supresión del tratamiento.
Se concluye que en las más de 4 décadas de utilización internacional del propranolol en niños para tratar una u otra afección, no se ha reportado ningún caso de muerte ni de efecto cardiovascular grave. Hasta el momento de la redacción del presente reporte, el propranolol de producción nacional se ha mostrado seguro para el tratamiento de los HI: es un eficaz recurso farmacológico de fácil administración, no invasivo y asequible financieramente.
REFERENCIAS BIBLIOGRÁFICAS
1. Drolet BA, Esterly NB, Frieden IJ. Hemangiomas in children. N Engl J Med. 1999;341(3):173-80.
2. Escutia Muñoz B, Febrer Bosch I. Tratamiento médico de los hemangiomas. Piel. 2002;17(3):139-44.
3. Cáseres H, Velásquez F. Lesiones vasculares. En: Cáseres H, Velásquez F. Dermatología Pediátrica. Lima: Fondo Editorial del Instituto Nacional para la Salud del Niño; 2010. p. 126-8.
4. Tumores benignos [homepage en internet]. Madrid, España [citado 30 de octubre de 2009]. Disponible en: http://www.uv.es/derma/
5. Sánchez Pérez R, Cortes Mora P, González Rodríguez JD, Rodríguez Sánchez F, De la Peña de Torres J. Tratamiento del hemangioma infantil con propranolol. An Pediatr (Barc). 2010;72(2):152-4.
6. Bozan I, León C, Díaz M, Lago YZ. Comportamiento de los defectos congénitos en el municipio de Cabaiguán. Año 2006-2011. Gaceta Médica Espirituana [serie en Internet]. 2012 [citado 2 de febrero de 2013];14(3). Disponible en: http://revgmespirituana.sld.cu/index.php/gme/article/view/194
7. Zaher H, Rasheed H, Hegazy RA, Abedelhalim DM, Gawdat HJ. Oral propranolol: an effective, safe treatment for infantile hemangiomas. Eur J Dermatol. 2011;21(4):558-63
8. Léauté-Labréze C, Hubiche T, Boralevi F, Dumas de la Roque E, Thambo JB, Taibeb A. Les bétabloquates: une alternative á la corticotheérapie générales dans le traitement des hemangiomes infantiles. Comunicación oral. Journées Dermatologique de Paris, Société Française de Dermatologie. Paris, Francia, 4-8 de diciembre de 2007.
9. Léauté-Labréze C, Hubiche T, Boralevi F, Dumas de la Roque E, Thambo JB, Taibeb A. Propranolol for severe hemangiomas of infancy. N England J Med. 2008;358:2 649-51.
10. Baselga E. Propranolol for the treatment of infantile hemangiomas of infancy. Poster. 34th Annual Meeting of the Society for Pediatric Dermatology. Snowbird, UT, USA. 9-12 de Julio; 2008.
11. Cordisco MR. Propranolol en el tratamiento de los hemangiomas. Rev Dermat Ped Latinoamericana. 2008:6(2):95-6.
12. San V, de la Roque ED, Begel J, Boralevi F, Mazereeuw-Hautier J. Propranolol for severe infantile hemangiomas: follow-up report. Pediatrics. 2009;124:431-2.
13. Annabi B, Lachambre MP, Plouffe K, Moumdjian R, Beliveau R. Propranolol adrenergic blockade inhibits human brain endothelial cells tubulogenesis and matrix metalloproteinace-9 secretion. Pharmacol Res. 2009;60:438-45.
14. Moredo E, de la Peña T, Matos VL, Monzón M, Cárdenas MM. Presentación de 3 casos de hemangiomas infantiles tratados con propranolol. Rev Cubana Pediatr [serie en Internet]. 2011 [citado 20 de diciembre de 2012];83(3). Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0034-75312011000300012&lng=es&nrm=iso&tlng=es
15. Moredo E, Pastrana F. Tratamiento exitoso de un hemangioma de parótida con propranolol. Rev Cubana Pediatr [serie en Internet]. 2012 [citado 20 de diciembre de 2012];84(2). Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0034-75312012000200011&lng=es&nrm=iso&tlng=es
16. Metry DW, Hebert AA. Benign Cutaneous Vascular tumors of infancy: When to worry, what to do. Arch Dermatol. 2000;136:905-14.
17. Kramer D, Muñoz P, Alfaro P, Aranibar L, Cardenas L, Morovic CG, et al. Propranolol en el Tratamiento de los Hemangiomas de la Infancia. Rev Chil Pediatr. 2010;81(6):523-30.
18. Greco MF, Cardisco MR. Lesiones Vasculares. En: Laralde M, Abad E, Luna P. Dermatología Pediátrica. 2da. ed. Buenos Aires: Ediciones Journal; 2010. p. 505-24.
19. Weston WL, Lane AT, Morell JG. Lesiones vasculares. En: Dermatología Pediátrica. 4ta. ed. Barcelona: Elsevier; 2008. p. 237-55.
20. Sánchez R, Cortes P, González JD, Rodríguez F, De la Pena J. Tratamiento del hemangioma infantil con Propranolol. An Pediatr. 2010;72(2):152-4.
21. Fuchsmann C, Quintal MC, Giguere C. Propranolol as first-line treatment of head and neck hemangiomas. Archives of Otolaryngology-Head and Neck Surgery. 2011:137(5):471-8.
22. Zvulunov A, McCuaig C, Frieden IJ, Mancini AJ, Puttgen KB, Dohil M, et al. Oral propranolol therapy for infantile hemangiomas beyond the proliferation phase: a multicenter retrospective study. Pediatr Dermatol. 2011 Mar-Apr;28(2):94-8.
23. Sans V, de la Roque ED, Berge J, Grenier N, Boralevi F, Mazereeuw-Hautier J, et al. Propranolol for severe infantile hemangiomas: follow-up report. Pediatrics. 2009 Sep;124(3):e423-e431.
24. Bagazgoitia L, Torrelo A, Gutiérrez JC, Hernández-Martín A, Luna P, Gutiérrez M, et al. Propranolol for infantile hemangiomas. Pediatr Dermatol. 2011 Mar-Apr;28(2):108-14.
Recibido: 29 de julio de 2013.
Aprobado: 4 de agosto de 2013.
Edelisa Moredo Romo. Hospital Pediátrico "Juan Manuel Márquez". Ave 31 y 76, municipio Marianao. La Habana, Cuba. Correo electrónico: edelisa.moredo@infomed.sld.cu