Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Pediatría
versión On-line ISSN 1561-3119
Rev Cubana Pediatr vol.88 no.3 Ciudad de la Habana jul.-set. 2016
ARTÍCULO DE REVISIÓN
Mecanismos implicados en la aparición y regulación del proceso de remodelación del tejido adiposo y estado de lipoinflamación en la obesidad
Mechanisms involved in occurence and regulation of the process of adipose tissue remodelation and the state of lipoinflammation in obesity
José María Basain Valdés,I María del Carmen Valdés Alonso,II Margarita Pérez Martínez,I Guadalupe Layne Socorro Sarracent,II Dayamí Duany Álvarez,II Ivis Mesa MartínIII
IPoliclínico Universitario "Carlos Manuel Portuondo Lambert". La Habana, Cuba.
IIHospital Pediátrico Docente "Juan Manuel Márquez". La Habana, Cuba.
IIIFacultad de Ciencias Médicas "Finlay-Albarrán". La Habana, Cuba.
RESUMEN
Introducción: la obesidad se acompaña de un estado inflamatorio crónico, lo cual trae efectos negativos a la salud.
Objetivo: describir los mecanismos implicados en la aparición y regulación del proceso de remodelación del tejido adiposo y estado de lipoinflamación en la obesidad.
Métodos: se realizó una búsqueda en Medline/PubMed y Bireme, de artículos publicados en inglés y español en el período comprendido entre enero de 2006 y diciembre de 2015. Los términos de búsqueda fueron energy balance, regulation, nutritional homeostasis.
Desarrollo: las alteraciones del balance energético positivo determinan un balance de energía incrementado en el adipocito, en el cual ocurre hiperplasia e hipertrofia, lo que provoca resistencia molecular, hiperproducción de ácidos grasos libres, adipocitocinas y mediadores inflamatorios con promoción de disfunción sistémica; al mismo tiempo que se produce una hipoxia. Esta hipoxia provoca cambios en la expresión de algunas adipocinas y citocinas inflamatorias, y la muerte celular de los adipocitos más periféricos, que se traduce en un aumento de la reacción inflamatoria, la cual aumenta con la transformación de los macrófagos secretores de adipocitocinas antiinflamatorias a macrófagos secretores de adipocitocinas proinflamatorias, e infiltración de estos últimos en el tejido adiposo, todo lo cual lleva a una disregulación de la homeostasis.
Consideraciones finales: existen diferentes mecanismos implicados en la aparición y regulación del proceso de remodelación del tejido adiposo y estado de lipoinflamación en la obesidad, los cuales determinan una comunicación alterada del tejido adiposo con otros órganos.
Palabras clave: obesidad; tejido adiposo; lipoinflamación.
ABSTRACT
Introduction: obesity is accompanied by chronic inflammatory condition and brings negative health effects.
Objective: to describe the mechanisms involved in occurence and regulation of the process of adipose tissue remodelling and state of lipoinflammation in obesity.
Methods: a search of articles published in English and Spanish from January 2006 to December 2015 was made in Medline/PubMed and Bireme. The search terms were energy balance, regulation, and nutritional homeostasis.
Development: alterations in the positive energy balance determine an increased energy balance in the adipocyte in which hiperplasia and hypertrophy occur, which leads to molecular resistance, hyperproduction of free fatty acids, adipocytokines and inflammatory mediators with promotion of systemic dysfunction and at the same time hipoxia. Hypoxia causes changes in expression of some inflammatory adipokines and cytokines and the cell death of most peripheral adipocytes, all of which leads to increase of inflammatory reactions, the transformation of anti-inflammatory adipocytokine secretion macrophages into proinflammatory adipocytokine secretion macrophages and the infiltration of the latter in the adipose tissue and finally to homeostasis deregulation.
Final thoughts: there are several mechanisms involved in occurence and regulation of the process of the adipose tissue remodelling and state of lipoinflammation in obesity and they determine an altered communication of the adipose tissue with other body organs.
Keywords: obesity; adipose tissue; lipoinflammation.
INTRODUCCIÓN
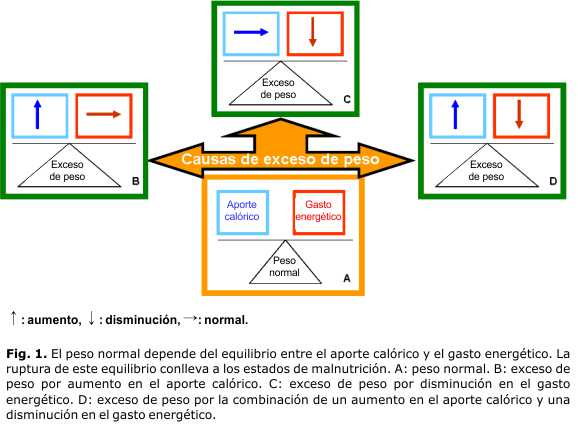
La obesidad es el resultado de un aumento de la grasa corporal,1 la cual se produce por un balance calórico positivo, ya sea por elevado aporte calórico, reducción del gasto energético, o combinación de ambos.2 En la figura 1 se representa este proceso de desequilibrio energético.
Anteriormente la obesidad se consideraba una enfermedad exclusiva de los sectores medios con mayor poder adquisitivo, pero los cambios ocurridos en los últimos 50-60 años en las naciones desarrolladas y en vías de desarrollo, como consecuencia del proceso de transición epidemiológica, permiten explicar las determinantes económico-sociales y culturales de su crecimiento a nivel mundial.3
Se han acumulado evidencias que sugieren que en los países en desarrollo, los pobres tienen una creciente tendencia a la obesidad, con un patrón típico de la transición nutricional, en el cual coexisten -en una misma comunidad- la desnutrición e infecciones, y el sobrepeso y la obesidad, con la aparición de las enfermedades asociadas. A pesar de los esfuerzos realizados para prevenir la obesidad, continúa incrementándose en proporciones epidémicas. Se considera una enfermedad preocupante, no solo por sus consecuencias a corto plazo, sino también porque se relaciona -de modo significativo- con el desarrollo posterior de enfermedades cardiovasculares, y potencialmente, con mayor riesgo de mortalidad en edades tempranas de la vida y/o disminución de la calidad de vida.3
Las alteraciones nutricionales por exceso (sobrepeso y obesidad), son un problema de salud pública a nivel mundial.4 En la región de Latinoamérica, casi una cuarta parte de los adultos sufren sobrepeso y obesidad según estudios de la Organización de la Naciones Unidas para la Agricultura y la Alimentación,4 mientras que en Argentina las estimaciones indican que 1 de cada 3 adolescentes tiene problemas relacionados con el peso. En México la obesidad es un problema de salud pública que aqueja a la población pediátrica, y que impacta el panorama epidemiológico de ese país.5
La obesidad es un fenómeno global que afecta a todos los grupos socioeconómicos, independientemente de la edad, sexo y etnia.2 Tiene una etiología multifactorial y compleja, en la que influyen factores genéticos, neuroendocrinos, metabólicos, psicológicos, ambientales y socioculturales,3 entre los cuales solo 2-3 % de los obesos tendría como causa alguna enfermedad endocrinológica, entre las que destacan el hipotiroidismo, el síndrome de Cushing, el hipogonadismo y las lesiones hipotalámicas asociadas a la hiperfagia.2
La obesidad en los seres humanos se caracteriza por una gran variabilidad en la distribución corporal del exceso de grasa. Estos excesos en los depósitos pueden, a su vez, establecer riesgos y determinar enfermedades asociadas, lo cual conlleva a un aumento de la morbilidad cardiovascular y metabólica, y de la mortalidad.6-8 Cuando se producen los depósitos centrales de grasa, estos se asocian de forma significativa con alteraciones en varios sistemas, y esta asociación es mayor a la que representa la grasa periférica. Esto resulta mucho más evidente cuando aumentan los depósitos de grasa intraabdominal, y consecuentemente, visceral.9
El exceso progresivo de tejido graso puede producir secundariamente alteraciones de la regulación, metabolización y secreción de diferentes hormonas,2 ya que el tejido adiposo es un tejido endocrino complejo y metabólicamente muy activo, que desempeña un papel fundamental sobre las cascadas inflamatorias, procoagulantes, antifibrinolíticas y vasoactivas, lo que sugiere una influencia directa sobre el proceso inflamatorio.10,11
Teniendo en cuenta este último aspecto, la presente revisión bibliográfica tiene como objetivo describir los mecanismos implicados en la aparición y regulación del proceso de remodelación del tejido adiposo y estado de lipoinflamación en la obesidad.
MÉTODOS
La revisión bibliográfica se llevó a cabo en función de criterios cronológicos, temáticos y de autor, tanto para los artículos publicados en revistas nacionales, como internacionales. Se escogieron como punto de partida aquellos trabajos publicados sobre el proceso de remodelación del tejido adiposo y estado de lipoinflamación en la obesidad.
Se tomaron en cuenta los descriptores MESH (lipoinflamation, energy balance, nutricional homeostasis), y DESH (lipoinflamación, balance energético, homeostasis nutricional, remodelación del tejido adiposo y obesidad), para conformar la estrategia de búsqueda, con los calificadores: incidencia, prevalencia, regulación y factores de riesgo, entre otros, para recuperar información pertinente y relevante. Finalmente, la revisión se complementó con la búsqueda de los autores y grupos de investigación con los trabajos más relevantes, relacionados con el estudio de la remodelación del tejido adiposo y estado de lipoinflamación en la obesidad en nuestro medio.
El período revisado abarcó desde el año 2006 hasta 2015, y las bases de datos consultadas fueron Medline/PubMed, Bireme (Scielo, Lilacs, Comed).
El número total de citas bibliográficas recuperadas fue de 250 y se utilizaron las de mayor importancia; en el caso de las internacionales, se seleccionaron aquellas en función del factor de impacto de la revista donde fueron publicadas y la potencia del diseño del estudio (por ejemplo, estudios prospectivos). Este criterio también se estimó en las nacionales, además de hacer mención de aquellas con gran valor histórico dentro del período que abarcó la búsqueda. También se consideraron trabajos realizados en la población general, y grupos o poblaciones específicas.
Con los elementos antes mencionados, la segunda revisión del total de títulos recuperados, permitió seleccionar 21 de 97 trabajos que cumplían con los criterios expuestos, teniendo en cuenta su especificidad y relevancia, así como los puntos en común y controversias planteadas por los diferentes autores en torno a los principales mecanismos implicados en la aparición y regulación del proceso de remodelación del tejido adiposo y estado de lipoinflamación en la obesidad.
DESARROLLO
La consideración del tejido adiposo como reservorio de energía ha venido cambiando con los años, y desde 1987 se consideró como el principal sitio de producción de esteroides sexuales. Posteriormente, en 1994, se identificó la leptina,12 un factor proteico producido en el tejido adiposo, pero con acción en el sistema nervioso central, con lo cual se dio paso a la caracterización de una serie de factores secretados por este tejido: las adipoquinas, y algunas de las más importantes son: leptina, adiponectina, resistina, factor de necrosis tumoral alfa (TNF-α), interleucina-6 (IL-6), proteína quimioatrayente de monocitos 1 (MCP-1) e inhibidor del activador del plasminógeno (PAI-1).13 Estas adipoquinas tienen una acción endocrina, paracrina y autocrina,14 (figura 2), lo que ocurre de la manera siguiente: las adipoquinas pueden ser llevadas por el torrente circulatorio a órganos distantes (acción endocrina), actuar sobre órganos adyacentes (acción paracrina), o modificar su propio entorno (acción autocrina). De esta manera, en la actualidad se considera al tejido adiposo como un tejido endocrino.13
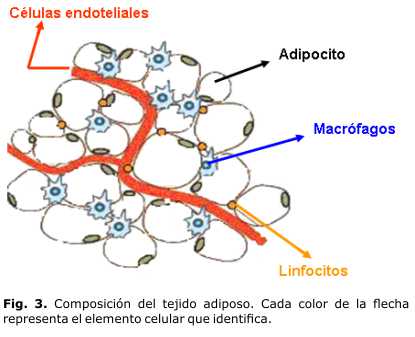
El tejido adiposo es un tejido que no está conformado solamente por adipocitos maduros, sino también por fibroblastos, linfocitos, células endoteliales y macrófagos, los cuales constituyen cerca del 50 % de su contenido celular total. Todas son células altamente activas y funcionan como una unidad integradora.12 En la figura 3 se representa la composición del tejido adiposo.
El tejido adiposo consiste, funcionalmente, en dos tipos de tejido diferente: el pardo y el blanco. Los adipocitos pardos se especializan en la producción de calor a partir de su almacenamiento lipídico, y se encuentran únicamente en mamíferos. Difieren de los adipocitos blancos en la expresión de la proteína desacoplante 1 (UCP-1), que disipa como calor, la energía creada por el gradiente de protones, generado por la cadena de transporte de electrones en la membrana mitocondrial. Morfológicamente los adipocitos pardos son multiloculares, contienen menos lípidos que los blancos, y son particularmente ricos en mitocondrias. En humanos, el tejido adiposo pardo rodea el corazón y los grandes vasos durante la infancia, y tiende a desaparecer con el tiempo, de forma tal que solo escasas células se pueden encontrar en los cojinetes grasos.15
Por otra parte, el tejido adiposo blanco, por medio de la captación de ácidos grasos libres, de su conversión en triglicéridos y de su hidrólisis a ácidos grasos libres como fuente energética, provee una reserva de combustible a largo plazo. En los mamíferos representa la principal reserva de energía, y se distribuye en múltiples depósitos corporales, tanto visceral como subcutáneamente, al igual que en nódulos linfáticos y en músculo esquelético. Adicional al almacenamiento de combustible, el tejido adiposo blanco puede actuar como un aislante térmico y como protector de órganos.12
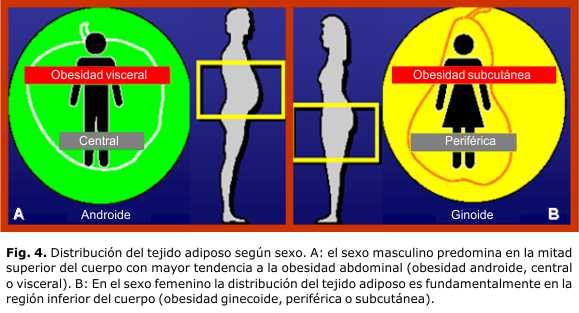
La cantidad y localización del tejido adiposo varía en las diferentes etapas de la vida. El cuerpo humano tiene, al momento de nacer, aproximadamente 12 % de grasa, y puede llegar hasta el 17 % a los 5 años de edad. A partir de esa edad, el tejido adiposo se va incrementando constantemente, y alcanza en la edad adulta entre 30 y 40 % de la masa corporal. La distribución del tejido adiposo es diferente según el sexo (figura 4). En las mujeres predomina en la región inferior del cuerpo (obesidad ginecoide) y en el tejido subcutáneo; mientras que en los varones, se distribuye en la mitad superior del cuerpo, con mayor tendencia a la obesidad abdominal profunda (obesidad androide).16
La homeostasis normal de la energía requiere de un balance impecable entre los depósitos energéticos en forma de grasa del tejido adiposo, y su utilización metabólica. Esta función es llevada a cabo por las cerca de 1 000 millones de células adiposas que constituyen el mayor órgano endocrino del cuerpo. Esta circunstancia fisiológica es necesaria para mantener un grado de adiposidad normal, y puede ser modificada a partir de los estados de malnutrición.17
Por su parte, el exceso de adiposidad determina la síntesis y secreción de las moléculas inflamatorias, sobre todo, a partir de los depósitos incrementados de grasa visceral, lo que origina un estado virtual de inflamación crónica con alteraciones en la percepción periférica de los mensajeros endocrinos involucrados en la homeostasis metabólica.17
Las alteraciones del balance energético positivo determinan un almacenamiento incrementado de energía en el adipocito,17 el cual se acumula en el tejido adiposo subcutáneo. Este va aumentando por hiperplasia, es decir, a partir de la proliferación y diferenciación de los pre-adipocitos. Cuando el tejido adiposo subcutáneo es incapaz de almacenar apropiadamente el exceso de energía -o se ha rebasado el umbral de almacenamiento- aumentan los depósitos de grasa visceral, que al tener menor capacidad adipogénica, crecen por hipertrofia, es decir, por aumento del tamaño de los adipocitos.10
Los procesos de hipertrofia o hiperplasia adipocitaria están asociados con alteraciones en la función celular, particularmente a nivel del retículo endoplásmico rugoso y de las mitocondrias. Las consecuencias celulares de estas alteraciones incluyen la resistencia molecular, hiperproducción de ácidos grasos libres, adipocitocinas y mediadores inflamatorios, con promoción de disfunción sistémica, que determinan las consecuencias clínicas y las complicaciones de la obesidad.17 Por tanto, en condiciones de obesidad, el aumento por hiperplasia y principalmente por hipertrofia de los adipositos, se ha asociado a la disregulación del tejido adiposo, que conlleva un remodelado de su estructura y posterior inflamación, con repercusiones a nivel local y sistémico.10
Durante el balance energético positivo, el tejido adiposo acumula el exceso de energía. Para ello aumenta el tamaño y número de los adipocitos; al mismo tiempo, el incremento en el tamaño del adipocito requiere de mayor cantidad de oxígeno (O2).18 La hipoxia afecta alguna de las funciones biológicas, tales como: la angiogénesis, la apoptosis, la inflamación y ocurre un cambio en el metabolismo celular. Además, media su efecto a través de la activación del factor inducible por hipoxia (HIF), un factor de transcripción básico.18
Estudios realizados en adipocitos han demostrado que la hipoxia provoca cambios en la expresión de algunas adipocinas y citocinas inflamatorias.18 Se ha observado que en estas zonas de tejido adiposo, en el paciente obeso, la secreción de adipocitoquinas pro-inflamatorias como: factor inhibidor de la migración de macrófagos (MIF), matriz de metaloproteinasas (MMP2 y MMP9), IL-6, PAI-1, factor de crecimiento endotelial vascular (VEGF) y leptina, están regulados por el incremento de la hipoxia.19 Paralelamente, la escasez de O2 provoca la muerte celular de los adipocitos más periféricos, que se traduce en un aumento de la reacción inflamatoria.10
Asimismo, aunque el adipocito es el elemento clave de los cambios y remodelado del tejido adiposo, los macrófagos presentes en el tejido adiposo obeso desempeñan también un papel fundamental, por lo que se ha descrito el fenómeno de "cambio fenotípico", definido como una transformación en el estado de polarización de los macrófagos, es decir, la transformación de un estado antiinflamatorio M2 (la forma predominante durante el balance negativo de energía), a una forma M1 más pro-inflamatoria,10 presentándose de esta manera en el tejido adiposo una infiltración masiva de macrófagos M1 secundaria al incremento de la secreción de la MCP-1, que juega un papel crucial en la respuesta inflamatoria en la obesidad, y es el factor nuclear potenciador de las cadenas ligeras kappa de las células β activadas (NF-kβ), uno de los mayores inductores de la expresión de esta adipocina.20
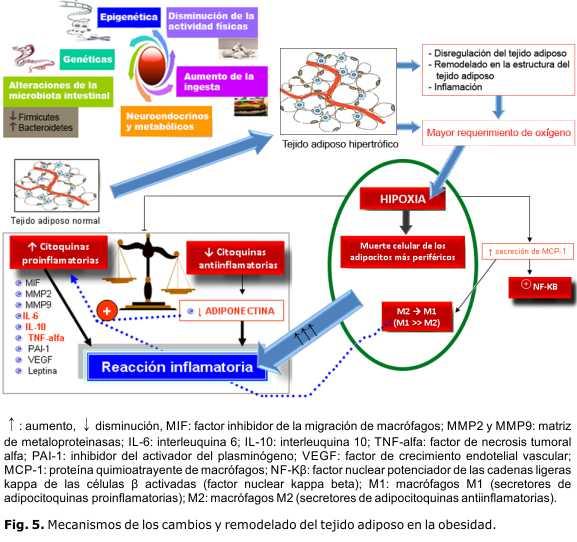
Todos estos eventos ocurridos en el adipocito (figura 5): la hipoxia en el tejido adiposo, la muerte celular de los adipocitos periféricos, la infiltración de células inmunes y la transformación de los macrófagos M2 (secretores de adipocitoquinas antiinflamatorias) a macrófagos M1 (secretores de adipocitoquinas proinflamatorias), e infiltración de estos últimos en el tejido adiposo, la angiogénesis y la sobreproducción de matriz extracelular, producen una disregulación de la homeostasis, debido al aumento de la secreción de adipocitoquinas proinflamatorias principalmente IL-6, IL-10 y TNF-α, así como el descenso de adipocitoquinas antiinflamatorias, tales como, la adiponectina (que suprime la síntesis de varias citoquinas proinflamatorias, como TNF-α), e interferón gamma (IFN-γ). Esta disregulación se debe a la inhibición que ejerce la adiponectina sobre la activación del NF-kβ, principal regulador de la transcripción de citoquinas.21
CONSIDERACIONES FINALES
Finalmente, se concluye que, el tejido adiposo es un órgano endocrino complejo y metabólicamente muy activo, que participa en número considerable de funciones reguladoras de la homeostasis del organismo, las cuales, con el incremento de este tejido en el paciente con exceso de peso, causado por un balance energético positivo mantenido en el tiempo, se acompaña de otros cambios en las características biológicas habituales del tejido, que se vuelve disfuncional, lo que determina alteraciones y conduce a remodelaciones a este nivel, con la participación de múltiples factores y elementos implicados en todo el proceso. Para explicar estas alteraciones existen múltiples hipótesis sobre cuál sería la razón por la que las células infamatorias infiltran el tejido adiposo, una de ellas destaca la hipertrofia adipocitaria, con la consecuente hipoxia tisular, el aumento en la expresión de citoquinas, las alteraciones de la matriz extracelular, la liberación de ácidos grasos, y finalmente, la muerte adipocitaria.
El depósito visceral de la grasa, la hipertrofia y el cambio del perfil secretor de los adipocitos, junto con la infiltración del tejido adiposo por células infamatorias, son algunas de las características que determinan una comunicación alterada del tejido adiposo con otros órganos.
REFERENCIAS BIBLIOGRÁFICAS
1. Prados-Bo A, Gómez-Martínez S, Nova E, Marcos A. El papel de los probióticos en el manejo de la obesidad. Nutr Hosp. 2015;31(supl 1):10-8.
2. Baudrand BR, Arteaga UE, Moreno GM. El tejido graso como modulador endocrino: Cambios hormonales asociados a la obesidad. Rev Med Chile. 2010;138(10):1294-301.
3. Lima Rabelo Y, Ferrer Arrocha M, Fernández Rodríguez C, González Pedroso MT. Sobrepeso en adolescentes y su relación con algunos factores sociodemográficos. Rev Cubana Med Gen Integr. 2012;28(1):26-33.
4. Betina A, Valeria S, Salazar R, Sal J, Ale M, Filgueira J, et al. Características de personalidad en adolescentes con sobrepeso y obesidad. Psicología y Salud. 2015;25(1):5-14.
5. Cu Flores L, Villarreal RE, Rangel PB, Galicia RL, Vargas DE, Martínez GL. Factores de riesgo para sobrepeso y obesidad en lactantes. Rev Chil Nutr. 2015;42(2):139-44.
6. Cedeño Morales R, Castellanos González M, Benet Rodríguez M, Mass Sosa L, Mora Hernández C, Parada Arias JC. Indicadores antropométricos para determinar la obesidad, y sus relaciones con el riesgo cardiometabólico. Revista Finlay. 2015;5(1):12-23.
7. Navarro E, Vargas F. Riesgo coronario según ecuación de Framingham en adultos con síndrome metabólico de la ciudad de Soledad, Atlántico. 2010. Rev Colomb Cardiol. 2012;19(3):109-18.
8. Abraham W, Blanco G, Coloma G, Cristaldi A, Gutiérrez N, Sureda L. Estudio de los Factores de Riesgo Cardiovascular en Adolescentes. Rev Fed Arg Cardiol. 2013;42(1):29-34.
9. Ruiz AJ, Aschner PJ, Puerta MF, Alfonso R. Prevalencia de obesidad abdominal y factores de riesgo asociados en atención primaria en Colombia. Biomédica (Bogotá). 2012;32(4):790-9.
10. Izaola O, de Luis D, Sajoux I, Carles Domingo J, Vidal M. Inflamación y obesidad (lipoinflamación). Nutr Hosp. 2015;31(6):2352-8.
11. Flores-Lázaro JR, Rodríguez-Martínez E, Rivas-Arancibia S. Metabolic consequences of the functional alterations of adipose tissue in obese patients. Rev Med Hosp Gen Méx. 2011;74(3):157-65.
12. Pérez Mayorga M. El adipocito como órgano endocrino. Implicaciones fisiopatológicas y terapéuticas. Rev Med. 2007;15(2):225-42.
13. Reyes JM. Características biológicas del tejido adiposo: el adipocito como célula endocrina. Rev Med Clin Condes. 2012;23(2):136-44.
14. Gómez-Hernández A, Perdomo L, Escribano O, Benito M. Papel del tejido adiposo blanco en las complicaciones vasculares asociadas a la obesidad. Clínica e Investigación en Arteriosclerosis. 2013;25(1):27-35.
15. Rosen ED, Spiegelman BM. Adipocytes as regulators of energy balance and glucosa homeostasis. Nat. 2006;444(5483):848-53.
16. Rodríguez Anzardo BR, Plasencia Concepción D. Afecciones por exceso y por defecto. En: Álvarez Sintes R. Medicina General Integral. 3ra ed. La Habana: Editorial Ciencias Médicas; 2014. p. 1349-56.
17. Godínez-Gutiérrez SA, Valerdi-Contreras L. Obesidad: Resistencia endocrina múltiple. Revista de Endocrinología y Nutrición. 2012;20(4):152-68.
18. Nava Reyes HJ, Zamudio Cortés P, García Cruz A, Noyola Ugalde MC, Pizaña Venegas A, Hernández Jiménez C, et al. Papel del adipocito en la expresión del factor inducible por hipoxia (HIF) asociado a la obesidad. Neumol Cir Torax. 2011;70(4):261-6.
19. Sun K, Kusminski CM, Scherer PE. Adipose tissue remodeling and obesity. J Clin Invest. 2011;121(6):2094-101.
20. Prieur X, Mok CY, Velagapudi VR, Núñez V, Fuentes L, Montaner D, et al. Differential lipid partitioning between adipocytes and tissue macrophages modulates macrophage lipotoxicity and M2/M1 polarization in obese mice. Diabetes. 2011;60:797-809.
21. Tilg H, Moschen AR. Adipocytokines: mediators linking adipose tissue, inflammation and immunity. Nat Rev Immunol. 2006;6(10):772-83.
Recibido: 3 de enero de 2016.
Aprobado: 9 de febrero de 2016.
José María Basain Valdés. Policlínico Universitario "Carlos Manuel Portuondo Lambert". Calle 49, entre 82 y 84, municipio Marianao. La Habana, Cuba. Correo electrónico: josemb@infomed.sld.cu