Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Medicina Militar
versión On-line ISSN 1561-3046
Rev Cub Med Mil vol.46 no.2 Ciudad de la Habana abr.-jun. 2017
ARTÍCULO DE INVESTIGACIÓN
Utilidad de una escala de riesgo para identificar pacientes con disglucemia
Utility of a risk scale to identify patients with dysglycemia
Rubén González Tabares, Frank Abel Acosta González
Hospital Militar Docente Dr. Mario Muñoz Monroy.
RESUMEN
Introducción: la prevalencia de diabetes y prediabetes ha ido en aumento a nivel global y en Cuba. Para identificar individuos en riesgo de disglucemia se han desarrollado varias escalas.
Objetivo: evaluar el desempeño de la escala de Bang y otros, para identificar individuos con disglucemia, en una población cubana laboralmente activa.
Métodos: se realizó un estudio transversal en 2 902 pacientes, fueron clasificados en portadores o no de disglucemia, a través de las pruebas de glucemia en ayunas, de tolerancia a la glucosa y hemoglobina glucosilada. Se determinó la frecuencia de factores de riesgo de diabetes mellitus tipo 2 comprendidos en la escala de Bang y otros, y en el proceder enfocado en factores de riesgo de American Diabetes Association. Se determinó sensibilidad, especificidad, valor predictivo positivo, valor predictivo negativo y Odds Ratio de ambas estrategias. En ambos se calculó el área bajo la curva operativa del receptor.
Resultados: se encontró relación entre cada uno de los factores de riesgo previstos en ambos procederes con el diagnóstico de disglucemia. Se encontró sensibilidad de 96,5 % y 79,9 %; especificidad de 20,9 % y 59,1 %; valor predictivo positivo de 10,7 % y 16,1 %; valor predictivo negativo de 98,4 % y 96,8 %; OR de 7,33 y 6,76 y área bajo la curva 0,77 y 0,79 para la escala de Bang y otros, y el procedimiento enfocado en factores de riesgo, respectivamente.
Conclusiones: ambos procederes identificaron de forma aceptable el grupo de pacientes con disglucemia.
Palabras clave: diabetes insípida; glucemia; disglucemia; sensibilidad; especificidad; valor predictivo positivo; valor predictivo negativo.
ABSTRACT
Introduction: The prevalence of diabetes and prediabetes has been increasing globally and also in Cuba. Several scales have been developed to identify individuals at risk for dysglycemia.
Objective: To evaluate the performance of the Bang et al. scale to identify individuals with dysglycemia in a Cuban labor-active population.
Methods: A cross-sectional study was carried out on 2 902 patients, classified as having or not suffering from dysglycemia, through fasting glycemia, glucose tolerance test and glycosylated hemoglobin. The frequencies of risk factors for type 2 diabetes mellitus included in the Bang et al. scale and in the risk factor approach of the American Diabetes Association were determined. Sensitivity, specificity, positive predictive value, negative predictive value and Odds Ratio of both strategies were determined. In both, the area under the receiver operating curve was calculated.
Results: A relationship was found between each of the predicted risk factors in both procedures with the diagnosis of dysglycemia. Sensitivity was 96.5 % and 79.9 %; Specificity of 20.9 % and 59.1 %; Positive predictive value of 10.7 % and 16.1 %; Negative predictive value of 98.4% and 96.8 %; OR of 7.33 and 6.76 and area under the curve 0.77 and 0.79 for the scale of Bang et al. and the procedure focused on risk factors respectively.
Conclusions: Both procedures identified in an acceptable manner the group of patients with dysglycemia.
Key words: Diabetes insipidus; blood glucose; dysglycemia; sensitivity; specificity; positive predictive value; negative predictive value.
INTRODUCCIÓN
La prevalencia de diabetes ha ido en aumento a nivel global y en Cuba.1 Según estimaciones, 422 millones de adultos en todo el mundo tenían diabetes en 2014, frente a 108 millones en 1980. Más del 90 % padecen diabetes mellitus tipo 2 (DM2), ello supone un incremento en los factores de riesgo conexos, como el sobrepeso y la obesidad.2 De forma alarmante, hasta el 46 % de los diabéticos no conocen que tienen la enfermedad.3 Sin embargo, la DM2 tiene una larga fase preclínica, conocida como prediabetes (PD), donde se establecen complicaciones vasculares, renales, oftalmológicas y neuropáticas.4-6
El número de pacientes con prediabetes también ha ido en aumento y su prevalencia se incrementa con la edad, se estima que afecta el 6,9 % de los adultos a nivel mundial.3 La detección temprana, seguida de cambios en hábitos y estilos de vida, así como el tratamiento farmacológico en los casos indicados, puede retrasar la progresión a diabetes manifiesta o el desarrollo de complicaciones vasculares en pacientes con prediabetes.7-9
El diagnóstico oportuno de disglucemia (entiéndase prediabetes y diabetes) permitiría prevenir el daño en los pacientes en riesgo. Es además factible, dado su alta prevalencia e historia natural bien conocida, en la que existe un largo periodo entre los primeros síntomas y la enfermedad clínica. Sin embargo, la glucemia en ayunas, prueba diagnóstica que también se utiliza en el tamizaje, es sensible y específica pero no barata. Por este motivo, lo más costo-efectivo es emplearla enfocada en grupos de riesgo.
Con el objetivo de identificar dentro de una población, a los individuos en riesgo de disglucemia, se han desarrollado varias escalas. Están dirigidas a detectar pacientes con DM2 no diagnosticada o individuos con disglucemia.
La American Diabetes Association (ADA) ha propuesto criterios para evaluar diabetes y prediabetes en adultos asintomáticos, según estos criterios, deben ser evaluados todos los adultos de 45 años o más, además quienes tengan índice de masa corporal (IMC) de 25 Kg/m2 y al menos un factor de riesgo adicional.10 Propone además emplear una escala de riesgo basada en siete variables: edad, sexo, antecedente de diabetes gestacional en las mujeres, antecedentes de diabetes en familiares de primer grado (madre, padre o hermanos), antecedentes de hipertensión arterial, sedentarismo y peso corporal para la talla. Esta herramienta fue desarrollada originalmente por Bang y otros11 en 2009 y alcanza un valor máximo de 11 puntos. Con 5 puntos permite identificar DM2 no diagnosticada y con 4 puntos prediabetes, en la población de EE.UU. Con procedimientos análogos se han desarrollado herramientas similares para otras poblaciones.12
El objetivo de esta investigación es evaluar el desempeño de la escala de Bang y otros, para identificar individuos con disglucemia, en una población cubana laboralmente activa.
MÉTODOS
Se realizó un estudio descriptivo, transversal, que incluyó 2 902 trabajadores que acudieron a examen médico preventivo en el Hospital Militar Central "Dr. Carlos J. Finlay" desde julio de 2012 hasta junio de 2013.
En todos los pacientes se recolectaron datos generales: edad, sexo, peso y talla; a partir de estos dos últimos se calculó el IMC, según la división del peso en kilogramos entre el cuadrado de la talla en metros. Se consideró diabético a quienes tenían antecedentes de DM2 o quienes llevaban medicación con hipoglucemiantes orales y/o insulina. Como familiares de primer grado con diabetes se consideró madre, padre o hermano/a. Se estimó hipertenso a quienes tuvieran antecedentes de esta enfermedad, usaran medicamentos antihipertensivos o se les detectaran cifras de tensión arterial igual o superior a 140/90 mmHg en dos ocasiones durante el estudio. Se consideró sedentarismo según el paciente realizara o no al menos dos sesiones de ejercicios físicos programados de más de 30 minutos en la semana. Como enfermedad cardiovascular se consideró el antecedente de cardiopatía isquémica o enfermedad cerebrovascular. En las mujeres se buscaron antecedentes de diabetes gestacional. No fue incluida ninguna gestante ni paciente diagnosticado con diabetes mellitus tipo 1.
A todos se les realizó glucemia en ayunas a través de auto analizadores Mindray BS 400 e HITACHI-902; se usó el mmol/L como unidad de medida según el Sistema Internacional de Unidades.
La serie se clasificó en tres grupos: 1) no diabéticos, 2) prediabético y 3) diabético, a partir del siguiente algoritmo: quienes no tenían antecedentes de diabetes y presentaron cifras de glucemia inferior a 5,6 mmol/L se consideraron como no diabéticos y no requirieron estudios posteriores. Quienes presentaron glucemias mayores o iguales a 5,6 mmol/L, pero inferiores a 7,0 mmol/L se consideraron en riesgo y se les realizó prueba de tolerancia a la glucosa (PTG) y determinación de HbA1c, con el fin de poner de manifiesto diabetes no diagnosticada.
Los resultados de glucemia en ayunas, PTG y HbA1c se interpretaron según los criterios propuestos por la Organización Mundial de la Salud (OMS), por tanto para el análisis estadístico se consideró 6,1 mmol/L como el punto de corte para GAA15,16. Fueron considerados portadores de disglucemia los diabéticos y prediabéticos.
Se aplicó la escala de Bang y otros con valores de corte de 4 y 5 puntos, así como los criterios para evaluar diabetes y prediabetes en adultos asintomáticos de la ADA a toda la serie.
Los datos se presentan en tablas y gráficos con frecuencias absolutas y por cientos. Las medias de las variables cuantitativas se compararon con prueba t de Student. Para probar asociación entre las variables categóricas se empleó prueba de Chi cuadrado con nivel de significación estadística de 95 %. Se calculó sensibilidad (S), especificidad (E), valor predictivo positivo (VPP), valor predictivo negativo (VPN) de ambos sistemas de tamizaje para identificar individuos en riesgo de disglucemia. Se calculó el área bajo la curva (AUC) de ambos procederes, a través de la curva operativa del receptor (ROC). Para conseguir este objetivo, con el sistema de criterios para evaluación de prediabetes y diabetes en adultos asintomáticos de la ADA, se empleó la sumatoria de los factores de riesgo.
RESULTADOS
La serie contó con 2 902 pacientes, donde predominó el sexo masculino (2 162; 74,5 %). Eran diabéticos conocidos 154 (5,3 %); diabéticos no conocidos 45 (1,6 %) y prediabéticos 60 (2,1 %) pacientes. De esta forma fueron portadores de disglucemia 259 (8,9 %) pacientes.
La edad (53,04 ± 10,39 años), peso (85,34 ± 15,76 Kg), IMC (30,20 ± 4,86 Kg/m2), triglicéridos (2,20 ± 1,85 mmol/L) y colesterol total (5,21 ± 1,11 mmol/L) fueron mayores en pacientes con disglucemia. La glucemia en ayunas (8,00 ± 3,27 mmol/L) y HbA1c (6,90 ± 2,26 %) también fueron mayores en el grupo disglucémico. La talla y ácido úrico tuvieron valor similar en ambos grupos.
La frecuencia de factores de riesgo de disglucemia que considera la escala de Bang y otros, se comportó de acuerdo a la puntuación pre establecida para todos los ítems (tabla 1). Esta diferencia alcanzó significación estadística en todos, excepto en la pregunta referente al sexo (p= 0,229).
A medida que aumenta la edad se aprecia un progreso de la frecuencia de disglucemia: 2,3 % en menores de 40 años; 7,4 % en el grupo de 40 a 49 años; 12,3 % en el grupo de 50 a 59 años y 25,2 % en los que tienen 60 años o más; lo cual es proporcional a la puntuación que asigna la escala para cada grupo de edad.
La disglucemia fue más frecuente en hombres (9,3 %) que en mujeres (7,8 %), aunque sin alcanzar significación estadística (p= 0,229).
El antecedente de diabetes gestacional se encontró en 46 mujeres, de ellas 11 (23,9 %) fueron diagnosticadas con disglucemia, mientras que solo 6,8 % de las que no tenían el antecedente desarrollaron disglucemia.
Los antecedentes familiares de primer grado (madre, padre o hermano/a) con diabetes fueron positivos en 14,4 % de los pacientes con disglucemia y negativos en solo 6,2 %.
La hipertensión arterial (HTA) se encontró en 17,6 % de los pacientes con disglucemia y no se diagnosticó en 6,2 % de este grupo.
El sedentarismo fue muy frecuente en la serie estudiada, 2003 pacientes (69,0 %). La disglucemia se observó en 9,9 % de los que respondieron "No mantenerse físicamente activos" en la pregunta sobre actividad física y solo en 6,7 % de los que respondieron "Sí mantenerse físicamente activos".
El sobrepeso y la obesidad, fueron otros factores de riesgo muy frecuentes en esta serie, observándose en 2 140 (73,7 %) pacientes. La frecuencia de disglucemia aumentó con el IMC y se observó en 3,6 % de los pacientes con IMC < 25,0 Kg/m2; en 8,3 % de los que tenían IMC >= 25,0 Kg/m2 y < 30,0 Kg/m2; en 14,5 % de los que tenían IMC >= 30,0 Kg/m2 y < 40,0 Kg/m2 y en 22,6 % de aquellos con IMC >= 40,0 Kg/m2.
Se encontró que la escala de Bang y otros, con valor de corte de 4 puntos, identificó a 239 de los 259 pacientes con disglucemia; a su vez descartó a 992 pacientes. Con este valor de corte, fue necesario evaluar para disglucemia a 1910 pacientes, que representaron el 65,8 % de la serie. Estos resultados arrojan una S de 92,3 %; E de 36,8 %; VPP de 12,5 % y VPN 98,0 % (tabla 2). El OR fue de 6,95. Con valor de corte de 5 puntos se requirió evaluar menos pacientes: 1287, el 44,3 % de la serie. Sin embargo, solo identificó a 207 de los 259 verdaderos positivos. Este valor arroja una S de 79,9 %; E de 59,1 %; VPP de 16,1 %; VPN de 96,8 % y OR de 5,76.
Al emplear los criterios de la ADA para evaluar diabetes y prediabetes en adultos asintomáticos (tabla 2), se encontró que la combinación de IMC >= 25,0 Kg/m2 más cada uno de los factores de riesgo propuestos, es más frecuente en el grupo de pacientes con disglucemia, diferencia estadísticamente significativa (p< 0,05) en todos los casos. De forma similar los pacientes con 45 años o más tienen mayor frecuencia de disglucemia (p= 0,000), con OR de 3,85. Con este proceder fue necesario evaluar 2 341 pacientes, que representaron el 80,7 % de la serie. Estos datos arrojaron S de 96,5 %; E de 20,9 %; VPP de 10 % y VPN de 98,4 %. El AUC fue de 0,793 (tabla 3).
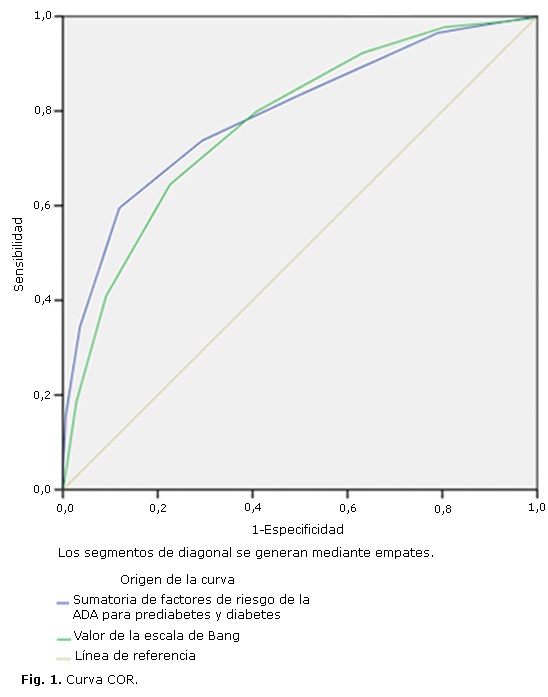
La figura 1 representa la curva operativa del receptor de ambos procederes en función del diagnóstico de disglucemia.
Independientemente del proceder que se utilizó para identificar los pacientes en riesgo de disglucemia, a medida que se acumularon factores de riesgo aumentó la frecuencia de la enfermedad (figura 2).
DISCUSIÓN
La diferencia de los valores de las variables continuas entre los pacientes con disglucemia y los que no la tenían se ha encontrado y corroborado en múltiples series. El grupo de pacientes con disglucemia fue aproximadamente 8 años mayor, ya que la edad es un factor de riesgo reconocido para desarrollar diabetes mellitus.15
De forma individual, todas las preguntas de la escala de Bang y otros diferencian entre los grupos con y sin disglucemia. A pesar de ser más frecuente la disglucemia entre mujeres, no alcanzó significación estadística con respecto a los hombres debido a la composición de la serie donde la proporción hombre/mujer fue 3/1. En la población cubana, la DM2 ha sido más frecuente en las mujeres;1 por lo que los autores consideran que la diferencia de puntuación que establece la escala de Bang y otros es aplicable a esta serie.
Bang y otros 11 al usar como valor de corte 5 puntos obtuvieron S de 79 %, E de 67 %, VPP de 10 % y VPN de 99 %. Además, con valor de corte de 4 puntos aumentaron la S (97 %) a expensas de identificar un mayor número de pacientes de alto riesgo (51 %). Resultados similares se obtuvieron en esta serie con valor de corte de 5 puntos: S de 79,9 %; E de 59,1 %; VPP de 16,1 % y VPN de 96,8 %. Ellos encontraron área bajo la curva (0,74) semejante a la de esta serie (0,77). Con valor de corte de 5 puntos, sería necesario evaluar por riego de disglucemia 1287 pacientes, 44,3 % del total.
Con valor de corte 4 puntos la S asciende a 92,3 %, pero a expensas de evaluar un número mucho mayor de pacientes: 1910, el 65,8 % de la serie. Esto se debe a que la escala fue desarrollada originalmente con la diabetes no diagnosticada como variable de salida, sin embargo, incluir a los diabéticos conocidos permite evaluar la capacidad de cada herramienta para identificar los verdaderos positivos. Otra razón es que las variables utilizadas no son sesgadas para que el paciente conozca o no que es diabético, ya que el tratamiento no influye sobre ellas.
Escalas de otras poblaciones alcanzan resultados similares, una desarrollada en Sri Lanka, a partir de su población, obtuvo un área bajo la curva de 0,78; S, E, VPP y VPP de 77,9 %; 65,6 %; 9,4 % y 98,3 % respectivamente;16 aunque utilizaron otra combinación de variables, incluidas balanitis o vulvitis y síntomas osmóticos. Incluso con tres variables (circunferencia abdominal, edad e historia familiar de diabetes), se ha descrito un score que identifica el riesgo de disglucemia en 40,8 % de una población de la India, con sensibilidad de 81,0 %.15 En un enfoque más simplista, el U.S. Preventive Services Task Force (USPSTF) identifica en riesgo de diabetes a todo paciente con tensión arterial de 140/90 mmHg o más. Casagrande y otros17 analizaron con esta estrategia los datos del National Health and Nutrition Examination Survey II (NHANES II) y encontraron sensibilidad de 44,4 %; especificidad 74,8 %; advierten que llevar a cabo esta estrategia de tamizaje conllevaría dejar de diagnosticar a más de la mitad de los diabéticos no conocidos. Aplicar este proceder a la serie arroja los peores resultados (los datos no se muestran). Habría que evaluar al 30,8 % de la población y sólo diagnosticaría el 52,4 % de los disglucémicos, además tiene el peor OR (2,95).
Usar el proceder propuesto por la ADA rinde mayor sensibilidad (96,5 %) y VPN (98,4 %) pero a expensas de identificar en riesgo de disglucemia a un número mayor de pacientes: 80,5 % del total, 2 337 pacientes. Esto se debe a que impone la condición de evaluar a todo el que tenga sobrepeso/obesidad o que sea mayor o igual a 45 años, factores de riesgo de muy alta frecuencia en la serie (73,7 % y 61,7 % respectivamente). Este enfoque niega la existencia de disglucemia en individuos sin sobrepeso, hecho que no se ajusta a la fisiopatología de la diabetes.18 Además, se debe considerar que la DM2 es una enfermedad crónica, cuya incidencia se incrementa a medida que aumentan los factores de riesgo dentro de la población, fenómeno que se aprecia en la figura 2.
La escala de Bang y otros es de utilidad en el contexto de la atención primaria de salud o en investigaciones poblacionales, ya que utiliza siete preguntas en el entorno clínico, sin necesidad de exámenes complementarios. Solamente el estado nutricional del paciente requiere medir peso y talla, además de contar con la tabla de valores para asignar la puntuación. Sin embargo, sería de gran utilidad desarrollar una herramienta a partir de la población cubana, donde se pondere cada variable de forma específica.
Este trabajo tiene como limitación que la serie no es representativa de la población general cubana, ya que no se obtuvo de un marco poblacional. Como fortaleza se señala el hecho de haberse realizado un programa estructurado de diagnóstico del estado glucémico, con pruebas de confirmación como se recomienda internacionalmente.10,13,14
En conclusión, ambas estrategias permiten identificar individuos con riesgo de desarrollar disglucemia, con similar valor predictivo positivo y área bajo la curva en la serie estudiada; sin embargo, la escala de Bang y otros tiene mejor especificidad y valor predictivo positivo; mientras que el proceder enfocado en factores de riesgo de la ADA tiene mejor sensibilidad y OR.
Se recomienda la difusión de esta herramienta que permitiría la autoevaluación de la población, esto contribuiría a disminuir el número de casos de diabetes no diagnosticada. Se sugiere la creación de una herramienta similar a partir de la población cubana.
Conflictos de intereses
Los autores no refieren conflictos de interés.
REFERENCIAS BIBLIOGRÁFICAS
1. Bess Constanten S, Alonso Alomá I, Torres Vidal RM, López Nistal LM, Sánchez Sordo E, Martínez Morales MÁ, et al. Anuario Estadístico de Salud 2016. La Habana: Ministerio de Salud Pública; 2017 [citado 13 mar 2017]. Disponible en: http://files.sld.cu/dne/files/2017/05/Anuario_Estad%C3%ADstico_de_Salud_e_2016_edici%C3%B3n_2017.pdf
2. Organización Mundial de la Salud. Informe Mundial sobre la Diabetes: Resumen de orientación. Geneva: World Health Organization; 2016 [citado 13 mar 2017]. Disponible en: http://apps.who.int/iris/bitstream/10665/204877/1/WHO_NMH_NVI_16.3_spa.pdf?ua=1
3. Han Cho N, Whiting D, Forouhi N, Guariguata L, Hambleton I, Li R, et al. Atlas de la DIABETES de la FID 2015 [cited 2017 Mar 13]. Available from: http://www.diabetesatlas.org/
4. Lamparter J, Raum P, Pfeiffer N, Peto T, Hohn R, Elflein H, et al. Prevalence and associations of diabetic retinopathy in a large cohort of prediabetic subjects: the Gutenberg Health Study. J Diabetes Complications [Internet]. 2014 [cited 2017 Mar 13];28(4):[about 4 p.]. Available from: http://www.sciencedirect.com/science/article/pii/S1056872714000506?via%3Dihub
5. McGinn JT, Shariff MA, Bhat TM, Azab B, Molloy WJ, Quattrocchi E, et al. Prevalence of Dysglycemia Among Coronary Artery Bypass Surgery Patients with No Previous Diabetic History. Journal of Cardiothoracic Surgery [serial on the Internet]. 2011 [cited 2017 Mar 13];6(104):[about 5 p.]. Available from: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3178483/
6. Xing FY, Neeland IJ, Gore MO, Ayers CR, Paixao AR, Turer AT, et al. Association of prediabetes by fasting glucose and/or haemoglobin A1c levels with subclinical atherosclerosis and impaired renal function: observations from the Dallas Heart Study. Diab Vasc Dis Res [serial on the Internet]. 2014 [cited 2017 Feb 14];11(1):[about 5 p.]. Available from: http://journals.sagepub.com/doi/pdf/10.1177/1479164113514239
7. Group DPPR. Reduction in the Incidence of Type 2 Diabetes with Lifestyle Intervention or Metformin. New England Journal of Medicine [Internet]. 2002 [cited 2017 Mar 13];346(6):[about 7 p.]. Available from: http://www.nejm.org/doi/full/10.1056/NEJMoa012512
8. Roumen C, Corpeleijn E, Feskens EJM, Mensink M, Saris WHM, Blaak EE. Impact of 3-year lifestyle intervention on postprandial glucose metabolism: the SLIM study. Diabetic Medicine [Internet]. 2008 [cited 2017 Mar 13];25(5):[about 8 p.]. Available from: http://dx.doi.org/10.1111/j.1464-5491.2008.02417.x
9. Tuomilehto J, Lindström J, Eriksson JG, Valle TT, Hämäläinen H, Ilanne-Parikka P, et al. Prevention of Type 2 Diabetes Mellitus by Changes in Lifestyle among Subjects with Impaired Glucose Tolerance. New England Journal of Medicine [Internet]. 2001 [cited 2017 Mar 13];344(18):[about 6 p.]. Available from: http://www.nejm.org/doi/full/10.1056/NEJM200105033441801
10. 2. Classification and Diagnosis of Diabetes. Diabetes Care [Internet]. 2017 [cited 2017 Feb 14];40(Supplement 1):[about 3 p.]. Available from: http://care.diabetesjournals.org/content/diacare/40/Supplement_1/S11.full.pdf
11. Bang H, Edwards AM, Bomback AS, Ballantyne CM, Brillon D, Callahan MA, et al. A patient self-assessment diabetes screening score: development, validation, and comparison to other diabetes risk assessment scores. Annals of Internal Medicine [Internet]. 2009 [cited 2017 Feb 14];151(11):[about 5 p.]. Available from: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3633111/
12. Lindström J, Tuomilehto J. The Diabetes Risk Score. A practical tool to predict type 2 diabetes risk [Internet]. Diabetes Care. 2003 [cited 2017 Mar 13];26(3):[about 3 p.]. Available from: http://care.diabetesjournals.org/content/diacare/26/3/725.full.pdf
13. Alberti KGMM, Zimmet PZ. Definition, diagnosis and classification of diabetes mellitus and its complications. Part 1: diagnosis and classification of diabetes mellitus. Provisional report of a WHO Consultation. Diabetic Medicine [serial on the Internet]. 1998 [cited 2017 Mar 13];15(7):[about 3 p.]. Available from: http://dx.doi.org/10.1002/(SICI)1096-9136(199807)15:7<539::AID-DIA668>3.0.CO;2-S
14. World Health Organization. Use of Glycated Haemoglobin (HbA1c) in the Diagnosis of Diabetes Mellitus: Abbreviated Report of a WHO Consultation. Geneva 2011 [cited 2017 Mar 13]. Available from: http://www.who.int/diabetes/publications/report-hba1c_2011.pdf
15. Sathish T, Kannan S, Sarma PS, Thankappan KR. Achutha Menon Centre Diabetes Risk Score: A Type 2 Diabetes Screening Tool for Primary Health Care Providers in Rural India. Asia-Pacific journal of public health / Asia-Pacific Academic Consortium for Public Health [Internet]. 2015 [cited 2017 Mar 13];27(2):[about 10 p.]. Available from: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4573642/
16. Katulanda P, Hill NR, Stratton I, Sheriff R, De Silva SDN, Matthews DR. Development and validation of a Diabetes Risk Score for screening undiagnosed diabetes in Sri Lanka (SLDRISK). BMC Endocrine Disorders [Internet]. 2016 [cited 2017 Mar 13];16:[about 8 p.]. Available from: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4960842/
17. Casagrande SS, Cowie CC, Fradkin JE. Utility of the U.S. Preventive Services Task Force Criteria for Diabetes Screening. American journal of preventive medicine [serial on the Internet]. 2013 [cited 2017 Feb 14];45(2):[about 5 p.]. Available from: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3752602/
18. Cagliero E. Diabetes and Long-Term Complications. En: Jameson JL, de Kretser DM, Marshall JC, De Groot LJ. Endocrinology: Adult and Pediatric (7th Ed.). Philadelphia: W.B. Saunders; 2016.p.898-906.
Recibido: 8 de junio de 2017.
Aprobado: 17 de agosto de 2017.
Rubén González Tabares. Hospital Militar Clínico-Quirúrgico Docente Dr. Mario Muñoz Monroy. Correo electrónico: rubengt@infomed.sld.cu