Presentación de caso
Sobrevida de un paciente adulto mayor con cáncer de pulmón, tratado con quimioterapia de primera línea
Survival of an elderly patient with lung cancer treated with first-line chemotherapy
0000-0003-3145-872XOscar Augusto Quintana Blancas
1
, 0000-0002-7368-4306Rita Emily Vallejos Garcia
1
, 0000-0002-8536-3577Rodolfo Cristóbal Olmos Soldevilla
2
, 0000-0001-7076-6093José Fernando Salvador Carrillo
2
*
, 0000-0001-5975-6898José Luis Salinas Paz
3
1Escuela Profesional de Medicina Humana, Universidad Privada San Juan Bautista. Lima, Perú.
2Escuela Profesional de Medicina Humana, Universidad Privada San Juan Bautista - Filial Chincha. Ica, Perú.
3Servicio de Oncología, Hospital Nacional Arzobispo Loayza. Lima, Perú.
RESUMEN
Introducción:
El cáncer de pulmón está afectando cada vez más a la población de adultos mayores, a medida que la expectativa de vida aumenta. Sin embargo, es difícil establecer la eficacia de la quimioterapia y el pronóstico de estos pacientes es grave.
Objetivo:
Presentar un caso de paciente adulto mayor con cáncer de pulmón avanzado de células no pequeñas, con una prolongada sobrevida que recibió solamente quimioterapia de primera línea.
Caso clínico:
Paciente no fumador, de 71 años, diagnosticado con cáncer de pulmón de células no pequeñas avanzado, del subtipo adenocarcinoma, con compromiso pleural. Inició tratamiento con carboplatino 5 AUC y gemcitabina 1,1 g. En el noveno ciclo, se encontró reducción de los nódulos pulmonares, pero también metástasis en el nivel D6-D7. Inició la segunda línea de tratamiento con carboplatino 5,4 AUC, paclitaxel 200 mg y ácido zolendrónico en dosis de 4,0 mg. Debido a eventos adversos, el tratamiento fue cambiado a vinorelbina 2,5 g y ácido zolendrónico 4,0 mg. Tras dos ciclos, el paciente fallece, alcanzando 21 meses de sobrevida global, solo con quimioterapia.
Conclusión:
El tratamiento del paciente adulto mayor con cáncer de pulmón es complejo. En el presente esquema de quimioterapia, el paciente pudo alcanzar 21 meses de sobrevida global, a pesar de que no fue caracterizado molecularmente.
Palabras-clave: sobrevida; adenocarcinoma; cáncer de pulmón de células no pequeñas avanzado; adulto mayor; quimioterapia
ABSTRACT
Introduction:
Lung cancer is taking an increasing toll on the older population as life expectancy increases. However, the efficacy of chemotherapy is difficult to establish and the prognosis of these patients is severe.
Objective:
Report a case of an older adult patient with advanced non-small cell lung cancer with prolonged survival who received only first-line chemotherapy.
Case report:
A 71-year-old non-smoker patient diagnosed with advanced non-small cell lung cancer, adenocarcinoma subtype, with pleural involvement. He started treatment with carboplatin 5 AUC and gemcitabine 1,1 g. In the ninth cycle, reduction of pulmonary nodules was found, but he also had metastases at the D6-D7 level. He started the second line of treatment with carboplatin 5,4 AUC, paclitaxel 200 mg and zolendronic acid at a dose of 4,0 mg. Due to adverse events, the treatment was changed to vinorelbine 2,5 g and zolendronic acid 4.0 mg. After two cycles, the patient died, reaching 21 months of overall survival, only with chemotherapy.
Conclusion:
The treatment of the older adult patient with lung cancer is challenging. In the present chemotherapy treatment, the patient was able to achieve 21 months of overall survival, despite the fact that he was not molecularly characterized.
Key words: survival; adenocarcinoma; advanced non-small lung cancer; aged; chemotherapy
INTRODUCCIÓN
El cáncer de pulmón (CP) es la primera causa de muerte por cáncer y el más frecuentemente diagnosticado en la población.1 El CP de células no pequeñas (CPCNP) es uno de los más comunes y afecta cada vez más a la población adulta mayor, debido al incremento de la expectativa de vida. Estos pacientes tienen menor participación en estudios clínicos comparados con la población adulta, debido principalmente a la toxicidad del tratamiento, la vulnerabilidad fisiológica asociada a su edad y la pobre expectativa de los médicos.
En algunos estudios, se ha observado que solo el 16,5-25,8 % de los pacientes de edad avanzada reciben quimioterapia.2,3
Diversos ensayos clínicos han mostrado que el promedio de supervivencia de los pacientes depende del tratamiento,4 sin embargo, los pacientes adultos mayores que consiguen sobrevivir después de los 24 meses de quimioterapia, oscilan entre el 4 y 6 %.5,6,7) La terapia biológica ha demostrado mejorar el tiempo de supervivencia del paciente,8,9 pero este tratamiento no siempre es accesible en los hospitales públicos y los médicos deben enfocarse en los tratamientos disponibles que ofrezcan la mejor calidad de vida.
La limitada evidencia sobre la eficacia y la pobre expectativa de vida de la quimioterapia en adultos mayores con CPCNP avanzado, es una dificultad para los médicos durante la práctica clínica. Este trabajo tiene como objetivo presentar un caso de un paciente adulto mayor con CPCNP avanzado, de tipo adenocarcinoma, quien sobrevivió 21 meses solo con tratamiento de quimioterapia sin radioterapia o procedimientos quirúrgicos.
CASO CLÍNICO
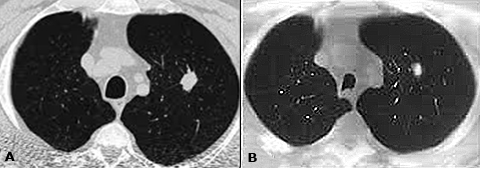
Paciente no fumador, de 71 años, que ingresó en un hospital público del Perú con tos, disnea, dificultad para hablar, dolor en el pecho e hiporexia. No contaba con antecedentes familiares de cáncer. Una tomografía axial computarizada del tórax reveló una imagen nodular y calcificada en el hemitórax izquierdo y el granuloma en el hemitórax derecho (Fig. 1A).
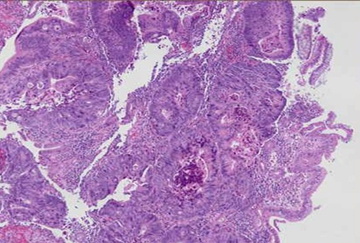
Después de la biopsia, el paciente fue diagnosticado con CPCNP avanzado del tipo adenocarcinoma con compromiso pleural (Fig. 2). El tamaño inicial del tumor era de 56 mm en el hemitórax izquierdo y se clasificó como T4N0M1, estadio IV según la clasificación TNM de la Unión Internacional de Control del Cáncer (UICC).
El paciente inició 9 ciclos de quimioterapia de primera línea, a dosis del 75 % con carboplatino (CBDCA) 5 AUC y gemcitabina 1,1 g. Al inicio del tratamiento, según la escala de ECOG, tuvo una puntación de 1; los niveles séricos del antígeno carcinoembrionario (CEA) y los fragmentos de citoqueratina 19 (CYFRA), fueron de 7,0 ng/mL y 12,5 ng/mL, respectivamente. Debido a la falta de equipo adecuado, no se pudo realizar la prueba inmunohistoquímica para el ligando de muerte programada-1 (PD-L1) y el receptor del factor de crecimiento epidérmico (EGFR).
Durante el tratamiento se reportó tos y dolor (6/10), trombocitopenia (7000/mm3) y ECOG 2 desde el tercer ciclo de la quimioterapia. En el octavo ciclo, el nivel sérico de CEA aumentó a 7,14 ng/mL. Además, el paciente informó sobre un grave dolor de espalda y por estas razones, se requirió la resonancia magnética y la tomografía axial computarizada espiral multicorte, para descartar la progresión de la enfermedad y observar el estado de sus pulmones.
En el noveno ciclo, se presenció reducción de nódulos pulmonares (Fig. 1B), sin embargo, se presentaron metástasis en el nivel vertebral (D6-D7) y se comenzó la segunda línea de tratamiento con CBDCA 5,4 AUC más paclitaxel 200 mg y ácido zolendrónico (ZA) 4,0 mg.
Presentó disnea leve, ECOG 2, tos y dolor de espalda serios (6/10) durante el inicio del tratamiento. En el ciclo 12, reportó tos irritante, dolor en el pecho (7/10), disnea moderada con ECOG 3 y aumento de los niveles séricos de CEA (9,4 ng/mL). El médico decidió cambiar el tratamiento a vinorelbina 2,5 g y ZA 4,0 mg después de 3 meses de tratamiento. La condición del paciente mejora desde el segundo ciclo, sin embargo, la tos leve persistió con un notable aumento del nivel sérico de CEA (18,14 ng/ml) y CYFRA (35,5 ng/ml), cuando el paciente decide abandonar el tratamiento.
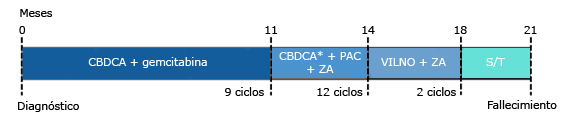
Luego de 3 meses, el paciente fallece debido a la progresión de metástasis en la columna vertebral. Completó 21 meses de supervivencia global, solo con tratamiento de quimioterapia. El esquema seguido se resume en la figura 3.
COMENTARIOS
El manejo de los adultos mayores con CPCNP avanzado es complejo. En este caso, fue tratado un adulto mayor en un hospital público, en el cual no se pudo realizar la inmunohistoquímica para PDL-1 o EGFR y esto limitó las opciones de tratamiento, y tuvo que recibir quimioterapia. Inesperadamente, el paciente alcanzó los 21 meses de supervivencia global. Otros estudios han reportado una supervivencia global de hasta de más de 5 años cuando reciben tratamientos biológicos más específicos.10,11
Un estudio retrospectivo realizado por Kyoichi y otros,10 mostró que 10 de 124 pacientes sobrevivieron más de 5 años de tratamiento a largo plazo. El esquema consistió en quimioterapia con platino seguido de gefitinib como segunda o tercera línea de tratamiento.
Otro estudio retrospectivo mostró que 20 pacientes con adenocarcinoma pulmonar con EGFR mutado, sobrevivieron más de 5 años con gefitinib o erlotinib. Los autores encontraron que la deleción del exón 19, ausencia de metástasis extratorácica, metástasis cerebral y ser no fumador, fueron factores de pronóstico favorables.11
En el presente reporte, el paciente recibió inicialmente CBDCA y GEM por 9 meses, con mantenimiento continuado hasta que hubo progresión, se cambió a CBDCA + paclitaxel + ZA y finalmente una tercera línea con vinorelbina.
Seguramente, el uso de las pruebas moleculares en el momento de la progresión hubiera ayudado a administrar una terapia más específica y aumentar el tiempo de supervivencia global como en los estudios previamente comentados. Esto es una limitante importante en la práctica médica en los hospitales públicos del Perú. Aun así, este estudio es el primer reporte de caso que describe a un adulto mayor latinoamericano, con CPCNP avanzado, que alcanza los 21 meses de supervivencia global solo con quimioterapia, a pesar de que esta población no suele tolerar este tipo de tratamiento a largo plazo.
Se requieren más estudios para establecer qué tipo de quimioterapia debería ser administrada en los pacientes adultos mayores con CPCNP avanzado.
En este estudio, con CBDCA + GEM se alcanzó los 11 meses libre de progresión.
REFERENCIAS BIBLIOGRÁFICAS
1.
Bray F, Ferlay J, Soerjomataram I, Siegel RL, Torre LA, Jemal A. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2018 [acceso: 31/07/2020]; 68(6):394-424. Disponible en: Disponible en: https://acsjournals.onlinelibrary.wiley.com/doi/full/10.3322/caac.21492
1.
[ Links ]
2.
Jennens RR, Giles GG, Fox RM. Increasing underrepresentation of elderly patients with advanced colorectal or non-small-cell lung cancer in chemotherapy trials. Intern Med J. 2006 [acceso: 01/01/2020]; 36(4):216-20. Disponible en: Disponible en: https://onlinelibrary.wiley.com/doi/abs/10.1111/j.1445-5994.2006.01033.x
2.
[ Links ]
3.
Davidoff AJ, Tang M, Seal B, Edelman MJ. Chemotherapy and survival benefit in elderly patients with advanced non - small-cell lung cancer. J Clin Oncol. 2010 [acceso: 31/01/2020]; 28(13):2191-7. Disponible en: Disponible en: https://ascopubs.org/doi/10.1200/JCO.2009.25.4052?url_ver=Z39.882003&rfr_
3.
[ Links ]
4.
Takayuki N, Keiko T, Junji U, Yoshiko K, Nobuyo T, Tadaaki Y, et al. Advanced Non-Small-Cell Lung Cancer in Elderly Patients: Patient Features and Therapeutic Management. Biomed Res Int. 2018 [acceso: 03/03/2020];18:8. Disponible en: Disponible en: https://www.hindawi.com/journals/bmri/2018/8202971/
4.
[ Links ]
5.
Okamoto T, Maruyama R, Shoji F, Asoh H, Ikeda J, Miyamoto T, et al. Long-term survivors in stage IV non-small cell lung cancer. Lung Cancer. 2005 [acceso: 04/04/2020]; 47(1):85-91. Disponible en: Disponible en: https://www.lungcancerjournal.info/article/S0169-5002(04)00301-0/fulltext
5.
[ Links ]
6.
Satoh H, Ishikawa H, Ohara G, Kagohashi K, Kurishima K, Ohtsuka M, et al. Long-term survivors after chemotherapy in advanced non-small cell lung cancer. Anticancer Res. 2007 [acceso: 03/07/2020]; 27(6 C):4457-60. Disponible en: Disponible en: http://ar.iiarjournals.org/content/27/6C/4457.long
6.
[ Links ]
7.
Albain KS, Crowley JJ, LeBlanc M, Livingston RB. Survival determinants in extensive-stage non-small-cell lung cancer: The southwest oncology group experience. J Clin Oncol. 1991 [acceso: 04/10/2020]; 9(9):1618-26. Disponible en: Disponible en: https://ascopubs.org/doi/pdf/10.1200/JCO.1991.9.9.1618
7.
[ Links ]
8.
Jara Exebio JJ, Cabrera Sandoval RN, Amaro Palomino JK, Revilla López JC. Adenocarcinoma pulmonar metastásico con evolución favorable al tratamiento con ITK-EGFR en un paciente fumador Metastaticlung adenocarcinoma favorable outcomewith ITK-EGFR treatment in a smoker. An Fac Med. 2011[acceso: 02/09/2020]; 76:199-202. Disponible en: Disponible en: http://www.scielo.org.pe/pdf/afm/v76n2/a14v76n2.pdf
8.
[ Links ]
9.
Castro C, Cardona F, Revéiz L, Serrano J, Carranza H, Vargas C, et al. Cáncer de pulmón de célula no pequeña metastásico. Acta Médica Colomb. 2010[acceso:04/04/2020]; 35(2):53-81. Disponible en: Disponible en: http://www.scielo.org.co/pdf/amc/v35n2/v35n2a04.pdf
9.
[ Links ]
10.
Kaira K, Takahashi T, Murakami H, Tsuya A, Nakamura Y, Naito T, et al. Long-term survivors of more than 5 years in advanced non-small cell lung cancer. Lung Cancer. 2010 [acceso: 05/07/2020]; 67(1):120-3. Disponible en: Disponible en: https://www.lungcancerjournal.info/article/S0169-5002(09)00137-8/fulltext
10.
[ Links ]
11.
Lin JJ, Cardarella S, Lydon CA, Dahlberg SE, Jackman DM, Jänne PA, et al. Five-Year Survival in EGFR -Mutant Metastatic Lung Adenocarcinoma Treated with EGFR-TKIs. J Thorac Oncol .2016 [acceso: 05/05/2020]; 11(4):556-65. Disponible en: Disponible en: https://linkinghub.elsevier.com/retrieve/pii/S1556086415002658
11.
[ Links ]