Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de Salud Animal
versión impresa ISSN 0253-570X
Rev Salud Anim. v.32 n.1 La Habana ene.-abr. 2010
Artículo reseña
MELAMINA. UN PROBLEMA POTENCIAL PARA LA SALUD ANIMAL Y HUMANA COMO ADULTERANTE EN LOS ALIMENTOS CON ÉNFASIS EN LA LECHE
MELAMINE. A POTENTIAL PROBLEM FOR ANIMAL AND HUMAN HEALTH AS ADULTERANT IN FOOD ESPECIALLY IN MILK
A. Escobar*, R. Faure*, Dayana Sosa*, P. Ponce*, S.Vega**
*Dirección de Salud y Producción Animal, Centro Nacional Sanidad Agropecuaria (CENSA), Apartado 10, San José de las Lajas, La Habana, Cuba. Correo electrónico: escobar@censa.edu.cu; **Universidad Autónoma Metropolitana, Unidad Xochimilco. Departamento de Producción Agrícola y Animal, México, D.F.
RESUMEN
El consumo de melamina, sustancia química empleada en la industria del plástico, constituye un riesgo para la salud humana y animal. La presencia de melamina en la leche u otro alimento puede ocurrir de forma natural, por adulteración o transformación metabólica del plaguicida ciromaxina. En el presente artículo se aborda los antecedentes de la adulteración de alimentos con melamina, los aspectos toxicológicos y una compilación de criterios de diferentes expertos en cuanto a las ventajas y desventajas de la metodología analítica para la determinación de melamina en alimentos. En el CENSA el departamento del CENLAC cuenta una metodología analítica que posibilita detectar problemas de adulteración, presencia de residuos y contaminantes en leche lo cual posibilita evaluar su inocuidad.
Palabras clave: melamina; adulteración; leche; métodos analíticos
ABSTRACT
Melamine is a chemical substance used in the manufacturing of plastics, which added to the milk constitutes a risk for human and animal health, if it is consumed. The presence of melamine in the milk or another food can happen in a natural way, by adulteration or metabolic transformation of the pesticide cyromazine. In the present review, the antecedents of melamine adulteration in foods are showed, the toxicological aspects and a compilation of criteria from different experts about the advantages and disadvantages of the analytic methodology for the melamine determination in foods are analyzed. CENLAC department from the National Center for Animal and Plant Health (CENSA), has implemented an analytic methodology which facilitates to detect adulteration problems and the presence of residuals and contaminants in milk allowing the evaluation of food safety.
Key words: melamine; adulteration; milk; analytic methods
INTRODUCCIÓN
La adulteración de los alimentos constituye una práctica fraudulenta y tiene fines económicos al alcanzar productos más baratos. Se considera adulterado un alimento cuando su naturaleza o composición no correspondan a la información mostrada en la etiqueta (1). Los fraudes en materias primas como en productos alimenticios terminados han aumentado considerablemente en los últimos años y no sólo se manifiesta en los países pobres sino también en los desarrollados. Las adulteraciones cada día son más difíciles de detectar ya que las sustancias implicadas presentan una composición muy similar a las del producto de origen, de ahí la necesidad de contar con métodos más selectivos y específicos para poder detectar a los adulterantes.
La adulteración es una práctica penalizada por los organismos regulatorios y se establecen reglamentos y normas para definir la autenticidad de un producto alimenticio; de esta forma contribuir a la inocuidad del mismo.
En el caso específico de la leche, la Federación Internacional de Lechería (FIL), considera que la misma es el producto de la secreción normal de la glándula mamaria, obtenido por uno o varios ordeños, sin ninguna adición o sustracción (2), por tanto la incorporación de sólidos no lácteos, de origen vegetal o animal a la leche fluida, constituye una adulteración. Entre las adulteraciones más frecuentes que se hacen en la leche se puede mencionar la adición de agua y sales neutralizantes (3), agregado de suero de queserías en leche fluida y deshidratada (4) y la sustitución de grasa láctea por otras de origen vegetal o animal (5,6).
Los altos precios de la leche en polvo en el mercado internacional en los últimos años y su tendencia mantenida (7), hace que personas inescrupulosas traten de engañar al consumidor adulterando los alimentos con la finalidad de obtener ganancias, ejemplos recientes muestran la sustitución con grasa vegetal en una marca de leche pasteurizada de amplio consumo en la Ciudad de México (6) y la presencia de melamina en leche y derivados lácteos en China (8).
La intención de este artículo es ofrecer una información útil para los profesionales de Medicina Veterinaria y de Alimentos sobre una sustancia química empleada en la fabricación de plástico conocida como melamina y que estuvo implicada en un escándalo mundial ocurrido en empresas Chinas cuándo se detectó su presencia en leche para infantes, causando una enfermedad renal en las personas que consumieron el alimento adulterado.
Antecedentes
En marzo del 2007 en Estados Unidos algunos productores de alimentos para mascotas retiraron del mercado sus productos, ya que se vincularon con la presencia de una insuficiencia renal en gatos y perros (9). Un estudio toxicológico con unos de los alimentos retirados del mercado evidenció que nueve gatos murieron con la misma sintomatología presentado durante la intoxicación (10). Estudios posteriores corroboraron que el alimento sospechoso estaba contaminado con dos sustancias químicas empleada en la industria del plástico conocido como melamina y ácido cianúrico (11,12,13); sin embargo a pesar de relacionar la presencia de estos dos residuos industriales en el alimento, no se pudo explicar directamente la causa de las enfermedades renales, debido a las bajas concentraciones de los mismos (14). Un estudio posterior confirmó que los agentes causantes de la insuficiencia renal eran la melanina y el ácido cianúrico al encontrarse el aducto del ácido de melamina cianúrico estable en la orina de las mascotas enfermas (15,16).
El gluten del trigo empleado como materia prima en la elaboración de alimentos para mascotas fue identificado como la fuente de contaminación y el mismo procedía de la empresa China "Xuzhou Anying Biologic Technology" (17). La razón por la cual contenía melamina la materia prima no está claro, sin embargo medios de noticias reportan que la adulteración pudo haber sido de manera intencional por razones económicas (9). Inicialmente los reportes sugieren que la contaminación fue confinada para alimentos para mascotas, sin embargo se han descubierto la presencia de melamina en alimentos concentrados destinados al consumo de aves, cerdo y pez gato (18,19).
El 13 de septiembre del 2008 se hace pública la adulteración de leche de lactantes por melamina, donde 400 niños se encuentran intoxicados y se teme por la vida de varios. De hecho un niño de la provincia noroccidental de Gansu falleció por cálculos renales. En pocos días se tienen nuevos datos y la cifra de bebés y niños intoxicados siguió aumentando como resultado del consumo de estos productos (20). Una semana después el Ministerio de Salud Chino reportó que alrededor de 40 000 niños recibieron tratamiento, de los cuales 12 900 estaban actualmente hospitalizados y se habían confirmado tres defunciones por esta causa (21).
La Agencia de Inspección Nacional de China encontró niveles de melamina que oscilaron entre 0.09 y 2.560mg/Kg en diversos productos lácteos (22). Las principales compañías implicada en el escándalo fueron: Shijiazhuang Sanlu Group Co, Inner Mongolia Yili Industrial Group Co 600887.SS y Mengniu Dairy 2319.HK, estas dos últimas líderes del sector lácteo chino.
Otros países afectados por recibir importaciones de leche proveniente del mercado Chino fueron: Bangladesh, Brunei, Burundi, Gabón, Hong Kong, Japón, Malasia, Myanmar, Filipinas, Singapur, Corea del Sur, Taiwán y Vietnam. Los cuales retiraron sus productos de las estanterías, prohibieron las importaciones chinas o comenzaron a realizar controles de calidad (23).
Entre las marcas internacionales afectadas están: la marca suiza Nestlé y la Dairy Farm UHT ambas de fabricación China, que retiraron todos sus productos de los comercios de Hong Kong después de que una serie de pruebas indicaran que tenían melamina, aunque en concentraciones bajas. Por otra parte la cadena de cafeterías Starbucks retiró la leche de sus 300 locales en China, al temer haber comprado leche contaminada al proveedor Mengniu Dairy 2319.HK (23).
Regulaciones
La Organización Mundial de la Salud informó que la melamina no tiene nada que hacer en los alimentos como la leche y ratificó que hasta el momento la adición de la melamina en los alimentos no es aprobada por la OMS, la FAO ni el Codex Alimentarius, máximo órgano internacional que fija los estándares de calidad de los alimentos.
A partir del escándalo de intoxicación infantil en China por la presencia de melamina en leche, la Unión Europea (UE) establece un límite máximo de 2 mg/kg (ppm) a la importación de productos que contienen leche o productos lácteos originarios o procedentes de la China (24). También la UE estableció una dosis máxima diaria tolerable de 0,5 miligramos de melamina por kilo de peso.
La agencia de Inspección de alimentos de Canadá (CFIA-Canadian Food Inspection Agency conocido por sus siglas en inglés) estableció patrones interinos para la presencia de melamina y ácido cianúrico en productos importados que contengan leche, fijando niveles de 1 ppm para fórmulas lácteas infantiles y 2.5 ppm para productos lácteos, fundamentándose que bajos niveles de estas sustancia, no son indicativos de una adulteración, y sí debido a una exposición ambiental (por ejemplo el embalaje o el procesamiento). Por otra parte la presencia de melamina en un alimento en concentraciones baja no indica que hay un riesgo automáticamente a la salud humana (25).
La FDA de Estados Unidos (US FDA- U.S. Food and Drug Administration conocido por sus siglas en Inglés) fijó un límite de 2.5 ppm de melamina en productos lácteos para adultos, no estableciendo ningún valor para niños (26).
En China se definió aceptar niveles de melamina de 1 ppm para las fórmulas lácteas infantes y 2.5 ppm para leche líquida, en polvo y otros productos lácteos.
Propiedades físico químicas y síntesis de la melamina
La melamina es un químico industrial tóxico usado en la fabricación de plástico. Fue sintetizada por primera vez por el científico alemán Justus von Liebig en 1834. Es una base orgánica que presenta una fórmula química C3H6N6 y se conoce con el nombre 1,3,5-triazina-2,4,6-triamina. Es un polvo blanco cristalino y es soluble ligeramente en agua. Presenta propiedades de retardar el fuego, debido a su liberación de nitrógeno gaseoso cuando es quemado o carbonizado.
Inicialmente la producción de melamina ocurre cuando la cianamida de calcio es convertida en una dicianidiamida y esta es calentada por encima del punto de fusión, sin embargo en la actualidad se emplea la urea para la producción de melamina. Este último proceso ocurre en dos pasos, una primera reacción endotérmica donde la urea se descompone para formar el ácido cianúrico (HCNO) más amoniaco. En la segunda etapa ocurre la polimerización del ácido ciánico para formar la melamina y la liberación de dióxido de carbono, este proceso es exotérmico.
6 (NH2)2CO ® C3H6N6 + 6 NH3 + 3 CO2
Durante la síntesis química pueden ocurrir diferentes productos intermedios como son ácido cianúrico, ammelina y ammelida (Figura 1), estos metabolitos también puede aparecer por la degradación microbiológica de la melamina (27).
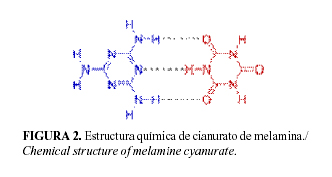
La combinación de la melamina con el ácido cianúrico forma el cianurato de melanina, también conocido como aducto ácido de melamina cianúrico o complejo ácido de melamina ácido cianúrico, la unión de estos dos compuestos ocurre a través de enlace de hidrógeno (Figura 2).
A continuación se muestra un resumen sobre las características físico químicas de las cuatro antes citadas en la Tabla 1.
Metabolismo y toxicidad de la melamina
La melamina no es metabolizada por los animales y es excretada en más del 90% en la orina dentro de las 24 horas. Estudios realizados en animales muestran que la melamina tiene un rango de vida media entre 2.7 y 4.04 h cuando es administrada por vía oral o endovenosa (28). Un estudio farmacocinético de una aplicación intravenosa de la melamina (6.13 mg/kg) en puercos destetados mostró un aclaramiento de 0.11 ±0.01 L/h/kg y un volumen de distribución de 0.61±0.04 L/kg (29), mientras en el modelo de rata el valor de la vida media de la melamina fue 1.5 veces menor y el volumen de distribución 3 veces mayor, estas diferencias se atribuyen a la velocidad de filtración glomerular (29).
Otro estudio farmacocinético en cerdos estimó que el intervalo de retiro de la carne fue de 19.2 a 20.9 h cuando fueron expuestos a una dosis única de melamina de 3.0 y 5.12 mg/kg, mientras un estudio de dosis repetida durante dos veces al día por un tiempo de 7 días mostró un intervalo de 20.1 a 21.3 h. Los intervalos de retiro fueron fundamentados por la determinación directa de la melamina en el tejido del riñón con un nivel de seguridad de 50 ppb (30).
Un estudio controlado en vacas Holstein en lactación se le suministró en la dieta 17 g de melamina por día, apareciendo en la leche 8 horas después de la primera ingestión alcanzando su máxima excreción a las 56 horas, donde el porcentaje de melamina en la leche osciló entre 1.7 y 2% con respecto a la cantidad consumida diariamente. Una vez retirado el alimento contaminado se mantuvo los niveles detectables de melamina en la leche hasta 152 h. Estos resultados son de gran importancia porque hasta el momento se pensaba que la presencia de melamina se debía solo a problemas de adulteración directa de la leche (31).
Cuando existe adulteración por melamina los niveles de nitrógeno en leche se incrementan lo que falsea los resultados en proteína bruta , sin embargo la aparición de forma natural no muestra diferencia significativa en la composición físico químico de la leche entre los grupos tratados con melamina y el control (Tabla 2). Esto se debe en primer lugar al bajo nivel de excreción y en segundo lugar al efecto dilución por el nivel producción de leche.
También se ha reportado la presencia de melamina en alimentos debido a la transformación metabólica del plaguicida ciromazina dentro del cuerpo, un estudio en gallina ponedoras donde se suministró el plaguicida ciromazina en la dieta a una concentración de 5ppm, se encontró residuos de melamina y ciromazina en carne y huevo a una concentración de 0.25 ppm (32).
La mayor parte de los estudios toxicológicos se habían realizado siempre en el supuesto de exposición laboral (por inhalación o contacto con la piel), no de ingesta por vía oral, además de existir muy poca información sobre lo que puede ocurrir a largo plazo. De manera general se puede decir, que la toxicidad de la melanina es baja y puede producir irritación de las vías respiratorias, ojos, piel y aparato digestivo, además hipersensibilización y posible daño renal. La ingestión de melamina puede provocar daños en el sistema reproductor, en la vejiga o en formación de cálculos renales. Esto último ocurre cuando la melamina se combina con el ácido cianúrico formando el cianurato de melamina un producto insoluble que obstruye las vías urinarias impidiendo la correcta eliminación de la orina, por otra parte el flujo sanguíneo dentro del riñón también se afecta.
Toxicidad aguda
Reportes de publicaciones informan que el valor más bajo de LD50 por vía oral en ratas es de 3161 mg/kg y la LD50 para el ensayo de irritación dérmica en conejo fue 1000 mg/Kg. Estudios toxicológicos realizados con el cianurato de melamina en ratas y ratones sugieren que presenta mayor toxicidad que cuando se analiza la melamina o el ácido cianúrico solos (la LD50 del cianurato de melamina vía oral en rata fue de 4.1g/kg, para la misma especie pero evaluando melamina y ácido cianúrico, las LD50 fueron 6 y 7.7 g/kg respectivamente) (33). Un estudio realizado para evaluar la toxicidad de la melamina y el ácido cianúrico y su combinación en gatos, corroboran que esta última es la responsable de los daños renales agudos en gatos (34).
Con relación a la concentración de efectos adverso no observados (NOAELs por sus siglas en inglés) se han reportados valores de 63 mg/kg.pc/día en ratas alimentadas durante 13 semanas; 240 mg/kg pc/día en ratas alimentadas durante 28 días; 417 mg/kg pc/día en ratas alimentadas por 14 días y 1600 mg/kg pc/día en ratones alimentados durante 13 semanas. Otros cálculos de NOAELs para ratas en estado reproductivo y de desarrollo mostraron valores de 400 y 1060 mg/kg pc/día para el estado maternal y fetal respectivamente. Los principales síntomas clínicos observados en los experimentos anteriormente mencionados cuando la melamina fue administrada por vía oral son: disminución en el consumo de los alimentos, pérdida de peso, cálculos renales, hiperplasia epitelial en la vejiga y una baja tasa de supervivencia (14).
Toxicidad crónica
La ingestión de melamina además de los daños antes mencionados puede desarrollar cáncer de vejiga. Un estudio realizado en perros donde se suministró melamina al 3% mezclado con el alimento durante un año (1200 mg/kg/day) provocó los siguientes cambios: disminución de la gravedad específica de la orina, poliuria, presencia de cristales de melamina, proteína y sangre oculta (35)
Un estudio controlado en ratas durante dos años expuestas a una dieta alta de melamina (4500 ppm or 263 mg/kg pc/día), encontraron asociaciones con un aumento de cálculos renales y un incremento de la incidencia de tumores en la vejiga de ratas hembras (14).
En diversos protocolos toxicológicos donde se evalúa la toxicidad de la melamina y sus metabolitos en distintas especies corroboran el efecto sinérgico entre ellos. Un estudio en ratas muestra que la mezcla de melamina, ammelina, ammelida y ácido cianúrico (400/40/40/40 mg/kg) y de melamina y ácido cianúrico (400/400 mg/kg) presentan mayor toxicidad que los elementos independientes (36); otro estudio en puerco y peces corroboran el mismo efecto sinérgico de las combinaciones incrementando la presencia de cristales renales (37) y en gatos a las 12 horas de consumir la combinación de melamina y ácido cianúrico se presenta ligera depresión, vómitos y anorexia (34).
Los principales hallazgos anatomopatológicos son: riñones edematosos con un incremento de su peso y presencia de precipitado de color amarillo carmelita en los túbulos.
En histopatología en secciones congeladas se observa la presencia de cristales en la fracción larga de los túbulos renales particularmente en la medula, mientras en secciones fijadas con formalina aparecen dilatación tubular extensiva y debris basofílico en túbulos distal y lazos de Henlen.
Análisis químicos
Varios métodos han sido desarrollados para los análisis de melamina en diferentes sustratos. Estos incluyen cromatografía gaseosa (GC), cromatografía líquida de alta resolución (CLAR o HPLC en sus siglas en ingles); CG o HPLC acoplada a un espectrómetro de masa, electroforesis capilar e inmunoensayos entre otros.
Un análisis compilado por diferentes expertos de los principales procedimientos se refleja a continuación:
HPLC-MS/MS. Es el método más seguro para la cuantificación de melamina en diferentes matrices en el orden de las partes por billón (ppb) por su alta sensibilidad y selectividad en una amplia variedad de productos. Las muestras son extraídas con una mezcla
de acetonitrilo:agua, el extracto es purificado por extracción líquido-líquido seguido por extracción en fase sólida. El uso de estándares internos marcados isotópicamente permite la cuantificación confiable a niveles bajos. La instrumentación requerida es de alta tecnología y costosa (38).
HPLC-MS. En muchos casos sus resultados de selectividad y límite de cuantificación son comparables con el HPLC-MS/MS, su principal limitación está en la valoración de la muestra por las interferencias que pueden coincidir con la masa molecular protonada de la melanina 127.07 daltons Se requiere de una limpieza eficiente empleando columna de intercambio catiónico. El procedimiento permitiría una cuantificación confiable y al igual que el procedimiento anterior la instrumentación requerida es de alta tecnología (38).
CG-MS. Las muestras son extraídas con una mezcla de acetonitrilo agua dietilamina y requieren de una mayor purificación para su posterior derivatización con TMS ante de aplicar la misma. El método una vez desarrollado presenta alta selectividad y sensibilidad, pudiendo ser aplicado a una amplia variedad de matrices. El método original propuesto por la FDA de Estados Unidos alcanzó un límite de cuantificación de 2 mg/kg, sin embargo puede determinar hasta 0.01 mg/kg. El sistema CG-MS requiere mayor atención cuando se trabaja con muestras derivatizadas. Los controles de calidad son más estrictos debido a una mayor probabilidad de error por la manipulación de la muestra en su preparación. La instrumentación requerida es de alta tecnología y costosa.
HPLC-UV. Puede proporcionar una información cuantitativa (generalmente emplea UV 240 nm). Las muestras son extraídas con una mezcla de acetonitrilo y agua empleando un sistema de par iónico en sus análisis. Muestras complejas como galletas y golosinas presentan una variedad de interferencias que absorben a la longitud de onda de 240 nm. Por lo general las muestras positivas requieren de un segundo método para su confirmación y cuantificación. Requiere de tecnología pero no tan costosa como la anterior (38).
ELISA. Son métodos de alta especificidad por su principio de reacción antígeno anticuerpo. Son ensayos cuantitativos y se emplean fundamentalmente en las matrices de leche fluida y en polvo, gluten de trigo y comida de mascota. Las muestras no requieren de purificación para ser analizadas. Los juegos de reactivos están disponibles comercialmente y constituye una herramienta de pesquisaje adecuado. En ocasiones no se alcanzan los límites de detección requeridos para algún tipo de matriz (38).
En la Tabla 3 se muestran un resumen de los diferentes procedimientos para la determinación de melamina y compuestos análogos en distintos sustratos.
En el Centro de Ensayo para el Control y Calidad de la Leche (CENLAC), del Centro Nacional de Sanidad Agropecuaria (CENSA) cuenta con las condiciones tecnológicas que permite detectar problemas de adulteración y la presencia de residuos y contaminantes en leche a través de metodologías analíticas de avanzadas aplicando las normas ISO 9004-2 e ISO 17025 para ofrecer servicios analíticos especializados.
REFERENCIAS
1. Banglapedia. Food Adulteration. Updated 2009, cited March 2009. Available from: http://banglapediasearchcombd/commentsphp. 2009.
2. FIL/IDF. Dictionary of dairy terminology. Amsterdam Elsevier. 1983;(v.1) (328 p).
3. Ahmad Hassabo A. Milk Adulteration by Adding Water and Starch at Khartoum State. Pakistan. Journal of Nutrition. 2009;8(4):439-40.
4. Reyes J, Bon F, Moreno JL, Franchini CR. Adulteracion de leche con suero de queserías en la ciudad de Aguascalientes. Update 2006 cited Marzo 2009. Available from: http://www.respynuanlmx/especiales/2006/ee-14-2006/documentos/Art08pdf 2006.
5. Vega S, Gutiérrez R, Díaz G, Coronado M, Salas JH, Pérez JJ. Avances en el estudio de la adulteración de la grasa láctea. CARNILAC 2006;Octubre /Noviembre 10-6.
6. Díaz G, Gutiérrez R, Pérez N, Vega S, González M, Prado G, et al. Detección de adulteraciones en la grasa de leche pasteurizada mexicana. Rev Salud Anim. 2002;24(1):54-9.
7. INFOLECHE. Infoleche Newsletter Boletin Infoleche/FEPALE, Julio, 2007.
8. ANO. CHINESE BABY-FOOD TRAGEDY INTENSIFIES. Chemical & Engineering News. 2008;86(39):18.
9. Weise E, Schmit J. Melamine in pet food may not be accidental. USA Today. Available from: http://www.usatodaycom/money/industries/2007-04-24-fda-pet-food-probe_Nhtm and http://www.usatodaycom/money/industries/2007-04-19-pet-food -usat_Nhtm. 2007.
10.Herdon MUS. Food and Drug administration. Press Release P07-48 17 March 2007 Availablefrom: http://www.fdagov/bbs/topics/NEWS/2007/NEW01590html. 2007.
11.Barboza D. Another Chemical Emerges in Pet Food Case. The New York Times. Update May 9 2007, cyted 27 octuber 2008. Avialable from: http://www.nytimescom/2007/05/09/business/worldbusiness/09foodhtml. 2007.
12.Cornell-University. Cornell Details Effect of Pet Food Contaminant, Melamine. April 10, 2007. ScienceDaily. Available from: http://www.sciencedaily. com/releases/2007/04/070409185542.htm. 2007.
13.Vail T, Jones PR, Sparkman OD. Rapid and unambiguous identification of melamine in contaminated pet food based on mass spectrometry with four degrees of confirmation. J Anal Toxicol. 2007;31(6):304-12.
14.USFDA. Interim Melamine and analogues safety/risk assessment. . US Food and Drug Administration May 25, 2007. Available from: http://www.cfsanfdagov/~dms/melamrahtml. 2007.
15.Johns J, Ruetenik D. May 1, 2007. Mix of chemicals may be key to pet-food deaths. CNN. Available from: http://www.cnn.com/2007/US/05/01/recall.riddle/index.html. 2007.
16.Daily S. May 2, 2007b. Melamine contaminant found in chicken feed. Available from: http://www.sciencedaily.com/releases/2007/05/070502072434.htm. 2007.
17.Sivaraman A. May 30, 2007. Melamine in pet food, wheat gluten from China: FDA. Reuters.Available from: http://www.reuters.com/article/domestic News/idUSWEN594320070330. 2007.
18.Andersen WC, Turnipseed SB, Karbiwnyk CM, Madson MR. Determination of Melamine Residues in Catfish Tissue by Triple Quadrupole LC-MS-MS with HILIC Chromatography. 2007.
19.Andersen WC, Turnipseed SB, Karbiwnyk CM, Clark SB, Madson MR, Gieseker CM, et al. Determination and confirmation of melamine residues in catfish, trout, tilapia, salmon, and shrimp by liquid chromatography with tandem mass spectrometry. J Agric Food Chemistry. 2008;56(12):4340-7.
20.Pintxo. Crónica del caso de la leche adulterada con melamina. DirectoalPaladar Update 2009 cyted March 2009 available from: http://imgdirectoalpaladarcom/lp2/css/iecss. 2008.
21.ANO. Melamine-contaminated powdered infant formula, China. Weekly Epidemiological Record. 2008;83(39):350.
22.WHO. Melamine-contamination event, China, September - October 2008. World Health Organization Update 2008 cyted March 2009 available from http://www.whoint/foodsafety/fs_management/infosan_events/ar/indexhtml. 2008.
23.ELUNIVERSO. ¿Qué es la melamina? El Universocom Noticias del Ecuador y del mundo. update 22 septiembre 2008, cyted 27 octubre 2008. Available from http://wwweluniversocom/2008/09/22/0001/14/internacionaleshtml. 2008.
24.UE. DECISIÓN DE LA COMISIÓN de 26 de septiembre de 2008 por la que se establecen las condiciones particulares de importación de productos que contienenleche o productos lácteos originarios o procedentes de China. Diario Oficial de la Unión Europea. Update 2792008. 2008;(2008/757/CE).
25.CFIA. Canadian Food Inspection Agency - New Import Requirements for Food Products from China Containing Milk or Milk-derived Ingredients..Melamine - Certain products from China [update 6 octuber 2008 cyte 27 octuber 2008* available from wwwinspectiongcca "http://wwww3org/TR/xhtml1/DTD/xhtml1-transitionaldtd" 2008.
26.USFDA. Melamine Contamination in China. (Updated: October 18, 2008) available from http://www.fdagov/comments.html. 2008.
27.Ehling S, Tefera S, Ho IP. High-performance liquid chromatographic method for the simultaneous detection of the adulteration of cereal flours with melamine and related triazine by-products ammeline, ammelide, and cyanuric acid. Food Additives & Contaminants. 2007;24(12):1319-25.
28.Hau AK, Kwan TH, Li PK. Melamine toxicity and the kidney. J Am Soc Nephrol. 2009;20(2):245-50.
29.Baynes RE, Smith G, Mason SE, Barrett E, Barlow BM, Riviere JE. Pharmacokinetics of melamine in pigs following intravenous administration. Food and Chemical Toxicology. 2008;46:1196-200.
30.Buur JL, Baynes RE, Riviere JE. Estimating meat withdrawal times in pigs exposed to melamine contaminated feed using a physiologically based pharmacokinetic model. Regulatory Toxicology and Pharmacology. 2008;51:324-31.
31.Cruywagen CW, Stander MA, Adonis M, Calitz T. Hot topic: pathway confirmed for the transmission of melamine from feed to cow's milk. J Dairy Sci. 2009;92(5):2046-50.
32.Meek ME, Bucher JR, Cohen SM, Dellarco V, Hill RN, Lehman-McKeeman LD, et al. A Framework for Human Relevance Analysis of Information on Carcinogenic Modes of Action. Critical Reviews in Toxicology: Taylor & Francis Ltd; 2003. p. 591-653.
33.Wikipedia. Melamine cyanurate. Wikipedia, the free encyclopedia. Update 14 October 2008 cite 29 October 2008. Available from: http://enwikipediaorg/wiki/Melamine_cyanurate. 2008.
34.Puschner B, Poppenga RH, Lowenstine LJ, Filigenzi MS, Pesavento PA. Assessment of melamine and cyanuric acid toxicity in cats. J Vet Diagn Invest. 2007;19:616-24.
35.EPA. SUMMARY OF TOXICOLOGY DATA TRICHLOROMELAMINE "Chronic Feeding - Dogs". Update april 2002 cited 29 octiber 2008. Available from: http://wwwcdprcagov/docs/risk/toxsums/pdfs/1023pdf. 2002.
36.Dobson RLM, Motlagh S, Quijano M, Cambron RT, Baker TR, Pullen AM, et al. Identification and characterization of toxicity of contaminants in pet food leading to an outbreak of renal toxicity in cats and dogs. Toxicol Sci. 2008;106(1):251-62.
37.Reimschuessel R, Gieseker CM, Miller RA, Ward J, Boehmer J, Rummel N, et al. Evaluation of the renal effects of experimental feeding of melamine and cyanuric acid to fish and pigs. Amer J Vet Res. 2008;69(9):1217-28.
38.WHO/HSE-FOS. Melamine: Comments on analytical methods. Update 2 octuber 2008 cited 29 octuber 2008. Available from: http://wwwwhoint/foodsafety/fs_management/Melamine_methods_commentspdf. 2008.
39.WHO/HSE-FOS. Analytical Methods Available for Detecting and Quantifying Melamine and Cyanuric Acid in Food (and Feed). 2008.
40.Wang L, Xiaodong L, Tracy M, Schnute B, Birznieks I, Pohl C. Determination of Melamine and Cyanuric Acid by LC-MS Using an Acclaim Mixed-Mode WAX-1 Column and MSQ Plus Mass Spectrometric Detection. LC-GC North America. 2007;25:40.
41.Litzau JJ, Mercer GE, Mulligan KJ. GC-MS Screen for the Presence of Melamine, Ammeline, Ammelide, and Cyanuric Acid. Laboratory Information Bulletin LIB No 4423. Update octuber 2008. Availabel from http://wwwcfsanfdagov/~frf/lib4423html. 2008;24.
42.Cai M, Yu C, Zou Y, Luan W. Rapid Screening of Melamine and Cyanuric Acid in Milk Products Using Agilent J&W HP-5ms GC Column and Agilent 7890A/5975C GC/MSD with Column Backflushing. Agilente Technologies Update 2008 cyted March 2009 avilable from http://www.agilentcom/chem. 2008.
43.Filigenzi MS, Tor ER, Poppenga RH, Aston LA, Puschner B. The determination of melamine in muscle tissue by liquid chromatography/tandem mass spectrometry. Rapid Communications In Mass Spectrometry: RCM. 2007;21(24):4027-32.
44.Filigenzi MS, Puschner B, Aston LS, Poppenga RH. Diagnostic determination of melamine and related compounds in kidney tissue by liquid chromatography/tandem mass spectrometry. Journal of Agricultural And Food Chemistry. 2008;56(17):7593-9.
45.Varelis P, Jeskelis R. Preparation of 13C3-melamine and 13C3-cyanuric acid and their application to the analysis of melamine and cyanuric acid in meat and pet food using liquid chromatography-tandem mass spectrometry. Food Additives & Contaminants. 2008;25(10):1210-7.
46.Luan W, Fang Y, Zweigenbaun J. A total solution for the analysis Melamine and Cyanuric acid in pet food by GC/MS and aqueous normal phase LC/MS/MS. Agilent Tecnology update 2007 cyte March 2009 available from wwwagilentcomchem. 2007.
47.Turnipseed S, Casey C, Nochetto C, Heller DN. Determination of Melamine and Cyanuric Acid
Residuesin Infant Formula using LC-MS/MS. Laboratory Information Bulletin No 4421. Update October 2008, available from: http://www.cfsanfdagov/~frf/lib4421html. 2008;24.
48.Smoker M, Krynitsky AJ. Interim Method for Determination of Melamine and Cyanuric Acid Residues In Foods using LC-MS/MS: Version 1.0. Laboratory Information Bulletin No 4422, update October 2008, available from: http://www.cfsanfdagov/~frf/lib4422.html. 2008.
49.Garber EAE. Detection of Melamine Using Commercial Enzyme-Linked Immunosorbent Assay Technology. Journal of Food Protection. 2008;71(3):590-4.
50.He L, Liu Y, Lin M, Awika J, Ledoux DR, Li H, et al. A new approach to measure melamine, cyanuric acid, and melamine cyanurate using surface enhanced Raman spectroscopy coupled with gold nanosubstrates. Sens & Instrumen Food Qual 2008;2:66-71.
(Recibido 5-5-2009; Aceptado 20-11-2009)