Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Cultivos Tropicales
versión impresa ISSN 0258-5936
cultrop vol.31 no.3 La Habana jul.-set. 2010
Efecto de los biorreguladores del crecimiento en la embriogénesis somática demandarina Cleopatra(Citrus reshni Hort. ex Tan.)
Effect of growth bioregulators in somatic embryogenesis demandarina Cleopatra (Citrus reshni Hort. Ex Tan)
Reina M. HernándezI. E-mail: rmargarita@cuij.co.cu, rmargarita@fbio.uh.cu, Dra.C. Esther DiosdadoII y Dr.C. F. CollIII; Dr.C. J. C. CabreraIV
I Profesora de la Universidad Jesús Montané Oropesa, Isla de la Juventud
II Profesora de la facultad de Biología, departamento de Biología Vegetal
III Profesor de la facultad de Química, Universidad de La Habana
IV Investigador Auxiliar de la Universidad de Notre-Dame de la Paix, Unidad de investigaciones en Biología Celular Vegetal, Namur 5000, Bélgica.
RESUMEN
La regeneración de plantas in vitro vía embriogénesis somática es un prerrequisito indispensable, para la aplicación de algunas herramientas de la Biotecnología en la mejora genética de las plantas y más aún en el caso de los cítricos. Para aumentar la cantidad de estos cultivos en las plantaciones, se pueden usar técnicas de propagación in vitro, como la embriogénesis somática, que requieren de medios de cultivo artificiales y fitohormonas. Debido a los altos costos de las fitohormonas, una alternativa cubana es el uso de biorreguladores del crecimiento de producción nacional, como el Pectimorf® y los análogos de brasinoesteroides: Biobras-6 y MH5. Estos biorreguladores, al igual que el 24-Epibrasinólido, son efectivos en los procesos morfogenéticos, generalmente a bajas concentraciones, como sustitutos o complementos de las auxinas y citoquininas. Se empleó la técnica de cultivo de óvulos fecundados in vitro, para obtener una línea celular embriogénica de Citrus reshni Hort. ex Tan y como fuente de óvulos fecundados, se tomaron ovarios de dicha especie procedentes de árboles de la Estación de Cítricos de Ceiba del Agua en Caimito, provincia La Habana. Para el mantenimiento de la línea embriogénica, se utilizaron callos embriogénicos de la línea celular establecida. Este trabajo estuvo dirigido a evaluar el efecto del Pectimorf® y los brasinoesteroides, MH5, Biobras-6 y 24-Epibrasinólido, en la obtención y el mantenimiento de la línea celular embriogénica de mandarina Cleopatra (Citrus reshni Hort. ex Tan.). En los resultados se pudo comprobar un incremento en la masa fresca del callo embriogénico en un menor tiempo de cultivo mediante el uso de estos biorreguladores.
Palabras clave: Citrus, embriogénesis somática, brasinoesteroides, Pectimorf®.
ABSTRACT
Plant regeneration through in vitro somatic embryogenesis is an indispensable prerequisite, to implement some biotechnological tools in plant genetic improvement and even more in the case of citrus. To increase the amount of these crops in plantations, the in vitro propagation techniques, such as somatic embryogenesis, can be used, which require artificial culture media and phytohormones. Due to the high costs of plant hormones, a Cuban alternative is the use of national growth bioregulators, such as Pectimorf® and brassinosteroid analogues: Biobras-6 and MH5. These bioregulators, like the 24-Epibrasinolide, are effective in morphogenetic processes, usually at low concentrations, to substitute or complement auxins and cytokinins. The technique for growing in vitro embryos was employed, to obtain an embryogenic cell line of Citrus reshni Hort. ex Tan and, as an embryo source, the ovaries of this species were taken, which came from trees of Citrus station of Ceiba del Agua, Caimito, Havana province. To maintain the embryogenic line, the embryogenic calluses from the established cell line were used. This work was aimed at evaluating the effect of Pectimorf® and the brassinosteroids MH5, Biobras-6 and 24-Epibrasinolide, to obtain and keep the embryogenic cell line of Cleopatra mandarin (Citrus reshni Hort. ex Tan.). Results proved an increased fresh weight of embryogenic callus in a shorter cropping time by means of these bioregulators.
Key words: Citrus, somatic embryogenesis, brassinosteroids Pectimorf®.
INTRODUCCIÓN
Los cítricos están entre los principales frutales del mundo y dan un gran impacto en nuestra sociedad, desde el punto de vista económico, social y cultural. No obstante, existen varios factores que limitan los programas de multiplicación, entre los que se encuentran el prolongado período juvenil y la elevada heterocigosis que caracterizan al género Citrus (1).
La disponibilidad de diversos procedimientos biotecnológicos ha abierto nuevas vías, para la solución de una parte importante de los problemas existentes, ya que permiten superar algunas limitaciones de los métodos tradicionales y ofrecen nuevas estrategias de trabajo más eficientes.
En el caso particular del género Citrus, se realiza la inducción de embriones somáticos in vitro en más de 20 especies, mediante el empleo de explantes tales como: nucelas, óvulos, protoplastos y embriones somáticos (2).
En este sentido, se han utilizado técnicas de propagación in vitro, encaminadas principalmente al mejoramiento de las plantas de interés económico, por medio de la callogénesis, embriogénesis somática, fusión de protoplastos, las suspensiones celulares y transformaciones de plantas (3).
Para el caso de los cítricos, la regeneración de plantas in vitro vía embriogénesis somática es un prerrequisito indispensable. Existen exigencias muy específicas en la capacidad de división y regeneración de este cultivo, en cuanto a la composición del medio, especialmente en lo referente a los reguladores del crecimiento. La introducción de nuevos biorreguladores cubanos en la tecnología de regeneración in vitro puede constituir una alternativa promisoria, para mejorar la eficiencia económica del proceso, con insumos nacionales y el uso de técnicas sencillas, confiables y menos costosas, con el fin de viabilizar este proceso.
Entre estos biorreguladores pueden citarse los análogos de brasinoesteroides, sintetizados por la facultad de Química de la Universidad de La Habana y los oligogalacturónidos, como el Pectimorf®, sintetizados por el Instituto Nacional de Ciencias Agrícolas (INCA).
Varios autores los han utilizado como sustitutos de las auxinas y citoquininas, o como complemento de estas, para así conocer su efectividad en los procesos morfogenéticos y estudiar los posibles efectos sobre la estabilidad genética de los cultivos (4, 5).
Por tal motivo, los objetivos de este trabajo estuvieron encaminados a:Establecer in vitro una línea embriogénica de mandarina Cleopatra(Citrus reshni Hort. ex Tan.).Evaluar el efecto de diferentes biorreguladores del crecimiento en los medios de cultivo, para la obtención y el mantenimiento de la línea embriogénica de mandarina Cleopatra (Citrus reshni Hort. ex Tan.).
MATERIALES Y MÉTODOS
Material vegetal. Se utilizaron óvulos fecundados de ovarios inmaduros de mandarina Cleopatra (Citrus reshni Hort. ex Tan.), procedentes de árboles de 15 años de edad cultivados en el banco de semilla, perteneciente a la Estación de Cítricos de Ceiba del Agua, provincia La Habana.
La colecta de los ovarios se realizó en la época de la floración, dos semanas después de la antesis floral. Se tomaron ovarios de 6 mm de diámetro, los cuales se lavaron con agua corriente y posteriormente se desinfectaron durante 20 minutos en una solución de hipoclorito de sodio (3 % v/v), añadiendo dos gotas de Twem-20 y tres lavados con agua destilada estéril.
Se empleó la técnica del cultivo de óvulos fecundados in vitro, para obtener una línea celular embriogénica de mandarina Cleopatra (6). El medio de cultivo utilizado fue el constituido por las sales minerales propuesto por Murashige y Skoog (7). En todos los casos, el medio de cultivo fue suplementado con las vitaminas de White (clorhidrato de piridoxina 1 mg.L-1, ácido nicotínico 1 mg.L-1, clorhidrato de tiamina 0.2 mg.L-1), inositol 100 mg.L-1, sacarosa 50 g.L-1, extracto de malta (EM) 500 mg.L-1 y solidificado con agar 10 g.L-1 (Difco Bacto Agar). El pH del medio de cultivo fue ajustado a 5,7±0,01.
Los óvulos se cultivaron en placas Petri de 10 cm de diámetro, que contenían 20 mL del medio de cultivo MS y las modificaciones para cada uno de los seis tratamientos (Tabla I); se colocaron 12 óvulos en cada placa y se realizaron 10 réplicas por tratamiento. Al final se cultivaron un total de 120 óvulos por cada tratamiento y 720 para todo el experimento.
Para evaluar el efecto del Pectimorf®, los análogos de brasinoesteroides (MH-5, Biobras-6) y el 24-Epibrasinólido en el cultivo de óvulos, se establecieron seis tratamientos, uno de ellos sin biorreguladores del crecimiento Control- (Tabla I).

Condiciones de cultivo. Se colocaron todas las placas con los óvulos cultivados en la oscuridad durante 30 días y, al cabo de este tiempo, se pasaron a la luz artificial continua; la radiación fotosintética activa (PAR) fue de 24-36 μmol.m-2.S-1, el valor de la humedad relativa de 80-85 % y la temperatura promedio de 25±2oC.
A partir de los 30 días se observaron los diferentes estadios del desarrollo embrionario, se realizó un conteo semanal de los embriones en cada una de estas fases y se determinó su coloración, con ayuda del código de colores hexadecimal. Los embriones se observaron con ayuda de un estéreo-microscopio, acoplado a una cámara digital y las imágenes se capturaron con un aumento de 10X. La fotos se editaron con el programa Motic Images (versión 1.2, 2000).
Análisis estadístico. A los cuatro meses del cultivo, se evaluó la cantidad de embriones formados en los diferentes tratamientos. Los resultados se procesaron mediante un análisis no paramétrico, según la prueba de comparación de proporciones. En todos los casos, se empleó el paquete estadístico TONYSTAT (8).
Mantenimiento de la línea embriogénica. Para este fin, se evaluó el efecto de los biorreguladores sobre el incremento en masa fresca de los callos embriogénicos de Citrus reshni Hort. ex Tan. (mandarina Cleopatra). Estos callos se obtuvieron a partir del cultivo de óvulos en el medio de cultivo MS sin reguladores del crecimiento (tratamiento control) y se sub-cultivaron mensualmente para su mantenimiento. En todos los casos se tomaron callos de seis meses de edad.
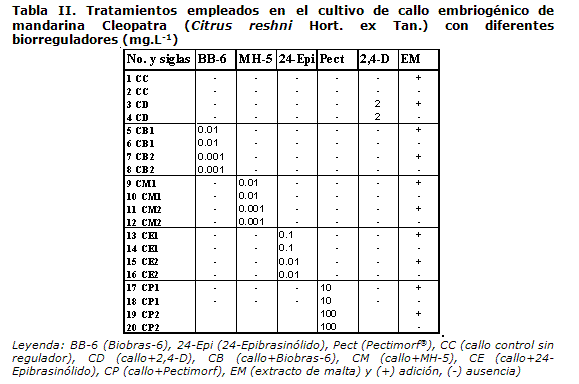
Los callos embriogénicos se sub-dividieron en fragmentos de masa igual a 80 mg. El medio de cultivo se suplementó con diferentes combinaciones de los biorreguladores a evaluar y el extracto de malta (6), además de un tratamiento con ácido diclorofenoxiacético (2,4-D) y el tratamiento control sin reguladores del crecimiento, contando al final con 20 tratamientos (Tabla II).
Para cada uno de los tratamientos, se emplearon tres placas Petri y en cada una se colocaron tres fragmentos de callos. Las placas se mantuvieron a la oscuridad a una temperatura de 25±2oC.
Análisis estadístico. A los 30 días se evaluó el incremento en masa fresca de los callos embriogénicos. Los resultados se procesaron mediante un análisis no paramétrico, según la prueba de Kruskal-Wallis (K-W), a un nivel de significación del 5 % y las sumas de rangos se compararon por la prueba de Student-Newman-Keuls (SNK). En todos los casos, se empleó el paquete estadístico TONYSTAT (8).
RESULTADOS Y DISCUSIÓN
Los primeros embriones se formaron a las cuatro semanas de cultivo en el tratamiento que contenía Pectimorf® (10 mg.L-1); sin embargo, en los tratamientos suplementados con Biobras-6 (10-3 mg.L-1), MH-5 (10-3 mg.L-1) y 24-Epibrasinólido (10-2 mg.L-1), estas estructuras se observaron entre las cinco y seis semanas de cultivo (Figura 1a-d). Además, se comprobó que la embriogénesis somática que se presenta en este cultivo es de tipo directa, ya que la formación del embrión no transcurre por la etapa previa del callo.

Figura 1. Primeros signos de crecimiento y estructuras obtenidas del cultivo de óvulos de mandarina Cleopatra (Citrus reshni Hort. ex Tan.): a) 2 semanas de óvulos en crecimiento, b) 3 semanas de óvulos en crecimiento, c) 4 semanas de masa proembriogénica y embriones globulares, d) 8 semanas de embrión con cotiledones, e) 10 semanas de multiembriones en diferentes fases del desarrollo embrionario, f) 16 semanas de embriones y callos con estructuras embriogénicas, g) callo con estructuras embriogénicas, h) plántulas enraizadas
Resultados similares obtuvieron Diosdado (6) en naranjo agrio (Citrus aurantium L.) y Bao (9) en Citrus macrophylla Wester, quienes señalan que el desarrollo in vitro de los óvulos en estas especies se registró entre las cinco y siete semanas de cultivo, respectivamente, al utilizar análogos de brasinosteroides y Pectimorf®. Sin embargo, en Citrus volkameriana Tan et Pasq y Citrus limon (L)Burm se requiere de cuatro meses al menos para el crecimiento del óvulo, cuando se utilizan las fitohormonas tradicionales (2, 10). Por lo que en este trabajo se logra acortar el tiempo de obtención de los embriones de cuatro meses a un mes, cuando se adiciona el Pectimorf®, o a mes y medio o dos meses, cuando se utilizan los brasinoesteroides, ambos biorreguladores de producción nacional.
Sin embargo, en Citrus reticulata Blanco y Citrus jambhiri Lush se obtuvieron buenos resultados, en la obtención de embriones somáticos a partir de segmentos cotiledonares, al suplementar el medio de cultivo con ácido bencil-aminopurina (BAP) 2.0 mg.L–1, 6-furfuril aminopurina (kin) 0.5 mg L–1 y ácido naftalenacético (ANA) 1.0 mg.L–1 (11). Todo esto demuestra que la respuesta morfogenética depende de la especie y el explante utilizado.
A los 30 días del cultivo de óvulos, se observó un incremento en los primeros estadios embrionarios –globulares- (Figura 1c-e) en todos los tratamientos, los cuales continuaron transitando por los diferentes estadios de desarrollo típico de este proceso: acorazonado, torpedo y cotiledonar (Figura 1e), etapas morfogenéticamente idénticas a las encontradas en el embrión cigótico (9).
Los embriones somáticos completamente formados en el estadio globular presentaron una coloración crema amarillo (H489980) en todos los tratamientos (Figura 1c), color que se mantuvo en el estadio de corazón por un período de tiempo promedio de cinco días. Los embriones en estadio de torpedo aparecen 15 días después con una estructura alargada y coloración verde, oscilando desde verde musgo (H559883) para el control, verde bosque (H5DB59E) para los tratamientos con análogos de brasinoesteroides y verde palma (H55B39E) para el tratamiento con Pectimorf. Por último, a los 65 días se observó el estadio cotiledonar, con cotiledones bien desarrollados, que mantuvieron el color verde intenso (Figura 1e).
Resultados similares se encontraron en los cultivos de café (Coffea sp.) (12) y boniato (Ipomoea batatas L. Lam.) (3), los que encontraron fases similares a las nuestras y pocas diferencias en el tiempo de tránsito por cada una de ellas.
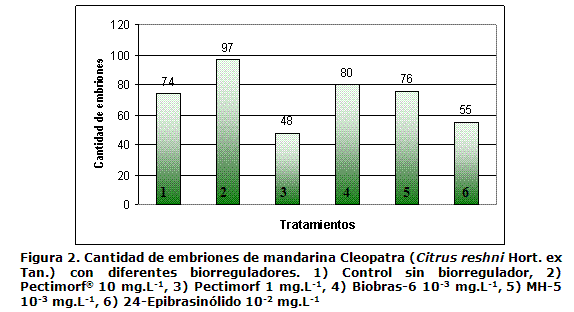
Al realizar la comparación de proporciones (8), se observaron diferencias significativas (p<0.001) para el tratamiento con Pectimorf® 10 mg.L-1, en relación con el resto de los tratamientos, donde se lograron obtener 97 embriones, mientras que para el caso del Biobras-6 y el MH-5, se formaron 80 y 76 embriones respectivamente y no existieron diferencias significativas respecto al control (74 embriones) pero sí en relación con el 24-Epibrasinólido y el Pectimorf® 1 mg.L-1, los cuales produjeron 55 y 48 embriones respectivamente (Figura 2).
La mejor concentración utilizada y el biorregulador de mejor comportamiento fue el Pectimorf® 10 mg.L-1, en cuanto al porcentaje de embriones y desarrollo más uniforme respecto al resto de los biorreguladores. Sin embargo, en la embriogénesis de Citrus macrophylla Wester (9), no se encontraron diferencias significativas entre los tratamientos empleados y el control sin regulador del crecimiento.
En yuca (Manihot esculenta Crantz (24) se obtuvieron porcentajes muy bajos en la formación de embriones (27 %), aun cuando los medios de cultivo estaban suplementados con altas concentraciones de 2,4-D (8 mg.L-1).
El Pectimorf® 10 mg.L-1 resultó el mejor tratamiento, en relación con el resto de las variantes probadas para la obtención de embriones somáticos, en cuanto al número, tiempo de formación y desarrollo uniforme, además de la coloración más intensa verde palma (H55B39E).
Los embriones obtenidos alrededor de los 40 días formaron multiembriones (Figura 1e), lo que facilita la propagación masiva de este material. Esto también ha sido descrito en el cultivo de óvulos de naranjo agrio(Citrus aurantium L.), Citrus sinensis L. y C. limon L. (6, 13),losque plantean que la formación de los nuevos embriones es continua, bien por la evolución de los proembriones o gemación de los pre-existentes. La diferencia entre estos autores y los resultados aquí expuestos radica en la especie utilizada y los reguladores del crecimiento utilizados.
En la caña de azúcar (Saccharum spp.) se demostró que la combinación de Pectimorf 5 mg.L-1 y 2,4-D 1.5 mg.L-1 produjo un efecto positivo sobre la formación de embriones (14), favoreciendo el número de embriones por gramo de tejido y la homogeneidad de estos en los estadios más avanzados de desarrollo; sin embargo, para la mandarina Cleopatra, se demostró que la concentración de Pectimorf® 10 mg.L-1 fue la más efectiva sin requerir la presencia de 2,4–D, fitohormona necesaria para inducir los eventos morfogenéticos en otras especies.
Del total de embriones obtenidos, el 49 % desarrolló raíces y de ellos el 33 % formó brotes, aún permaneciendo en los medios de cultivo iniciales con los biorreguladores suministrados (MH-5 10-3 mg.L-1, Biobras-6 10-3 mg.L-1, 24-Epibrasinólido 10-2 mg.L-1 y Pectimorf®10 mg.L-1), además del medio control (Figura 1h).
Los resultados demuestran que estos biorreguladores no solo pueden sustituir de forma parcial o total a los reguladores del crecimiento tradicionales, sino que en la mayoría de los casos, se obtienen resultados superiores, ya que sin agregar ningún otro regulador del crecimiento, continúan su desarrollo morfogenético, obteniéndose una planta completa (Figura 1h).
En diferentes cultivos como el café (Coffea canephora) (12), los pecíolos de violeta africana (Saintpaulina ionata) (15), embriones de naranjo agrio (6), el crecimiento in vitro del arroz (Oryza sativa L.) (10), la micropropagación de limón rugoso (Citrus jambhiri Lush.) y el clon de banano FHIA-18 (Musa sp. AAAB) (16, 17), se observó también estimulación en la producción de raíces en estos cultivos, cuando se aplicó el Pectimorf® 10 mg.L-1. Todo esto confirma, una vez más, la capacidad de este oligopectato para inducir y desarrollar el enraizamiento, que lo valida como una alternativa promisoria en la biotecnología vegetal cubana.
Otro fenómeno que se pudo comprobar en esta especie es que en la misma medida que se desarrollaban los embriones somáticos, aparecía una nueva estructura a las 16 semanas del cultivo, el callo embriogénico (Figura 1f-g), que por competencia morfogenética debía ser retirado del medio de cultivo, para su utilización en el mantenimiento de la línea embriogénica. En algunos casos, se observó que ambas estructuras (embrión y callo embriogénico) (Figura 1f) aparecen simultáneamente (6, 9). Sin embargo, Olivares (2) refiere que para obtener estas estructuras, se necesita hasta un año y medio o dos, mientras que en nuestra investigación, se logró acortar el tiempo de aparición del callo embriogénico a seis meses.
Efecto de los biorreguladores sobre el incremento en masa fresca del callo embriogénico. En la Figura 3 aparece el incremento de la masa fresca en los diferentes tratamientos analizados a los 30 días de cultivo. Se observa que, en todos los casos, se presentó un aumento de esta variable aunque de forma diferencial. El análisis estadístico para el incremento en la masa fresca de los callos con estructuras embriogénicas, corroboró que existen diferencias significativas entre los tratamientos para H= 51.2158**. Los resultados de la prueba de Student-Newman-Keuls refleja que el mayor incremento en peso de los callos se presentó en el medio suplementado con Biobras-6 10-3 mg.L-1, con EM (0.19 g) (tratamiento 7) y con MH-5 10-3 mg.L-1 sin EM (0.22 g) (tratamiento 12), lo que equivale a un aumento en la masa fresca de 2,3 y 2,7 veces respectivamente, mientras que los menores valores se presentaron en el medio que contenía solo Pectimorf® 100 mg.L-1 con EM (0.037 g) (tratamiento 20) y el que contenía 2,4-D a la concentración de 2 mg.L-1 con o sin EM (0.028 y 0.036 g) (tratamientos 3 y 4). Esto difiere de lo obtenido en la embriogénesis somática del banano Williams subgrupo Cavendish (Musa sp. grupo AAA), donde los mejores resultados fueron al utilizar 2,4-D 1,5 mg.L-1 en los medios de cultivo (18).
Todo indica que en la mandarina Cleopatra (Citrus reshni Hort. ex Tan.), los tratamientos con los análogos de brasinoesteroides se ven favorecidos con una mayor inducción del desarrollo de los callos con estructuras embriogénicas de mejor calidad y mayor velocidad en su formación y crecimiento.
Resultados similares se encontraron en la callogénesis en papa (Solanum tuberosum L.) y arroz (Oryza sativa L.) (19, 20), donde se observó un efecto favorable en el crecimiento, desarrollo y la calidad de los callos, al utilizar el MH-5 a las mismas concentraciones que las utilizadas en esta investigación. Este resultado puede ser explicado a partir del hecho de que las estructuras químicas de estos dos análogos son muy similares, presentan un anillo espirocetálico que hace que su reconocimiento por el receptor de membrana sea más lento (21, 22) y de ahí que su acción se prolongue más en el tiempo, quedando bien establecida la relación estructura química y actividad biológica en los brasinoesteroides (23, 24).

En cuanto al incremento en la masa fresca producida por el Pectimorf® 10 mg.L-1 (0.12 g) sin EM (tratamiento 18), se considera bueno, si se tiene en cuenta que aumentó en 1,6 veces su peso inicial. Este resultado coincide con lo informado por Cevallos (12) en el cultivo del café (Coffea canephora var. Robusta), quien logró respuestas positivas al analizar esta variable a los 30 días del cultivo, con este mismo biorregulador y a la misma concentración.
Conclusiones
Se logró el establecimiento de una línea celular embriogénica a partir del cultivo de óvulos fecundados de mandarina Cleopatra (Citrus reshni Hort. ex Tan.).El Pectimorf® 10 mg.L-1 resultó el mejor tratamiento para la obtención de embriones somáticos de mandarina Cleopatra. Los biorreguladores Biobras-6 y MH-5 (10-3 mg.L-1) son efectivos en el incremento de la masa fresca del callo con estructuras embriogénicas.
REFERENCIAS
- Valle, N. Del. Conferencia magistral. Evento de Fruticultura. La Habana. 2007.
- Olivares, O. Hibridación somática de cítricos. Tesis en opción al grado de Doctor en Ciencias Biológicas. Universidad Politécnica Valencia. España. 1998, 202 p.
- González, O. P. Establecimiento de una metodología de micropropagación mediante la embriogénesis somática en el cultivo del boniato (Ipomoea batatas (L.) Lam.). Tesis presentada en opción al grado científico de Doctor en Ciencias Agrícolas. Instituto Nacional de ciencias Agrícolas. 2006, 93 p.
- Acosta, A. Estudio del efecto de dos oligosacarinas sintéticas sobre el cultivo del tabaco (Nicotiana tabacum L.). Tesis en opción al título de Master en Biología Vegetal. Facultad de Biología. Universidad de La Habana. 2006, 75 p.
- Castilla, Y. Micropropagación del clavel español (Dianthus caryophyllus L.). Tesis de Maestría. Facultad de Biología. Universidad de La Habana. 2008, 61 p.
- Diosdado, E. Efecto de biorreguladores sobre el proceso de embriogénesis somática y el cultivo y fusión de protoplastos de naranjo agrio (Citrus auriantum L.). Tesis presentada en opción al grado científico de Doctor en Ciencias Biológicas. Facultad de Biología, Universidad de La Habana. 1997, 120 p.
- Murashige, T. y Skoog, F. A revised medium for rapid growth and bioassay with tobacco tissue culture. Plant Physiol., 1962, p. 473-479.
- Sigarroa, A. Biometría y diseño experimental. La Habana: Ed. Pueblo y Educación. 1985, 793 p.
- Bao, L. Efecto del Pectimorf y diferentes brasinosteroides en la embriogénesis somática de Citrus macrophylla Wester. de Biología, Universidad de La Habana. 2009, 57 p.
- Orbović, V; Calović, M.; Vitoria, Z; Nielsen, B; Gmitter, F. G. Jr., Castle, W. S. Analysis of genetic variability in various tissue culture-derived limon plant populations using RAPD and flow citometry. Euphytica, 2008, vol. 161, p. 329-335.
- Ramkrishna, N. K. y Sanjay, K. S. In vitro adventitive embryony in Citrus: A technique for citrus germplasm exchange. Current Science, 2005, vol. 88, no. 8, p. 1309-1311.
- Cevallos, A. Establecimiento de una metodología eficiente en el proceso de embriogénesis somática en el cultivo de cafeto (Coffea spp.) mediante el uso de marcadores morfohistológicos y moleculares. Tesis de Doctorado. La Habana. INCA. 2000, 121 p.
- Dolce, N. R., Faloci, M. M., Medina, R. D, Scocchi, A. M., Mroginski, L. A. Análisis de la estabilidad genética en plantas de Citrus sinensis L. y C. limon L. regeneradas in vitro. Universidad Nacional del Nordeste. Laboratorio de Cultivo de Tejidos. IBONE–CC209. Facultad de Ciencias Agrarias. UNNE. Argentina. 2005, 4 p.
- Nieves, N; Poblete, A; Cid, N; Lezcano, Y; González-Olmedo, J. L.; Cabrera, J. C. Evaluación del Pectimorf como complemento del 2,4-D en el proceso de la embriogénesis somática de la caña de azúcar (Saccharum spp.). Cultivos Tropicales. 2006, vol. 27, no. 1, p. 25-30.
- Falcón, R. y Cabrera, J. C. Actividad enraizadora de una mezcla de oligogalacturónidos en pecíolos de violeta africana (Saintpaulia ionantha). Cultivos Tropicales, 2007, vol. 28, no. 2, p. 87-90.
- Shawkat, A. y Bushra, M. Micropropagation of rough lemon (Citrus jambhiri Lush.): Effect of explants type and hormone concentration. Acta Bot. Croat., 2006, vol. 65, no. 2, p. 137–146.
- Pinzón, F. E. Influencia del oligopectato Pectimorf y el análogo de brasinosteroides Biobras-6 en la propagación in vitro del clon de banano FHIA-18 (Musa sp. AAAB). Trabajo de Diploma (en opción al título de Ingeniero Agrónomo). Universidad Agraria de La Habana. Cuba. 2004, 72 p.
- González, J. U.; Valerio, R.; Vargas, T. E. y García, E. de. Aspectos morfoanatómicos de callos originados durante el proceso de embriogénesis somática en banano Williams subgrupo Cavendish (Musa sp. grupo AAA). Agronomía Tropical, 2006, vol. 56, no. 4, p. 697-703.
- Moré, O.; Hernández, M.; Núñez, M.; Estévez, A. y González, M. E. Empleo de dos análogos de brasinosteroides en la formación de callos embriogénicos de papa (Solanum tuberosum L.). Cultivos Tropicales, 2001, vol. 22, no. 4, p. 29-35.
- García, A.; Rodríguez, T.; Héctor, E.; Núñez, M. Efecto del análogo de brasinoesteroide MH-5 en el crecimiento in vitro del arroz (Oryza sativa L.) en condiciones de déficit hídrico. Cult. Trop., 2005, vol. 26, no. 1, p. 89-93.
- Núñez, M.; Robaina, C. y Col, F. Synthesis and practical applications of brassinosteroid analogs. En: Hayat S., Ahmad A. Brassinosteroids. Bioactivity and Crop Productivity. Kluwer Academic Publishers. The Netherlands. 2005, p. 87-117.
- Mazorra, L. M. Los brasinoesteroides y su relación con la tolerancia de plántulas de tomate (Solanum lycopersicum L.) ante el choque por temperatura alta. Tesis de Doctorado. 2008, 100 p.
- Li, J. y Jin, H. Regulation of brassinosteroid signaling. Trends Plant Sci., 2007, vol. 12, no. 1, p. 37-41.
- Medina, R. D., Faloci, M. M., Solis Neffa, V., Mroginski, L. A. Embriogénesis somática y regeneración de plantas de Mandioca Manihot esculenta Crantzcultivares de interés para Argentina. RIA, 2003, vol. 32, no. 3, p. 143-160.
Recibido: 18 de noviembre de 2009
Apreobado: 4 de junio de 2010