INTRODUCCIÓN
La calidad del agua para riego está determinada por la cantidad y el tipo de sales que la constituyen, siendo los principales parámetros establecidos para medir la aptitud agrícola de un agua, la relación de adsorción de sodio (SAR) y la conductividad eléctrica (CE), esto se debe a que el riesgo más importante relacionado con el riego está en crear suelos salinos 1.
No obstante, la calidad del agua para riego, si esta proviene de sitios cercanos a fuentes contaminantes, no debe ser determinada solamente teniendo en cuenta los parámetros antes mencionados. Cada vez más a las aguas, tanto superficiales como subterráneas, arriban contaminantes químicos (ya sea orgánicos o inorgánicos), que son puestos a disposición de las plantas y que pueden provocar su acumulación en éstas, con la consecuente magnificación a lo largo de las cadenas tróficas 2. El hombre como último eslabón de la mayoría de las cadenas alimentarias se ve involucrado en este ciclo, observándose afectaciones inmunológicas, embriológicas, neurológicas y sistémicas 3. Estas aguas pueden verse afectadas también por contaminantes biológicos que, al igual que los químicos, pueden afectar la cadena trófica, provocando graves enfermedades. Estos contaminantes pueden ser: helmintos, protozoos, bacterias y virus 4.
En Cuba el monitoreo de la calidad de las aguas superficiales y subterráneas se realiza a partir de la red de calidad de agua (RedCal), perteneciente al Instituto de Recursos Hidráulicos, utilizando como instrumento para la integración de los resultados analíticos el Índice de Calidad de las Aguas Superficiales (ICAsup). Dentro de los indicadores que lo componen están: pH (acidez o basicidad), conductividad eléctrica (CE: contenido de sales solubles), oxígeno disuelto (ODSAT: estado del cuerpo de agua con respecto a su contenido de oxígeno disuelto), demanda química de oxígeno por el método del dicromato (DQO: materia orgánica presente) y coliformes fecales (densidad de bacterias fecales) 5. Otros países poseen su propio índice teniendo en cuenta además el contenido de N-NH4, N-NO3 y PO46,7.
Desde el punto de vista regulatorio, Cuba cuenta con normas para la determinación de la calidad de agua potable 8 y regula los vertimientos a cuerpos de aguas terrestres y el alcantarillado 9. Sin embargo, la evaluación de contaminantes metálicos inorgánicos no se realiza de forma programada y extendida en el país, sino a nivel de proyectos de investigación que financian los estudios de una determinada área de interés.
La subcuenca Mampostón, objeto del presente estudio, cubre un área de 157,8 km2. Se encuentra fuertemente antropizada, pues recibe el vertimiento directo de siete industrias, numerosas granjas agropecuarias, poblados y carreteras. El agua superficial es utilizada desde el punto de vista agrícola para el riego de hortalizas (1 026,63 ha) y en el cultivo del arroz (Oryza sativa L.), con una extensión de 67,60 ha, según datos del Ministerio de la Agricultura 10. Existe, además, una gran extensión cultivada con pastos y cultivos forestales que no recibe riego directo 11. Por lo anteriormente expuesto el presente trabajo tuvo como objetivo evaluar la calidad químico-física y microbiológica del agua superficial de la subcuenca Mampostón para su uso en el riego agrícola.
MATERIALES Y MÉTODOS
Descripción del área de estudio
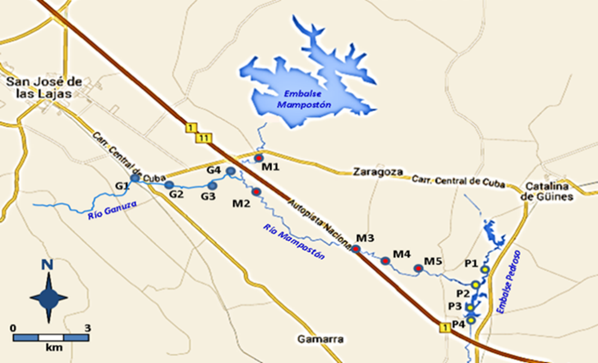
La subcuenca Mampostón es de origen cársico y su extensión abarca los territorios comprendidos al Norte por la presa Mampostón, al Este por la derivadora Pedroso, al Oeste por las lomas Cueto-Ganuza y al Sur por las lomas de Güines (Figura 1).
Los muestreos se realizaron aguas arriba y aguas abajo de los siete focos contaminantes directos (Tabla 1) reportados por el Instituto Nacional de Recursos Hidráulicos 11, con 100 m de separación entre ellos para un total de 16 estaciones de muestreo: cuatro sobre el afluente Ganuza (G1-G4), cinco en el afluente Mampostón (M1-M5), tres en la derivadora Pedroso (P1-P3), uno en la salida del agua hacia Güines (P4) y tres en la presa Mampostón (PM1-PM3). Los muestreos se realizaron al finalizar las dos épocas del año diferenciadas por el clima en Cuba (época lluvia y época poca lluvia).
Tabla 1 Empresas relacionadas con la carga contaminante del sitio en estudio
| Foco contaminante | Estaciones de muestreo | Coordenadas | Residual | Categoría |
|---|---|---|---|---|
| Pasteurizadora “Aljibe” | G1-G2 | N 22º 55´ 47.59” O 82º 7´ 4.02” | Orgánico: Desechos Lácteos | III |
| Fábrica de Ron “San José” | G2-G3 | N 22º 55´ 48.8” O 82º 6´ 58.06” | Orgánico: vinaza entre otros | V |
| Fábrica de Pintura "Raúl Cepero Bonilla" | G3-G4 | N 22º 55´ 40.77” O 82º 5´ 45.5” | Inorgánico: químicos complejos | I |
| CEPAM | antes de M1 | N 22º 56´ 14.71” O 82º 5´ 26.77” | Orgánicos: desechos del proceso de cría de alevines | III |
| Fábrica de Aluminio | M1-M2 | N 22º 56´ 27.11” O 82º 4´ 39.45” | Inorgánico: desechos sólidos | V |
| Planta de Asfalto | M2-M3 | N 22º 55´ 49.95” O 82º 5´ 0.20” | Inorgánico y orgánico: residuos sólidos y gaseosos | V |
| Instituto de Ciencia Animal | M4-M5 | N 22º 54´ 8.44” O 82º 2´ 19.18” | Orgánico: Albañales y desechos de cría animal | III |
Evaluación de parámetros químico-físicos
En las 16 estaciones de muestreo se tomaron muestras de agua colectadas en recipientes plásticos inertes de cinco litros de capacidad. Las muestras se tomaron manualmente a un metro de la superficie, siempre en la zona media del río. En los embalses se utilizó un bote de remo para la colecta.
La preparación de las muestras para los análisis se realizó en Cuba (laboratorios de química de la Universidad Agraria de La Habana) y en Francia (laboratorios Ecolab, Toulouse), La filtración para las determinaciones de metales pesados (MP) se realizó acorde con la metodología de Casanueva y colaboradores 12. Las muestras para determinaciones orgánicas (COD y análisis multielemental) se filtraron con un filtro de fibra de vidrio GMA de 70 µm previamente lavado con HCl 1 N.
pH y CE
Ambos indicadores se midieron en los laboratorios de química de la UNAH, mediante el método potenciométrico utilizando un pHmetro modelo PHSJ-3F con una sensibilidad de 0,001.
Aniones mayoritarios
Los aniones (Cl-, NO3 -, SO4 2-, HCO3 -) se determinaron, en los laboratorios de química de la UNAH, utilizando procedimientos volumétricos establecidos por la RedCal en su monitoreo de la calidad del agua 13.
Composición orgánica de las fases disuelta y particular transportada en suspensión
Ambos parámetros se determinaron en los laboratorios EcoLab (Toulouse, Francia). La oxidación catalítica se realizó a 680 oC en un equipo TOC-5000 Shimadzu. El CO2 resultante se cuantificó por detección infrarroja y comparación con una curva patrón a 0, 2, 5 y 10 ppm de diftalato de potasio 14. La lectura se realizó en un equipo NA 2100 Protein de ThermoFisher mediante combustión a 1800 oC y posterior separación de la mezcla de gases por cromatografía en fase gaseosa. Para la cuantificación se compararon los resultados con una curva patrón de ácido aspártico con 36,09 % de C, 5,30 % de H, 12,52 % de N y 0 % de S.
A partir de los resultados de la fase particular (COP y NOP) se estimó la relación C/N con la finalidad de establecer el origen de la materia orgánica.
DBO5 y DQO
Ambos parámetros se determinaron, utilizando procedimientos establecidos por la RedCal en su monitoreo de la calidad del agua 13. A partir de sus resultados se calculó la relación DBO5/DQO con vistas a determinar la degradabilidad de la materia orgánica presente 15.
Composición de cationes mayoritarios y metales pesados en la fase disuelta
Ambos procedimientos se llevaron a cabo en los laboratorios EcoLab (Toulouse, Francia). No se realizó ningún tratamiento de concentración, la medición se realizó directamente utilizando un equipo ICPMS. Para la validación de los resultados se utilizó el material de referencia internacionalmente certificado SLRS-5 16, que es un indicador externo de la calidad de la manipulación. En las determinaciones de ICPMS se dopó cada muestra con una concentración conocida de 115In/187Re (2,032 µg L-1) como estándar interno, con el objetivo de corregir cualquier desviación en el análisis, siguiendo las fórmulas:
donde:
δIn/Re: identifica la relación entre la concentración dopada y la lectura del equipo
C(In): representa la concentración de In
C(Re): representa la concentración de Re
Cx: rectificada indica el factor de corrección para los metales evaluados
Además, se utilizaron controles de calidad (HNO3 0,37N, STD-2B en diluciones 100, 50, 25 y 5 %, EPOND-1 y SLRS-5) cada ocho muestras, para calcular el ruido de fondo del equipo y determinar la pérdida de sensibilidad en el tiempo. En todos los casos esta fue corregida a partir de la corrección del estándar interno.
Determinación de parámetros microbiológicos
Las determinaciones se realizaron en los laboratorios de microbiología de la UNAH. El conteo de microorganismos se realizó a partir de las muestras de agua tomadas en las estaciones de monitoreo Aljibe (G2), ICA (M5) y Violento (M3), las dos primeras por recibir una carga contaminante orgánica importante (derivados lácteos y desechos animales) y la última por estar ubicada entre ellas, como forma de control del proceso de depuración del propio río.
Para el aislamiento de microorganismos totales se utilizó la técnica de diluciones cuantitativas y siembra en placa Petri 17, con un orden de dilución de hasta 109 para bacterias. El aislamiento se realizó en medio de cultivo Agar Nutriente con incubación por 72 h. La identificación morfofisiológica se realizó según la técnica descrita por Bergey 18. Para el conteo de microorganismos coliformes fecales se utilizó el método del número más probable NMP 19 y la norma cubana que determina la calidad microbiológica del agua 20.
Análisis Estadísticos
Las diferencias espacio-temporales en la composición del pH, CE, elementos mayoritarios y la composición orgánica se determinó a partir de un análisis de varianza multivariado de clasificación doble (ANOVA bifactorial), con el objetivo de conocer si existía variabilidad por la interacción de ambos factores (Estaciones de muestreo y Época de muestreo) o sólo por sus efectos principales (factores por separado). A los parámetros con diferencias significativas se les realizó posteriormente la dócima de Duncan (p<0,05).
El contenido de metales pesados y de coliformes fecales se comparó con la norma cubana para agua potable 8 y con la norma de la OMS para agua de riego 4.
RESULTADOS Y DISCUSIÓN
El análisis de varianza bifactorial para la determinación de las diferencias espacio-temporales en la composición del agua superficial de la subcuenca Mampostón mostró que, para el caso de la interacción entre los factores propuestos (Estaciones de muestreo y Época de muestreo), no existen diferencias estadísticamente significativas en ninguno de los parámetros analizados (Tabla 2), por lo que se valoraron los efectos principales por separado.
Tabla 2 Análisis multivariado de clasificación doble para el caso de la interacción de los factores evaluados
| Factores | Parámetros | Suma de cuadrados tipo II | Media cuadrática | F | p | |
|---|---|---|---|---|---|---|
| Efectos de la Interacción entre Estaciones de muestreo y Época de muestreo. | pH | 2,10 | 0,14 | 0,303 | 0,992 ns | |
| CE | 359871,93 | 23991,46 | 0,648 | 0,813 ns | ||
| Materia Orgánica | COD | 232,29 | 15,48 | 0,847 | 0,623 ns | |
| COP | 25367,33 | 1691,15 | 0,662 | 0,800 ns | ||
| NOP | 465,79 | 31,05 | 1,069 | 0,420 ns | ||
| DQO | 116823,25 | 7788,21 | 0,586 | 0,864 ns | ||
| DBO5 | 142312,85 | 9487,52 | 1,845 | 0,072 ns | ||
| Aniones mayoritarios | HCO3 - | 37123,23 | 2141,54 | 1,010 | 0,761 ns | |
| SO4 2- | 613,93 | 40,92 | 0,599 | 0,853 ns | ||
| Cl- | 3160,00 | 210,66 | 1,719 | 0,097 ns | ||
| NO3 - | 27,10 | 1,80 | 0,783 | 0,686 ns | ||
| Cationes mayorita-rios | Na+ | 277,37 | 18,49 | 0,538 | 0,898 ns | |
| K+ | 275,94 | 18,39 | 1,271 | 0,275 ns | ||
| Mg2+ | 66,61 | 4,44 | 0,652 | 0,809 ns | ||
| Ca2+ | 5190,22 | 346,01 | 0,916 | 0,556 ns | ||
| Metales pesados | Cr total | 1497,88 | 99,85 | 0,872 | 0,599 ns | |
| Cu2+ | 1191,08 | 79,40 | 0,897 | 0,574 ns | ||
| Zn2+ | 466301,98 | 31086,79 | 0,950 | 0,524 ns | ||
| As total | 0,96 | 0,06 | 0,702 | 0,763 ns | ||
| Pb2+ | 51003,2 | 3400,21 | 0,923 | 0,550 ns | ||
F-F de Fisher; p-probabilidad; ns-no existen diferencias estadísticamente significativas
Diferencias espaciales en la composición físico-química de las aguas superficiales de la subcuenca Mampostón
pH y CE
El pH de las aguas superficiales de la subcuenca Mampostón presentó poca variabilidad espacial (Tabla 3), lo que está en consonancia con el poderoso efecto tampón que producen los iones HCO3 - y Ca2+ al ser disueltos 21. La media general fue de 7,26, pero sin diferencias significativas entre las estaciones de monitoreo para p>0,05.
Las determinaciones de CE fueron superiores a los 318 µS cm-3, lo que indicó que no existen problemas de permeabilidad del agua en el suelo de acuerdo a lo señalado anteriormente 22.
Tabla 3 Determinación de las diferencias espaciales para los parámetros pH y CE
| Parámetro | Hidrosistema | N | ẋ | DE (ẋ) | F | p |
|---|---|---|---|---|---|---|
| pH | Río Ganuza | 16 | 6,79 | 0,53 | 1,15 | 0,33 ns |
| Río Mampostón | 16 | 6,81 | 0,44 | |||
| Derivadora Pedroso | 16 | 7,29 | 0,82 | |||
| Presa Mampostón | 16 | 7,38 | 0,64 | |||
| CE | Río Ganuza | 16 | 696,18 a | 272,9 | 9,60 | 0,000* |
| Río Mampostón | 16 | 496,40 b | 89,68 | |||
| Derivadora Pedroso | 16 | 441,30 b | 60,02 | |||
| Presa Mampostón | 26 | 330,61 c | 20,04 |
N- número de muestras; ẋ- media aritmética; DE (ẋ)- Desviación estándar de la media; F- F de Fisher; p- probabilidad; ns- no existen diferencias estadísticamente significativas; letras diferentes en la misma columna indican diferencias significativas según Duncan para p<0,05
Espacialmente existen diferencias estadísticamente significativas en la CE de los diferentes hidrosistemas evaluados (ríos y presas), teniendo una mayor concentración de sales disueltas el río Ganuza y una menor concentración la presa Mampostón. Sin embargo, al desglosar en el gráfico de barras (Figura 2), las diferentes estaciones de muestreo, puede observarse claramente cómo estas diferencias están relacionadas con el aporte antrópico en las estaciones G2 y G3 sobre el río Ganuza y M5 sobre el río Mampostón.
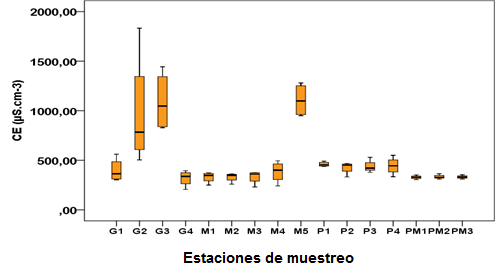 Las cajas representan los valores del 25-75 % de la muestraLa media es representada como una línea negra horizontal. Las barras verticales representan el error estándar de la media (N=64)
Las cajas representan los valores del 25-75 % de la muestraLa media es representada como una línea negra horizontal. Las barras verticales representan el error estándar de la media (N=64)Figura 2 Conductividad eléctrica de la fase disuelta
El uso del agua de estas tres estaciones de muestreo para el riego, implica riesgo de salinización del suelo, ya que los valores observados son superiores a la norma FAO 23). La CE está influenciada, tanto por la conductividad eléctrica específica (CEi) de los iones disueltos en agua, como por los aportes de materia orgánica (MO) provenientes del medio que pueden disociarse (como ácidos débiles), liberando iones hidronio con elevada CEi. Al respecto se informó que, mientras mayor cantidad de ambos exista, mayor será la CE de un agua en un sitio determinado 21,24.
Elementos mayoritarios (aniones y cationes)
El Ca2+ fue el catión predominante (Tabla 4), el que al parecer su aporte es antrópico, en forma orgánica (G2), a partir del proceso de producción de yogurt de soya, lo que puede inducir la precipitación de metales tóxicos 24. El resto de las diferencias espaciales que se constataron son provocadas por diferentes procesos geopedológicos locales 25 y coincide con informes realizados en esta misma área en la década anterior 26. Los cationes Na+ y K+, presentaron mayores concentraciones en las estaciones G1, G2 y G3, indicando aportes antrópicos como parte del vertimiento de residuales de las fábricas de productos lácteos y de ron. Los procesos productivos que se realizan en estas empresas introducen concentraciones elevadas de sales, principalmente NaCl, NaHCO3, Mg (NO3)2 y KNO3.
El agua superficial que corre por los ríos Ganuza y Mampostón, así como, la que se embalsa en la derivadora Pedroso y la presa Mampostón presentaron elevados contenidos de HCO3 - disuelto, en una composición variable, espacialmente de acuerdo con la geología del área (Tabla 5), lo que coincide con los resultados obtenidos anteriormente 26.
Las diferencias espaciales en las concentraciones de Cl- y NO3 -, se relacionan con los procesos productivos anteriormente referidos (empresas cuyo vertimiento se realiza en las aguas del afluente Ganuza), incluyéndose para el primer anión el vertimiento de residuales proveniente del Instituto de Ciencia Animal (M5).
La clasificación de las aguas superficiales que circulan por la cuenca se consideran como bicarbonatadas, sulfatadas cálcico sódicas (HCO3 ->Ca2+=SO4 2->Na+), correspondiendo a la constitución litológica del área. Al respecto otros autores señalan que la disolución de la calcita produce aguas con una relación Ca/Mg entre 4-50 mmol L -1 (26) , siendo en el presente estudio entre 8,38-21,55 mmol L-1.
Composición orgánica de las fases disuelta y particular transportada en suspensión
La evaluación del contenido de carbono orgánico disuelto (COD) mostró que existieron diferencias espaciales estadísticamente significativas entre la estación de monitoreo G3 y el resto. Las estaciones con mayor concentración de carbono orgánico particular (COP) fueron G2 y G3, el resto poseen valores inferiores de COP. Por lo que se consideró que se observó una amplia variabilidad en las determinaciones de carbono (Tabla 4).
La relación entre el C y el N que se transporta en la materia en suspensión se mostraron a través de la relación C/N. Los valores de C/N entre 2,6 y 8,0 indicaron predominio de materia orgánica de carácter autóctono, ya sea por la fotosíntesis o quimiosíntesis bacteriana o por la presencia de fitoplancton fluvial 27,28. Siguiendo el criterio anteriormente referido, las estaciones de monitoreo donde predomina la materia orgánica autóctona son G2 y G3. Esto podría deberse a que los residuales de la fábrica de yogurt y de ron son fácilmente degradables y originan un intenso crecimiento microbiano en la superficie del agua, observable a simple vista por la formación de una película de floculación 29.
Tabla 4 Variación espacial de los cationes mayoritarios y metales pesados en aguas superficiales de la subcuenca Mampostón
| Cationes (estadísticos) | Río Ganuza | Río Mampostón | Derivadora Pedroso | Presa Mampostón | F | p | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| G1 | G2 | G3 | G4 | M1 | M2 | M3 | M4 | M5 | P1 | P2 | P3 | P4 | PM1 | PM2 | PM3 | ||||
| Elementos mayoritarios | (mg L-1) | ||||||||||||||||||
| Ca2+ | ẋ | 60,9bc | 119,3a | 78,3b | 43,8cd | 47,7cd | 41,3cd | 39,0d | 71,9bc | 57,9bc | 73,2bc | 64,8bc | 57,9bc | 52,2bc | 38,8d | 38,0d | 38,8d | 4,5 | 0,000* |
| DE (ẋ) | 16,7 | 32,4 | 31,1 | 6,7 | 19,7 | 10,6 | 21,2 | 29,2 | 25,9 | 15,8 | 23,3 | 7,6 | 19,0 | 8,7 | 9,4 | 9,2 | |||
| Mg2+ | ẋ | 4,2 | 5,6 | 7,2 | 4,2 | 4,2 | 4,4 | 4,1 | 5,4 | 3,9 | 5,9 | 5,8 | 5,8 | 6,2 | 4,6 | 4,6 | 4,7 | 0,6 | 0,8 ns |
| DE (ẋ) | 1,0 | 1,3 | 0,8 | 0,5 | 0,8 | 0,7 | 1,2 | 3,3 | 0,4 | 4,6 | 3,9 | 4,1 | 4,6 | 0,4 | 0,5 | 0,8 | |||
| Na+ | ẋ | 10,7b | 63,3a | 59,7a | 11,4b | 13,1b | 13,6b | 12,9b | 15,7b | 10,8b | 13,0b | 12,9b | 12,3b | 11,7,b | 14,6b | 14,8b | 15,2b | 37,9 | 0,000* |
| DE (ẋ) | 5,6 | 10,7 | 4,8 | 7,0 | 2,3 | 2,8 | 4,2 | 10,4 | 2,6 | 4,4 | 3,3 | 2,3 | 3,6 | 2,9 | 3,8 | 4,5 | |||
| K+ | ẋ | 5,8bc | 9,9b | 22,0a | 4,4bc | 4,1bc | 4,6bc | 4,5bc | 5,3bc | 4,9bc | 2,7c | 3,2bc | 2,3c | 2,3c | 4,6bc | 4,4bc | 4,4bc | 5,5 | 0,000* |
| DE (ẋ) | 3,6 | 3,8 | 14,3 | 1,0 | 1,5 | 0,9 | 0,5 | 3,3 | 1,9 | 0,9 | 0,8 | 0,5 | 0,6 | 0,6 | 0,4 | 0,5 | |||
| Metales Pesados | (µg L-1) | - | |||||||||||||||||
| Cr total | ẋ | 7,4 | 23,6 | 19,3 | 8,4 | 9,3 | 6,3 | 8,0 | 13,4 | 8,0 | 7,1 | 10,0 | 8,0 | 7,0 | 16,2 | 8,9 | 4,9 | 0,4 | 0,9 ns |
| DE (ẋ) | 5,2 | 16,5 | 11,1 | 3,1 | 5,9 | 3,8 | 1,2 | 9,4 | 3,5 | 2,6 | 5,7 | 4,5 | 4,7 | 9,7 | 4,0 | 1,7 | |||
| Cu2+ | ẋ | 3,4 | 4,8 | 9,1 | 5,0 | 10,3 | 4,6 | 4,8 | 24,3 | 2,6 | 4,0 | 2,8 | 3,2 | 2,4 | 4,1 | 3,7 | 2,6 | 0,9 | 0,5 ns |
| DE (ẋ) | 2,5 | 2,2 | 5,7 | 1,4 | 5,2 | 2,7 | 2,7 | 19,7 | 1,7 | 1,4 | 1,4 | 2,3 | 1,6 | 2,5 | 1,2 | 1,5 | |||
| Zn2+ | ẋ | 25,8 b | 78,8 b | 277,4 a | 32,2 b | 329,7a | 30,3 b | 26,8 b | 33,7 b | 41,0 b | 53,4 b | 264,3 a | 36,0 b | 23,3 b | 40,4 b | 33,5 b | 36,1 b | 30,9 | 0,000* |
| DE (ẋ) | 13,9 | 36,1 | 143,4 | 12,7 | 173,7 | 18,5 | 16,1 | 17,3 | 22,7 | 22,4 | 138,2 | 22,0 | 11,7 | 12,2 | 7,1 | 15,4 | |||
| As total | ẋ | 0,7 | 0,4 | 0,7 | 0,5 | 0,5 | 0,7 | 0,5 | 0,9 | 0,5 | 0,5 | 0,5 | 0,4 | 0,5 | 0,7 | 0,7 | 0,7 | 1,0 | 0,4 ns |
| DE (ẋ) | 0,2 | 0,2 | 0,1 | 0,3 | 0,2 | 0,1 | 0,1 | 0,4 | 0,1 | 0,2 | 0,1 | 0,1 | 0,2 | 0,2 | 0,1 | 0,1 | |||
| Pb2+ | ẋ | 27,2 b | 97,2 a | 12,8 c | 38,6 b | 4,6 c | 20,5 b | 87,9 a | 5,4 c | 3,6 c | 85,5 a | 10,0 c | 6,8 c | 2,0 c | 2,8 c | 2,4 c | 2,4 c | 35,4 | 0,000* |
| DE (ẋ) | 15,3 | 64,4 | 8,4 | 20,1 | 3,8 | 10,9 | 32,9 | 2,5 | 1,9 | 33,2 | 1,1 | 4,0 | 0,6 | 1,1 | 0,9 | 0,5 | |||
ẋ- media aritmética; DE (ẋ)- Desviación estándar de la media; F- F de Fisher; p- probabilidad; ns- diferencias no significativas para la misma fila y letras diferentes en la misma fila- diferencias estadísticamente significativas según Duncan para p<0,05
Tabla 5 Variación espacial de los aniones mayoritarios en las aguas superficiales de la subcuenca Mampostón
| Aniones mayoritarios (estadísticos) | Río Ganuza | Río Mampostón | Derivadora Pedroso | Presa Mampostón | F | p | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| G1 | G2 | G3 | G4 | M1 | M2 | M3 | M4 | M5 | P1 | P2 | P3 | P4 | PM1 | PM2 | PM3 | ||||
| (mg L-1) | |||||||||||||||||||
| HCO3 - | ẋ | 343,5b | 364,0 b | 305,7 b | 280,7 bc | 199,7cd | 186,7 cd | 288,7 bc | 351,0b | 523,2 a | 262,0 bc | 275,2 bc | 232,5 bc | 289,7 bc | 135,0 d | 133,2 d | 140,0 d | 14,0 | 0,000* |
| DE (ẋ) | 67,3 | 140,1 | 9,9 | 23,7 | 25,2 | 61,7 | 65,1 | 16,4 | 42,3 | 43,1 | 61,9 | 51,0 | 49,2 | 12,9 | 14,1 | 12,1 | |||
| Cl- | ẋ | 25,7b | 54,7a | 21,5c | 23,7c | 22,2c | 17,7cd | 22,7c | 22,7c | 44,0a | 23,2c | 18,7cd | 20,0c | 26,0b | 14,2cd | 14,7cd | 15,2cd | 3,0 | 0,02 ns |
| DE (ẋ) | 2,7 | 14,5 | 2,3 | 3,8 | 3,1 | 4,1 | 3,28 | 2,6 | 14,1 | 3,7 | 2,5 | 4,0 | 2,9 | 0,9 | 0,5 | 0,9 | |||
| NO3 - | ẋ | 2,4b | 2,4b | 15,0a | 1,4b | 0,8b | 1,1b | 1,1b | 4,1b | 0,8b | 2,0b | 0,9b | 1,9b | 0,8b | 0,8b | 0,8b | 0,8b | 22,4 | 0,000* |
| DE (ẋ) | 2,0 | 2,1 | 2,4 | 0,6 | 0,1 | 0,5 | 0,5 | 2,8 | 0,1 | 0,1 | 0,1 | 1,5 | 0,1 | 0,1 | 0,2 | 0,1 | |||
| SO4 2- | ẋ | 20,5 | 20,7 | 16,7 | 20,7 | 20,7 | 13,5 | 22,2 | 16,2 | 41,0 | 16,2 | 16,5 | 19,2 | 20,0 | 20,2 | 20,0 | 20,2 | 2,1 | 0,2ns |
| DE (ẋ) | 1,7 | 7,4 | 2,8 | 9,5 | 7,1 | 2,3 | 6,2 | 3,2 | 22,4 | 4,6 | 5,9 | 13,3 | 6,8 | 0,9 | 0,8 | 1,2 | |||
ẋ- media; DE (ẋ)- Desviación estándar de la media; F- F de Fisher; p- probabilidad; ns- diferencias no significativas y letras diferentes en la misma fila- diferencias estadísticamente significativas según Duncan para p<0,05)
Tabla 6 Variación espacial de la composición orgánica en las aguas superficiales de la subcuenca Mampostón
| Parámetros | Río Ganuza | Río Mampostón | Derivadora Pedroso | Presa Mampostón | F | p | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| G1 | G2 | G3 | G4 | M1 | M2 | M3 | M4 | M5 | P1 | P2 | P3 | P4 | PM1 | PM2 | PM3 | ||||
| (mg L-1) | |||||||||||||||||||
| COD | ẋ | 8,3bc | 7,4bc | 17,1a | 6,7bc | 12,3b | 7,5c | 8,1bc | 5,5c | 5,2c | 5,0c | 4,6c | 6,7bc | 6,0bc | 8,7bc | 9,3bc | 6,7bc | 2,9 | 0,020 ns |
| DE (ẋ) | 3,8 | 4,4 | 2,9 | 2,3 | 3,3 | 3,6 | 3,3 | 1,8 | 1,3 | 1,9 | 1,9 | 4,4 | 2,6 | 2,8 | 3,4 | 2,5 | |||
| COP | ẋ | 24,2c | 172,1a | 107,4a | 8,1c | 13,7c | 9,8c | 10,1c | 22,0c | 67,7b | 76,1b | 30,0bc | 29,3bc | 28,5bc | 32,0bc | 52,5b | 43,7bc | 3,9 | 0,001* |
| DE (ẋ) | 20,4 | 74,5 | 69,6 | 5,8 | 14,2 | 8,6 | 8,2 | 17,8 | 63,7 | 67,7 | 25,0 | 25,3 | 18,0 | 24,1 | 43,0 | 37,7 | |||
| NOP | ẋ | 2,7c | 21,5a | 13,7b | 0,8c | 1,0c | 0,7c | 0,9c | 1,9c | 7,0c | 7,8c | 2,2c | 2,6c | 2,5c | 2,9c | 3,9c | 2,7c | 4,2 | 0,000* |
| DE (ẋ) | 2,3 | 11,5 | 13,2 | 0,2 | 0,9 | 0,5 | 0,6 | 1,3 | 6,7 | 5,7 | 1,4 | 2,3 | 1,7 | 2,1 | 3,6 | 2,3 | |||
| Relación C/N | 8,9 | 8,0 | 7,2 | 10,1 | 13,7 | 14 | 11,2 | 11,5 | 9,6 | 9,7 | 13,6 | 11,2 | 11,4 | 12,0 | 13,4 | 16,1 | - | - | |
| DBO5 | ẋ | 17,0c | 27,2c | 178,5b | 4,7c | 3,9c | 1,8c | 7,4c | 7,3c | 482,2a | 1,8c | 8,7c | 8,5c | 2,6c | 1,8c | 1,7c | 1,9c | 8,7 | 0,000* |
| DE (ẋ) | 11,8 | 25,1 | 92,1 | 2,0 | 2,2 | 0,9 | 7,1 | 6,4 | 298,1 | 0,4 | 6,3 | 6,5 | 1,0 | 0,6 | 0,8 | 0,4 | |||
| DQO | ẋ | 39,2c | 55,5c | 355,7b | 15,2c | 14,5c | 8,0c | 17,2c | 11,2c | 664,5a | 8,0c | 19,5c | 30,0c | 11,7c | 8,4c | 8,7c | 8,5c | 11,1 | 0,000* |
| DE (ẋ) | 11,0 | 17,1 | 281,7 | 9,3 | 10,4 | 1,2 | 11,6 | 9,3 | 317,8 | 1,8 | 10,3 | 26,4 | 4,7 | 2,4 | 1,9 | 2,0 | |||
| Relación DBO5/DQO | 0,4 | 0,5 | 0,5 | 0,3 | 0,2 | 0,2 | 0,4 | 0,6 | 0,7 | 0,2 | 0,4 | 0,3 | 0,2 | 0,2 | 0,2 | 0,2 | - | - | |
ẋ- media; DE (ẋ)- Desviación estándar de la media; F- F de Fisher; p- probabilidad; ns- diferencias no significativas para la misma fila y letras diferentes en la misma fila- diferencias estadísticamente significativas según Duncan ra p<0,05
Por otra parte, valores de C/N entre 8,1 y 12,0 indicaron un carácter alóctono, proveniente de contaminación por residuales de empresas pecuarias que vierten directamente a la subcuenca Mampostón, por lo que valores superiores a 12,1 se consideran que proviene de suelos fertilizados 25. Las estaciones de muestreo con materia orgánica de origen animal son: G1, G4, M1, M3, M4, M5, P1, P3 y P4; presentaron un origen edáfico de materia orgánica las estaciones de muestreo: M2, P2, PM1, PM2 y PM3 (Tabla 6).
DBO5 y DQO
Desde el punto de vista espacial, la estación con mayor DBO5 y DQO fue la M5, seguida de G3 (Tabla 6). El resto de las estaciones no presentan diferencias significativas para ambos parámetros. Según la Sociedad Americana de Salud Pública 30, el agua potable tiene una DBO5 de 0,75-1,5 mg L-1 de oxígeno y se considera que el agua está contaminada si la DBO5 es mayor de 5,0 mg L-1, los desechos industriales y agrícolas contienen niveles de DBO5 y DQO por encima de la centena.
Por otra parte, la relación DBO5/DQO indicó que la materia orgánica es fácilmente biodegradable en las estaciones G2, G3, M4 y M5 con valores iguales o superiores a 0,5 15. Aspecto que se relaciona estrechamente con el tipo de residual vertido en estos puntos.
Metales pesados
Los valores que se reportan de metales pesados para el estándar internacional SLRS-5 satisficieron las especificaciones de la literatura especializada 20, para la certificación satisfactoria del trabajo de procesamiento de las muestras y el funcionamiento del equipo, ya que todos los valores medidos en el material de referencia oscilaron entre el 80 % y el 120 % del factor de recubrimiento, con respecto a los valores certificados (Tabla 7). Esto indicó que los valores que se reportaron para las muestras de la subcuenca son confiables.
Tabla 7 Validación del trabajo analítico en el procesamiento de muestras para la determinación de metales pesados
| Metal | Estándar Internacional SLRS-5 | ||
|---|---|---|---|
| Concentración medida | Concentración certificada | Factor de Recubrimiento (%) | |
| (µg L-1) | |||
| Cr | 0,36±0,1 | 0,31±0,003 | 115 |
| Cu | 13,8±0,1 | 17,4±1,3 | 80 |
| Zn | 0,8 | 0,8±0,1 | 99 |
| As | 0,46 | 0,41±0,003 | 114 |
| Pb | 0,078 | 0,081±0,006 | 97 |
Entre los metales pesados evaluados sólo mostraron diferencias estadísticas en su distribución espacial el Zn2+ y el Pb2+.
El Zn2+ presentó su mayor concentración en las estaciones G3, M1 y P2 (Tabla 5); sin embargo, en ninguno de los casos sobrepasa la Norma Cubana para agua potable 8 y la Norma de la OMS para agua de riego 4 que fijan el valor máximo de este elemento en 5 000 µg L-1 para una explotación segura, por lo que las concentraciones reportadas no constituyen una limitante para su uso.
En cuanto al contenido medio de Pb, existe una extendida contaminación por este elemento en las aguas superficiales de los afluentes Ganuza y Mampostón y una estación de la derivadora Pedroso. Las estaciones de muestreo con mayores concentraciones son G2, M3 y P1, con diferencias estadísticas, respecto al resto de las estaciones. Un segundo grupo con contenido medio de Pb en solución, está constituido por las estaciones G1, G4 y M2. En todos los casos, presumiblemente, porque el poco caudal de ambos afluentes produce un retroceso de las aguas en algunos puntos y, por tanto, la materia orgánica y los cationes aportados por los vertimientos de las industrias quedan estancados, acumulándose en los sedimentos hasta el comienzo de la época de lluvia 31. Estas seis estaciones de muestreo exceden los niveles permisibles establecidos para agua potable por la regulación cubana 8 y los reglamentos de la OMS para agua de riego 4 fijados en 10 µg L-1.
A pesar del uso de combustibles sin plomo, desde el año 2000 en Cuba, el Pb es un metal de poca movilidad, lo que resulta en su acumulación en suelos de zonas de alto tráfico, debido a la contaminación de décadas anteriores 32. Por lo tanto, el contenido de Pb acumulado en los suelos alrededor de la fábrica de asfalto (estación M2) y la carretera nacional (estación M3) puede haber sido arrastrado por la lluvia, el viento o las actividades humanas, y depositado en estas áreas del río. Otra fuente de este elemento puede estar relacionada con desechos de la fábrica de pintura (G4), punto anterior a la estación M2 y las fugas de aceites usados en las calderas de la pasteurizadora “El Aljibe”, que contamina las estaciones G1 y G2.
Es de notar que la contaminación del agua de la estación P1 (derivadora Pedroso) pudo deberse al vertimiento negligente en sus márgenes de residuos sólidos urbanos y aguas albañales, aspecto notificado a las autoridades pertinentes y corregidas con posterioridad.
Diferencias temporales en la composición físico-química de las aguas superficiales de la subcuenca Mampostón
Existe poca variabilidad estacional en los parámetros físico-químicos evaluados (Tabla 8). Estos resultados indicaron la influencia antrópica sobre la composición de las aguas superficiales en el territorio, ya que las diferencias estacionales propias de la concentración de elementos en época poco lluviosa, se ven eliminadas por los constantes aportes recibidos, a partir de los residuales de las empresas. Además, se informó que este fenómeno también puede deberse al sistema de intercambio bidireccional de agua entre la derivadora Pedroso y la presa Mampostón que puede ocurrir, tanto a través del canal artificial, como a través del río 31. Existen diferencias significativas en el pH, que se incrementa 0,6 unidades en época poco lluviosa, aunque su carácter continúa oscilando alrededor de la neutralidad.
El contenido de SO4 2- disuelto en el agua, es superior en época poco lluviosa (Tabla 8). Las concentraciones de SO4 2- encontradas no se justifican litológicamente y constituyen un aporte antrópico, de acuerdo con lo informado por otros autores 21. El contenido de SO4 2- y Cl- en cuencas cársicas depende de la presencia de yeso (inexistente en esta subcuenca) o rocas salinas, respectivamente, o de procesos producidos por la actividad del hombre y que se encuentran relacionados con la fertilización agrícola, que se incrementa en los meses de octubre-febrero, según reportes de la Delegación de la Agricultura de Mayabeque 33.
Estos resultados indicaron la influencia antrópica sobre la composición de las aguas superficiales en el territorio, ya que las diferencias estacionales propias de la concentración de elementos en época poco lluviosa, se ven eliminadas por los constantes aportes recibidos a partir de los residuales de las empresas. Además, se informó que este fenómeno también puede deberse al sistema de intercambio bidireccional de agua entre la derivadora Pedroso y la presa Mampostón que puede ocurrir, tanto a través del canal artificial, como a través del río 31.
Tabla 8 Determinación de las diferencias temporales de los parámetros evaluados
| Parámetro | Época | ẋ | DE (ẋ) | F | p | |
|---|---|---|---|---|---|---|
| pH | Poca Lluvia | 7,4 a | 0,5 | 8,20 | 0,006* | |
| Lluvia | 6,8 b | 0,5 | ||||
| CE (µS cm-3) | Poca Lluvia | 477,2 | 289,8 | 0,37 | 0,542 ns | |
| Lluvia | 526,0 | 345,0 | ||||
| Aniones mayoritarios | HCO3 - (mg L-1) | Poca lluvia | 279,9 | 122,2 | 0,581 | 0,449 ns |
| Lluvia | 258,9 | 96,3 | ||||
| SO4 2- (mg L-1) | Poca lluvia | 22,6 a | 11,0 | 4,394 | 0,04* | |
| Lluvia | 17,9 b | 6,1 | ||||
| Cl- (mg L-1) | Poca lluvia | 25,7 | 18,4 | 0,642 | 0,426 ns | |
| Lluvia | 22,7 | 10,3 | ||||
| NO3 - (mg L-1) | Poca lluvia | 4,0 | 2,4 | 0,172 | 0,68 ns | |
| Lluvia | 3,2 | 2,0 | ||||
| Cationes mayoritarios | Na+ (mg L-1) | Poca lluvia | 18,6 | 16,9 | 0,066 | 0,798 ns |
| Lluvia | 19,6 | 17,0 | ||||
| K+ (mg L-1) | Poca lluvia | 7,3 | 6,3 | 0,906 | 0,345 ns | |
| Lluvia | 4,9 | 3,6 | ||||
| Mg2+ (mg L-1) | Poca lluvia | 5,3 | 3,0 | 0,706 | 0,404 ns | |
| Lluvia | 4,8 | 1,3 | ||||
| Ca2+ (mg L-1) | Poca lluvia | 52,7 | 23,2 | 2,295 | 0,135 ns | |
| Lluvia | 62,8 | 29,8 | ||||
| Materia orgánica | COD (mg L-1) | Poca lluvia | 9,0 | 5,1 | 3,77 | 0,05 ns |
| Lluvia | 6,7 | 4,0 | ||||
| COP (mg L-1) | Poca lluvia | 53,4 | 35,6 | 1,10 | 0,29 ns | |
| Lluvia | 64,4 | 51,2 | ||||
| NOP (mg L-1) | Poca lluvia | 6,5 | 3,8 | 0,99 | 0,32 ns | |
| Lluvia | 7,8 | 5,3 | ||||
| DBO5 (mg L-1) | Poca lluvia | 179,0 | 60,0 | 0,10 | 0,74 ns | |
| Lluvia | 79,0 | 29,0 | ||||
| DQO (mg L-1) | Poca lluvia | 223,7 | 39,5 | 0,79 | 0,37 ns | |
| Lluvia | 169,0 | 79,6 | ||||
| Metales pesados | Cr total (mg L-1) | Poca lluvia | 9,5 | 4,1 | 0,70 | 0,40 ns |
| Lluvia | 9,9 | 2,1 | ||||
| Cu2+ (mg L-1) | Poca lluvia | 4,3 | 2,4 | 0,98 | 0,32 ns | |
| Lluvia | 6,6 | 3,1 | ||||
| Zn2+ (mg L-1) | Poca lluvia | 97,0 | 54,3 | 0,71 | 0,40 ns | |
| Lluvia | 91,9 | 35,1 | ||||
| As total (mg L-1) | Poca lluvia | 0,6 | 0,2 | 0,31 | 0,57 ns | |
| Lluvia | 0,6 | 0,3 | ||||
| Pb2+ (mg L-1) | Poca lluvia | 28,1 | 9,2 | 0,06 | 0,79 ns | |
| Lluvia | 31,9 | 7,5 | ||||
ẋ- media; DE (ẋ)- Desviación estándar de la media; F- F de Fisher; p- probabilidad; ns- diferencias no significativas; letras diferentes en la misma columna para cada parámetro indican diferencias estadísticamente significativas según Duncan para p<0,05
Contenido de microorganismos totales y coliformes fecales
En cuanto al conteo microbiano total en agua (Tabla 9), así como las concentraciones de coliformes fecales, mostraron que la presencia de coliformes fecales en el agua de la estación Aljibe (G2) no supera los límites permisibles para agua de uso agrícola, por lo que la restricción del uso del agua de esta estación para el riego se debe a su contenido de Na+ y Pb2+ y no a la presencia de patógenos fecales.
El agua en el tramo del río Mampostón, comprendido por la estación de muestreo M5, acorde con este indicador, no debe utilizarse en el riego de cultivos de raíces y hojas, así como para cosechas de tallo largo, si el riego aplicado es por goteo; ni en agricultura de labor intensiva o altamente mecanizada 34. En el caso de la estación Violento (M3) los resultados muestran que el agua no debe ser utilizada para el riego, sin importar el tipo de cultivo.
Tabla 9 Conteo de microorganismos totales y coliformes fecales en tres estaciones de muestreo de la subcuenca Mampostón
| Estación de monitoreo | Microorganismos totales (UFC mL-1) | Morfotipos | Coliformes fecales (UFC mL-1) |
|---|---|---|---|
| G2 | 13x103 | 6 | 11x103 |
| M3 | 2x105 | 8 | 2x105 |
| M5 | 2.8x105 | 7 | 2x106 |
UFC-Unidades formadoras de colonias
La evaluación de las diferencias espacio-temporales de los parámetros químico físicos permitió establecer la influencia de las diversas fuentes contaminantes del territorio, sobre la composición media de las aguas superficiales con respecto a una gran diversidad de parámetros y además comprobar la aptitud para el riego en las estaciones de muestreo evaluadas. Este enfoque ha sido utilizado ampliamente en la evaluación del aporte antrópico a los suelos y las aguas, tanto superficiales como subterráneas 35-38.
Este trabajo ha permitido establecer una herramienta de trabajo para el diseño de un plan de manejo adecuado, con vistas a revertir los impactos de la contaminación orgánica e inorgánica por parte del Consejo Territorial de Cuencas Hidrográficas, teniendo en cuenta que la implementación de un trabajo coordinado entre decisores y gestores medioambientales garantiza poner en práctica estrategias de compensación ecológica y la optimización de la estructura industrial, como bases para obtener un ecosistema sostenible 39.
CONCLUSIONES
La variabilidad espacial es el factor determinante para explicar la varianza de los diferentes parámetros evaluados relativos a la calidad de las aguas en la subcuenca Mampostón. Su análisis permite determinar la aptitud para el riego de 16 estaciones de muestreo, a partir del conocimiento de los principales contaminantes y sus fuentes de vertimiento.
Las estaciones de muestreo G2, G3 (río Ganuza) y M5 (río Mampostón), presentan aportes orgánicos y de sales solubles que establecen limitaciones para su uso en el riego agrícola. Mientras que las concentraciones medias de Pb disuelto, inhabilitan la explotación de las estaciones G1, G2, G4 (río Ganuza), M2 y M3 (río Mampostón) y P1 (derivadora Pedroso). La estación M5 además presenta concentraciones peligrosas a la salud humana de coliformes fecales.
El resto de las estaciones ubicadas en la derivadora Pedroso y la presa Mampostón, cumplen con todas las normas de calidad para el riego agrícola.
Debe diseñarse un programa de monitoreo y manejo del área, que posibilite la evaluación del riesgo de exposición a contaminantes y la implementación de un plan de acción que permita su mitigación.











 texto en
texto en