INTRODUCCIÓN
La soya (Glycine max (L.) Merrill) es una leguminosa que establece una asociación mutualista con bacterias del grupo de los rizobios, lo cual le permite asimilar parte importante del nitrógeno que necesita para satisfacer sus necesidades nutricionales 1,2. Este cultivo cuenta con un notable valor económico, pues constituye un alimento altamente proteico para la dieta animal y humana 3,4.
Dado el aporte que realizan los rizobios en la nutrición nitrogenada de la soya, este cultivo se biofertiliza en gran parte del mundo 5, por lo que diversos biofertilizantes se comercializan con este fin 5,6. Un ejemplo de ello lo constituye Azofert®-S, biofertilizante a base de la cepa Bradyrhizobium elkanii ICA 8001 y factores de nodulación, el cual se emplea como parte del manejo integrado de la soya 7.
En la elaboración de un biofertilizante, el control de calidad es fundamental para el óptimo desempeño del producto. La pureza del cultivo microbiano y la concentración celular por encima de 1 x 108 UFC mL-1 (Unidades Formadoras de Colonia por mililitro del inoculante), son los indicadores principales que determinan su calidad en la producción 8, pero es necesario establecer el tiempo de vida útil del inoculante en las condiciones de almacenamiento, lo que es vital para mantener la calidad del producto y su permanencia en el mercado. El objetivo del presente estudio fue evaluar la viabilidad en el tiempo de la cepa B. elkanii ICA 8001 en el biofertilizante Azofert®-S, cuando se produce en diferentes momentos del año y se mantiene a temperatura ambiente.
MATERIALES Y MÉTODOS
Se utilizó la cepa B. elkanii ICA 8001, procedente del cepario del Laboratorio de Microbiología del Departamento de Fisiología y Bioquímica Vegetal del INCA, a partir de la cual se prepararon inoculantes en cuatro momentos: verano (agosto-febrero), otoño (octubre-abril), invierno (diciembre-junio) y primavera (mayo-octubre), entre los años 2014-2016.
Una asada de colonias puras de la cepa, conservada a 4 oC en medio Levadura-manitol (LM) 9, se inoculó en Erlenmeyers de 50 mL de capacidad, que contenían 10 mL del medio de cultivo Bradyfact 7 estéril. Los frascos se mantuvieron en condiciones de agitación a 130 rpm y 28 °C, durante 72 horas. Posteriormente, se escaló la multiplicación de la bacteria a medio fresco, a razón de 1:10 (v/v), en iguales condiciones de agitación y temperatura, hasta obtener 1000 mL del inoculante. En todos los casos se emplearon frascos cuyo volumen de inóculo representara la quinta parte del volumen total de estos, para garantizar un ambiente aerobio. Los inóculos que se obtuvieron se envasaron en cinco frascos estériles de 240 mL y se conservaron a temperatura ambiente.
En el momento de la elaboración de los inoculantes y cada 30 días, durante 180 días de conservación, se eligieron tres frascos al azar y se les determinó la pureza de los cultivos mediante la Tinción de Gram. Para ello, se tuvo en cuenta las características morfológicas de las células bacterianas, la respuesta a la tinción, la presencia de endosporas y la presencia de microorganismos contaminantes 10. Además, se determinó la concentración celular, para lo cual se tomó 1 mL de inoculante y se realizaron diluciones decimales seriadas, de las cuales se sembraron 100 µL en placas con medio LM sólido y se incubaron a 30 °C durante siete días. Se determinó entonces el número de UFC mL-1, según la expresión:
UFC mL-1 = No. col x 10-1 x d
donde:
No. col: número de colonias
d: factor de dilución
Análisis estadístico
Los frascos se conservaron según diseño experimental completamente aleatorizado.
Los datos de concentración celular se procesaron por un análisis de varianza de clasificación simple. La prueba de comparación de medias de Tukey para p<0,05 se utilizó para discriminar diferencias entre tratamientos, los que correspondieron a las diferentes épocas de producción de los inoculantes 11. Los datos se procesaron en el programa Statgraphics Plus versión 5.1, 2001 y se graficaron en el programa Microsoft Excel, 2016.
RESULTADOS Y DISCUSIÓN
Las evaluaciones de pureza mostraron, en todos los casos, solo bacilos Gram negativos, sin endosporas, características típicas de la cepa ICA 8001 7.
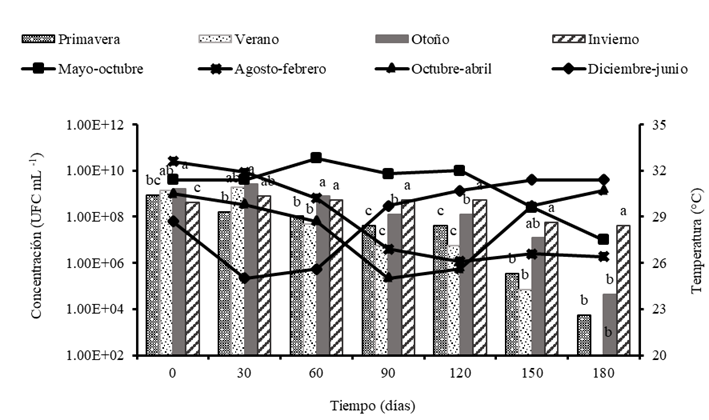
La viabilidad de la cepa en el inoculante Azofert®-S, durante el almacenamiento en las diferentes épocas, se muestra en la Figura 1. Se puede apreciar que la cepa se mantuvo en concentraciones de 1 x 108 UFC mL-1 durante los primeros 30 días de almacenamiento, en todas las épocas que se produjo. Concentraciones iguales o superiores a 1 x 108 UFC mL-1 resultan adecuadas para emplear un inoculante a base de rizobios 12. La temperatura de almacenamiento durante este período se comportó entre los 25-32 °C, según las diferentes épocas.
 El análisis estadístico se realizó en cada momento de evaluaciónEn las barras, medias con letras iguales no difieren estadísticamente (Tukeyp≤0,05, n=3)Las líneas representan el comportamiento de la temperatura en los diferentes períodos
El análisis estadístico se realizó en cada momento de evaluaciónEn las barras, medias con letras iguales no difieren estadísticamente (Tukeyp≤0,05, n=3)Las líneas representan el comportamiento de la temperatura en los diferentes períodosFigura 1 Viabilidad de la cepa B. elkanii ICA 8001 en el biofertilizante Azofert®-S, producido y almacenado durante 180 días, a temperatura ambiente
Los inoculantes que se produjeron en las épocas de otoño e invierno presentaron una concentración de 108 UFC mL-1 hasta los 120 días de conservación, mientras que aquellos producidos en primavera sólo mostraron esos valores de concentración hasta los 60 días y los que fueron elaborados en verano no mantuvieron ese nivel de bacterias viables más allá de los 30 días.
A los 120 días, los inoculantes que se produjeron en la época de invierno presentaron una mayor concentración bacteriana que aquellos que se prepararon en otoño y ambos superaron los resultados de viabilidad de aquellos que se elaboraron en primavera y verano. Si tenemos en cuenta el comportamiento de la temperatura, coincide que los inóculos que se elaboraron en invierno se sometieron a los valores más bajos durante los primeros 60 días de conservación (28,7-25-25,6 °C) y en este mismo rango de tiempo, le siguen los valores de temperatura a las que fueron expuestas las muestras de la época de otoño (30,5-29,8-28,7 °C). Respuestas similares, en la conservación de inoculantes bacterianos en ambientes con valores de temperatura inferiores a 30 °C, evidencian que es posible mantener la concentración bacteriana sin variaciones significativas 13.
Sin embargo, los inoculantes que se produjeron durante la primavera en los dos primeros meses de conservación se sometieron a temperatura de 31,4 °C, valores que se incrementaron en los próximos tres meses, lo que sin dudas influyó en la disminución de la viabilidad bacteriana. Los inóculos que se elaboraron en verano se expusieron a 32,6 y 31,9 °C, las mayores en el momento de elaboración de todas las muestras que se analizaron en el trabajo. Se conoce el efecto negativo de la temperatura en la conservación de los inoculantes 13.
A pesar de la influencia negativa de la temperatura en la conservación de la cepa en estudio, especialmente en el momento de la elaboración de los productos, se pudo apreciar también que el tiempo durante el almacenamiento ejerce un efecto desfavorable en la viabilidad de esta bacteria. De manera similar, otros autores informan que el tiempo de conservación también constituye un factor importante a tener en cuenta en la supervivencia de especies como Sinorhizobium meliloti14, Rhodotorula mucilaginosa15 y Pseudomonas fluorescens16.
CONCLUSIONES
La estabilidad en el tiempo de la cepa B. elkanii ICA 8001, presente en inoculantes de Azofert®-S, depende de la época del año en que se elaboren, lo cual está dado por su sensibilidad a la exposición a temperaturas superiores a 31 °C.
RECOMENDACIONES
Se recomienda producir estos inoculantes para soya en las épocas de otoño e invierno y si es necesario conservarlos a temperatura ambiente, que no sea por más de 120 días. Si se producen en primavera o verano, deben utilizarse en los primeros 60 y 30 días, respectivamente.
Se sugiere evaluar el efecto de compuestos preservantes en el inoculante, para extender el período de caducidad del producto.











 texto en
texto en 


