Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Hematología, Inmunología y Hemoterapia
versión On-line ISSN 1561-2996
Rev Cubana Hematol Inmunol Hemoter v.19 n.2-3 Ciudad de la Habana Mayo-dic. 2003
Instituto de Hematología e Inmunología
Efecto in vitro del VIMANG® sobre los linfocitos humanos
Lic. Lázaro O. del Valle Pérez, Lic. Bertha B. Socarrás Ferrer, Lic. Isabel
Torres Leyva, Dra. Vianed Marsán Suárez, Dra. Consuelo Macías Abraham, Dr. Porfirio Hernández Ramírez y Dr. José M. Ballester Santovenia
Resumen
El VIMANG® es un producto desarrollado por el Centro de Química Farmacéutica de Ciudad de La Habana a partir de la corteza de ciertas variedades de árboles de mango (Mangifera indica Lin). Se estudió el efecto in vitro del VIMANG® sobre los linfocitos de 20 donantes voluntarios de sangre y de 20 enfermos con diagnóstico de inmunodeficiencia celular mediante la prueba de transformación linfoblástica, con el empleo de timidina tritiada y la técnica de roseta activa. Se hallaron diferencias estadísticamente significativas entre las condiciones experimentales sin VIMANG® (25mg/mL) y con diluciones de este (desde 1:2 hasta 1:2048) en la prueba de transformación blástica. En la roseta activa se observaron diferencias estadísticamente significativas entre los linfocitos sin VIMANG® y los cultivados con la dilución (1:512), tanto en los donantes sanos como los enfermos.
DeCS: MANGIFERA INDICA/ uso terapéutico; ACTIVACION DE LINFOCITOS; IN VITRO.
Las plantas han sido utilizadas por el hombre con diversos fines desde sus orígenes hasta nuestros días, entre los que se destacan su uso como remedios medicinales y para la obtención de sustancias no nutritivas con actividad biológica, lo que ha sido motivo de especial atención, por sus efectos antivirales y antitumorales, la antimutagenicidad, y por su efecto sobre el sistema inmune del hombre y de animales.1,2
El VIMANG® es un producto desarrollado por el Centro de Química Farmacéutica de Ciudad de La Habana. Ha sido obtenido de la corteza de ciertas variedades de mango (Mangifera indica Lin.). Esta especie, introducida en Cuba en 1782, pertenece a la familia de las anacardiáceas, es originaria de la región tropical asiática y se ha propagado ampliamente en nuestro país. También crece en las restantes Antillas Mayores y Menores, en la Florida, en la América continental y en los trópicos del viejo mundo. 3-6
El VIMANG® está constituido por una mezcla de polifenoles (40-70 %); entre los que se hallan flavonoides como la mangiferina, cuyas propiedades antioxidantes son reconocidas. Su presencia se ha relacionado con la disminución del riesgo coronario, la disminución de proteínas de baja densidad y el efecto quimiopreventivo de algunos tipos de neoplasias, terpenoides, esteroides,ácidos grasos y cerca de 70 microelementos. La presencia de microelementos en el nuevo producto natural como Se, Ca, Mg y Zn, le aportan propiedades dietéticas al suministrar componentes poco comunes en la dieta alimentaria. En el caso del Se, su concentración le permite alcanzar el valor de la dosis diaria recomendada. El contenido de ácidos grasos poli-insaturados (mirístico, palmítico y oleico, entre otros) en concentraciones entre el 1-5 % del ingrediente activo, constituyen un importante aporte del VIMANG® a la dieta, además de contribuir a la actividad antioxidante por su elevado grado de insaturación que le permite captar radicales libres. 7,8
El VIMANG® es un producto que no es tóxico ni irritante por vía oral, tópica, rectal, vaginal u ocular; no tiene actividad mutagénica o potencial genotóxico y no induce daños en la molécula de ADN. 4,9-17
El objetivo de este trabajo fue conocer el efecto in vitro del VIMANG® sobre la proliferación de los linfocitos humanos mediante la transformación blástica (TB) y la formación de roseta activa (RA) de donantes supuestamente sanos y pacientes con diagnóstico de inmunodeficiencia celular.
Métodos
Se estudiaron 20 donantes voluntarios del Banco de Sangre del Instituto de Hematología e Inmunología y 20 enfermos con diagnóstico de inmunodeficiencia celular que no habían recibido ningún medicamento en el mes anterior a la extracción de la muestra. En cada caso, se extrajeron 20 mL de sangre heparinizada (15 UI/mL) con jeringuillas plásticas desechables. El aislamiento de las células mononucleares se efectuó según el método de Böyum modificado sobre un gradiente de Ficoll- Hypaque (densidad 1,077 g/mL, Sigma EE.UU.).18
Para evaluar la respuesta al VIMANG® los linfocitos se incubaron a una concentración de 2X105 /pocillo en placas de 96 pozos (NUNC Dinamarca) en 200mL de RPMI 1640 al 20 % de suero fetal bovino (SIGMA, EE.UU.) sin exposición al VIMANG® y con diluciones dobles de este producto (25mg/mL) desde 1:2 hasta 1:2048 durante 72 horas a 37 °C, en atmósfera húmeda al 5 % de CO2 en una incubadora (ASSAB, Suecia). Para determinar la viabilidad celular se utilizó la técnica de exclusión del azul tripán que en todos los casos fue superior al 98 %. Seis horas antes de culminar el cultivo se le añadió a cada pozo 1mCi de timidina tritiada (amersham, Inglaterra), (actividad específica 20 Ci/mmol). Las placas se procesaron en un cosechador de células (Flow Laboratories, Inglaterra). La detección de partículas b se realizó en un equipo RAK b (LKB, Suecia). Los resultados se expresaron en conteos por minutos (CPM).19
El estudio del efecto del VIMANG® sobre la formación de RA se efectuó con la incubación de los linfocitos con VIMANG® (dilución 1/512), a 4 °C durante las 24 horas previas a la formación de la roseta. 20
Preparación de la solución de VIMANG®: se realizó a partir del Lote No. 1, elaborado por la Empresa Laboratorio Farmacéutico "Roberto Escudero", con un contenido de polifenoles totales del 0,6 %. Se disolvieron 250 mg en 10 mL de RMPI 1640 y se incubó a 4 °C durante 1 hora. Posteriormente la solución se centrifugó a 3 500 rpm durante 15 min a 4 °C, y finalmente se filtró por un dispositivo de 0,2 mm (Sartorius, RFA).
Para comparar los resultados obtenidos entre las muestras en que se expusieron al VIMANG® y aquellos en que no se usó este producto, se utilizó la prueba estadística t de Student para muestras pareadas.
Bioética: a los pacientes y a los donantes se les explicó el objetivo del estudio, los posibles beneficios derivados de los resultados y la ausencia de riesgos asociados. Se confeccionó una planilla para el consentimiento informado de los donantes y enfermos que participaron en el mismo.
Resultados
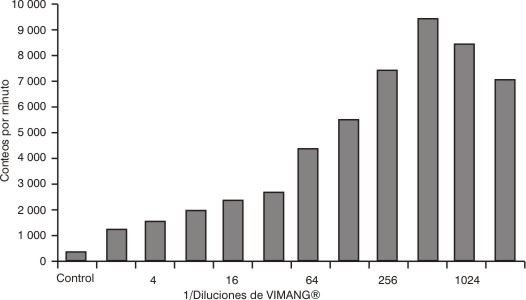
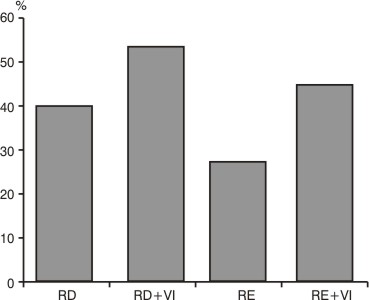
La proliferación in vitro de los linfocitos sin VIMANG® y con diluciones desde 1:2-1:2048 en donantes y enfermos con diagnóstico de inmunodeficiencia celular, produjo cambios estadísticamente significativos (p£ 0,001) (figs. 1 y 2). En los linfocitos de donantes y pacientes con inmunodeficiencia celular previamente incubados sin VIMANG® y con (dilución 1/512) antes de la formación de la RA, hubo también diferencias estadísticamente significativas (p£ 0,001) (fig. 3).
Fig.1. Proliferación in vitro de los linfocitos de donantes sanos.
Fig.1. Proliferación in vitro de los linfocitos de enfermos con inmunodeficiencia celular.
RD: roseta activa de donantes (linfocitos sin exposición previa al VIMANG®); RD+VI: roseta activa de donantes (linfocitos con exposición previa al VIMANG®); RE: roseta activa de enfermos con inmunodeficiencia ( linfocitos sin exposición previa al VIMANG®); RE+VI: roseta activa de enfermos con inmunodeficiencia celular (linfocitos con exposición previa al VIMANG®).
Discusión
El VIMANG® aumentó la proliferación de los linfocitos humanos tanto de los controles sanos como de los enfermos con diagnóstico de inmunodeficiencia celular, lo que coincide con otro reporte donde se indica que a dosis inferiores a 30 mg/mL aumenta la proliferación de los linfocitos.21 En nuestro estudio se comprobó que estos resultados podían obtenerse tanto en donantes sanos como en pacientes con inmunodeficiencia celular. Esto podría deberse a la propia composición del VIMANG®, que tiene entre sus constituyentes al Se, Mg, Zn, Cu, Ca, Fe, los cuales se conoce que participan en diferentes vías metabólicas como cofactores de enzimas y componentes de otras proteínas. El Zn es necesario para varios procesos celulares como: las interacciones celulares, las etapas del ciclo celular, el metabolismo del RNAm y la función de más de 70 enzimas, algunas como la timidina-cinasa DNA polimerasa, que interviene en la síntesis del ADN, por lo que este metal tiene un efecto estimulante sobre las células en división activa.
También podría deberse a los otros componentes como los polifenoles, en especial la mangiferina, los ácidos grasos poli-insaturados que participan también en la actividad antioxidante y la acción beneficiosa de estas sustancias para la respuesta inmune. 7,22
Estos resultados dan la posibilidad del uso del VIMANG® en pacientes con trastornos del sistema inmune, teniendo en cuenta que no es ni tóxico ni mutagénico y abre nuevas posibilidades terapéuticas para el tratamiento de las inmunodeficiencias.
Consideramos de interés estudiar también el efecto in vitro del extracto acuoso del VIMANG® sobre los linfocitos humanos, para determinar su efecto sobre la expresión de los marcadores de activación HLA-DR, CD25 y CD2R, así como la realización de un estudio clínico controlado del VIMANG® en enfermos con inmunodeficiencia.
Summary
VIMANG® is a product from the bark of certain varieties of mango tress (Mangifera indica Lin), devised by the Pharmaceutic Chemistry Center in the City of Havana. The effect in vitro of VIMANG on lymphocytes from 20 blood donors and 20 patients diagnosed with cellular immunodeficiency was studied through the lymphoblastic transformation test with titrated thymidine and the active rosette technique. Statistically significant differences were found under experimental conditions without VIMANG®(25mg/ml) and with VIMANG® dilutions (from1:2 to1:2048) in the blastic transformation test. Likewise, statistically significant difference between lymphocytes without VIMANG® and those cultured with VIMANG® dilution (1:512) were found in both healthy donors and patients in the active rosette test.
Subject headings: MANGIFERA INDICA/therapeutic use; LYMPHOCYTE ACTIVATION; IN VITRO.
Referencias bibliográficas
- Muanza DN, Euler KL, Williams L. Screening and antitumour and anti-VIH activities of nine medicinal plants from Zaire. Int J Pharmacogn 1995;33:98-106.
- An D, Putt D, Kresty I, Stoner GD, Fromm D, Hollenberg PH. The effects of dietary ellagic acid on rat hepatic and esophageal mucosal cytochrones P450 and phase II enzymes. Carcinogenesis 1996;17:821-8.
- Loy S, Simón R, Delgado R. VIMANG, un potencial protector de la peroxidación lipídica en lipoproteínas de baja densidad. Rev Cubana Invest Biomed 2002;21:167-70.
- Martínez G, Delgado R, Garrido G, Guevara M, García D, Paéz E, et. al. Vimang. Nuevo producto antioxidante. Mitos y realidades de la terapia antioxidante. Ciudad de La Habana. MINSAP. 2003
- MINSAP. Plantas medicinales. Fitomed II. Ciencias Médicas. Ciudad de La Habana;1993:76-7.
- Roig JT. Plantas medicinales, aromáticas o venenosas. La Habana: Ed. Científico-Técnica; 1988:610-2.
- Martínez G, Giuliani A, León OS, Pérez G, Núñez AJ. Effect of Mangifera indica L. extract (QF808) on protein and hepatic microsome peroxidation. Phytother Res 2001;15:581-5.
- García L, García V, Rojo DM, Sánchez E. Plantas con propiedades antioxidantes. Rev Cubana Invest Biomed 2001;20:231-5.
- Centre of Pharmaceutical Chemistry (CPC) (1998) Pharmaceutical compositions including a mixture of polyphenols, terpenoids, steroids, fatty acids and microelements with antioxidant, analgesic, anti-inflammatory and anti-spamolic properties. Patent Pending 203/98, OCPI, Cuba.
- Rovillard LF, Thiais AJ, Robin JR. Cosmetic or pharmaceutical composition containing, as active ingredient, mangiferine or its derivates, in pure or in plant extracts. US Patent 1998;5:824.
- Martínez G, Jalil E, Giuliani A, León S, Sam S, Delgado R, et al. Mangifera indica L. extract (QF808) reduces ischaemia-induced neuronal loss and oxidative damage in the Gerbil Brain. Free Radical Res 2001;35:465-73.
- Tamayo D, Mari E, González S, Guevara M, Garrido G, Delgado R, et al. VIMANG as natural antioxidant supplementation in patients with malignant tumours. Minerva Med 2001;92:(suppl 1-3):95-7.
- Delgado R, Garrido G, González D, Herrera B, Beltrán A, Lemus Y, et al. Mangifera indica L. extract (VIMANG) as a natural antioxidant with antinoceptive and anti-inflammatory properties. Minerva Med 2000;92(suppl 1-3):98-102.
- Núñez A, Vélez HT, Agüero J, González J, Naddeo F, Simone F, et al. Isolation and quantitative analysis of phenolic antioxidants, free sugar, and polyols from mango (Mangifera indica L) stem bark aqueous decoction used in Cuba as a nutritional supplement. J Agric Food Chem 2002; 50:762-6
- Cancino L, Leyva A, Garrido G, Cossio M, Prieto E. VIMANG: los efectos antigenotóxico y modulador de las enzimas glutatión peroxidadasa y Glutatión -S-transferasa. Rev Cubana Invest Biomed 2001:20:48-53.
- Concepción A, Peña R de la, Fariñas L. Gel del VIMANG con actividad antifotoenvejecimiento; estudio histológico preliminar. Rev Cubana Invest Biomed 2003;22: 21-5.
- Hernández M, Prieto E. Plantas que contienen polifenoles. Antioxidantes dentro del estilo de vida. Rev Cubana Invest Biomed 1999;18:12-4.
- Böyum A. Isolation of mononuclear cells and granulocytes from human blood. Scand J Clin Lab Invest 1968;10:1041-9.
- Del Valle LO, Macías C, Torres I, Socarrás BB, Marsán V, Sánchez M. Efecto in vitro de la espirulina sobre los linfocitos humanos. Rev Cubana Hematol Inmunol Hemoter 2002;18(2).
- Cruz C, Fernández NL, Bernal B, Hernández P, Ballester JM. Técnicas de rosetas. La aplicación en pacientes con alteraciones inmunológicas. Rev Cubana Med 1981;20:379-87.
- Sánchez GM, Re L, Giuliani A, Núñez AJ, Davison GP, León OS. Protective effects of Mangifera indica L. extract, mangiferin, and selected antioxidants against TPA-induced biomolecules oxidation and peritoneal macrophage activation in mice. Pharmacol Res 2000;42:565-73.
- Stites D, Stobo J, Fudenberg, Wells J. Inmunología Básica y Clínica. La Habana: Ed. Científico-Técnica;1987:296-302.
Recibido: 12 de enero de 2004. Aprobado: 2 de febrero de 2004.
Lic. Lázaro O. del Valle Pérez. Instituto de Hematología e Inmunología. Apartado 8070, CP 10800, Ciudad de La Habana, Cuba. Tel (537) 578268, 544214. Fax (537) 442334. e-mail: ihidir@hemato.sld.cu