Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Hematología, Inmunología y Hemoterapia
versión On-line ISSN 1561-2996
Rev Cubana Hematol Inmunol Hemoter v.22 n.2 Ciudad de la Habana Mayo-ago. 2006
Artículos de revisión
Instituto de Hematología e Inmunología
Reacción transfusional hemolítica inmune inmediata
Dr. Lázaro Cortina Rosales y Dra. María del Rosario López de Roux
Resumen
La reacción hemolítica inmediata inmunológica representa la principal causa de muerte por transfusión. La reacción antígeno-anticuerpo con la subsiguiente hemólisis de los eritrocitos, desencadena un síndrome de respuesta inflamatoria sistémica como consecuencia de la liberación de citocinas (factor de necrosis tumoral a, interleucina 1, interleucina 8, interleucina 6) y activación de sistemas enzimáticos de amplificación (coagulación, fibrinólisis, calicreína-bradicinina). La coagulación intravascular diseminada y el fallo renal agudo son los eventos fisiopatológicos que dominan el cuadro. Se han desarrollado protocolos pre-transfusionales que ofrecen múltiples peldaños de seguridad, cuyo cumplimiento descarta la ocurrencia de reacciones fatales. Sin embargo, aún están presentes y se señalan como sus causas fundamentales los errores de identificación, la falta de conocimiento y la negligencia.
Palabras clave: hemólisis, reacción antígeno anticuerpo, citocinas, protocolo pre-transfusional.
Hace un siglo, Landsteiner descubrió el grupo sanguíneo ABO, evento trascendental para el desarrollo de la transfusiología moderna. Hasta ese entonces, los intentos de transfusión de sangre alogénica fueron desafortunados, debido a la ocurrencia de reacciones severas que generalmente terminaban con la muerte del paciente.1 La reacción transfusional hemolítica aguda (RTHA) se conoce desde las primeras prácticas. En 1667, Jean Baptiste Denis describió los signos clásicos de esta en un paciente que recibió una transfusión de sangre de cordero.1 Hoy, el conocimiento de sus causas, ha llevado al desarrollo de protocolos pretransfusionales estrictos que han disminuido considerablemente su presentación; sin embargo, aún representa la causa principal de muerte asociada con la transfusión.2
La existencia de anticuerpos (Ac) en el plasma del receptor contra antígenos (Ag) presentes en los eritrocitos transfundidos, desencadena la reacción, que con la formación del complejo Ag-Ac, dispara la respuesta fisiopatológica que involucra a múltiples sistemas enzimáticos, los cuales determinarán la extensión y severidad de los daños orgánicos.
La mayoría de las reacciones hemolíticas fatales y de las reacciones peligrosas que causan morbilidad importante, resultan de la transfusión de eritrocitos incompatibles para el sistema ABO. Otros Ac como los dirigidos contra los sistemas Rh, Kell, Duffy o Kidd son capaces de causar la RTHA, pero rara vez sus resultados son catastróficos.2,3
Mecanismos inmunohemolíticos
En las RTHA están presentes 2 tipos de hemólisis: intravascular y extravascular. Una de estas suele predominar, lo que está en relación con el tipo de inmunoglobulina, la concentración de Ac y el estado del sistema inmunológico.4,5
En las reacciones mediadas por IgM predomina la hemólisis intravascular, debido a la capacidad de estos Ac para activar el complemento hasta la formación del complejo de ataque a la membrana (C5-9).4,5 La destrucción de los eritrocitos ocurre directamente en el torrente circulatorio, lo que determina la presencia de hemoglobinemia y hemoglobinuria. Una proporción pequeña de células no son lisadas por este mecanismo debido a la acción protectora de las proteínas reguladoras del complemento presentes en el plasma y de las proteínas inhibitorias de la membrana celular o porque moléculas de IgG se unen a los Ag. Estas células son capturadas por el sistema mononuclear fagocítico a través de los receptores para la fracción Fc de las inmunoglobulinas G y del componente C3b del complemento, lo que permite su fagocitosis o su destrucción por citotoxicidad celular dependiente de Ac.5,6 La incompatibilidad ABO es el ejemplo clásico de esta reacción.4,5
Cuando los aloanticuerpos son de clase IgG predomina la hemólisis extravascular, ya que estos no activan el complemento o solo lo hacen parcialmente hasta C3. La destrucción de los eritrocitos recubiertos por inmunoglobulinas y componentes del complemento ocurre en el hígado y el bazo, después de ser capturados por monocitos y macrófagos a través de sus receptores para la fracción Fc de la IgG y del componente C3b del complemento. Es por eso que no suele acompañarse de hemoglobinemia ni hemoglobinuria, sino más bien de aumento de la bilirrubina indirecta. Una proporción de células sufren hemólisis por el mecanismo de citotoxicidad celular dependiente de Ac. 4-6 Ejemplos de estos Ac son los dirigidos contra los sistemas Rh, Kell, Duffy y Kidd.7
Factores moduladores de las RTHA2
La transfusión de eritrocitos incompatibles desencadena la reacción Ac-Ag. Sin embargo, la magnitud de esta difiere de un paciente a otro, lo que está determinado por la existencia de una serie de factores que afectan la intensidad de la reacción, entre los cuales tenemos:
- Clase y sub-clase de Ac.
- Capacidad de activar al sistema de complemento.
- Concentración plasmática, afinidad y especificidad del Ac.
- Densidad y movilidad de los Ag eritrocitarios.
- Actividad de los macrófagos del sistema reticuloendotelial.
- Sensibilidad de la membrana eritrocitaria al sistema de complemento.
- Cantidad de sangre incompatible transfundida.
- Condición clínica del paciente.
- Amplitud térmica del Ac.
- Localización de la hemólisis: intravascular o extravascular.
Papel de las citocinas y mediadores inflamatorios en la RTHA
Las citocinas constituyen una gran variedad de proteínas hormonas que están involucradas en la comunicación celular. Actualmente, su papel en la fisiopatología de la RTHA es considerado trascendental.8 En este acápite se describen las citocinas que intervienen en la RTHA.
Citocinas pro-inflamatorias
Interleucina 1(IL-1):
Producida por células del sistema mononuclear fagocítico. Tiene un potente efecto pirógeno, el cual es mediado por la acción de la prostaglandina E2 sobre el hipotálamo. Sus efectos sistémicos son importantes: estimula la hematopoyesis y la movilización de neutrófilos de la médula ósea; en concentraciones suficientes, es capaz de producir colapso vascular, shock y muerte; activa las células B y T; induce la expresión de genes de: factor de necrosis tumoral a, interleucina 8 (IL-8), la proteína 1 quimiotáctica para los monocitos (MCP), interleucina 6 (IL-6), antagonista del receptor de la IL-1(IL-1ra), proteínas del complemento, moléculas de adhesión (ICAM-1, ELAM-1), endotelina y factor tisular. 8
Factor de necrosis tumoral a(FNT a):
Citocina multifuncional producida por los monocitos y macrófagos. Tiene un potente efecto pro-inflamatorio sinérgico con la IL-1. Su acción sobre las células endoteliales estimula la liberación de diversos mediadores: IL-8, MCP, prostaglandinas, óxido nítrico, IL 6 y factor tisular,9 los cuales aparecen vinculados con los efectos fisiopatológicos que se presentan durante la reacción hemolítica: aumento de la permeabilidad vascular, vasodilatación y activación de los sistemas extrínsecos y alternativos de la coagulación.3,4,10 Estimula además la desgranulación de los neutrófilos, la expresión en las células endoteliales de moléculas de adhesión para los neutrófilos y monocitos (ICAM-1, ELAM) y produce fiebre mediada por el hipotálamo.10
El FNTa suprime la transcripción del gen de la trombomodulina y promueve su internalización por la célula endotelial. También desregula la síntesis de proteína S por dichas células, factores que contribuyen a la pérdida de la propiedad anticoagulante del sistema proteína C-proteína S.7,11,12
Disminuye la actividad fibrinolítica porque estimula la producción y la liberación del inhibidor del activador tisular del plasminógeno tipo 1(PAI-1).12
Su acción sobre el activador tisular del plasminógeno (t-PA) es contradictoria. Según lo apreciado en modelos experimentales, al inicio ocurre un aumento transitorio, que se cree debido a la liberación de los gránulos preformados en las células endoteliales; sin embargo, posteriormente produce un descenso mantenido de los niveles de t-PA.12 Esto contribuye a la reducción de la actividad fibrinolítica.
IL-6:
Producida por células del sistema mononuclear fagocítico. Estimula la proliferación y diferenciación de los linfocitos B, lo cual favorece la producción de autoanticuerpos y aloanticuerpos. Activación de los linfocitos T. Responsable de la síntesis de proteínas de fase aguda: fibrinógeno, complemento y proteína C reactiva.3,7,13,14
Quimocinas:
Son producidas por células del sistema mononuclear fagocítico, con propiedades inflamatorias, pero tienen un rango más restringido de células diana.
IL-8:
Tiene acción quimiotáctica sobre los neutrófilos e induce su activación, desgranulación y altera la adhesión de las moléculas de superficie. Acción quimiotáctica sobre los linfocitos. Induce la liberación de histamina por los basófilos.15,16
MCP-1:
Tiene acción quimiotáctica sobre los monocitos e induce la producción de IL-1 e IL-6.3,4,15,17
Citocinas antiinflamatorias
Receptor antagonista de la IL-1(IL-1ra):
Producida por células del sistema mononuclear fagocítico. Es antagonista competitivo de la IL-1. El balance entre la IL-1 y el IL-1ra determina la variabilidad clínica de las reacciones hemolíticas mediadas por IgG.3,4,13,18
Citocinas en la hemólisis intravascular por incompatibilidad ABO:
La infusión de células ABO incompatibles inducen la expresión de los genes de FNT a y de IL-1. Los niveles de FNT a alcanzan cifras máximas de 2-4 horas después de la infusión de los eritrocitos incompatibles, para luego disminuir progresivamente, sin embargo, la actividad de la IL-1 en plasma es mínima, lo cual se cree que es debido a que se encuentra asociada con células o con una proteína transportadora, o a la presencia de una sustancia que causa interferencia.8,10 La IL-8 y la MCP se secretan después de a las 4-6 horas y alcanzan niveles máximos a las 24 horas.14,17
La producción de citocinas en respuesta a la incompatibilidad ABO, requiere de un factor plasmático lábil al calor, posiblemente el complemento activado.8
Citocinas en la hemólisis mediada por Ac IgG:
En las citocinas se aprecian 2 categorías de respuesta:
- Altos niveles de respuesta: IL-8, MCP, IL-1ra.
- Bajos niveles de respuesta: FNT a, IL-1 e IL-6.
No se aprecia aumento significativo en el FNT a hasta después de las 6 horas de transfundida la sangre incompatible. La IL-1 y la IL-6 quizás promuevan la producción de aloanticuerpos y autoanticuerpos. La activación del gen de la IL-1ra ocurre posteriormente, pero independiente de la IL-1. La variabilidad de la reacción mediada por IgG, puede estar en relación con el balance IL-1-IL-1ra. La IL-8 y la MCP son producidas de manera progresiva.16
Estas citocinas y mediadores están presentes tanto en las hemólisis intravasculares como en las extravasculares. Pero en la primera, estas sustancias son liberadas hacia la circulación sistémica y ejercen su acción sobre muchos tipos celulares, mientras que en la segunda, su acción queda circunscrita al sitio de eritrofagocitosis, fundamentalmente el ámbito esplénico; de ahí la menor intensidad de sus efectos sistémicos.8,16
Mediadores inflamatorios
Factor de Hageman:
Es activado por el complejo Ag-Ac y actúa como disparador de varios sistemas de amplificación asociados con las reacciones inmunológicas:3,19
- La fibrinólisis, a través del activador tisular del plasminógeno.
- El sistema calicreína-bradicinina.
- La coagulación, al activar la vía intrínseca.
El papel del factor de Hageman como activador de la vía intrínseca en la coagulación intravascular diseminada (CID) ha sido discutido, y después de múltiples experimentos, existe el consenso de que su contribución a la activación de la coagulación es pobre y su efecto principal en la reacción hemolítica es sobre estado hemodinámico, ya que estimula la producción de bradicinina, la cual, directa o indirectamente causa vasodilatación por la generación de óxido nítrico y prostaciclina.20,21
Anafilotoxinas C 3a y C 5a:
Generadas a partir de la activación del complemento. Activan a los mastocitos, neutrófilos y células mononucleares, en los cuales se produce:
- La expresión del receptor (R) C3b.3,19
- Liberación de los gránulos que contienen histamina, prostaglandinas y leucotrienos, responsables de vasodilatación, aumento de la permeabilidad vascular y finalmente, de la hipotensión que se desarrolla durante la reacción.3,19
- Ocurre el estallido respiratorio oxidante con la generación de anión superóxido, peróxido de hidrógeno, O2 libre y radicales hidroxilo, todos ellos potentes agentes de destrucción celular.3,19
- Producción de mediadores solubles de células mononucleares: FNT, IL-8, PGs, factores activadores de la quimiotaxis y activación de los neutrófilos.3,19
Endotelina 1:
Es una sustancia vasoactiva producida por las células endoteliales vasculares. Su liberación es inducida por: trombina, bradicinina, epinefrina e interleucina 1. Es un poderoso agente vasoconstrictor. En la RTHA se considera uno de los agentes causantes de la isquemia a los tejidos.3,4
Principales eventos fisiopatológicos
Hipotensión inicial:
Evento trascendental por lo que significa directamente sobre el estado clínico del paciente y por las respuestas fisiopatológicas que se generan. En su génesis se han involucrado varios sistemas: el complemento con la generación de anafilotoxinas C 3a –C 5a y su acción en la liberación de histamina, el sistema calicreína-bradicina activado por el factor de Hageman y la secreción de óxido nítrico por las células endoteliales estimulada por el FNT a y la IL-1.22,23
Coagulación intravascular diseminada (CID):
La CID iniciada como consecuencia de la reacción Ag-Ac puede causar formación de trombos en la microcirculación, consumo de factores de la coagulación y plaquetas, activación del sistema fibrinolítico, generación de productos de degradación del fibrinógeno y hemorragia incontrolada.3,22,23
La reacción Ag-Ac y la hemólisis activan varios sistemas enzimáticos que intervienen en la génesis de esta coagulopatía. Se destacan: la secreción del factor tisular generado a partir de las células endoteliales y por la desgranulación de los neutrófilos; 12,21 la activación del factor de Hageman y su acción sobre la fibrinólisis (su papel en la activación de la coagulación es considerado secundario, como ya se señaló); 12,21 la generación de plasmina por la acción de la trombina; la supresión de la fibrinólisis por la acción del FNT a y la IL-1, los cuales producen: disminución de los niveles de t-PA y aumento del PAI-1 y la pérdida de la actividad anticoagulante de la proteína C como consecuencia de la acción del FNT a, que reduce la expresión de la trombomodulina por las células endoteliales y disminuye la síntesis de proteína S. Esta última también se ve afectada por el aumento de su inhibidor natural C4bBP que se comporta como un reactante de fase aguda.12,21
Otros elementos que promueven la CID son: la actividad pro-coagulante de los fosfolípidos de estromas eritrocitarios derivados de la hemólisis, la activación plaquetaria por la liberación de ADP intraeritrocitario, la liberación de materiales tromboplásticos por leucocitos y plaquetas, y la disminución del óxido nítrico neutralizado por la hemoglobina libre, con afectación de la tromborresistencia.3,22,23
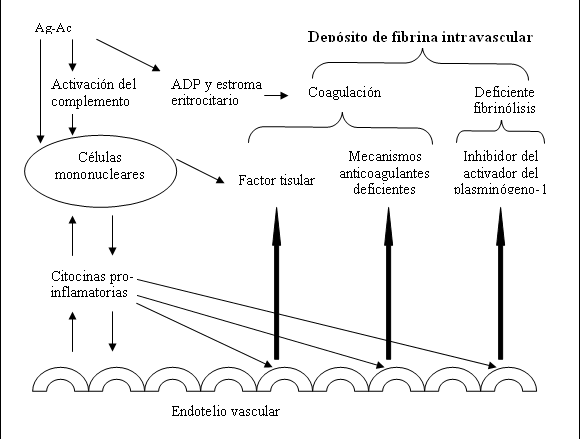
Todos estos cambios originan un desbalance coagulación-fibrinólisis, que determinan un estado pro-coagulante varias horas después de ocurrida la reacción hemolítica. Este desbalance contribuye al desarrollo de la disfunción y el fallo de órganos (fig. 1).21
Fallo renal:
Su aparición y gravedad determina en gran medida la morbimortalidad de la RTHA De esto se deriva la gran importancia de su prevención al más leve signo. En su etiología aparecen asociados varios mecanismos como es la hipotensión inicial que origina isquemia tisular y desencadena la respuesta neuroendocrina, caracterizada por la estimulación del sistema nervioso simpático con secreción de noradrenalina y otras catecolaminas, las cuales provocan vasoconstricción en las áreas con alta concentración de receptores adrenérgicos (como el riñón) y manteniendo el cuadro de isquemia. Esta acción vasoconstrictora se ve perpetuada por la producción de endotelina por las células endoteliales estimuladas por catecolaminas, trombina, FNT a, IL-1 y otros mediadores, y por la pérdida de la acción vasodilatadora del óxido nítrico tras su neutralización por la hemoglobina libre. Otro elemento que contribuye a la disminución del flujo renal es el depósito intravascular de estroma eritrocitario y de microtrombos (fig. 2).
La hemólisis intravascular tiene efectos fisiopatológicos sistémicos, y aunque el riñón suele ser el órgano más afectado, cualquier otro órgano puede sufrir el daño de la CID, de la hipotensión y de la isquemia. La acción sobre el sistema respiratorio puede conducir al síndrome de distrés respiratorio del adulto.3,12
Manifestaciones clínicas
Las manifestaciones de la RTHA son de carácter variable, lo cual depende del Ag involucrado y de las características del Ac (isótopo y concentración) y del estado clínico del paciente.2
En la incompatibilidad ABO los síntomas comienzan a los pocos minutos de iniciado el acto transfusional con sensación de calor en el punto de la flebotomía, enrojecimiento facial, fiebre, escalofríos, inquietud, dolor lumbar y/o abdominal, opresión subesternal acompañada de disnea, náuseas, sudoración, coluria, pérdida de sangre excesiva por las heridas, taquicardia, hipotensión, shock o hipertensión.2
Los pacientes con hemólisis extravascular tienen antecedentes transfusionales y/o de embarazos. El cuadro puede ser poco manifiesto o presentar fiebre, escalofríos, malestar general e ictericia franca o subclínica.2
Conducta ante una RTHA
La investigación y el tratamiento de una presunta reacción transfusional hemolítica deben ser ejecutados por un grupo multidisciplinario que comprenda personal de enfermería, del departamento de medicina transfusional, médicos hematólogos, nefrólogos, intensivistas y otros, que pudieran ser consultados según la necesidad de los pacientes. Aunque la severidad del cuadro clínico es variable, los lineamientos para el accionar deben estar adecuadamente protocolizados.
Medidas de carácter general 6,22
- Detener inmediatamente la transfusión, para limitar el volumen de sangre infundida.
- Mantener la vía intravenosa con solución salina al 0,9 %.
- Avisar al médico responsable y al servicio de medicina transfusional.
- Rectificar la identificación del paciente y precisar su correspondencia con los formularios y la bolsa de sangre.
- El médico responsable debe evaluar al paciente para confirmar si se ha producido una reacción hemolítica y determinar las acciones futuras.
- Se deben enviar al servicio de medicina transfusional muestras de sangre con y sin anticoagulante obtenidas con posterioridad a la reacción, la bolsa de sangre, el equipo de transfusión, las soluciones intravenosas y todos los formularios relacionados.
Investigaciones a realizar ante una presunta RTHA6,22
- Corroborar los datos administrativos: realizar la identificación del receptor y de la unidad transfundida. Si se descubre que ha ocurrido un error, debe determinarse de qué tipo y si están involucrados otros pacientes.
- Control visual de la hemólisis: se debe inspeccionar el suero o plasma de las muestras pre y postransfusionales y compararlas. Un cambio de coloración a rosado, rojo o púrpura después de la reacción, es indicativo de hemólisis. Cantidades tan pequeñas como 10 mL pueden producir hemoglobinemia. En los casos donde la muestra postransfusional se extrae tardíamente, la coloración del plasma suele ser amarilla o parda, como consecuencia de la degradación de la hemoglobina a bilirrubina.El examen de orina debe hacerse en el líquido sobrenadante, luego de centrifugación de una muestra fresca, lo que permite diferenciar la hemoglobinuria de la hematuria.
- Investigación del grupo ABO y Rh: en la sangre de la unidad transfundida y en la sangre del receptor, pre y postransfusional.
Si la tipificación de la bolsa no coincide con el grupo anotado en el rótulo, entonces ha ocurrido un error en el rotulado de la unidad.
- Prueba de antiglobulina directa (PAD): la PAD positiva en la muestra postransfusional con una PAD negativa en la muestra previa, es sugestiva de la existencia de un aloanticuerpo que se ha unido con los hematíes incompatibles transfundidos, pero que no fueron destruidos de inmediato. En estos casos, la prueba muestra aspecto de campo mixto (áreas con aglutinación y otras no). La PAD negativa en la muestra postransfusional no niega la existencia de una reacción hemolítica, lo cual puede suceder si las células transfundidas han sido rápidamente destruidas.
- Pruebas cruzadas de compatibilidad: a los glóbulos rojos de la unidad transfundida con el suero del paciente pre y postransfusional.
En caso de RTHA, se deben de rectificar las pruebas cruzadas de compatibilidad con la muestra pretransfusional y verificar sus resultados con la muestra postransfusional. El estudio debe incluir los 3 métodos: en salina, en albúmina y en Coombs. En las reacciones agudas tanto por incompatibilidad ABO como por otros Ag, por lo general los estudios con muestras pre y postransfusionales suelen ser positivos. Los Ac involucrados en estas reacciones se encuentran en títulos altos, tienen elevada avidez por el Ag y capacidad para activar el complemento, todo lo cual favorece el desarrollo de hemólisis aguda y que sean detectados en las pruebas pretransfusionales.
En casos raros de RTHA, las pruebas en las muestras pretransfusionales pueden ser negativas y en las muestras postransfusionales pueden ser positivas, lo que está en relación con el título de Ac previo y la respuesta anamnésica posterior a la reacción.
- Pruebas de detección de Ac: a las muestras previas y posteriores a la reacción y a la sangre del donante.
En estos casos, es necesario que, cuando se realice la prueba a la muestra pretransfusional, se usen técnicas de identificación más sensibles: LISS, polibrene, PEG o técnicas de enzimas.
Si se detecta un Ac, este debe ser identificado y posteriormente sometido a prueba con las muestras retenidas de las unidades transfundidas.
Si se detecta un Ac en una muestra posterior y no en la previa, la razón puede radicar en la respuesta anamnésica de Ac que se produce después de una reciente transfusión, o una transferencia pasiva de Ac en un componente recién transfundido. Esta última es menos probable.
El estudio de una primera muestra postransfusional puede ser negativa si todas las moléculas de Ac están fijadas a las células transfundidas incompatibles. En estos casos, se debe repetir la detección de Ac en muestras adicionales obtenidas a intervalo. El nivel de Ac en días ulteriores se elevaría rápidamente, lo que posibilitará su detección e identificación.
- Otros exámenes complementarios que ayudan al diagnóstico:
- Hemoglobina y hematócrito: para precisar si se produce la elevación terapéutica esperada.
- Haptoglobina a las muestras previas y posteriores a la transfusión y comparación de los resultados.
- Detección de hemoglobina en la orina.
- Bilirrubina, deshidrogenasa láctica.
- Marcadores de CID: prueba de paracoagulación, productos de degradación del fibrinógeno, complejo trombina antitrombina, complejo plasmina antiplasmina, entre otros.
- Cultivo bacteriológico y tinción de Gram de la sangre de la bolsa para descartar la hemólisis por infección.
Conducta médica 6,22
Los estudios anteriormente expuestos consumen cierto tiempo, y en estos casos no es permitido esperar los resultados, por lo cual es aconsejable iniciar simultáneamente el tratamiento.
En las reacciones severas es pertinente que los pacientes sean atendidos en una unidad de cuidados intensivos. El tratamiento debe estar dirigido al mantenimiento de la tensión arterial y el flujo sanguíneo renal. Si el shock es prevenido y tratado adecuadamente, la insuficiencia renal aguda puede ser generalmente evitada.6,22,23
Para aumentar el flujo sanguíneo renal y aumentar la diuresis, la terapia con líquido debe garantizar un flujo urinario mayor de 100 mL/h, durante un mínimo de 24 horas. La furosemida es aconsejable para aumentar la diuresis. Los agentes vasoopresores que disminuyen el flujo sanguíneo renal están contraindicados. La dopamina en dosis menores de 5 µg/kg/min dilata la vasculatura renal y aumenta el gasto cardíaco; puede ser útil en la fase aguda de la RTHA. Si el paciente desarrolla anuria, se recurrirá al tratamiento habitual de la insuficiencia renal aguda.
Vigilar estrechamente la función pulmonar por si fuera necesario la oxigenoterapia y el soporte ventilatorio.
La CID suele ser un fenómeno autolimitado y el uso de la heparina es controversial. Sin embargo, en situaciones en que el volumen de sangre incompatible exceda los 200 mL y la causa de la reacción es la incompatibilidad ABO, se pudiera usar por un período de 6 a 24 horas; aunque en pacientes quirúrgicos esta conducta es de alto riesgo. Para el control de los sangramientos se debe recurrir a la administración de crioprecipitado, plasma fresco congelado y concentrado de plaquetas.6,22,23
Estrategias futuras de tratamiento12,21
El futuro de las intervenciones terapéuticas en la RTHA, está encaminado a la modulación de las alteraciones fisiopatológicas disparadas por la reacción Ag- Ac. La meta de tal intervención es la desregulación de la respuesta inmune, la inhibición de la coagulación y de los efectos vasomotores. Las citoquinas, con su función prominente en la génesis de tales efectos, constituyen el blanco central de estos tratamientos, entre los que se destacan:
- IL-1ra.
- AcMo contra el FNT.
- Receptores solubles del FNT.
- Receptores solubles de la IL-1.
- Ac contra los receptores de la IL-1.
- Corticosteroides.
- Concentrados de antitrombina III.
- Concentrados de proteína C.
- Inhibidor del factor tisular (TFPI).
- AcMo contra el factor VII.
- AcMo contra el factor XII.
Prevención
Para organizar una prevención adecuada se deben identificar las causas de errores que ocasionan la RTHA, lo cual se debe realizar en cada centro hospitalario y ajustar las conductas necesarias para su erradicación. Se han señalado múltiples causas, entre las que destacan:2,3,24-26
- Identificación errónea del paciente.
- Identificación errónea de la muestra.
- Identificación errónea de la bolsa.
- Tipificación ABO incorrecta.
- Colocación incorrecta de los componentes en el refrigerador.
- Incumplimiento del protocolo técnico administrativo pretransfusional.
- Conocimiento insuficiente por parte del personal.
Los errores de identificación constituyen la fuente más común de RTHA.16 Desde la toma de muestra al paciente hasta la administración de la sangre, se desarrollan múltiples pasos que dependen de los seres humanos, y la identificación es fundamental. Todas las pruebas realizadas con extrema calidad se tornan insatisfactorias si la muestra no es la correcta, si se ha etiquetado la bolsa con el nombre de otro paciente o si no se identifica adecuadamente al paciente.2,23,26,27
La tipificación ABO incorrecta a la bolsa o al paciente puede ocurrir en varios puntos, desde que se extrae la sangre al donante hasta que se administra al paciente. Esto puede ser corregido si se cumple con los pasos del protocolo pretransfusional. Los casos que pueden originar complicaciones son aquellos de extrema urgencia, en los que las pruebas pretransfusionales deben ser postergadas.2,27 El almacenamiento incorrecto en el refrigerador de las unidades de componentes de la sangre es peligroso en las situaciones de urgencia por el hecho comentado.
En Cuba está normado un protocolo para el aseguramiento técnico administrativo pretransfusional, cuyo cumplimiento garantiza un sistema de seguridad múltiple donde es improbable la RTHA por incompatibilidad ABO y de muy baja probabilidad la asociada con otros Ag.28 Sin embargo, estas reacciones se presentan. Hay que considerar entonces la existencia de otros factores subjetivos como son la experiencia, el entrenamiento y la destreza del personal. El personal debe ser evaluado periódicamente y se deben realizar cursos de superación para mejorar las deficiencias encontradas. Además, en cada institución deben estar disponibles los procedimientos estándares para cada tarea del protocolo. Estas tareas incluyen: consentimiento informado, solicitud de transfusión, identificación del paciente, obtención de la muestra, pruebas pretransfusionales, etiquetado del componente, nueva identificación del paciente, prueba de cabecera, prueba biológica y llenado de los registros.
Consideración aparte merece la posible negligencia del personal, lo que exige la correspondiente acción disciplinaria.
La reducción del uso de componentes produce una disminución en la exposición del paciente a productos sanguíneos, lo que a su vez reduce el riesgo de reacciones hemolíticas y otras complicaciones relacionadas con la transfusión. Se debe establecer una política transfusional rigurosa que establezca la revisión periódica del uso de los productos de la sangre.29,30 Las complicaciones de la transfusión son lamentables, pero lo son más si este proceder no es necesario.
Summary
Immediate immune hemolytic transfusional reaction
The immediate immunological hemolytic reaction is the main cause of death associated with transfusion. The antigen-antibody reaction with the subsequent .hemolysis of erythrocytes triggers a systemic inflammatory response syndrome resulting from the release of cytokines (tumoral a necrosis factor, interleukin 1, interleukin 8, interleukin 6) and from the activation of enzymatic amplification systems (coagulation, fibrinolysis, calicrein-bradykinin). The disseminated intravascular coagulation and the acute renal failure are physiopathological events that stand out in the clinical picture. Pretransfusional protocols that provide multiple safety steps, and whose fulfiment discards the occurrence of fatal reactions, have been developed. However, the idenfication erros, the lack of knowledge and negligence are still present and are considered as its fundamental causes.
Key words: Hemolysis, antigen-antibody reaction, cytokines, pretransfusional protocol.
Referencias bibliográficas
1. Genetet B, Mannoni P. Antecedentes históricos. En: Genetet B, Mannoni P. La transfusión. La Habana: Científico-Técnica; 1984. p. 1-9.
2. Indrikovs AJ. Transfusión accidental con sangre ABO incompatible: proceso de análisis de las causas contribuyentes. Sangre 1997;42:205-13.
3. Capon SM, Goldfinger D. Acute hemolytic transfusion reaction, a paradigm of the systemic inflammatory response: New insights into pathophysiology and treatment. Transfusion 1995;35:513-20.
4. Nieto MD. Papel de las citoquinas en las reacciones adversas asociadas a transfusión. Rev Arg Transf 1999;25:253-70.
5. Pruss A, Salama A, Ahrens N, Hansen A, Kiesewetter H, Koscielny J, et al. Immune hemolisis serological and clinical aspects. Clin Exp Med. 2003;3:55-64.
6. Engelfriet CP, Overbeeke MAM, von der Borne ARGKR. Autoimmune hemolytic anemia. Sem Hematol 1992;29:3-12.
7. Worl Health Organization. Adverse effects of transfusion. Worl Health Organization. The clinical use of blood. Malta; 2001. p 60-70.
8. Davenport DD, Kunkel SL. Cytokine roles in hemolytic and nonhamolytic transfusion reactions. Transfus Med Rev 1994;3:157-68.
9. Van der Poll T, Levi M, Hack CE. Effects on leukocytes after injection of tumor necrosis factor into healthy humans. Blood 1992;79:693-8.
10. Davenport RD, Streiter RM, Kumkel SL. Red cell ABO incompatibility and production of tumour necrosis factor-alfa. Br J Haematol 1991;78:540-4.
11. Lenz SR, Tsiang M, Sadler JE. Regulation of thrombomoduli by tumor necrosis factor- a : Comparison of transcripcional and posttranscriptional mechanism. Blood 1991;77:542-50.
12. Vervloet MG, Lambertus GT, Hack E. Derangements of coagulation and fibrinolysis in critically III patients with sepsis and septic shock. Sem Thromb Hemost 1998;24:33-44.
13. Popovsky M. Transfusión reaction. Bethesda: AABB Press; 1996.
14. Davenport RD, Burdick M, Moore SA, Kumkel SL. Cytokine production in IgG- mediated red cell incompatibility. Transfusion 1993;33:19-24.
15. Davenport RD, Burdick M, Streiter RM, Kumkel SL. Monocyte chemoattractant protein production in red cell incompatibility. Transfusion 1994;34:16-9.
16. Davenport RD, Standiford TJ, Streiter RM and Kumkel SL. Interleukin-8 production in red blood cell incompatibility. Blood 1990;76:2439-42.
17. Davenport RD. Cytokines and erythricyte incompatibility. Hematology 1994;1:452-6.
18. Davenport RD, Burdick M, Streiter RM, Kumkel SL. In vitro production of interleukin-1 receptor antagonist in IgG-mediated red cell incompatibility. Transfusion 1994;34:297-303.
19. Welles JV. Mecanismos inmunitarios de daño tisular. En: Stites DP, Stobo JD, Fudenberg HH, Welles JV, eds. Inmunología básica y clínica. 5 ed. México: El Manual Moderno; 1985. p. 132-51.
20. Toda N, Okamura T. Endothelium-dependent and independent response to vasoactive substances of isolated human coronary artery. Am J Phhysiol 1992;262:H995-9.
21. Hambleton J, Leung LL and Levi M. Coagulation: Consultative hemostasis. The American Society of Hematology; 2002.
22. Brecher ME. Technical manual. 14 ed. Bethesda: American Association of Blood Banks; 2002.
23. Carreras LA. Efectos secundarios inmunológicos y no inmunológicos de la hemoterapia. Borrasca AL, Arocha CL, Campos CC, Parreira A, Pavlovsky S, Ruiz G, eds. En: Enciclopedia Iberoamericana de Hematología IV. Salamanca: Europa Artes Gráficas; 1992. p. 279-92.
24. Cregan P, Donegan E, Gotelli G. Hemolytic transfusion reaction following transfusion of frozen and washed autologous red cells. Transfusion 1991;31:401-3.
25. Murphy WG, McClellannd DBL. Deceptively low morbidity from failure to practice safe blood transfusion: An analysis of serious blood transfusion errors. Vox Sang 1989;57:59-62.
26. Stainsby D, Jones H, Todd A, Knowles S, Taylors C, Beatty C, et al. Serious hazards of transfusion. Summary of Annual Report 2001- 2002. SHOT Office; 2003.
27. Bryan S. Hemolytic transfusion reaction: safeguards for practice. J Perianesth Nurs 2002;17:399-403.
28. Comité de Normas de la Comisión Nacional de Medicina Transfusional del Ministerio de Salud Pública de Cuba. Procederes de Bancos de Sangre y Servicios de Transfusiones. La Habana; 2003 ( en imprenta).
29. Cortina L, López R. Utilización de los componentes celulares de la sangre. Rev Cubana Hematol Inmunol Hemoter 2000;16:78-89. 30. Rosen NR, Bates LH, Herod G. Transfusion therapy: improved patient care and resource utilization. Transfusion 1993;33:341-7.
Recibido: 20 de agosto de 2006. Aprobado: 13 de septiembre de 2006.
Dr. Lázaro Cortina Rosales . Instituto de Hematología e Inmunología. Apartado Postal 8070, Ciudad de La Habana, CP 10800, Cuba. Tel (537) 643 8268, 643 8695, Fax (537) 44 2334. e-mail: ihidir@hemato.sld.cu